역학 부문 모델
Compartmental models in epidemiology구획 모형은 매우 일반적인 모델링 기법입니다.그것들은 종종 전염병의 수학적 모델링에 적용된다.모집단은 라벨이 있는 구획에 할당됩니다(예: Susceptible, Infectious 또는 Recoveryed).사람들은 칸 사이를 이동할 수 있다.라벨의 순서는 일반적으로 구획 간의 흐름 패턴을 나타냅니다.예를 들어 SEIS는 민감, 노출, 감염, 다시 취약함을 의미합니다.
이러한 모델의 기원은 20세기 초이며, 1916년 로스, 1917년 로스,[2][3] 1917년 허드슨, 1927년[4] 커맥과 맥켄드릭, [5]1956년 켄달 등의 중요한[1] 작품들이 있다.
모델은 보통 미분 방정식(결정론적)과 함께 실행되지만 확률적(랜덤) 프레임워크와 함께 사용될 수도 있습니다. 확률적(랜덤) 프레임워크는 더 현실적이지만 분석하기가 훨씬 더 복잡합니다.
모델은 질병이 어떻게 퍼지는지, 감염된 총 수 또는 유행 기간과 같은 것들을 예측하고, 생식 횟수 같은 다양한 역학 변수를 추정하려고 합니다.그러한 모델은 다른 공중 보건 개입이 전염병의 결과에 어떻게 영향을 미칠 수 있는지를 보여줄 수 있다. 예를 들어, 주어진 인구에서 제한된 수의 백신을 발행하기 위한 가장 효율적인 기술은 무엇인가.
SIR 모델
SIR[6][7][8][9] 모델은 가장 단순한 구획 모델 중 하나이며, 많은 모델이 이 기본 형식의 파생 모델입니다.이 모델은 다음의 3개의 구획으로 구성됩니다.
- S: 민감한 개인의 수.민감하고 전염성이 있는 개인이 "감염성 접촉"을 하게 되면, 민감성이 있는 개인은 질병에 감염되어 감염 구획으로 이행한다.
- 감염자 수이 사람들은 감염된 적이 있고 민감한 사람들을 감염시킬 수 있는 사람들이다.
- 제거(및 면역)된 개인 또는 사망한 개인 수를 나타내는 R.이 사람들은 감염되어 질병에서 회복되어 제거된 칸에 들어가거나 사망한 사람들입니다.사망자의 수는 전체 인구에 대해 무시할 수 있다고 가정한다.이 구획은 "복구됨" 또는 "내성"이라고도 합니다.
이 모델은 사람에게서 사람에게로 전염되는 감염성 질환에 대해 합리적으로 예측할[10] 수 있으며, 회복이 홍역, 유행성 이하선염, 풍진과 같은 지속적인 내성을 갖게 한다.
이러한 변수(S, I 및 R)는 특정 시간에 각 구획에 있는 인구 수를 나타냅니다.민감하고 감염되며 제거된 개인의 수는 시간에 따라 달라질 수 있음을 나타내기 위해(전체 모집단 크기가 일정하더라도), 정확한 숫자를 t(시간)의 함수로 만든다: S(t), I(t) 및 R(t).특정 집단의 특정 질병에 대해 이러한 기능은 발생 가능성을 예측하고 통제하기 [10]위해 고안될 수 있다.
t의 가변 함수에 의해 암시되었듯이, 모형이 동적인 이유는 각 구획의 숫자가 시간에 따라 변동할 수 있기 때문입니다.이 동적 측면의 중요성은 1968년 백신이 도입되기 전 영국의 홍역과 같이 감염 기간이 짧은 풍토병에서 가장 뚜렷하다.그러한 질병은 시간에 따른 민감성 수(S(t)의 변동으로 인해 발병 주기에 발생하는 경향이 있다.전염병이 유행하는 동안, 감염되기 쉬운 사람들의 수가 빠르게 감소하여 감염되고 제거된 칸으로 들어갑니다.이 질병은 감염자의 수가 다시 증가하기 전까지는 재발할 수 없다. 예를 들어, 감염된 구획에서 태어난 자손의 결과이다.
인구의 각 구성원은 전형적으로 감염되기 쉬운 것에서 회복되는 것으로 발전한다.이는 박스가 여러 구획을 나타내고 화살표가 구획 간 전환을 나타내는 흐름도(flow diagram)로 나타낼 수 있습니다.
이행률
모델의 전체 사양을 위해 화살표에는 컴파트먼트 간 전환 속도를 라벨로 표시해야 합니다.S와 I 사이의 전이율은 d(S/N)/dt = -βSI/N으로2 가정한다.여기서 N은 총 모집단, β는 1인당 1회당 평균 접촉자 수이며, β는 감수성 피험자와 감염자 간의 접촉에서 질병 전염 확률을 곱한 것이며, SI2/N은 이들 접촉자와 감염자 간의 접촉자 비율이다.민감한 사람이 감염되는 결과를 초래하는 민감한 개인.(이는 분자 간의 무작위 충돌이 화학 반응을 일으키고 부분 비율이 두 반응물의 농도에 비례하는 화학 물질에서의 질량 작용의 법칙과 수학적으로 유사합니다.
I와 R 사이의 전이율은 감염자 수인 δI에 비례한다고 가정한다.이는 감염자가 임의의 시간 간격 dt에서 회복할 확률을 단순히 µdt로 가정하는 것과 같다.개인이 평균 D 기간 동안 감염되면 θ = 1/D가 된다.이는 또한 감염 상태에 있는 개인이 보내는 시간이 지수 분포를 갖는 랜덤 변수라는 가정과 동일합니다."고전적" SIR 모델은 I-R 전이율에 대해 보다 복잡하고 현실적인 분포(예[11]: Erlang 분포)를 사용하여 수정할 수 있다.
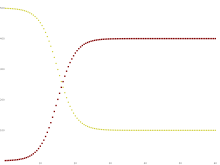
감염구획에서 제거가 없는 특수한 경우(θ=0), SIR 모델은 로지스틱 솔루션을 가진 매우 단순한 SI 모델로 환원되며, 모든 개인이 최종적으로 감염된다.
바이탈 다이내믹스가 없는 SIR 모델

유행병, 예를 들어 독감의 역학관계는 종종 출생과 사망의 역학관계보다 훨씬 더 빠릅니다. 따라서 출생과 죽음은 종종 단순한 구분 모델에서 생략됩니다.위에서 설명한 소위 바이탈 다이내믹스(생생과 사망, 때때로 인구통계학)가 없는 SIR 시스템은 다음과 같은 일반 미분 [7][12]방정식으로 표현될 수 있다.
서 S S는 취약인구의 주식 (\I)는 의 , R(\ R은 제거인구의 주식, N(\ N은이 세 가지를 합한 것입니다.
이 모델은 William Ogilvy Kermack과 Anderson Gray McKendrick에 의해 현재 Kermack-McKendrick 이론이라고 불리는 특별한 사례로 처음 제안되었으며 McKendrick이 Ronald Ross와 함께 수행한 작업을 따랐습니다.
이 시스템은 비선형이지만 암묵적인 [6]형태로 분석 솔루션을 도출할 수 있습니다.먼저 다음 사항에 주의해 주십시오.
다음과 같습니다.
N N의 항상성을 수학적인 용어로 표현합니다. 위의 관계는 세 변수 중 두 변수만 연구하면 된다는 것을 의미합니다.
둘째, 감염 클래스의 역학은 다음 비율에 따라 달라집니다.
이른바 기본 재생산 번호(기본 재생산 비율이라고도 함)이 비율은 모든 환자가 감염되기 [13][14]쉬운 모집단의 단일 감염에서 예상되는 새로운 감염 수(이 새로운 감염을 2차 감염이라고 부르기도 한다)로 도출된다.이 아이디어는 접촉자 간의 일반적인 시간이 c -1 { T_} = \^{-이고 제거까지의 일반적인 시간이 r 1 { style{} = \^{-1이라고 하면 더 쉽게 알 수 있습니다. 여기서 감염자 수에 따라 평균이렇게 됩니다.감염이 제거되기 전에 감염자와 함께 l: T / c. { / } 。
첫 번째 미분 방정식을 세 번째 방정식으로 나누면 변수를 분리하고 적분하면
서 S {(0 및( {R(0은 민감하고 제거된 피험자의 초기 번호입니다.한 개인의 초기 비율에 s = S( ) / N{ _ { () /N { \ s _ { \ } ( \ ) / ( r) / display (\ inftyle 。 t \display t \\ ,has 。
(감염 구획은 이 제한으로 비워집니다).이 초월 방정식은 Lambert W [15]함수의 관점에서 해답을 가진다.
는 s 0 {\}=이 한 SIR 모델의 단순한 가정에 부합하는 전염병 말미에 모든 모집단이 제거된 것은 아니므로 일부 개체는 영향을 받기 쉬운 상태로 남아 있어야 한다는 것을 보여준다.전염병의 종식을 이끄는 원동력은 감염자 수의 감소이다.전염병은 일반적으로 감수성이 예민한 개인이 완전히 부족하기 때문에 끝나지 않는다.
기본 재생산 번호와 초기 감수성의 역할은 매우 중요합니다.실제로 감염자에 대한 방정식을 다음과 같이 다시 작성합니다.
다음과 같은 경우에 발생합니다.
그 후, 다음과 같이 합니다.
즉, 감염자 수의 증가와 함께 적절한 전염병 발생이 있을 것이다(이는 인구의 상당 부분에 이를 수 있다).반대로 만약
그리고나서
즉, 감염되기 쉬운 인구의 초기 규모와는 별개로 이 질병은 결코 적절한 전염병 발생을 야기할 수 없다.그 결과, 기본 재생수와 초기 감수성 모두 매우 중요한 것이 분명하다.
감염의 힘
위 모델에서 기능은 다음과 같습니다.
민감한 개인의 구획에서 감염 개인의 구획으로의 전환 속도를 모델링하여 감염의 힘이라고 합니다.단, 대규모 전염성 질환의 경우 감염 대상자의 절대 수가 아니라 비율(총 상수 N과 관련하여에 따라 달라지는 감염력을 고려하는 것이 보다 현실적이다.
이후[16] 카파소와 다른 저자들은 감염 과정을 보다 현실적으로 모델링하기 위해 비선형 감염력을 제안했다.
SIR 모델에 대한 정확한 분석 솔루션
2014년 Harko와 공동 저자들은 SIR [6]모델에 대해 정확한 분석 솔루션(숫자로만 계산할 수 있는 적분 포함)을 도출했다.바이탈 다이내믹스 설정이 없는 경우 S( ) ) {)= 등의 다음과 같은 시간 매개변수에 해당합니다.
위해서
초기 조건으로
서 tI( T 를 만족합니다. 의 R{\({\displaystyle }})에 초월방정식에 T - ( - () / ( / (0) { }- }(=infty0(0 0 0 { 0인
Miller 수율에 의해[17][18] 발견된 동등한 분석 솔루션(숫자만 계산할 수 있는 적분 포함)
서 ( ){ )는 개인이 t { t까지 수신한 예상 전송 수로 해석할 수 있습니다. 가지 솔루션은 - ( t ) {\ e (t)}=에 관련됩니다.
사실상 같은 결과를 커맥과 [4]맥켄드릭의 원작에서도 찾을 수 있다.
이러한 해법은 원래 미분 방정식의 오른쪽에 있는 모든 항이 I I에 비례한다는 점에 주목하면 쉽게 이해할 수 있습니다.따라서 방정식은 I{\ I로 할 수 있으며, 왼쪽의 미분 연산자가 단순 {d/}가 되도록 시간을 조정할 수 있습니다. 서 d = ddisplay style = d\ style style = d\style int tstyle \style = d\display int = display int int display이제 미분 방정식은 모두 선형이며, d / d { =} const 의 세 번째 방정식은 { style \와 R{\R}(및 의 { })이 단순히 선형으로 관련되어 있음을 나타냅니다.
그래서 필요가 없는 수치 inte을 하는 것이다는 주요 사건 보고 모델의 대단히 정밀한 분석적 approximant뿐만 아니라 최종 값 S에 정확한 분석적 표현({\displaystyle S_{\infty}}, 나는}{\displaystyle I_{\infty}∞, R({\displaystyle R_{\infty}}Kröger과 Schlickeiser,[8]에 의해 제공되었다.graSIR 모델을 해결하기 위한 방법(Microsoft Excel을 사용한 COVID-19 수치 시뮬레이션에 대한 단순화된 사례 사례는 여기에서 찾을 수 있음)은 기존 데이터에서 매개변수를 얻거나 SIR 모델에 의해 모델링된 전염병의 미래 역학을 예측하기 위한 것이다.근사치는 Microsoft Excel, MATLAB 및 Mathematica와 같은 모든 기본 데이터 시각화 소프트웨어의 일부인 Lambert W 함수를 포함합니다.
반면 Kendall[5]이 초기 조건 S(0){S(0)\displaystyle}, 나는(0){I(0)\displaystyle}, R(0){R(0)\displaystyle}위의 관계를 통한 결합하는 소위 사상 SIR 모델을 고려하고 있을 때 Kermack과 McKendrick[4]더 일반적인 semi-time 경우에 S(0){공부할 것을 제안했다.\displS( I( {(0는 둘 다 임의입니다.반시간 SIR [8]모델로 표시된 이 후자 버전은 미래 t에 대해서만 예측합니다. 반시간 모델에서도 [9]최종 값에 대한 분석적 근사식 및 정확한 식을 사용할 수 있습니다.
바이탈 다이내믹스와 일정한 모집단을 가진 SIR 모델
μ와로 특징지어지는 인구와 전염병이 [7]확산되고 있는 인구를 생각해보자매스액션 전송 모델은 다음과 같습니다.
무병균형(DFE)은 다음과 같다.
이 경우 기본 복제 번호를 도출할 수 있습니다.
임계값 속성을 가집니다.실제로 생물학적으로 유의한 초기값과는 별개로 다음과 같이 나타낼 수 있다.
EE 지점은 풍토균형이라고 불린다.휴리스틱 인수를 통해 R 0은 전적으로 민감한 모집단에서 단일 감염 대상자에 의해 발생한 평균 감염 수로 해석될 수 있으며, 위의 관계는 생물학적으로 이 수치가 1 이하이거나 같은 경우, 반면 이 수치가 gr이면 멸종됨을 의미한다.그 질병은 인구에서 영구히 풍토병이 될 것이다.
SIR 모델

1927년 W.O. Kermack과 A.G. McKendrick은 3개의 구획만을 가진 고정집단을 검토하는 모델을 만들었습니다.() \ S () ; infected , (t )\ () ;recovered , () .이 모델에 사용되는 컴파트먼트는 다음 세 가지 [4]클래스로 구성됩니다.
- { S는 시간 t에 아직 질병에 감염되지 않은 개인 또는 인구의 질병에 취약한 사람을 나타내는 데 사용됩니다.
- ( ) \ I ( )는 이 질병에 감염되어 감염되기 쉬운 카테고리에 속하는 사람들에게 질병을 전파할 수 있는 인구의 개인을 나타냅니다.
- () \ R ( )는 면역 또는 사망에 의해 감염되어 질병에서 제거된 개인에게 사용되는 구획입니다.이 범주에 속하는 사람은 다시 감염되거나 다른 사람에게 감염될 수 없습니다.
이 모델의 흐름은 다음과 같이 생각할 수 있습니다.
SIR 모델을 해결하기 위해 시뮬레이션을 사용하는 경우, 세 기능에서 N ( t ) + I( t ) + ( N)+을 사용하여 N { N 이 시뮬레이션 내에서 일정하게 유지되어야 함을 해결합니다.혹은 시뮬레이션을 실시하지 않고 해석적[8] 근사치를 사용할 수 있다.모델은 S S 0 { I R { R의 으로 시작합니다.감염 및 제거된 범주의 감염자 수는 0이 됩니다.SIR 모델이 항상 유지된다고 가정할 경우 이러한 초기 조건은 [8]독립적이지 않다.이후 흐름 모델은 β\displays β(\displaystyle \displays에 설정 값으로 매 시점마다 3개의 변수를 업데이트합니다. 시뮬레이션은 먼저 감염된 환자로부터 감염된 환자를 업데이트한 후 제거된 범주를 다음 시점(t=1).이것은 3개의 카테고리 사이의 플로우 퍼슨에 대해 설명합니다.전염병 발생 중에는 이 모델에서는 영향을 받기 쉬운 범주가 이동하지 (\도 전염병 발생 과정에 따라 변화합니다 이러한 변수는 전염병의 길이를 결정하며 각 사이클에 따라 업데이트되어야 합니다.
이들 방정식의 공식화에는 다음과 같은 몇 가지 가정이 있었다.첫째, 인구 중 개인은 단위시간당 접촉하는 사람의 비율 a과 한 비율(\ b로 질병에 걸릴 확률이 다른 모든 개인과 동일한 것으로 간주되어야 한다.다음으로β(\를 a a와 b b의 곱셈으로 .이것은, 송신 확률에 컨택 레이트를 곱한 것입니다.또한 감염자는 단위시간당 b명 b과 접촉하지만 그 중 극히 일부인 S만이 감염될 수 있다.따라서 모든 감염자가 S (\=\ S 민감자를 시킬 수 있으므로 단위시간당 감염자에 의해 감염되는 전체 감염자 는 SI (\ SI이다. 두 번째 및 세 번째 등식에 대해 민감계급을 동일한 수치로 간주한다.감염된 클래스에 들어갑니다.단, 단위시간당 감염률 회복/사망률 /{\(\1/\을 나타내는)과 동일한 수치가 이 클래스를 떠나 제거된 클래스로 들어갑니다.동시에 일어나는 이러한 과정을 매스 액션의 법칙이라고 합니다.이것은 집단에서 두 집단 사이의 접촉률이 관련된 각 집단의 크기에 비례한다는 널리 받아들여지고 있는 생각입니다.마지막으로, 감염과 회복 속도는 출생과 사망의 시간 척도보다 훨씬 빠르기 때문에 이 [20]모델에서는 이러한 요인들이 무시된다고 가정한다.
안정 상태 솔루션
되는 감수성 지속시간은 [min ( LTS )]{ style \{ E [ \ ( T _ { } \ T _ { S} 。서T L { { }은 { S } 입니다다음과 같이 단순화할[21] 수 있습니다.
감수성 시간 중 감수성구획 \ N에 진입하는 인원의 수가 되어야 한다.
마찬가지로 정상상태 감염자수는 감염가능상태(감염가능수, 감염횟수) \=n}{ + {\style 의배이다.
기타 부문별 모델
SIR 모델에는 출생과 사망을 포함한 많은 수정 사항이 있다. 여기에는 회복 시 면역이 없는 경우(SIS 모델), 면역이 단기간 동안만 지속되는 경우(SIRS), 사람이 감염되지 않는 경우(SEIS 및 SEIR), 신생아가 면역으로 태어날 수 있는 경우 등이 포함된다.y(MSIR)
기본 SIR 모델의 변형
SIS 모델
예를 들어 감기나 인플루엔자에 의한 감염은 면역력이 오래가지 않는다.이러한 감염은 감염에서 회복되었을 때 면역력을 주지 않으며, 개인은 다시 취약해진다.
모델은 다음과 같습니다.
N으로 표시된 총 모집단은 다음과 같습니다.
다음과 같습니다.
즉, 감염의 역학은 로지스틱 함수에 의해 지배되므로§ ( {\I ( :
(변수를 변환하여) 이 모형에 대한 분석 솔루션을 찾을 수 있습니다. - (\ I 이를 평균장 [22]방정식에 대입함)로 하여 기본 재생률이 통일성보다 높다.해결 방법은 다음과 같습니다.
- ( ) 1 + e - t\ I ( t ) ={ I _ { \ { + { - \ t}}} 。
서 I ( - / ) { \ I _ { \ } ( 1 - \ / \ ) }은 풍토성 감염 집단이고, -- { \ \ ci \ display - 1 - display V / - 1 - { I in _ in .-( ){ S
특별한 로, { \ displaystyle 0 을 가정하면 일반적인 로지스틱 함수를 얻을 수 있다.이는 R 에서도 고려할 수 있습니다. 즉, 가수행되지 않습니다그것은 SI [23]모델입니다.S - S를 하는 미분 방정식 시스템은 다음과 같이 감소합니다.
장기적으로 SI 모델에서는 모든 개인이 감염될 것이다.
SIRD 모델
감수성-감염성-재발견성-사망 모델은 회복된 모델(특히 현재 면역이 된 개인)과 [13]사망 모델을 구분합니다.이 모델에서는 다음 미분 방정식 시스템을 사용합니다.
서 β \각각 [24]감염률, 회복률 및 사망률입니다.
SIRV 모델
Sensible-Impectious-Recovered-Vacced-Vacciped 모델은 취약 [25]모집단의 백신 접종을 설명하는 확장 SIR 모델이다.이 모델에서는 다음 미분 방정식 시스템을 사용합니다.
서 β, \ vdisplaystyle, 는 각각 감염률, 회복률, 예방접종률이다.반시간 초기 S ( ) ( - ) { ( 0 ) = ( 1 - \ )} , () {I ( 0 ) ( ) { R 0 ( 0 ) =0 ( 0 ) 모델이 대략적으로 [25]해결되었습니다.대 유행병의 격한 표현 중 사건이 중요한 감소 예방 접종률 bc{\displaystyle b_{c}}는 것을 넘어에 민감한 칸의 정상 크기 S({\displaystyle S_{\infty}}여전히 상대적으로 가까운 S(0)에{\disp은 k+b<1− 2η{\displaystyle k+b<, 1-2\eta}이 필요하다.layst S S( + ( + ( + ( {S ( + + R 0) + (0) 를 하는 임의의 초기 조건N은는) R ( ( 0 {\(0)=)=[25]인 해결된 특수 사례에 매핑할 수 있습니다.
MSIR 모델
홍역을 포함한 많은 감염의 경우, 아기는 민감한 구획에서 태어나지 않지만 모체 항체(태반을 통과하고 추가로 대장균을 통해)로부터의 보호로 인해 생후 처음 몇 달 동안은 질병에 면역이 된다.이것은 수동 면역이라고 불립니다.이 추가된 세부 사항은 모델 시작 부분에 M 클래스(material derived intermity)를 포함시킴으로써 나타낼 수 있다.
이를 수학적으로 나타내기 위해 구획 M(t)을 추가한다.그 결과 다음과 같은 미분방정식이 생성됩니다.
반송파 상태
결핵과 같은 전염병을 앓은 적이 있는 사람은 스스로 병을 앓지 않으면서 완전히 회복되지 않고 계속 감염을 가지고 있는 사람도 있습니다.그런 다음 감염 구획으로 다시 이동하여 (결핵과 같은) 증상을 겪거나, 증상을 겪지 않으면서 보균자 상태에서 다른 사람을 계속 감염시킬 수 있습니다.이것의 가장 유명한 예는 아마도 22명의 사람들을 장티푸스에 감염시킨 메리 말론일 것이다.캐리어 컴파트먼트에는 C라는 라벨이 붙어 있습니다.
SEIR 모델
많은 중요한 감염의 경우, 개인이 감염되었지만 아직 감염되지 않은 상당한 잠복기가 있다.이 기간 동안 개인은 (노출의 경우) 구획 E에 있습니다.
대기시간이 a, 평균 대기시간은 -(\1})의 지수 분포를 갖는 랜덤 변수라고 가정하고 출생률\ \Lambda 가 사망률 와 같다고 한다. (N(\ N이 일정하게 되도록) 모델이 있습니다.
S+ + + ,(\ Sdisplaystyle N)이 출생률과 사망률이 동일하다는 단순화된 가정 때문에 이 값은 일정합니다. 으로 N {\ N이 변수입니다.
이 모델의 경우 기본 복제 번호는 다음과 같습니다.
SIR 모델과 유사하게, 또한 이 경우, 우리는 무병균형(N,0,0,0)과 풍토균형 EE를 가지고 있으며, 생물학적으로 의미 있는 초기 조건과는 독립적으로 그것을 보여줄 수 있다.
다음과 같은 내용을 담고 있습니다.
주기적으로 변화하는 β () \ \ t )의 경우 DFE의 글로벌 매력 조건은 다음과 같은 주기 계수를 갖는 선형 시스템이다.
는 안정적입니다(즉, 복합 평면의 단위 원 내부에 Flocet의 고유값이 있습니다).
SEIS 모델
SEIS 모델은 마지막에 면역이 획득되지 않는다는 점을 제외하고 SEIR 모델(위)과 같다.
이 모델에서 감염은 면역력을 남기지 않기 때문에 회복된 개인은 다시 S(t) 구획으로 이동하면서 감수성으로 돌아간다.이 모델을 설명하는 미분방정식은 다음과 같습니다.
MSEIR 모델
질병의 경우, 수동 면역 인자와 잠복기를 포함한 MSEIR 모델이 있다.
MSEIRS 모델
MSEIRS 모델은 MSEIR와 유사하지만 R 클래스의 면역은 일시적인 것이므로 개인은 일시적인 면역이 종료될 때 감수성을 회복할 수 있다.
다양한 컨택 레이트
병에 걸릴 확률이 일정하지 않다는 것은 잘 알려져 있다.대유행이 진행됨에 따라 대유행에 대한 반응은 단순한 모델에서 일정하다고 가정되는 접촉률을 변화시킬 수 있다.마스크, 사회적 거리 두기, 봉쇄와 같은 대책은 전염병의 속도를 줄이는 방식으로 접촉률을 변화시킬 것이다.
게다가, 일반적인 감기 바이러스와 같은 어떤 질병들은 겨울에 더 많이 발생하는 계절적인 질병들이다.홍역, 유행성 이하선염, 풍진 등 소아기 질환은 학교 일정과의 상관관계가 강하기 때문에 방학 중에는 발병 확률이 크게 낮아진다.따라서 많은 종류의 질환에 대해 주기적으로('계절적') 접촉률이 변화하는 감염력을 고려해야 한다.
기간 T는 1년입니다.
따라서, 우리의 모델은
(회수된 역학은 - S -(\ R에서 쉽게 나타난다.) 즉, 주기적으로 다른 매개변수를 갖는 비선형 미분 방정식 세트이다.이러한 종류의 동적 시스템은 비선형 파라메트릭 공명의 매우 흥미롭고 복잡한 현상을 겪을 수 있다는 것은 잘 알려져 있습니다.다음과 같은 경우 쉽게 알 수 있습니다.
반면 적분이 1보다 크면 질병은 사라지지 않고 그러한 공명이 있을 수 있다.예를 들어 주기적으로 변화하는 컨택트 레이트를 시스템의 '입력'으로 간주하면 출력은 입력 주기의 배수가 되는 주기 함수이다.이것은 접촉률 변동 기간과 풍토균형 근처의 감쇠 진동의 의사 기간 사이의 상호작용으로서 일부 전염병의 다년(일반적으로 2년마다) 전염병 발생을 설명하는 데 기여하였다.놀랍게도, 몇몇 경우에, 그 행동은 또한 준주기적이거나 심지어 혼란스러울 수 있다.
확산 SIR 모델
시공간 구획 모델은 전체 수가 아니라 민감성/감염성/회복된 사람의 밀도를 설명한다.결과적으로, 그들은 또한 우주에서 감염된 사람들의 분포를 모델링할 수 있게 해준다.대부분의 경우, 이것은 SIR 모델과 확산 방정식을 결합함으로써 이루어집니다.
서 D S I 및 R은 확산 상수입니다.이것에 의해, 반응 확산 방정식을 얻을 수 있다.(치수를 위해 β(\는 단순한 SIR 모델과 비교하여 변경해야 합니다.)이런 종류의 초기 모델들은 [27]유럽에서 흑사병의 확산을 모델링하기 위해 사용되어 왔다.이 모델의 확장은 예를 들어 사회적 [28]거리두기와 같은 비약적 개입의 효과를 통합하기 위해 사용되어 왔다.
인터랙티브 서브그룹 SEIR 모델
사회적 접촉, 질병 심각도 및 치사성 및 예방 조치의 효과는 상호작용 하위 집단 간에 상당히 다를 수 있다. 예를 들어, 노인과 젊은이의 상호작용 [26]연결을 통해 상호 연결된 각 하위 그룹에 대한 별도의 SEIR 모델을 사용할 수 있다.그러한 Interacting Subpopulation SEIR 모델들은COVID-19 유행병 모델링에 대륙 규모에서 strategies[29]그 전염병의 단축과 사건과 죽음에 대해 백신에 대한 제한된 접근의 배경에서 바이러스의 단계에서 감소를 약속하는 가속이 가능하며, 개인 subpopulation-targeted 예방 접종을 개발하는 데 사용되었다.Va우려의 폭동
네트워크상의 SIR 모델
SIR 모델은 일반적으로 요구되는 균질 혼합 조건보다 더 현실적인 형태의 연결을 모델링하기 위해 다양한 종류의 네트워크에서 연구되어 왔습니다.개인이 특정 시간 단계에서 감염된 각 인접 라우터에 의해 감염될 확률이 p인 네트워크에서의 단순한 전염병 모델은 Erdos Renyi [30]랜덤그래프에서의 거대 컴포넌트 형성과 유사한 결과를 낳습니다.
SIRSS 모델 - SIR과 사회적 스트레스 모델링의 조합
전염병의 역학관계는 사람들의 행동이 시간에 따라 어떻게 변하느냐에 달려있다.예를 들어 유행 초기에 사람들은 무지하고 부주의하다 전염병이 발생하고 경보가 울리면 여러 가지 규제에 따르기 시작하고 전염병의 확산은 줄어들 수 있다.시간이 지남에 따라 일부 사람들은 이러한 제한에 지치고 좌절하며, 특히 새로운 사례가 줄어들면 이를 따르지 않게 됩니다.잠시 휴식을 취한 후 다시 제한을 따를 수 있습니다.하지만 이 일시정지 동안 제2의 물결은 제1의 물결보다 더 강해질 수 있다.사회 역학을 고려해야 한다.사회적 스트레스의 사회적 물리 모델은 고전적인 전염병 모델을 보완합니다.[31]
가장 단순한 SIR-사회적 스트레스(SIRSS) 모델은 다음과 같이 구성된다.민감한 개인(S)은 행동 유형에 따라 세 개의 하위 그룹으로 나눌 수 있다. 즉, 유행병(Sign), 이성적 저항(Sres), 외부 자극에 반응하지 않는 탈진(Sexh)이다(이는 일종의 난치 기간이다).즉, S(t) = Sign(t) + Sres(t) + S(t) + Sexh(t)이다.상징적으로, 사회적 스트레스 모델은 "반응 체계"에 의해 제시될 수 있다(여기서 나는 감염된 개인을 나타낸다).
- Sign + 2I → Sres + 2I – 동원 반응(여기서 자기촉매 형태는 전이율이 감염된 비율 I의 제곱에 비례한다는 의미)
- Sres → Sexh – 미끄럼 방지 제한으로 인한 피로로 인한 배기 프로세스;
- Sexh → Sign – 초기 상태(내화 기간의 끝)에 대한 느린 완화.
SIR의 주요 유행 반응
- S...+I → 2I
는 S, Sres 및exh S에 대해 서로ign 다른 반응 속도 β(\를 가집니다.S의 경우res S 및 S의ign 경우보다ign β가 낮을 수 있습니다.
국가 간 차이는 두 가지 운동 상수에 집중된다. 즉, 13개 [31]국가의 COVID-19 전염병에 대해 계산된 이동률과 소진률이다.모든 국가에서 이러한 전염병에 대한 상수는 SIR 모델을 공개적으로SS 사용 가능한 데이터에 적합시킴으로써 추출할 수 있다.
모형 예방접종
SIR 모델은 백신 [33]접종 모델에 맞게 수정할 수 있습니다.전형적으로, 이들은 접종된 개인들을 위해 SIR 인V\V에 추가 구획을 도입한다.다음은 몇 가지 예입니다.
신생아 예방접종
전염성 질환이 있는 경우, 주요 업무 중 하나는 예방 조치를 통해, 가능하면 집단 예방 접종 프로그램의 확립을 통해 근절하는 것이다.신생아가 (평생 면역력을 부여하는 백신을 사용하여) P ()({ P의 비율로 예방접종을 받는 질병을 고려해보자.
서 V V는 예방접종 대상자의 클래스입니다.즉시 다음 사항을 제시합니다.
따라서S(\ S와 I I의 인 동작에 대해 다음과 같이 설명합니다.
바꿔 말하면, 만약
예방접종 프로그램은 예방접종을 하지 않은 경우보다 낮은 수준이지만, 오히려 풍토병인 채로 남아있을 것이다.이는 수학모델이 기본 번식수가 18개인 질병은 최소 94.4%의 신생아에게 예방접종을 해야 근절을 할 수 있다는 것을 의미한다.
예방접종 및 정보
현대 사회는 "합리적" 면제의 도전에 직면해 있다. 즉, 감염으로 인한 인식된 위험과 백신으로 인한 손상 사이의 "합리적" 비교의 결과로 아이들에게 예방접종을 하지 않기로 한 가족의 결정이다.이러한 행동이 정말로 합리적인지, 즉 질병의 근절을 동등하게 이끌 수 있는지 평가하기 위해, 백신 접종률이 감염 피험자 수의 증가 함수라고 간단히 가정할 수 있다.
이 경우 제거 조건은 다음과 같습니다.
즉, 기준 예방접종률은 면제 시 유지할 수 없는 "예방접종" 임계값보다 커야 한다.따라서 "합리적" 면제는 높은 백신 커버리지로 인한 현재의 낮은 발병률에 기초하고 대신 커버리지 감소로 인한 향후 감염의 재발을 고려하기 때문에 근시안적일 수 있다.
비신생아 예방접종
②비신생아 예방접종이 있는 경우, 민감성 및 예방접종 대상자에 대한 등식은 다음과 같이 수정해야 한다.
다음과 같은 제거 조건이 발생합니다.
맥박 예방접종 전략
이 전략은 시간이 지남에 따라 민감한 모집단에서 정의된 연령 코호트(어린이나 노인 등)를 반복적으로 예방접종한다.이 전략을 사용하여 민감한 개인의 블록을 즉시 제거하여 전체 인구에서 감염성 질병(홍역 등)을 제거할 수 있습니다.T 시간 단위마다 민감 피험자의 일정 부분 p가 비교적 짧은 시간(질환의 역학 관계와 관련하여)에 백신 접종을 받는다.이로 인해 민감하고 예방접종된 피험자에 대해 다음과 같은 충동 미분 방정식이 도출된다.
I = 0으로 설정하면 민감 피험자의 역학이 다음과 같이 주어지는 것을 쉽게 알 수 있다.
제거 조건은 다음과 같습니다.
연령의 영향: 연령 구조 모델
연령은 인구의 질병 확산률, 특히 접촉률에 깊은 영향을 미친다.이 비율은 민감 피험자와 감염 피험자 간의 접촉 효과를 요약한 것입니다.유행성 s( ,) , ( ,) , ( ,t ) , r ( t , s , , ( , ) , r ( a ) display style s ( t , a ) ) ( s (감염성-감염성-감염성-감염성-제거) 스킴으로 한정합니다.
(서 M + { _ { M } \ + \ 는 최대 허용 연령이며, 이들의 역학은 "단순한" 편미분 방정식으로 기술되지 않고, 인테그로-미분 방정식으로 기술된다.
여기서:
감염력은 물론 연령 간의 상호작용에 따라 접촉 k ( , 1; k (a , _ {1 ; 이(가) 표시되지만, 이는 물론 의존합니다.
신생아(즉, a=0)에 대한 초기 조건에 따라 복잡성이 추가되며, 감염 및 제거는 간단하다.
하지만 민감한 신생아의 밀도에 대해서는 지역적이지 않습니다.
여기서 j () , , , \ 은 성인의 가성입니다.
총 n ( , ) ( ,) + ( , a) + ( ,) =( ) +( t , a( , a )의 밀도를 정의하면 다음과 같이 됩니다.
3가지 유행병 클래스에서 동일한 가임성의 가장 단순한 경우, 인구통계학적 평형을 유지하기 위해서는 다음과 같은 필요충분조건이 존재해야 ( .)\ \ (. )와 μ ( ) \ (a )를 연결되어야 한다.
인구통계학적 균형은
무병 솔루션의 존재를 자동적으로 보증합니다.
기본 재생수는 적절한 기능 연산자의 스펙트럼 반지름으로서 산출할 수 있다.
부문별 전염병 모델 내 기타 고려사항
수직 변속기
에이즈나 B형 간염 등 일부 질환의 경우 감염된 부모의 자녀들이 감염으로 태어날 수 있다.이 병이 어머니로부터 전염되는 것을 수직 전염이라고 합니다.감염된 [34]구획에 신생아 구성원의 일부를 포함시킴으로써 감염 범주에 추가 구성원의 유입을 모델 내에서 고려할 수 있다.
벡터 전송
사람에게서 사람에게 간접적으로 전염되는 질병, 즉 모기를 통해 전파되는 말라리아가 벡터를 통해 전염된다.이러한 경우, 사람에서 곤충으로의 감염과 유행 모델은 두 종 모두를 포함해야 하며, 일반적으로 직접 [34][35]전염을 위한 모델보다 훨씬 더 많은 구획을 필요로 한다.
다른이들
전염병을 모델링할 때 고려해야 할 다른 사건으로는 다음과 [34]같은 것들이 있습니다.
- 비균질 혼합
- 가변 감염성
- 공간적으로 균일하지 않은 분포
- 대식충에 의한 질병
결정론적 대 확률적 유행병 모델
여기에 제시된 결정론적 모델은 충분히 많은 모집단의 경우에만 유효하며,[36] 따라서 신중하게 사용해야 한다는 점을 강조하는 것이 중요하다.
더 정확히 말하면, 이러한 모형은 모집단이 사실상 무한대인 열역학 한계에서만 유효합니다.확률적 모델에서, 위에서 도출된 장기 풍토균형은, 감염된 개인의 수가 시스템에서 하나 이하로 떨어질 유한한 확률이 있기 때문에 유지되지 않는다.실제 시스템에서는 호스트가 감염되지 않기 때문에 병원체가 전파되지 않을 수 있습니다.그러나 결정론적 평균 필드 모델에서는 감염된 호스트의 정수 이외의 값을 실제로 취할 수 있으며, 모델 내의 호스트 수는 1개 미만일 수 있지만 0개 이상일 수 있으므로 모델 내의 병원체가 전파될 수 있습니다.부문별 모델의 신뢰성은 부문별 애플리케이션에 한정됩니다.
평균장 모델의 가능한 확장 중 하나는 침투 이론 [30]개념에 기초한 네트워크에서의 전염병 확산을 고려합니다.확률적 전염병 모델은 다른[37][38][39] 네트워크에서 연구되었으며 최근에는 COVID-19 [40]대유행에 적용되었다.
「 」를 참조해 주세요.
레퍼런스
- ^ Ross R (1 February 1916). "An application of the theory of probabilities to the study of a priori pathometry.—Part I". Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character. 92 (638): 204–230. Bibcode:1916RSPSA..92..204R. doi:10.1098/rspa.1916.0007.
- ^ Ross R, Hudson H (3 May 1917). "An application of the theory of probabilities to the study of a priori pathometry.—Part II". Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character. 93 (650): 212–225. Bibcode:1917RSPSA..93..212R. doi:10.1098/rspa.1917.0014.
- ^ Ross R, Hudson H (1917). "An application of the theory of probabilities to the study of a priori pathometry.—Part III". Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character. 89 (621): 225–240. Bibcode:1917RSPSA..93..225R. doi:10.1098/rspa.1917.0015.
- ^ a b c d Kermack WO, McKendrick AG (1927). "A Contribution to the Mathematical Theory of Epidemics". Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character. 115 (772): 700–721. Bibcode:1927RSPSA.115..700K. doi:10.1098/rspa.1927.0118.
- ^ a b Kendall DG (1956). "Deterministic and stochastic epidemics in closed populations". Proceedings of the Third Berkeley Symposium on Mathematical Statistics and Probability: Contributions to Biology and Problems of Health. 4: 149–165. doi:10.1525/9780520350717-011. ISBN 9780520350717. MR 0084936. Zbl 0070.15101.
- ^ a b c Harko T, Lobo FS, Mak MK (2014). "Exact analytical solutions of the Susceptible-Infected-Recovered (SIR) epidemic model and of the SIR model with equal death and birth rates". Applied Mathematics and Computation. 236: 184–194. arXiv:1403.2160. Bibcode:2014arXiv1403.2160H. doi:10.1016/j.amc.2014.03.030. S2CID 14509477.
- ^ a b c Beckley R, Weatherspoon C, Alexander M, Chandler M, Johnson A, Bhatt GS (2013). "Modeling epidemics with differential equations" (PDF). Tennessee State University Internal Report. Retrieved July 19, 2020.
- ^ a b c d e Kröger M, Schlickeiser R (2020). "Analytical solution of the SIR-model for the temporal evolution of epidemics. Part A: Time-independent reproduction factor". Journal of Physics A. 53 (50): 505601. Bibcode:2020JPhA...53X5601K. doi:10.1088/1751-8121/abc65d. S2CID 225555567.
- ^ a b Schlickeiser R, Kröger M (2021). "Analytical solution of the SIR-model for the temporal evolution of epidemics. Part B: Semi-time case". Journal of Physics A. 54 (17): 175601. Bibcode:2021JPhA...54X5601S. doi:10.1088/1751-8121/abed66.
- ^ a b Yang W, Zhang D, Peng L, Zhuge C, Hong L (2020). "Rational evaluation of various epidemic models based on the COVID-19 data of China". arXiv:2003.05666v1 [q-bio.PE].
- ^ Krylova O, Earn DJ (July 2013). "Effects of the infectious period distribution on predicted transitions in childhood disease dynamics". Journal of the Royal Society, Interface. 10 (84): 20130098. doi:10.1098/rsif.2013.0098. PMC 3673147. PMID 23676892.
- ^ Hethcote H (2000). "The Mathematics of Infectious Diseases". SIAM Review. 42 (4): 599–653. Bibcode:2000SIAMR..42..599H. doi:10.1137/s0036144500371907.
- ^ a b Bailey, Norman T. J. (1975). The mathematical theory of infectious diseases and its applications (2nd ed.). London: Griffin. ISBN 0-85264-231-8.
- ^ Sonia Altizer; Nunn, Charles (2006). Infectious diseases in primates: behavior, ecology and evolution. Oxford Series in Ecology and Evolution. Oxford [Oxfordshire]: Oxford University Press. ISBN 0-19-856585-2.
- ^ Wolfram Research, Inc. "Mathematica, Version 12.1". Champaign IL, 2020.
- ^ Capasso V (1993). Mathematical Structure of Epidemic Systems. Berlin: Springer. ISBN 3-540-56526-4.
- ^ Miller JC (September 2012). "A note on the derivation of epidemic final sizes". Bulletin of Mathematical Biology. 74 (9): 2125–2141. doi:10.1007/s11538-012-9749-6. PMC 3506030. PMID 22829179.
Section 4.1
- ^ Miller JC (February 2017). "Mathematical models of SIR disease spread with combined non-sexual and sexual transmission routes". Infectious Disease Modelling. 2 (1): 35–55. doi:10.1016/j.idm.2016.12.003. PMC 5963332. PMID 29928728.
Section 2.1.3
- ^ Hart KD, Thompson C, Burger C, Hardwick D, Michaud AH, Al Bulushi AH, et al. (November 2021). "Remote Learning of COVID-19 Kinetic Analysis in a Physical Chemistry Laboratory Class". ACS Omega. 6 (43): 29223–29232. doi:10.1021/acsomega.1c04842. PMC 8547164. PMID 34723043.
- ^ Padua RN, Tulang AB (2 December 2010). "A Density–Dependent Epidemiological Model for the Spread of Infectious Diseases". Liceo Journal of Higher Education Research. 6 (2). doi:10.7828/ljher.v6i2.62.
- ^ May RM, Anderson B (1992-09-24). Infectious Diseases of Humans: Dynamics and Control (Revised ed.). Oxford: Oxford University Press. ISBN 9780198540403.
- ^ Hethcote HW (1989). "Three Basic Epidemiological Models". In Levin SA, Hallam TG, Gross LJ (eds.). Applied Mathematical Ecology. Biomathematics. Vol. 18. Berlin: Springer. pp. 119–144. doi:10.1007/978-3-642-61317-3_5. ISBN 3-540-19465-7.
- ^ (p.19) SI 모델
- ^ 첫 번째 및 두 번째 미분 방정식은 변환되어 위의 SIR 모델과 동일한 형태로 제공됩니다.
- ^ a b c Schlickeiser R, Kröger M (2021). "Analytical Modeling of the Temporal Evolution of Epidemics Outbreaks Accounting for Vaccinations". Physics. 3 (2): 386. Bibcode:2021Physi...3..386S. doi:10.3390/physics3020028. S2CID 233589998.
- ^ a b Hunziker P (2021-07-24). "Personalized-dose Covid-19 vaccination in a wave of virus Variants of Concern: Trading individual efficacy for societal benefit". Precision Nanomedicine. 4 (3): 805–820. doi:10.33218/001c.26101.
- ^ Noble JV (August 1974). "Geographic and temporal development of plagues". Nature. 250 (5469): 726–729. Bibcode:1974Natur.250..726N. doi:10.1038/250726a0. PMID 4606583. S2CID 4210869.
- ^ Te Vrugt M, Bickmann J, Wittkowski R (November 2020). "Effects of social distancing and isolation on epidemic spreading modeled via dynamical density functional theory". Nature Communications. 11 (1): 5576. arXiv:2003.13967. Bibcode:2020NatCo..11.5576T. doi:10.1038/s41467-020-19024-0. PMC 7643184. PMID 33149128.
- ^ Hunziker P (2021-03-07). "Vaccination strategies for minimizing loss of life in Covid-19 in a Europe lacking vaccines". medRxiv: 2021.01.29.21250747. doi:10.1101/2021.01.29.21250747. S2CID 231729268.
- ^ a b Croccolo F, Roman HE (October 2020). "Spreading of infections on random graphs: A percolation-type model for COVID-19". Chaos, Solitons, and Fractals. 139: 110077. arXiv:2006.10490. Bibcode:2020CSF...13910077C. doi:10.1016/j.chaos.2020.110077. PMC 7332959. PMID 32834619. S2CID 219792089.
- ^ a b Kastalskiy, IA; Pankratova, EV; Mirkes, EM; et al. (2021). "Social stress drives the multi-wave dynamics of COVID-19 outbreaks". Scientific Reports. 11 (1): 22497. arXiv:2106.08966. doi:10.1038/s41598-021-01317-z. PMC 8602246. PMID 34795311.
- ^ COVID-19 데이터 저장소. Johns Hopkins University(JHU)의 시스템 과학 및 엔지니어링 센터(CSE). 전처리된 데이터는 World in Data 프로젝트입니다.
- ^ Gao S, Teng Z, Nieto JJ, Torres A (2007). "Analysis of an SIR epidemic model with pulse vaccination and distributed time delay". Journal of Biomedicine & Biotechnology. 2007: 64870. doi:10.1155/2007/64870. PMC 2217597. PMID 18322563.
- ^ a b c Brauer F, Castillo-Chávez C (2001). Mathematical Models in Population Biology and Epidemiology. NY: Springer. ISBN 0-387-98902-1.
- ^ 이런 유형의 모델에 대한 자세한 내용은 를 참조하십시오.
- ^ Bartlett MS (1957). "Measles periodicity and community size". Journal of the Royal Statistical Society, Series A. 120 (1): 48–70. doi:10.2307/2342553. JSTOR 2342553. S2CID 91114210.
- ^ May RM, Lloyd AL (December 2001). "Infection dynamics on scale-free networks". Physical Review E. 64 (6 Pt 2): 066112. Bibcode:2001PhRvE..64f6112M. doi:10.1103/PhysRevE.64.066112. PMID 11736241.
- ^ Pastor-Satorras R, Vespignani A (April 2001). "Epidemic spreading in scale-free networks". Physical Review Letters. 86 (14): 3200–3203. arXiv:cond-mat/0010317. Bibcode:2001PhRvL..86.3200P. doi:10.1103/PhysRevLett.86.3200. hdl:2117/126209. PMID 11290142. S2CID 16298768.
- ^ Newman ME (July 2002). "Spread of epidemic disease on networks". Physical Review E. 66 (1 Pt 2): 016128. arXiv:cond-mat/0205009. Bibcode:2002PhRvE..66a6128N. doi:10.1103/PhysRevE.66.016128. PMID 12241447. S2CID 15291065.
- ^ Wong F, Collins JJ (November 2020). "Evidence that coronavirus superspreading is fat-tailed". Proceedings of the National Academy of Sciences of the United States of America. 117 (47): 29416–29418. Bibcode:2020PNAS..11729416W. doi:10.1073/pnas.2018490117. PMC 7703634. PMID 33139561. S2CID 226242440.
추가 정보
- May RM, Anderson RM (1991). Infectious diseases of humans: dynamics and control. Oxford: Oxford University Press. ISBN 0-19-854040-X.
- Vynnycky E, White RG, eds. (2010). An Introduction to Infectious Disease Modelling. Oxford: Oxford University Press. ISBN 978-0-19-856576-5.
- Capasso V (2008). Mathematical Structures of Epidemic Systems. 2nd Printing. Heidelberg: Springer. ISBN 978-3-540-56526-0.
외부 링크
- SIR 모델:JSXGraph를 사용한 온라인 실험
- "Simulating an epidemic". 3Blue1Brown. March 27, 2020 – via YouTube.


![{\displaystyle \left\{{\begin{aligned}&{\frac {dS}{dt}}=-{\frac {\beta IS}{N}},\\[6pt]&{\frac {dI}{dt}}={\frac {\beta IS}{N}}-\gamma I,\\[6pt]&{\frac {dR}{dt}}=\gamma I,\end{aligned}}\right.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c2a8fd2e93bfcf1092a44cfec7ef32c1a80a26f4)

 취약인구의 주식
취약인구의 주식 제거인구의 주식, N(\
제거인구의 주식, N(\


































![{\displaystyle {\begin{aligned}S(t)&=S(0)e^{-\xi (t)}\\[8pt]I(t)&=N-S(t)-R(t)\\[8pt]R(t)&=R(0)+\rho \xi (t)\\[8pt]\xi (t)&={\frac {\beta }{N}}\int _{0}^{t}I(t^{*})\,dt^{*}\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6f6ac0eda5b1278f31690939cdfa1f4daa6b1762)






 R
R 단순히 선형으로 관련되어 있음을 나타냅니다.
단순히 선형으로 관련되어 있음을 나타냅니다.  둘 다 임의입니다.반시간 SIR
둘 다 임의입니다.반시간 SIR 


![{\displaystyle {\begin{aligned}{\frac {dS}{dt}}&=\Lambda -\mu S-{\frac {\beta IS}{N}}\\[8pt]{\frac {dI}{dt}}&={\frac {\beta IS}{N}}-\gamma I-\mu I\\[8pt]{\frac {dR}{dt}}&=\gamma I-\mu R\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0dad81f67db0f075bec720950feaeeb653916028)




 전적으로 민감한 모집단에서 단일 감염 대상자에 의해 발생한 평균 감염 수로 해석될 수 있으며, 위의 관계는 생물학적으로 이 수치가 1 이하이거나 같은 경우, 반면 이 수치가 gr이면 멸종됨을 의미한다.그 질병은 인구에서 영구히 풍토병이 될 것이다.
전적으로 민감한 모집단에서 단일 감염 대상자에 의해 발생한 평균 감염 수로 해석될 수 있으며, 위의 관계는 생물학적으로 이 수치가 1 이하이거나 같은 경우, 반면 이 수치가 gr이면 멸종됨을 의미한다.그 질병은 인구에서 영구히 풍토병이 될 것이다. 









 사용하여 N {
사용하여 N {









 감염될 수 있다.따라서 모든 감염자가
감염될 수 있다.따라서 모든 감염자가 


![{\displaystyle \operatorname {E} [\min(T_{L}\mid T_{S})]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c4a1be62e9d674a94ab536644fa3f56c77503cdf)

![{\displaystyle \operatorname {E} [\min(T_{L}\mid T_{S})]=\int _{0}^{\infty }e^{-(\mu +\delta )x}\,dx={\frac {1}{\mu +\delta }},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6cd0d8220231a82d54da2c2e818ee2b426c23e62)
 진입하는 인원의 수가 되어야 한다.
진입하는 인원의 수가 되어야 한다.




![{\displaystyle {\begin{aligned}{\frac {dS}{dt}}&=-{\frac {\beta SI}{N}}+\gamma I\\[6pt]{\frac {dI}{dt}}&={\frac {\beta SI}{N}}-\gamma I\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/605895c64d824511c45ba20ba151ce5b1cec12fc)



![{\displaystyle {\begin{aligned}&{\frac {\beta }{\gamma }}\leq 1\Rightarrow \lim _{t\to +\infty }I(t)=0,\\[6pt]&{\frac {\beta }{\gamma }}>1\Rightarrow \lim _{t\to +\infty }I(t)=\left(1-{\frac {\gamma }{\beta }}\right)N.\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/05a8022e25ade4141cdf7a411b25dbb8abfc66b9)



 풍토성 감염 집단이고,
풍토성 감염 집단이고, 








![{\displaystyle {\begin{aligned}&{\frac {dS}{dt}}=-{\frac {\beta IS}{N}},\\[6pt]&{\frac {dI}{dt}}={\frac {\beta IS}{N}}-\gamma I-\mu I,\\[6pt]&{\frac {dR}{dt}}=\gamma I,\\[6pt]&{\frac {dD}{dt}}=\mu I,\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1211c5146940bacb8a0df97780330a2599eb4625)

![{\displaystyle {\begin{aligned}&{\frac {dS}{dt}}=-{\frac {\beta (t)IS}{N}}-v(t)S,\\[6pt]&{\frac {dI}{dt}}={\frac {\beta (t)IS}{N}}-\gamma (t)I,\\[6pt]&{\frac {dR}{dt}}=\gamma (t)I,\\[6pt]&{\frac {dV}{dt}}=v(t)S,\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/15bce40926efffe7fce767afe2ead314829ff41c)
 각각 감염률, 회복률, 예방접종률이다.반시간 초기
각각 감염률, 회복률, 예방접종률이다.반시간 초기 




![{\displaystyle {\begin{aligned}{\frac {dM}{dt}}&=\Lambda -\delta M-\mu M\\[8pt]{\frac {dS}{dt}}&=\delta M-{\frac {\beta SI}{N}}-\mu S\\[8pt]{\frac {dI}{dt}}&={\frac {\beta SI}{N}}-\gamma I-\mu I\\[8pt]{\frac {dR}{dt}}&=\gamma I-\mu R\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f5a17da090fac7ceb0999445ceb4b217e575c524)




![{\displaystyle {\begin{aligned}{\frac {dS}{dt}}&=\mu N-\mu S-{\frac {\beta IS}{N}}\\[8pt]{\frac {dE}{dt}}&={\frac {\beta IS}{N}}-(\mu +a)E\\[8pt]{\frac {dI}{dt}}&=aE-(\gamma +\mu )I\\[8pt]{\frac {dR}{dt}}&=\gamma I-\mu R.\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3da10d1a165eef9e341aae30f70418730fbfa6e5)


![\left(S(0),E(0),I(0),R(0)\right)\in \left\{(S,E,I,R)\in [0,N]^{4}:S\geq 0,E\geq 0,I\geq 0,R\geq 0,S+E+I+R=N\right\}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3190cc59889dab0e9167d4241c117e8a2cefe0e0)


 경우 DFE의 글로벌 매력 조건은 다음과 같은 주기 계수를 갖는 선형 시스템이다.
경우 DFE의 글로벌 매력 조건은 다음과 같은 주기 계수를 갖는 선형 시스템이다.![{\displaystyle {\begin{aligned}{\frac {dE_{1}}{dt}}&=\beta (t)I_{1}-(\gamma +a)E_{1}\\[8pt]{\frac {dI_{1}}{dt}}&=aE_{1}-(\gamma +\mu )I_{1}\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e4e137f34047a193685ff0b616c6f86e702f677b)

![{\displaystyle {\begin{aligned}{\frac {dS}{dt}}&=\Lambda -{\frac {\beta SI}{N}}-\mu S+\gamma I\\[6pt]{\frac {dE}{dt}}&={\frac {\beta SI}{N}}-(\epsilon +\mu )E\\[6pt]{\frac {dI}{dt}}&=\varepsilon E-(\gamma +\mu )I\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c285f849fed79fdc4a6ef0798104d773cda7510a)

![{\displaystyle {\begin{aligned}{\frac {dM}{dt}}&=\Lambda -\delta M-\mu M\\[6pt]{\frac {dS}{dt}}&=\delta M-{\frac {\beta SI}{N}}-\mu S\\[6pt]{\frac {dE}{dt}}&={\frac {\beta SI}{N}}-(\varepsilon +\mu )E\\[6pt]{\frac {dI}{dt}}&=\varepsilon E-(\gamma +\mu )I\\[6pt]{\frac {dR}{dt}}&=\gamma I-\mu R\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/893a707bc8c2fec6f5ecd6cb93a46ab0652252c2)


![{\displaystyle {\begin{aligned}{\frac {dS}{dt}}&=\mu N-\mu S-\beta (t){\frac {I}{N}}S\\[8pt]{\frac {dI}{dt}}&=\beta (t){\frac {I}{N}}S-(\gamma +\mu )I\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6fc5024950a3e4b440788219d6c97f29cab91895)


![{\displaystyle {\begin{aligned}&\partial _{t}S=D_{S}\nabla ^{2}S-{\frac {\beta IS}{N}},\\[6pt]&\partial _{t}I=D_{I}\nabla ^{2}I+{\frac {\beta IS}{N}}-\gamma I,\\[6pt]&\partial _{t}R=D_{R}\nabla ^{2}R+\gamma I,\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2ff4604a302c4b9d30ea91a042665061ab969e00)


 확산 상수입니다.이것에 의해, 반응 확산 방정식을 얻을 수 있다.(치수를 위해
확산 상수입니다.이것에 의해, 반응 확산 방정식을 얻을 수 있다.(치수를 위해 

![{\displaystyle {\begin{aligned}{\frac {dS}{dt}}&=\nu N(1-P)-\mu S-\beta {\frac {I}{N}}S\\[8pt]{\frac {dI}{dt}}&=\beta {\frac {I}{N}}S-(\mu +\gamma )I\\[8pt]{\frac {dV}{dt}}&=\nu NP-\mu V\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/63771aa3a5908cf37d4614cbdc9d655f2d734f10)






![{\displaystyle {\begin{aligned}{\frac {dS}{dt}}&=\mu N(1-P)-\mu S-\rho S-\beta {\frac {I}{N}}S\\[8pt]{\frac {dV}{dt}}&=\mu NP+\rho S-\mu V\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b556735b37a851da6eeffe357d39ef0e64a20187)

![{\displaystyle {\begin{aligned}{\frac {dS}{dt}}&=\mu N-\mu S-\beta {\frac {I}{N}}S,\quad S(nT^{+})=(1-p)S(nT^{-}),&&n=0,1,2,\ldots \\[8pt]{\frac {dV}{dt}}&=-\mu V,\quad V(nT^{+})=V(nT^{-})+pS(nT^{-}),&&n=0,1,2,\ldots \end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fa20fd9c5facbd652241be938c9ac9fb3dae0204)






 최대 허용 연령이며, 이들의 역학은 "단순한" 편미분 방정식으로 기술되지 않고,
최대 허용 연령이며, 이들의 역학은 "단순한" 편미분 방정식으로 기술되지 않고, 



 (가) 표시되지만, 이는 물론 의존합니다.
(가) 표시되지만, 이는 물론 의존합니다. 











