헬라
HeLa

Hela(/ˈhiɑlː//; 또한 Hela 또는 Hela)는 과학 연구에서 사용되는 불멸의 세포주이다.그것은 가장 오래되고 가장 일반적으로 사용되는 인간 [1]세포주이다.이 라인은 1951년 [3]10월 4일 암으로 사망한 5명의 자녀를 둔 31세의 흑인 어머니 헨리에타 랙스에게서 1951년 [2]2월 8일 채취된 자궁경부암 세포의 이름을 따왔다.이 세포주는 놀라울 정도로 내구성이 높고 다산성이 있는 것으로 밝혀져 과학 [4][5]연구에 광범위하게 사용될 수 있다.
랙스의 암 자궁경부종양에서 나온 세포들은 그녀 몰래 또는 동의 없이 채취되었는데, 이것은 그 [6]당시 미국에서 흔한 관행이었다.세포생물학자 조지 오토 가이는 그들이 [7]살아있을 수 있다는 것을 발견하고 세포주를 개발했다.이전에, 다른 인간 세포로부터 배양된 세포들은 며칠 동안만 살아남을 수 있었다.랙스의 종양에서 나온 세포들은 다르게 행동했어요
역사
기원.
1951년, 헨리에타 랙스라는 이름의 환자가 불규칙한 질 출혈 증상으로 존스 홉킨스 병원에 입원했고, 이후 자궁경부암으로 치료를 [8]받았다.그녀의 첫 번째 치료는 로렌스 와튼 주니어에 의해 이루어졌는데, 그는 그녀의 동의 [9]없이 자궁경부로부터 조직 샘플을 채취했다.그녀의 자궁경부 생검에서는 다른 수술 절차와 마찬가지로 임상 평가와 조직 배양 연구소의 책임자인 조지 오토 게이가 연구하기 위한 조직 샘플을 제공했습니다.Gey의 실험실 조수 Mary Kubicek은 세포를 [8]배양하기 위해 롤러 튜브 기술을 사용했다.세포는 급격히 성장하여 소멸된 [10]이전 표본과 달리 20-24시간마다 두 배씩 증가하는 것으로 관찰되었다.
이 세포들은 1951년 랙스가 암으로 사망하기 직전에 가이에 의해 증식되었다.이것은 체외에서 성공적인 것을 증명한 최초의 인간 세포주였고, 이것은 의학 연구에 큰 미래 이익을 가져다주는 과학적 성과였다.Gey는 단순히 과학의 이익을 위해 세포를 요청하는 과학자들에게 그의 연구실에서 개발한 도구와 과정과 함께 자유롭게 이 세포들을 기증했다.랙스도 그녀의 가족도 그 세포들을 채취하는 것을 허락하지 않았지만, 그 당시에는 허가도 요구되지 않았고 관례적으로 [11]요구하지도 않았다.그 세포들은 원래 형태로 특허를 받은 적은 없지만 나중에 상업화 되었다.수술, 진단, 치료 과정에서 얻은 폐기물 또는 폐기물은 의사 또는 의료기관의 재산이기 때문에 당시에는 환자나 그 친족에게 알릴 필요가 없었다.
게이의 실험실 조교 관습처럼, 그 문화는 헨리에타 랙스의 이름과 [8]성의 처음 두 글자를 따서 명명되었다.1970년대에 그녀의 실명이 공개되기 전에, "Hela" 세포주는 "Helen Lane" 또는 "Helen Larson"[5][12]의 이름을 딴 것으로 잘못 생각되었다.
다른 세포 배양은 의심받는 Hela 세포에 의해 침입당하고 있었기 때문에, 한 연구 그룹은 오염된 세포주를 식별하는 것을 돕기 위해 DNA 샘플을 찾기 위해 랙스 가족에게 연락했다.가족들은 방문의 목적을 전혀 이해하지 못했지만, 연구원들이 그들에게 [12][13]말한 것에 대한 이해로 인해 괴로워했다.이 세포들은 Lacks의 [14]암 진단의 일환으로 자궁경부에 있는 눈에 보이는 병변에서 채취한 조직검사의 후손이기 때문에 암세포로 취급된다.
다른 세포주와 마찬가지로, Hela 세포는 기본적인 세포 생존 조건(적절한 환경에서 유지되고 유지되는 것)이 충족되는 한 실험실 세포 배양 접시에서 무제한으로 분할할 수 있다는 점에서 "불멸"이라고 불립니다.Hela 세포는 세포 배양에서 계속 변이하기 때문에 많은 변종이 있지만, 모든 Hela 세포는 Lacks에서 제거된 동일한 종양 세포로부터 파생됩니다.세포배양에서 증식된 헬라세포의 총수는 헨리에타 랙스의 [15]체내에 있던 총세포 수를 훨씬 웃돈다.
논란
랙스의 사례는 20세기 의학에서 정보에 입각한 동의가 결여된 많은 사례 중 하나이다.조직 공여자와 의사 사이의 의사소통은 사실상 존재하지 않았다(즉, 환자의 동의 없이 세포를 채취했고, 세포가 무엇에 사용될지도 말하지 않았다).존 홉킨스 병원은 볼티모어 지역에서 흑인 환자가 무료로 진료를 받을 수 있는 유일한 병원이었다.이 병원의 격리된 종단에서 무료 진료를 받는 환자들은 종종 자신도 [16]모르는 사이에 연구 대상이 되었다.랙스의 가족은 또한 그녀의 환자 파일에 접근할 수 없었고 누가 헬라 세포를 제공받았는지, 어떤 용도로 사용될지에 대한 발언권이 없었다.게다가 Hela 세포가 보급되어 과학계 전체에서 더 자주 사용됨에 따라, Lacks의 친척들은 재정적인 혜택을 받지 못하고 의료 서비스에 [17][12]대한 제한된 접근으로 계속 살고 있었습니다.
연구를 위해 채취한 조직 샘플을 누가 소유하느냐에 대한 이 문제는 캘리포니아 대학의 무어 대 레전츠 대법원에서 제기되었습니다.폐기된 조직과 세포는 그 사람의 소유물이 아니며 [18]상업화될 수 있다고 법원이 판결했다.
랙스의 사례는 1981년 공통규칙 제정에 영향을 미쳤다.통칙은 의사가 환자의 사례를 연구에 사용할 계획인 경우 환자에게 알리고 세부사항을 공개할 것인지 여부를 선택할 수 있도록 함으로써 사전동의서를 시행한다.기증자의 이름과 연결된 조직도 이 규칙에 따라 엄격하게 규제되며, 샘플은 더 이상 기증자의 이니셜을 사용하지 않고 코드 번호로 [18]명명됩니다.환자의 프라이버시 문제를 더욱 해결하기 위해 존스 홉킨스는 국립보건원 및 랙스의 가족과 함께 헨리에타 랙스의 [19]게놈에 누가 접근할 수 있는지 결정하기 위한 공동 위원회를 설립했다.
2021년 헨리에타 랙스의 재산은 Thermo Fisher [20]Scientific에 의해 허가되지 않고 널리 알려진 Hela 세포 판매에 대한 과거와 미래의 지불을 받기 위해 소송을 제기했다.랙스의 가족은 변호사를 고용하여 Hela [21]세포를 사용하여 이익을 취한 100개 이상의 제약회사에 보상을 요청했습니다.
연구에 사용
헬라 세포는 1953년 테오도르 퍽과 필립 1세에 의해 성공적으로 복제된 최초의 인간 세포였다. 덴버 [22]콜로라도 대학의 마커스입니다그 이후로, Hela 세포는 "암, 에이즈, 방사선과 독성 물질의 영향, 유전자 매핑, 그리고 다른 수많은 과학적 [23]연구에 계속 사용되어 왔다."작가 레베카 스클루트에 따르면, 2009년까지, "헬라에 대한 연구에 관한 6만 개 이상의 과학 기사가 발표되었고,[18] 그 숫자는 매달 300개 이상의 논문의 속도로 꾸준히 증가하고 있다."
소아마비 퇴치
헬라 세포는 조나스 솔크에 의해 1950년대에 최초의 소아마비 백신을 테스트하기 위해 사용되었다.이들은 소아마비염에 쉽게 감염돼 감염된 세포를 [2]죽게 하는 것으로 관찰됐다.이것은 결과를 쉽게 얻을 수 있었기 때문에 Hela 세포를 소아마비 백신 테스트에 매우 유용하게 만들었다.소크의 소아마비 백신 테스트를 위해 많은 양의 Hela 세포가 필요했고, NFIP는 [24]Hela 세포를 대량 생산할 수 있는 시설을 찾게 되었다.1953년 봄, Salk와 다른 실험실에 Hela [25]세포를 공급하기 위해 Tuskegee 대학에 세포 배양 공장이 설립되었습니다.1년도 채 지나지 않아, 소크의 백신은 인간 실험을 [26]할 준비가 되었다.
바이러스학
Hela 세포는 파르보바이러스가 사람, 개, [27]고양이의 세포를 어떻게 감염시키는지를 테스트하는데 사용되어 왔다.이 세포들은 또한 OROV와 같은 바이러스를 연구하는데 사용되어 왔다.OROV는 세포들이 감염된 직후 퇴화되기 시작하는 배양 세포들의 교란을 유발하고, 아포토시스의 [28]바이러스 유도를 일으킨다.Hela 세포는 유두종 바이러스 E2와 아포토시스의 [29]발현을 연구하는데 사용되어 왔다.Hela 세포는 또한 암세포주에서의 [30]세포자멸을 유도하는 개 디스템퍼 바이러스의 능력을 연구하는데 사용되어 왔는데, 이것은 방사선과 화학요법에 [30]내성이 있는 종양세포에 대한 치료법을 개발하는 데 중요한 역할을 할 수 있다.
Hela 세포는 또한 인간 유두종 바이러스(HPV) 백신 개발에도 중요한 역할을 해왔다.1980년대에 Harald zur Hausen은 Harless의 원래 조직검사로부터 얻은 세포에 HPV-18이 포함되어 있다는 것을 발견했는데, 이것이 나중에 Henrietta Lacks를 죽인 공격적인 암의 원인이라는 것이 밝혀졌다.HPV와 자궁경부암을 연계시킨 그의 업적은 노벨상을 수상했고 자궁경부암으로 인한 사망자를 [31]70%까지 줄일 수 있는 HPV 백신의 개발을 이끌었다.
수년간, Hela 세포는 새로운 백신과 약물을 시험하고 개발하기 위해 HIV, 지카, 헤르페스, 그리고 유행성 이하선염 등 다양한 종류의 바이러스에 감염되어 왔다.리처드 액셀 박사는 CD4 단백질을 Hela 세포에 추가함으로써 HIV에 감염되어 바이러스를 [32]연구할 수 있다는 것을 발견했다.1979년 과학자들은 홍역 바이러스가 헬라 세포를[33] 감염시키면 끊임없이 변이한다는 사실을 알게 됐고 2019년에는 지카가 헬라 [34]세포에서 증식할 수 없다는 사실을 발견했다.
암
Hela 세포는 케르세틴과 같은 에스트로겐 유사 화합물과 함께 에스트라디올, 에스트로겐 수용체와 에스트로겐 수용체와 같은 성 [35]스테로이드 호르몬과 관련된 많은 암 연구에 사용되어 왔다.또한 플라보노이드와 에스트라디올이 암세포 증식에 미치는 항산화제의 영향인 Hela 세포에 대한 연구도 있었다.
2011년, HeLa 세포는 의학 진단, 시라노스틱스 개발, PDT의 도움을 통한 암 환자의 개인화된 치료, 다른 약물과 공동 투여,[36][37] 방사선 조사에서의 독특한 사용, 현재 탐색되고 있는 새로운 헵타메틴 염료 IR-808 및 기타 아날로그의 테스트에 사용되었다.Hela 세포는 광역학적 치료의 일부로서 아포토시스를 유도하기 위해 플라렌을 포함한 연구 및 세포주를 [38]이용한 시험관내 암 연구에 사용되어 왔다.또한 Hela 세포는 RNA에서 암 마커를 정의하기 위해 사용되었으며 RNAi 기반 식별 시스템 및 특정 암 세포의 [39]간섭을 확립하기 위해 사용되어 왔다.
HeLa는 2014년 C57BL/6 누드 [40]생쥐에서 종양 이종 이식 세포주로서 생존 가능한 것으로 나타났으며, 이후 플루옥세틴과 시스플라틴이 자궁경부암에 미치는 생체 내 영향을 검사하는 데 사용되었다.
유전학
1953년, Hela 세포와 잘못된 액체를 섞는 실험의 실수는 연구자들이 처음으로 Hela 세포에서 각각의 염색체를 명확하게 보고 셀 수 있게 해주었다.이 우연한 발견으로 과학자 조 힌 티오와 알버트 레반은 염색체를 [31]염색하고 세는 더 나은 기술을 개발하게 되었다.그들은 이전에 믿었던 것처럼 인간이 24쌍이 아닌 23쌍의 염색체를 가지고 있다고 정확하게 설명한 최초의 사람들이다.이것은 염색체 수와 관련된 다운 증후군과 같은 발달 장애 연구에 중요했다.
1965년, 헨리 해리스와 존 왓킨스는 Hela 세포와 생쥐 배아 세포를 융합시킴으로써 최초의 인간과 동물의 잡종을 만들었다.이것은 유전자를 특정 염색체에 매핑하는 진보를 가능하게 했고, 이는 결국 인간 게놈 [31]프로젝트로 이어질 것이다.
우주 미생물학
1960년대에 헬라 세포는 소련의 인공위성 스푸트니크 6호와 인간 우주 임무에 보내져 우주 여행이 살아있는 세포와 조직에 미치는 장기적인 영향을 알아냈다.과학자들은 [41]무중력 상태에서 헬라 세포가 훨씬 더 빨리 분열한다는 것을 발견했다.
분석.
텔로머라아제
Hela 세포주는 암 연구에 사용하기 위해 파생되었다.이 세포들은 다른 암세포에 비해 비정상적으로 빠르게 증식한다.다른 많은 [42]암세포와 마찬가지로, Hela 세포는 세포 [43]분열 중에 텔로머라아제의 활성 버전을 가지고 있으며, 텔로미어를 계속해서 복제합니다.이것에 의해, 노화와 최종적인 세포 사멸에 관련하는 텔로미어의 증분 단축을 방지할 수 있습니다.이런 방식으로, 세포들은 헤이플릭 한계를 우회하는데, 헤이플릭은 대부분의 정상 세포들이 노화되기 전에 겪을 수 있는 제한된 수의 세포 분열이다.그 결과 무한 세포 분열과 불멸이 초래됩니다.
염색체수
인간 유두종 바이러스 18(HPV18)에서 인간 자궁경부 세포로의 수평적 유전자 이동은 Hela 게놈을 만들어 냈는데, 이것은 염색체 수를 포함한 다양한 면에서 헨리에타 랙스의 게놈과 다르다.의 게놈과 다르다.Hela 세포는 암세포를 빠르게 분열시키고 있으며, 암의 형성과 세포 배양 과정에서 염색체 수는 다양했다.현재 추정치(매우 작은 조각 제외)는 "하이퍼트리플로이드 염색체 수(3n+)"로, 이는 "Hela 시그니처 [44][45][46][47]염색체"로 알려진 22-25개의 클론 이상 염색체를 가진 총 76-80개의 염색체를 의미한다.시그니처 염색체는 여러 개의 원래 염색체에서 파생될 수 있으며, 원래 번호를 기준으로 까다로운 요약 카운트를 만든다.연구자들은 또한 이러한 비정상적인 핵형이 얼마나 안정적일 [44]수 있는지에 주목했다.스펙트럼 카리오타이핑, FISH 및 기존 세포 발생 기술을 결합한 연구는 Hela 게놈이 수년간의 [44]배양 후에도 안정된 상태를 유지하고 있기 때문에 검출된 염색체 이상이 자궁경부암을 대표할 수 있고 1차 종양에 존재할 가능성이 있다는 것을 밝혀냈다.
완전한 게놈 배열
Hela 세포의[48][49] 완전한 게놈은 랙스 [50]가족 몰래 2013년 3월 11일 배열되어 발표되었다.가족들에 의해 우려가 제기되었고, 그래서 저자들은 자발적으로 시퀀스 [50]데이터에 대한 접근을 보류했다.Jay Sendure는 워싱턴 대학에서 Hela 시퀀싱 프로젝트를 이끌었으며, 2013년 3월에 출판이 승인되었지만 Lacks 가족의 사생활 문제가 [51]해결되는 동안 이 또한 보류되었습니다.2013년 8월 7일, NIH의 프란시스 콜린스 소장은 랙스 [52]가족과의 세 차례의 회의 끝에 합의된 세포주 게놈에 대한 접근 통제 정책을 발표했다.데이터 접근 위원회는 연구원이 요청한 게놈 배열에 대한 요청을 의학 연구를 위한 것이며 사용자는 향후 공유를 위해 모든 NIH가 자금을 지원하는 모든 연구원이 단일 데이터베이스에 데이터를 보관한다는 내용을 포함하는 Hela 게놈 데이터 사용 계약 조건을 준수할 것입니다.위원회는 의학, 과학, 생명윤리 분야 대표 6명과 [52]랙스 가족 2명으로 구성된다.한 인터뷰에서 콜린스는 랙스 가족이 그들에게 강요된 이 상황에 기꺼이 참여하고자 하는 의지를 칭찬했다.그는 그들과의 모든 경험을 "강력한" 것으로 묘사하면서 "과학, 과학사, 윤리적 우려"를 독특한 방식으로 [53]하나로 모았다고 말했다.
오염
Hela 세포는 조직 배양판에서의 성장에 적응하고 다른 세포주를 침범하여 경쟁하는 능력 때문에 때때로 제어하기가 어렵습니다.부적절한 유지를 통해, 그들은 같은 실험실의 다른 세포 배양물을 오염시켜 생물학적 연구를 방해하고 연구자들이 많은 결과를 무효로 선언하도록 하는 것으로 알려져 왔다.이미 확립된 세포주의 정체성이나 순도를 테스트하는 연구자가 거의 없기 때문에 다른 세포 유형 중 Hela 세포 오염의 정도는 알려지지 않았다.시험관내 세포주 중 상당 부분이 Hela 세포에 오염되어 있는 것으로 나타났다. 추정치는 10% ~ 20%이다.스탠리 가틀러(1967)와 월터 넬슨 리스(1975)는 Hela에 [24]의한 다양한 세포주 오염에 대해 최초로 발표했다.가틀러는 "세포 배양 기술의 지속적인 확장으로 종간 및 종간 오염이 모두 [8]발생할 것이 거의 확실하다"고 말했다.
Hela 세포 오염은 세계적으로 널리 퍼지고 있으며, Jonas Salk를 포함한 많은 저명한 의사, 과학자 및 연구자들의 실험실에도 영향을 미치고 있습니다.헬라 오염 문제도 냉전의 긴장에 한몫했다.구소련과 미국은 리처드 닉슨 대통령이 시작한 암과의 전쟁에서 협력하기 시작했지만 교환된 세포가 헬라에 [54]의해 오염되었다는 것을 알게 되었다.
많은 과학자와 과학 저자들은 Hela 세포 오염 문제를 해결하는 방법에 초점을 맞추기 보다는 단순히 오염 문제로서 이 문제를 계속 문서화하고 있습니다.이는 인간의 실수나 단점이 아니라 Hela의 [55]견고성, 증식성 또는 과도한 성질에 기인하는 것입니다.최근의 데이터는 교차 오염이 여전히 현대 세포 [4][56]배양에서 주요한 진행 중인 문제임을 시사한다.International Cell Line Authentication Committee(ICLAC; 국제세포줄인증위원회)는 세포줄 오식별의 많은 사례가 빠르게 성장하는 다른 세포줄에 의한 배양물의 교차 오염의 결과라고 지적합니다.이는 완전히 다른 종이나 조직에서 유래할 수 있는 오염물질의 특정 속성이 [57]조사 대상 세포주에 잘못 속할 수 있기 때문에 오염된 세포주를 사용하여 수행된 연구의 타당성에 의문을 제기한다.
새로운 종의 제안
HeLa는 진화생물학자 Leigh Van Valen에 의해 무한 복제 능력과 인간 이외의 염색체 수 때문에 Helacyton gartleri라고 불리는 새로운 종의 현대적 창조의 한 예로 묘사되었다.이 종의 이름은 유전학자 스탠리 M. 가틀러의 이름을 따서 지어졌는데, 반 발렌은 "이 [58]종의 놀라운 성공"을 발견했다고 한다.그의 특정화 주장은 다음과 같은 점에 따라 달라집니다.
- Hela 세포와 인간의 염색체 비호환성.
- Hela 세포의 생태적 틈새.
- 인간 재배자의 욕망을 훨씬 뛰어넘어 지속적이고 확장되는 능력.
- Hela는 독자적인 복제핵형을 [59]가지고 있기 때문에 하나의 종으로 정의할 수 있다.
반 발렌은 같은 [60]논문에서 헬라 세포에 대한 새로운 종을 제안했을 뿐만 아니라 새로운 과와 헬라시톤속도 제안했습니다.
하지만, 이 제안은 다른 저명한 진화생물학자나 다른 분야의 과학자들에 의해 심각하게 받아들여지지 않았다.반 발렌은 헬라가 새로운 종이라는 주장은 헬라의 핵형이 불안정하고 엄격한 조상-후예 혈통이 [61]없기 때문에 독립적인 단세포 무성 번식 종의 기준을 충족하지 못한다.
갤러리
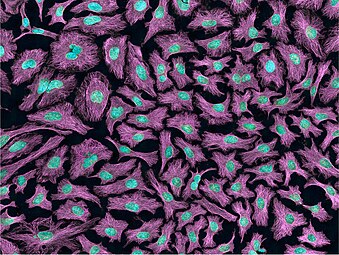
Hoechst 33258로 얼룩진 Hela 세포
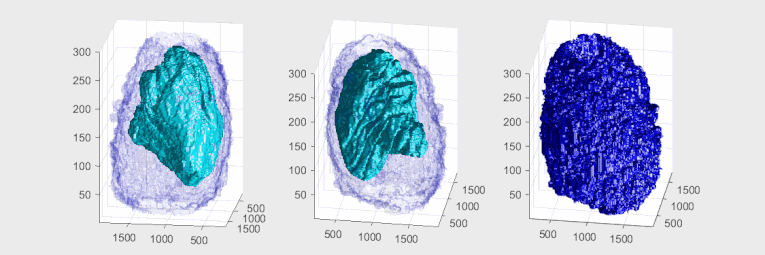
하나의 Hela 셀의 핵 엔벨로프의 부피면 렌더링(빨간색).세포는 300장의 전자현미경 검사에서 관찰되었고, 핵 외피는 자동으로 분할되어 렌더링되었다.참조용으로 수직 슬라이스와 수평 슬라이스가 각각 하나씩 추가됩니다.
미디어 내
1997년 아담 커티스의 다큐멘터리 '모든 살의 길'은 헬라의 역사와 의학 및 [62]사회에 미치는 영향에 대해 설명하고 있다.
헬라는 레베카 스클루트의 2010년 저서 '헨리에타 랙스의 불멸의 삶'의 주제로, 세포주의 역사적 맥락과 랙스 가족이 어떻게 [12]그 사용에 관여했는지를 조사했다.2017년 HBO 영화 헨리에타 랙스의 불멸의 삶은 이 책에 바탕을 두고 있다.이 영화에는 오프라 윈프리, 실비아 그레이스 크림, 록키 캐롤, 르네 엘리스 골드스베리가 헨리에타 랙스로 출연한다.작가 레베카 스클루트도 로즈 [63]번이 연기한 이 영화에서 캐릭터로 등장한다.
2010년 로앤오더 "불멸"의 에피소드는 헨리에타 랙스와 헬라 라인의 이야기를 크게 바탕으로 가상의 "NaRo"[64] 세포를 대리로 사용했다.
Hela 라인이 어떻게 탄생하게 되었는지에 대한 이야기는 팟캐스트 Radiolab의 [65]2010년 에피소드의 주제이기도 했다.
「 」를 참조해 주세요.
- 클론 전염성 암
- Moore v. Regents of California, 버려진 조직에 대한 선례가 된 사건
- 오염된 세포주 목록
- WI-38
레퍼런스
- ^ Rahbari R, Sheahan T, Modes V, Collier P, Macfarlane C, Badge RM (2009). "A novel L1 retrotransposon marker for HeLa cell line identification". BioTechniques. 46 (4): 277–284. doi:10.2144/000113089. PMC 2696096. PMID 19450234.
- ^ a b Scherer, W.F.; Syverton, J.T.; Gey, G.O. (1953). "Studies on the propagation in vitro of poliomyelitis viruses. IV. Viral multiplication in a stable strain of human malignant epithelial cells (strain HeLa) derived from an epidermoid carcinoma of the cervix". Journal of Experimental Medicine. 97 (5): 695–710. doi:10.1084/jem.97.5.695. PMC 2136303. PMID 13052828.
- ^ "Johns Hopkins Magazine -- April 2000". pages.jh.edu.
- ^ a b Capes-Davis A, Theodosopoulos G, Atkin I, Drexler HG, Kohara A, MacLeod RA, Masters JR, Nakamura Y, Reid YA, Reddel RR, Freshney RI (2010). "Check your cultures! A list of cross-contaminated or misidentified cell lines". Int. J. Cancer. 127 (1): 1–8. doi:10.1002/ijc.25242. PMID 20143388. S2CID 2929020.
- ^ a b Batts DW (2010-05-10). "Cancer cells killed Henrietta Lacks – then made her immortal". The Virginian-Pilot. pp. 1, 12–14. Archived from the original on 2016-11-25. Retrieved 2020-05-08.
- ^ Ron Claiborne; Sydney Wright, IV (2010-01-31). "How One Woman's Cells Changed Medicine". ABC World News. Retrieved 2012-08-19.
- ^ McKie, Robin (2010-04-03). "Henrietta Lacks's cells were priceless, but her family can't afford a hospital". The Guardian. London. Retrieved 18 July 2017.
- ^ a b c d Lucey, Brendan P.; Nelson-Rees, Walter A.; Hutchins, Grover M. (2009-10-21). "Henrietta Lacks, HeLa Cells, and Cell Culture Contamination". Archives of Pathology & Laboratory Medicine. 133 (9): 1463–7. doi:10.5858/133.9.1463. PMID 19722756.
- ^ Jones, Howard W. (1997-06-01). "Record of the first physician to see Henrietta Lacks at the Johns Hopkins Hospital: History of the beginning of the HeLa cell line". American Journal of Obstetrics and Gynecology. 176 (6): s227–s228. doi:10.1016/S0002-9378(97)70379-X. ISSN 0002-9378. PMID 9215212.
- ^ Butanis, Benjamin. "The Legacy of Henrietta Lacks". www.hopkinsmedicine.org. Retrieved 2020-05-07.
- ^ 워싱턴, 해리엇 "헨리에타 부족:"A Unsung Hero", Emerge Magazine, 1994년 10월
- ^ a b c d Zielinski, Sarah (2010-01-02). "Cracking the code of the human genome – Henrietta Lacks' 'immortal' cells". Smithsonian. Retrieved 2017-05-27.
- ^ White, Tracie (May 2, 2018), "Descendants of Henrietta Lacks discuss her famous cell line", Stanford Medicine News Center, retrieved 2021-12-09
- ^ del Carpio, Alexandra (April 27, 2014). "The Good, the Bad, and the HeLa". Berkeley Science Review. Archived from the original on 2017-05-23. Retrieved 2017-05-27.
- ^ Sharrer T (2006). ""HeLa" Herself". The Scientist. 20 (7): 22.
- ^ Stump, Jessica L. (2014). "Henrietta Lacks and The HeLa Cell: Rights of Patients and Responsibilities of Medical Researchers". The History Teacher. 48 (1): 127–180. ISSN 0018-2745. JSTOR 43264385.
- ^ Day, Jo Ann. "Upholding the Highest Bioethical Standards Johns Hopkins Medicine". www.hopkinsmedicine.org. Retrieved 2020-04-15.
- ^ a b c Skloot, Rebecca (2010). The Immortal Life of Henrietta Lacks. New York: Crown/Random House. ISBN 978-1-4000-5217-2.
- ^ "HeLa Cell Line Origins, Contamination, Controversy, and Cytogenetics". Retrieved 2020-04-15.
- ^ "Estate of Henrietta Lacks sues Thermo Fisher over the improper sale of her immortal cells".
- ^ "Family of Henrietta Lacks hires civil rights attorney to seek funds over famous cells". Washington Post. ISSN 0190-8286. Retrieved 2021-12-11.
- ^ Puck, T.T.; Marcus, P.I. (1955). "A rapid method for viable cell titration and clone production with Hela cells in tissue culture: The use of X-irradiated cells to supply conditioning factors". Proceedings of the National Academy of Sciences of the United States of America (published July 15, 1955). 41 (7): 432–437. Bibcode:1955PNAS...41..432P. doi:10.1073/pnas.41.7.432. PMC 528114. PMID 16589695.
- ^ Smith, Van (April 17, 2002). "Wonder Woman: The Life, Death, and Life After Death of Henrietta Lacks, Unwitting Heroine of Modern Medical Science". Baltimore City Paper. Archived from the original on August 14, 2004. Retrieved 2 March 2017.
- ^ a b Masters, John R. (2002). "HeLa cells 50 years on: The good, the bad and the ugly". Nature Reviews Cancer. 2 (4): 315–319. doi:10.1038/nrc775. PMID 12001993. S2CID 991019.
- ^ Turner, Timothy (2012). "Development of the Polio Vaccine: A Historical Perspective of Tuskegee University's Role in Mass Production and Distribution of HeLa Cells". Journal of Health Care for the Poor and Underserved. 23 (4a): 5–10. doi:10.1353/hpu.2012.0151. PMC 4458465. PMID 23124495.
- ^ Brownlee, K. A. (1955). "Statistics of the 1954 Polio Vaccine Trials*". Journal of the American Statistical Association. 50 (272): 1005–1013. doi:10.1080/01621459.1955.10501286.
- ^ Parker, J; Murphy W; Wang D; O'Brien S; Parrish C (2001). "Canine and feline parvoviruses can use human or feline transferrin receptors to bind, enter, and infect cells". Journal of Virology. 75 (8): 3896–3902. doi:10.1128/JVI.75.8.3896-3902.2001. PMC 114880. PMID 11264378.
- ^ Acrani, G.O.; Gomes, R.; Proença-Módena, J.L.; da Silva, A.F.; Carminati, P.O.; Silva, M.L.; Santos, R.I.; Arruda, E. (2010). "Apoptosis induced by Oropouche virus infection in HeLa cells is dependent on virus protein expression". Virus Research. 149 (1): 56–63. doi:10.1016/j.virusres.2009.12.013. PMID 20080135.
- ^ Hou, S.Y.; Wu, S.; Chiang, C. (2002). "Transcriptional activity among high and low risk human papillomavirus E2 proteins correlates with E2 DNA binding". The Journal of Biological Chemistry. 277 (47): 45619–45629. doi:10.1074/jbc.M206829200. PMID 12239214. S2CID 9203953.
- ^ a b del Puerto, H.L.; Martins, A.S.; Milsted, A.; Souza-Fagundes, E.M.; Braz, G.F.; Hissa, B.; Andrade, L.O.; Alves, F.; Rajão, D.S.; Leite, R.C.; Vasconcelos, A.C. (2011). "Canine distemper virus induces apoptosis in cervical tumor derived cell lines". Virol. J. 8 (1): 334. doi:10.1186/1743-422X-8-334. PMC 3141686. PMID 21718481.
- ^ a b c "5 Contributions HeLa Cells Have Made to Science". Cell Science from Technology Networks. Retrieved 2020-03-25.
- ^ Mondor, Isabelle; Ugolini, Sophie; Sattentau, Quentin J. (1998-05-01). "Human Immunodeficiency Virus Type 1 Attachment to HeLa CD4 Cells Is CD4 Independent and gp120 Dependent and Requires Cell Surface Heparans". Journal of Virology. 72 (5): 3623–3634. doi:10.1128/jvi.72.5.3623-3634.1998. ISSN 1098-5514. PMC 109583. PMID 9557643.
- ^ Wechsler, Steven L.; Rustigian, Robert; Stallcup, Kathryn C.; Byers, Karen B.; Winston, Stuart H.; Fields, Bernard N. (1979). "Measles Virus-Specified Polypeptide Synthesis in Two Persistently Infected HeLa Cell Lines". Journal of Virology. 31 (3): 677–684. doi:10.1128/jvi.31.3.677-684.1979. ISSN 0022-538X. PMC 353496. PMID 513191.
- ^ Li, Li; Collins, Natalie D.; Widen, Steven G.; Davis, Emily H.; Kaiser, Jaclyn A.; White, Mellodee M.; Greenberg, M. Banks; Barrett, Alan D. T.; Bourne, Nigel; Sarathy, Vanessa V. (2019-08-20). "Attenuation of Zika Virus by Passage in Human HeLa Cells". Vaccines. 7 (3): 93. doi:10.3390/vaccines7030093. ISSN 2076-393X. PMC 6789458. PMID 31434319.
- ^ Pamela Bulzomi; Paola Galluzzo; Alessandro Bolli; Stefano Leone; Filippo Acconcia; Maria Marino (2012). "The pro-apoptotic effect of quercetin in cancer cell lines requires ERβ-dependent signals". Journal of Cellular Physiology. 227 (5): 1891–1898. doi:10.1002/jcp.22917. PMID 21732360. S2CID 24034074.
- ^ Tan X, Luo S, Wang D, Su Y, Cheng T, Shi C (2011). "A NIR heptamethine Dye with intrinsic cancer targeting, imaging and photosynthesizing properties". Journal of Biomaterials China. 33 (7): 2230–2239. doi:10.1016/j.biomaterials.2011.11.081. PMID 22182749.
- ^ Pene, F.; Courtine, E.; Cariou, A.; Mira, J.P. (2009). "Toward theranostics". Crit Care Med. 37 (1 Suppl): S50–S58. doi:10.1097/CCM.0b013e3181921349. PMID 19104225. S2CID 37043095.
- ^ Briiuner., Thomas; Dieter F. Hulser (1990). "Tumor Cell Invasion and Gap Junctional Communication" (PDF). Invasion Metastasis. 10: 31–34. Retrieved 3 April 2012.
- ^ Xie, Z.; Wroblewska, L.; Prochazka, L.; Weiss, R.; Benenson, Y. (2011). "Multi-Input RNAi-Based Logic Circuit for Identification of Specific Cancer Cells" (PDF). Science. 333 (6047): 1307–1311. Bibcode:2011Sci...333.1307X. doi:10.1126/science.1205527. PMID 21885784. S2CID 13743291.
- ^ Arjomandnejad, M; et al. (2014). "HeLa cell line xenograft tumor as a suitable cervical cancer model: growth kinetic characterization and immunohistochemistry array" (PDF). Archives of Iranian Medicine. 17 (4): 273–277. PMID 24724604. S2CID 25652255. Archived from the original (PDF) on 2018-04-25.
- ^ Davies, Preston. "Significant Research Advances Enabled by HeLa Cells". Office of Science Policy. Retrieved 2020-03-25.
- ^ 노벨 생리의학상 2009년 nobelprize.org
- ^ Ivanković M, Cukusić A, Gotić I, Skrobot N, Matijasić M, Polancec D, Rubelj I (2007). "Telomerase activity in HeLa cervical carcinoma cell line proliferation". Biogerontology. 8 (2): 163–72. doi:10.1007/s10522-006-9043-9. PMID 16955216. S2CID 9390790.
- ^ a b c Macville M, Schröck E, Padilla-Nash H, Keck C, Ghadimi BM, Zimonjic D, Popescu N, Ried T (1999). "Comprehensive and definitive molecular cytogenetic characterization of HeLa cells by spectral karyotyping". Cancer Res. 59 (1): 141–50. PMID 9892199.
- ^ Landry JJ, Pyl PT, Rausch T, Zichner T, Tekkedil MM, Stütz AM, Jauch A, Aiyar RS, Pau G, Delhomme N, Gagneur J, Korbel JO, Huber W, Steinmetz LM (2013). "The genomic and transcriptomic landscape of a HeLa cell line". G3: Genes, Genomes, Genetics. 3 (8): 1213–24. doi:10.1534/g3.113.005777. PMC 3737162. PMID 23550136.
- ^ Bottomley, R.H.; Trainer, A.L.; Griffin, M.J. (1969). "Enzymatic and chromosomal characterization of HeLa variants". J. Cell Biol. 41 (3): 806–15. doi:10.1083/jcb.41.3.806. PMC 2107821. PMID 5768876.
- ^ Andrew Adey; Joshua N. Burton; Jacob O. Kitzman; Joseph B. Hiatt; Alexandra P. Lewis; Beth K. Martin; Ruolan Qiu; Choli Lee; Jay Shendure (2013). "The haplotype-resolved genome and epigenome of the aneuploid HeLa cancer cell line". Nature (published August 8, 2013). 500 (7461): 207–211. Bibcode:2013Natur.500..207A. doi:10.1038/nature12064. PMC 3740412. PMID 23925245.
- ^ Landry JJ, Pyl PT, Rausch T, Zichner T, Tekkedil MM, Stütz AM, Jauch A, Aiyar RS, Pau G, Delhomme N, Gagneur J, Korbel JO, Huber W, Steinmetz LM (2013). "The genomic and transcriptomic landscape of a HeLa cell line". G3: Genes, Genomes, Genetics. 3 (8): 1213–24. doi:10.1534/g3.113.005777. PMC 3737162. PMID 23550136.
- ^ Callaway, Ewen (March 15, 2013). "Most popular human cell in science gets sequenced". Nature. doi:10.1038/nature.2013.12609. S2CID 87549985. Retrieved 8 August 2013.
- ^ a b Callaway, Ewen (March 27, 2013). "HeLa publication brews bioethical storm". Nature. doi:10.1038/nature.2013.12689. S2CID 88020977. Retrieved 8 August 2013.
- ^ Callaway, Ewen (August 7, 2013). "Deal done over HeLa cell line". Nature. 500 (7461): 132–133. Bibcode:2013Natur.500..132C. doi:10.1038/500132a. PMID 23925220.
- ^ a b "NIH, Lacks family reach understanding to share genomic data of HeLa cells". The National Institutes of Health. August 7, 2013. Retrieved 8 August 2013.
- ^ Callaway, Ewen (August 7, 2013). "NIH director explains HeLa agreement". Nature. doi:10.1038/nature.2013.13521. S2CID 190871214.
- ^ Gold, Michael (1986). A conspiracy of cells: one woman's immortal legacy and the medical scandal it caused. State University of New York Press. ISBN 0-88706-099-4. OCLC 12805138.
- ^ Wang H, Huang S, Shou J, Su EW, Onyia JE, Liao B, Li S (2006). "Comparative analysis and integrative classification of NCI60 cell lines and primary tumors using gene expression profiling data". BMC Genomics. 7 (1): 166. doi:10.1186/1471-2164-7-166. PMC 1525183. PMID 16817967.
- ^ Nardone, R.M. (2007). "Eradication of cross-contaminated cell lines: A call for action" (PDF). Cell Biology and Toxicology. 23 (6): 367–372. CiteSeerX 10.1.1.432.8581. doi:10.1007/s10565-007-9019-9. PMID 17522957. S2CID 21077969. Archived from the original (PDF) on 2008-12-17. Retrieved 2007-12-04.
- ^ "ATCC® Standards Development Organization: The International Cell Line Authentication Committee (ICLAC)". Standards.atcc.org. Retrieved 2013-06-27.
- ^ Maiorana VC, Van Valen LM (7 February 1991). "Hela, a new microbial species" (PDF). Evolutionary Theory. 10 (2): 71–4. Archived (PDF) from the original on 29 March 2018.
- ^ Duesberg, P; Mandrioli, D; McCormack, A; Nicholson, JM (2011). "Is carcinogenesis a form of speciation?". Cell Cycle. Georgetown, Texas. 10 (13): 2100–2114. doi:10.4161/cc.10.13.16352. PMID 21666415.
- ^ van Valen, L.M.; Maiorana, V.C. (1991). "HeLa, a new microbial species". Evolutionary Theory & Review. 10: 71–74. ISSN 1528-2619.
- ^ Cohan, FM (2002). "What are bacterial species?". Annu. Rev. Microbiol. 56 (1): 457–487. doi:10.1146/annurev.micro.56.012302.160634. PMID 12142474.
- ^ "Modern Times: The Way of All Flesh - BBC Two England - 19 March 1997". The Radio Times (3815): 92. 1997-03-13.
- ^ "About The Immortal Life of Henrietta Lacks". Rebecca Skloot. Retrieved 24 April 2018.
- ^ Thomas, June (2010-05-19). "Ripped From Which Headline? "Immortal"". Slate Magazine. Retrieved 2021-08-03.
- ^ "Henrietta's Tumor".
추가 정보
- Hannah Landecker (2000). "Immortality, In Vitro: A History of the HeLa Cell Line". In Brodwin, Paul (ed.). Biotechnology and culture: bodies, anxieties, ethics. Bloomington: Indiana University Press. pp. 53–74. ISBN 978-0-253-21428-7.
- Rebecca Skloot (2010). The Immortal Life of Henrietta Lacks.
외부 링크
- ATCC 데이터베이스의 HeLa(CCL-2 셀)
- 미국 국립 의학 도서관 의학 주제 제목(MeSH)의 Hela Cells
- Hela 세포에 대한 Hela 트랜스펙션 및 선택 데이터
- 레베카 스클루트, 헨리에타의 불멸의 삶 추가 기능 포함 도서 웹사이트 (사진/비디오/오디오)
- 헨리에타 랙스 재단은 헨리에타 랙스의 가족에게 장학금과 건강보험을 제공하는 것을 돕기 위해 설립되었습니다.
- 레베카 스클루트, 생명을 구하는 세포는 어머니의 유산, 뉴욕타임즈
- "원더우먼: 현대 의학계의 무의식적인 여주인공 헨리에타 부족의 삶과 죽음, 그리고 사후 삶" 밴 스미스
- 앤 엔라이트의 "헨리에타 랙스의 왼쪽은?"
- 「생활의 양식: How Cells Become Technologies"는 Hela와 조직 배양 역사에 관한 Hanna Landecker의 책이다.
- Helacyton에 새로운 분류군을 만들었을 때의 분류학적 효과에 대한 논의.
- 셀 중심 데이터베이스– Hela 셀
- 레베카 스클루트와의 오디오 인터뷰 "헨리에타 부족의 불멸의 삶"
- 셀로사우루스 헬라 진입
- 헨리에타 부족의 유산