전기 배터리
Electric battery | |
| 유형 | 동력원 |
|---|---|
| 작업원리 | 전기화학반응, 기전력 |
| 제1차 생산 | 1800년대 |
| 전자 기호 | |
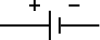 회로 다이어그램의 배터리 기호.그것은 가장 초기 유형의 배터리인 볼타 말뚝의 도식화로 시작되었다. | |
전기 배터리는 전기 장치에 전원을 공급하기 위한 외부 연결을[1] 가진 하나 이상의 전기 화학 셀로 구성된 전력 공급원이다.
배터리가 전력을 공급할 때 양극 단자는 음극이고 음극 단자는 양극이다.[2]음으로 표시된 단자는 외부 전기 회로를 통해 양극 단자로 흐르게 될 전자의 원천이다.배터리가 외부 전기 부하에 연결되면, redox 반응은 고에너지 반응제를 저에너지 제품으로 전환하고, 자유 에너지 차이는 전기 에너지로 외부 회로에 전달된다.[3]역사적으로 "배터리"라는 용어는 특히 다중 셀로 구성된 장치를 지칭했지만, 용도는 단일 셀로 구성된 장치를 포함하도록 진화했다.[4]
1차(단일 사용 또는 "폐기") 배터리는 방전 시 전극 재료가 불가역적으로 변경되기 때문에 한 번 사용하고 폐기한다. 일반적인 예는 손전등과 다수의 휴대용 전자 장치에 사용되는 알칼리성 배터리다.2차(재충전 가능) 배터리는 인가된 전류를 사용하여 여러 번 방전 및 재충전이 가능하며, 전극의 원래 구성은 역전류를 통해 복원할 수 있다.차량에 사용되는 납산 배터리와 노트북, 휴대전화 등 휴대용 전자제품에 사용되는 리튬이온 배터리 등이 대표적이다.
배터리는 보청기와 손목시계를 작동시키는 데 사용되는 축소형 세포에서부터 전화 교환과 컴퓨터 데이터 센터에 대기 또는 비상 전력을 제공하는 방 크기의 가장 큰 극한에 이르는 다양한 형태와 크기로 나온다.
배터리는 가솔린과 같은 일반 연료보다 특정 에너지(단위 질량당 에너지)가 훨씬 낮다.자동차의 경우, 이는 연소 엔진에 비해 전기 에너지를 기계적인 작업으로 전환하는 데 있어 전기 모터의 높은 효율에 의해 다소 상쇄된다.
역사
발명
바그다드 배터리(기원전 150년—650년)는 전류를 보유하는 장치였다고 이론화되었지만 이는 결론에 이르지 못한다.[citation needed]
이탈리아의 물리학자 알레산드로 볼타는 1800년에 최초의 전기 화학적 배터리인 볼타 더미를 만들고 묘사했다.[5]이것은 구리와 아연판을 쌓아 놓은 것으로, 소금에 절인 종이 원반에 의해 분리되어 상당한 시간 동안 일정한 전류를 생산할 수 있었다.볼타는 그 전압이 화학반응 때문이라는 것을 이해하지 못했다.그는 자신의 세포가 무진장한 에너지의 원천이며,[6] 전극의 관련 부식 효과는 1834년 마이클 패러데이가 보여준 것처럼 그 작동의 피할 수 없는 결과라기보다는 단지 성가신 결과라고 생각했다.[7]
초기 배터리는 실험용으로 큰 가치가 있었지만,[8] 실제로 전압은 변동했고 지속적인 기간 동안 큰 전류를 공급할 수 없었다.1836년 영국의 화학자 존 프레데릭 다니엘에 의해 발명된 다니엘 세포는 산업 표준이 되었고 전기 전신망의 동력원으로서 널리 채택된 최초의 실용적인 전기 공급원이었다.[9]그것은 황산동 용액을 채운 구리 항아리로 구성되었으며, 그 안에 황산을 채운 유약되지 않은 토기 용기와 아연 전극을 담갔다.[10]
이들 습전지는 액체 전해질을 사용했는데, 이를 올바르게 취급하지 않으면 누출과 유출이 일어나기 쉽다.많은 사람들이 유리 항아리를 사용하여 그 구성요소를 고정시켰고, 그것은 그것들을 깨지기 쉽고 잠재적으로 위험하게 만들었다.이러한 특성 때문에 젖은 셀은 휴대용 기기에 적합하지 않았다.19세기 말, 액체 전해질을 페이스트(paste)로 대체한 건전지 배터리의 발명은 휴대용 전기기기를 실용적으로 만들었다.[11]
진공관 배터리는 역사적으로 "A" 배터리의 경우 젖은 셀(필라멘트에 전원을 공급하기 위해)을, "B" 배터리의 경우 건전지(플레이트 전압을 공급하기 위해)를 사용했다.[citation needed]
미래
2010~2018년 연간 배터리 수요는 30% 증가해 2018년에는 총 180Gwh에 달했다.보수적으로 보면, 2030년에는 수요가 2600 Gwh에 도달하면서, 성장률은 약 25%로 유지될 것으로 예상된다.또 비용 절감으로 수요가 3562GwH까지 늘어날 것으로 전망된다.[12]
이러한 전기 배터리 산업의 높은 성장 속도의 중요한 이유로는 운송의 전기화와 전기 그리드의 대규모 배치, 화석 연료 연소 에너지원에서 청정, 재생 에너지원으로 탈피한 인공적인 기후 변화 주도의 이동에 의해 뒷받침되는 전기 그리드의 대규모 배치 등이 있다.[12][12]
배터리 전기 자동차(차량 대 그리드) 및 가정용 에너지 저장소에 사용되는 분산형 전기 배터리와 같이 스마트 계량 및 수요 대응을 위한 스마트 그리드에 연결되는 분산형 전기 배터리는 스마트 전원 공급 그리드의 적극적인 참여자다.[13]부분적으로 사용된 배터리의 에셀론 사용과 같은 새로운 재사용 방법은 전기 배터리의 전반적인 효용성을 증가시키고, 에너지 저장 비용을 절감하며, 수명을 연장함으로써 발생하는 오염/배출 영향을 감소시킨다.배터리 사용 시 배터리 용량이 보통 5~8년 사용 후 80% 미만으로 줄어든 차량용 전기 배터리는 백업 공급 또는 재생 에너지 저장 시스템으로 사용하기 위해 용도 변경된다.[14]
그리드 스케일 에너지 저장장치는 그리드나 발전소에서 에너지를 수집하고 저장한 후 나중에 그 에너지를 방출하여 필요할 때 전기 또는 기타 그리드 서비스를 제공하기 위해 배터리의 대규모 사용을 예상한다.그리드 스케일 에너지 저장장치(턴키 또는 분산형)는 스마트 전원 공급 그리드의 중요한 구성 요소다.[15]
화학 및 원리

배터리는 화학 에너지를 전기 에너지로 직접 전환한다.많은 경우에 방출되는 전기 에너지는 전기 화학 반응을 겪고 있는 금속, 산화물 또는 분자의 응집력[16] 또는 결합 에너지의 차이다.[3]예를 들어 에너지는 전이 금속과 달리 d-전자 본딩에 의해 안정화되지 않기 때문에 고에너지 금속인 Zn이나 Li에 저장할 수 있다.배터리는 전자가 회로의 외부를 통해 이동해야 정력적으로 유리한 리독스 반응이 발생할 수 있도록 설계됐다.
배터리는 몇 개의 볼타 전지들로 구성되어 있다.각 셀은 금속 양이온을 포함한 전도성 전해액에 의해 직렬로 연결된 두 개의 반전지들로 구성된다.한 반전지에는 음이온(음전하 이온)이 이동하는 전극인 전해질과 음전극이 있고, 다른 반전지에는 전해질과 양이온(양전하 이온)이 이동하는 양전극이 있다.음극에서 양이온(전자가 추가)되는 반면, 양극에서는 금속 원자가 산화(전자가 제거됨)[17]된다.일부 세포는 각 반전지마다 다른 전해질을 사용하며, 전기회로를 완성하기 위해 이온이 반전지 사이를 흐를 수 있도록 하면서 전해질이 섞이지 않도록 분리기를 사용한다.
각 반전지에는 표준에 상대적인 기전력(emf, 볼트 단위로 측정)이 있다.세포의 순 emf는 반세포의 emfs의 차이다.[18]Thus, if the electrodes have emfs and , then the net emf is ; in other words, the net emf is the difference between the reduction potentials of the half-반응들[19]
셀 단자에 걸쳐 전기 구동력 또는 V 을(를) 단자 전압(차이)이라고 하며 볼트 단위로 측정한다.[20]충전이나 방전되지 않는 셀의 단자 전압을 개방 회로 전압이라고 하며 셀의 emf와 동일하다.내부 저항 때문에 방전 중인 셀의 단자 전압은 개방 회로 전압보다 크기가 작고 충전 중인 셀의 단자 전압이 개방 회로 전압을 초과한다.[21][22]이상적인 셀은 내부 저항을 무시할 수 있으므로 의 일정한 단자 전압을 소진될 때까지 유지한 다음 0으로 떨어진다.만약 그러한 셀이 1.5볼트를 유지하고 하나의 쿨롱의 전하를 발생시킨다면 완전 방전 시 1.5줄의 작업을 수행했을 것이다.[20]실제 셀에서는 방전[21] 시 내부 저항이 증가하고 방전 시 개방 회로 전압도 감소한다.전압과 저항이 시간에 대해 표시되면 결과 그래프는 일반적으로 곡선이다. 곡선의 모양은 화학 및 내부 배열에 따라 달라진다.
셀 단자에 걸쳐 개발된 전압은 전극과 전해액의 화학적 반응의 에너지 방출에 따라 달라진다.알칼리성 및 아연-탄소성 세포는 화학 물질은 다르지만 거의 동일한 emf가 1.5볼트인데, NiCd와 NiMH 세포와 마찬가지로 화학 물질은 다르지만 거의 동일한 emf가 1.2볼트다.[23]리튬 화합물의 반응에서 전기화학적 전위 변화가 높으면 리튬 전지 emfs가 3V 이상 된다.[24]
전기 전도성을 갖기에 충분한 이온을 가지고 있는 거의 모든 액체나 습한 물체는 세포의 전해질 역할을 할 수 있다.참신함이나 과학시연으로서 레몬,[25] 감자 [26]등에 서로 다른 금속으로 만든 두 개의 전극을 삽입하여 소량의 전기를 발생시키는 것이 가능하다.
볼타 더미는 두 개의 동전(니켈과 1페니 등)과 소금물에 담근 종이 타월로 만들 수 있다.이러한 더미는 매우 낮은 전압을 발생시키지만, 직렬로 쌓이면 짧은 시간 동안 일반 배터리를 교체할 수 있다.[27]
종류들
기본 및 보조 배터리
배터리는 1차 및 2차 형식으로 분류된다.
- 기본 배터리는 에너지가 소진된 후 폐기될 때까지 사용하도록 설계되었다.그들의 화학 반응은 일반적으로 되돌릴 수 없기 때문에 재충전될 수 없다.배터리 내 리액터 공급이 소진되면 배터리에서 전류의 생성을 멈추고 무용지물이 된다.[28]
- 2차 배터리는 재충전할 수 있다. 즉, 전류를 세포에 가함으로써 화학 반응을 역전시킬 수 있다.이렇게 하면 원래의 화학반응 물질이 재생되어 여러 번 사용, 재충전, 재사용할 수 있다.[29]
예를 들어, 전신 회로에 사용되는 일부 유형의 기본 배터리는 전극을 교체하여 작동하도록 복원되었다.[30]2차 배터리는 활성 물질의 소산, 전해질 손실 및 내부 부식으로 인해 무한정 재충전이 가능하지 않다.
기본 배터리 또는 기본 셀은 조립 시 즉시 전류를 발생시킬 수 있다.이러한 기기는 전류의 배수가 낮거나, 간헐적으로만 사용되거나, 다른 전원이 간헐적으로만 사용 가능한 경보 및 통신 회로와 같은 대체 전원에서 멀리 떨어진 곳에서 주로 사용된다.일회용 1차 전지는 화학 반응이 쉽게 되돌릴 수 없고 활성 물질은 원래 형태로 되돌아가지 않을 수 있기 때문에 신뢰성 있게 충전될 수 없다.배터리 제조업체들은 1차 전지 충전을 시도하지 말 것을 권고한다.[31]일반적으로 이러한 배터리는 충전식 배터리보다 에너지 밀도가 높지만,[32] 일회용 배터리는 부하가 75옴(75Ω) 미만인 고배수 애플리케이션에서는 잘 작동하지 않는다.일반적인 일회용 배터리의 종류로는 아연-탄소 배터리와 알칼리성 배터리가 있다.
이차 전지 또는 충전식 배터리로도 알려진 이차 배터리는 처음 사용하기 전에 충전해야 한다. 이 배터리는 보통 방전 상태에서 활성 물질로 조립된다.충전식 배터리는 방전/사용 중 발생하는 화학반응을 역전시키는 전류를 가해 충전한다.적절한 전류를 공급하는 장치를 충전기라고 한다.가장 오래된 형태의 충전용 배터리는 납-산소형 배터리로서, 자동차와 보트 용도에 널리 사용된다.이 기술은 밀폐되지 않은 용기에 액체 전해액을 함유하고 있어 배터리를 똑바로 세우고 과충전 시 발생하는 수소 가스의 안전한 분산을 위해 환기를 잘해야 한다.납산 배터리는 공급할 수 있는 전기 에너지의 양에 비해 상대적으로 무겁다.낮은 제조 비용과 높은 서지 전류 레벨로 무게와 취급 문제보다 용량(약 10Ah 이상)이 더 중요한 곳에서 흔히 볼 수 있다.일반적으로 450암페어의 피크 전류를 전달할 수 있는 현대 자동차 배터리는 일반적인 응용 프로그램이다.
구성
많은 종류의 전기화학 전지가 생산되었고, 갈바닉 셀, 전해질 셀, 연료 셀, 플로우 셀, 볼타 말뚝을 포함한 다양한 화학적 과정과 설계가 이루어졌다.[33]
젖은 셀 배터리는 액체 전해질을 가지고 있다.액체가 모든 내부 부품이나 배기가스 셀을 덮고 있기 때문에 다른 이름들은 침수된 셀이다. 작동 중에 생성된 가스가 공기로 빠져나갈 수 있기 때문이다.젖은 세포는 건조한 세포의 전구체였으며 전기 화학의 학습 도구로 흔히 사용된다.그것들은 전기화학적 세포가 어떻게 작용하는지에 대한 시범을 위해 비커와 같은 일반적인 실험실 공급으로 건설될 수 있다.집중세포로 알려진 특정 유형의 습식세포는 부식을 이해하는 데 중요하다.젖은 셀은 일차 셀(비충전 가능) 또는 이차 셀(충전 가능)일 수 있다.원래 대니얼 셀과 같은 실용적 1차 배터리는 모두 오픈톱 유리 항아리 습전지로 만들어졌다.다른 주요 습세포는 레클란치 세포, 그로브 세포, 분센 세포, 크롬산 세포, 클라크 세포, 웨스턴 세포 등이다.레클란치 세포 화학은 최초의 건세포에 적응되었다.습전지는 여전히 자동차 배터리와 산업체에서 개폐장치, 통신 또는 대형 무정전 전원 공급의 대기 전력을 위해 사용되고 있지만, 많은 곳에서는 젤 전지가 있는 배터리를 대신 사용하고 있다.이러한 애플리케이션은 일반적으로 납산 또는 니켈-카드뮴 전지를 사용한다.녹은 염전지는 녹은 소금을 전해질로 사용하는 1차 또는 2차 전지다.고온에서 작동하며 열을 유지하려면 절연 상태가 양호해야 한다.
건전지에는 전류가 흐를 수 있을 정도의 수분만 있을 뿐 페이스트 전해질을 사용한다.건조전지는 습식전지와 달리 자유 액체가 들어 있지 않아 휴대용 장비에 적합하기 때문에 흘리지 않고 어떤 방향으로도 작동할 수 있다.이에 비해 첫 번째 젖은 셀은 일반적으로 열린 상부에 납이 매달린 깨지기 쉬운 유리 용기였으며 유출되지 않도록 세심한 취급이 필요했다.납산 배터리는 젤 배터리가 개발되기 전까지 건전지 안전성과 휴대성을 달성하지 못했다.일반적인 건전지란 건전지(둘 다 동일한 아연-망간 이산화 조합을 사용하기 때문에)는 공칭전압이 1.5V인 건성 레클란체 셀이라고도 한다.표준 건전지(standard dry cell)는 아연 양극으로 구성되는데, 보통 원통형 항아리 형태로, 중앙 막대의 형태로 탄소 음극이 있다.전해질은 아연 양극 옆에 페이스트 형태로 염화암모늄이다.전해질과 탄소 음극 사이의 남은 공간은 염화암모늄과 이산화망간으로 구성된 두 번째 페이스트에 의해 차지되며, 후자는 탈극자 역할을 한다.어떤 설계에서는 염화암모늄이 염화아연으로 대체된다.
예비 배터리는 조립되지 않은 상태로 장기간(아마도 수 년 동안) 저장할 수 있다.배터리가 필요할 때 조립한다(예: 전해질을 첨가하여). 일단 조립하면 배터리가 충전되어 작업할 준비가 된다.예를 들어, 전자 포병 연소를 위한 배터리는 총을 발사하는 충격에 의해 작동될 수 있다.그 가속은 배터리를 작동시키고 퓨즈의 회로를 작동시키는 전해질 캡슐을 깨뜨린다.예비 배터리는 보통 오래 보관(년)한 후 짧은 사용 수명(초 또는 분)을 위해 설계된다.해양학 기구 또는 군사 응용을 위한 물 작동 배터리는 물에 잠길 때 활성화된다.
2월 28일 2017년에, Austin에서 Texas의 대학교는 고체 배터리 새로운 유형의 팀lithium-ion 배터리 발명가 존 굿 이너프,"는 휴대용 모바일 장치, 전기 차들과 문구 에너지 저장소로 안전하고,faster-charging, longer-lasting 충전용 배터리로 이어질 수 있"에 의해 개발에 대한 보도 자료를 발표했다.[34]솔리드 스테이트 배터리는 또한 "에너지 밀도의 3배"를 가지고 있어 예를 들어 전기 자동차에서 유용 수명을 증가시킨다고 한다.또한 이 기술은 바닷물에서 추출한 나트륨과 같은 덜 비싸고, 지구 친화적인 물질을 사용하기 때문에 생태학적으로 더 건전해야 한다.그들은 또한 수명이 훨씬 길다.[35]
소니는 살아있는 유기체에서 관찰되는 과정과 유사한 방식으로 설탕으로부터 전기를 발생시키는 생물학적 배터리를 개발했다.배터리는 탄수화물을 분해하는 효소의 사용을 통해 전기를 발생시킨다.[36]
밀봉된 밸브 조절 납산전지(VRLA 배터리)는 납산 습전지 대체품으로 자동차 업계에서 인기가 높다.VRLA 배터리는 고정된 황산 전해질을 사용해 누수 가능성을 낮추고 저장 수명을 연장한다.[37]VRLA 배터리는 전해질을 고정시킨다.두 가지 유형은 다음과 같다.
다른 휴대용 충전용 배터리는 휴대폰과 노트북 컴퓨터와 같은 응용 분야에 유용한 밀봉된 "건전지" 타입을 포함한다.이러한 유형의 셀(전력 밀도와 비용 증가 순서)에는 니켈-카드뮴(NiCd), 니켈-진크(NiZn), 니켈-수화물(NiMH), 리튬이온(Li-ion) 셀이 포함된다.리온은 건전지 충전식 시장에서 단연 최고 점유율을 차지하고 있다.NiMH는 용량이 더 크기 때문에 대부분의 애플리케이션에서 NiCd를 대체했지만, NiCd는 여전히 전동 공구, 양방향 라디오, 의료 장비에서 사용되고 있다.
2000년대에는 USB 커넥터를 통해 AA 배터리를 충전할 수 있는 USBCELL과 같은 내장형 전자장치를 탑재한 배터리, 기존 배터리보다 100배 정도 높은 방전 속도를 허용하는 나노볼 배터리, 손상을 방지하는 충전 상태 모니터와 배터리 보호 회로가 장착된 스마트 배터리 팩 등이 개발되고 있다.과대평가되어낮은 자가 방전(LSD)은 2차 전지 충전 후 출하할 수 있다.
리튬-황 배터리는 가장 길고 높은 태양열 비행에 사용되었다.[38]
조합 및 관리
표준형 배터리는 이를 사용하는 장치의 배터리 홀더에 삽입된다.장치가 표준형 배터리를 사용하지 않는 경우, 배터리는 일반적으로 배터리 관리 시스템 및 배터리 아이솔레이터와 같은 기능 외에 여러 개의 배터리를 보관하는 맞춤형 배터리 팩으로 결합되어 배터리가 고르게 충전 및 방전되도록 한다.
사이즈
소비자가 쉽게 구할 수 있는 1차 배터리는 전기 시계에 사용되는 작은 버튼 셀부터 신호 회로나 기타 장시간의 응용에 사용되는 6번 셀까지 다양하다.2차 전지들은 매우 큰 크기로 만들어진다; 매우 큰 배터리는 잠수함에 전력을 공급하거나 전기 그리드를 안정시킬 수 있고 최대 부하를 평준화하는데 도움을 준다.
2017년[update] 현재 세계 최대 규모의 배터리가 테슬라에 의해 호주 남부에 건설되었다.129MWh를 저장할 수 있다.[39]중국 허베이성에 36MWh의 전기를 저장할 수 있는 배터리는 2013년 5억달러의 비용으로 건설됐다.[40]Ni-Cd 셀로 구성된 또 다른 대형 배터리는 알래스카의 페어뱅크스에 있었다.그것은 축구 경기장보다 더 큰 2,000 평방미터(2만 2천 평방피트)를 덮었고 무게는 1,300톤이었다.정전이 발생했을 때 예비 전력을 공급하기 위해 ABB가 제조한 것이다.배터리는 최대 7분 동안 40 MW의 전력을 공급할 수 있다.[41]나트륨-황산 배터리는 풍력을 저장하는 데 사용되어 왔다.[42]25분 동안 11 MW를 전달할 수 있는 4.4 MWh 배터리 시스템은 하와이 오와히 풍력 발전소의 출력을 안정시킨다.[43]
비교
이 글은 검증을 위해 인용구가 추가로 필요하다.– · · 책· · (2021년 6월)(이 템플릿 하는 |
전압, 에너지 밀도, 가연성, 가용 셀 구성, 작동 온도 범위 및 저장 수명과 같은 많은 중요한 셀 특성은 배터리 화학에 의해 결정된다.[citation needed]
| 화학 | 양극(-) | 음극(+) | 최대 전압, 이론적(V) | 공칭 전압, 실용적(V) | 특정 에너지(kJ/kg) | 정교 | 25°C에서의 저장 수명, 80%의 용량(개월) |
|---|---|---|---|---|---|---|---|
| 아연-탄소 | Zn | C | 1.6 | 1.2 | 130 | 비싸지 | 18 |
| 아연-염화물 | 1.5 | "무거운 일"이라고도 하며, 저렴하다. | |||||
| 알칼리성(진크망간 이산화물) | Zn | 엠노2 | 1.5 | 1.15 | 400-590 | 적당한 에너지 밀도.고배수 및 저배수 사용 시 좋다. | 30 |
| 니켈 옥시하이드록사이드(진크-망간 이산화물/니켈 옥시하이드록사이드) | 1.7 | 적당한 에너지 밀도.고배수 사용 시 좋다. | |||||
| 리튬(리튬-코퍼산화물) Li-CuO | 리 | CuO | 1.7 | 더 이상 제조되지 않음.산화은(IEC형 "SR") 배터리로 교체. | |||
| 리튬(리튬-이황화 철) LiFeS2 | 리 | FeS2 | 1.8 | 1.5 | 1070 | 비싸다'plus' 또는 'extra' 배터리에 사용됨. | 337[44] |
| 리튬(리튬-망간 이산화물) LiMnO2 | 리 | 엠노2 | 3.0 | 830–1010 | 비싸다자가 방전 비율이 매우 낮아서 배기가스 또는 긴 선반 수명에만 사용한다.'리튬'만 해도 대개 이런 종류의 화학을 가리킨다. | ||
| 리튬(리튬-탄소 불소화) 리–(CF)n | 리 | (CF)n | 3.6 | 3.0 | 120 | ||
| 리튬(리튬-크롬산화물) Li-CrO2 | 리 | CRO2 | 3.8 | 3.0 | 108 | ||
| 리튬(리튬-실리콘) | 리시225 | ||||||
| 산화 수은 | Zn | HGO | 1.34 | 1.2 | 높은 비와 일정한 전압.대부분의 국가에서 건강상의 문제로 금지된다. | 36 | |
| 아연-공기 | Zn | O2 | 1.6 | 1.1 | 1590[45] | 주로 보청기에 사용된다. | |
| 잠보니 더미 | Zn | 아그 또는 아우 | 0.8 | 아주 긴 인생.매우 낮음(나노 램프, nA) 전류 | >2,000 | ||
| 은산화질소(은색-진크) | Zn | 아고2 | 1.85 | 1.5 | 470 | 매우 비싸다.'버튼' 셀에서만 상업적으로 사용된다. | 30 |
| 마그네슘 | MG | 엠노2 | 2.0 | 1.5 | 40 |
| 화학 | 셀 전압 | 특정 에너지(kJ/kg) | 에너지 밀도(kJ/liter) | 평. |
|---|---|---|---|---|
| NiCd | 1.2 | 140 | 비싸지높은/낮은 비, 적당한 에너지 밀도.용량 손실 없이 매우 높은 방전 속도를 견딜 수 있다.적당한 자기 방전 속도.카드뮴으로 인한 환경 위험, 현재 유럽에서는 사실상 사용이 금지되어 있다. | |
| 리드-아시드 | 2.1 | 140 | 적당히 비싸다.적당한 에너지 밀도.적당한 자기 방전 속도.방전율이 높을수록 용량이 상당히 손실된다.납으로 인한 환경 위험.공용: 자동차 배터리 | |
| 니엠에이치 | 1.2 | 360 | 비싸지높은 배출 장치에서 알칼리성 배터리보다 우수한 성능전통 화학은 에너지 밀도가 높지만 자가 방전율도 높다.새로운 화학 물질은 자가 방전율은 낮지만 에너지 밀도는 25%까지 낮다. 일부 차에서는 사용된다. | |
| 니젠 | 1.6 | 360 | 적당히 싸다.고배수 장치 적합자체 방전율이 낮음.다른 2차 전지보다 알칼리성 1차 전지에 가까운 전압.유독성 구성 요소 없음시장에 새롭게 선보인(2009년).아직 트랙 기록을 세우지 못했다.제한된 크기 가용성. | |
| 아그진 | 1.86 1.5 | 460 | 등가 Li-ion보다 작은 볼륨.은으로 인해 엄청나게 비싸다.매우 높은 에너지 밀도.배출량이 매우 높음.수년 동안 높은 은값 때문에 쓸모없는 것으로 여겨졌다.세포는 사용하지 않으면 산화를 겪는다.반응은 완전히 이해되지 않는다.단자 전압은 매우 안정적이지만 70–80% 충전 시 1.5V로 갑자기 감소한다(양극 플레이트에 산화물과 산화물이 모두 존재하기 때문임, 1개가 먼저 소비됨).기본 배터리(문 버기) 대신 사용됨리온의 대체품으로 다시 한번 개발되고 있다. | |
| 리페포4 | 3.3 3.0 | 360 | 790 | 리튬-철-인산염 화학. |
| 리튬이온 | 3.6 | 460 | 매우 비싸다.매우 높은 에너지 밀도.일반적으로 "공통" 배터리 크기에서는 사용할 수 없음.리튬 폴리머 배터리는 노트북 컴퓨터, 디지털 카메라, 캠코더, 휴대폰 등에서 흔히 볼 수 있다.자가 방전 비율이 매우 낮음.단자 전압은 방전 중에 4.2~3.0V로 변화한다.휘발성:단락, 과열 또는 엄격한 품질 표준으로 제조되지 않은 경우 폭발 가능성. |
성능, 용량 및 방전
배터리의 특성은 내부 화학, 전류 방전 및 온도를 포함한 많은 요인으로 인해 부하 주기, 과충전 주기 및 수명에 따라 달라질 수 있다.저온에서는 배터리가 그만큼 많은 전력을 공급할 수 없다.이처럼 추운 날씨에는 소형 전기 난방 패드인 배터리 워머를 설치해 차량 배터리를 따뜻하게 유지해주는 차주도 있다.
배터리의 용량은 정격 전압에서 전달할 수 있는 전하의 양이다.셀에 더 많은 전극 물질이 들어 있을수록 그 용량은 더 커진다.작은 셀은 동일한 개방 회로 전압을 발생시키지만 같은 화학물질을 가진 큰 셀보다 용량이 적다.[46]용량은 A/h와 같은 단위로 측정한다.배터리의 정격 용량은 일반적으로 20시간의 곱에 68°F(20°C)에서 20시간 동안 지속적으로 새 배터리가 공급할 수 있는 전류를 곱한 값으로 표현되며, 셀당 지정된 단자 전압 이상을 유지한다.예를 들어, 100 A/h 정격 배터리는 실온에서 20시간 동안 5 A를 전달할 수 있다.배터리가 전달할 수 있는 저장 전하의 분율은 배터리 화학, 전하가 전달되는 속도(전류), 필요한 단자 전압, 저장 기간, 주변 온도 및 기타 요인에 따라 달라진다.[46]
방전율이 높을수록 수용량은 낮아진다.[47]납산 배터리의 전류, 방전 시간 및 용량 사이의 관계는 Pukert의 법칙에 의해 근사치(전류 값의 일반적인 범위에 걸쳐)로 계산된다.
어디에
- 은(는) 1A의 비율로 방전했을 때의 용량이다.
- 은(는) 배터리(A)에서 끌어온 전류다.
- 은(는) 배터리가 지속할 수 있는 시간(시간 단위)이다.
- 는 1.3 전후의 상수다.
장기간 보관되거나 용량의 작은 부분에 방전된 배터리는 전류를 발생시키지 않고 충전 캐리어를 소비하는 일반적으로 되돌릴 수 없는 측면 반응이 존재하기 때문에 용량이 줄어든다.이러한 현상을 내부 자기 방전이라고 한다.또한 배터리를 재충전할 때 추가적인 측면 반응이 일어나 후속 방전을 위한 용량이 감소할 수 있다.충전을 충분히 한 후, 본질적으로 모든 용량이 손실되고 배터리가 전력 생산을 중단한다.내부 에너지 손실과 이온이 전해질을 통과하는 속도의 제한은 배터리 효율을 변화시킨다.최소 임계값을 초과하면 낮은 속도로 방전하면 높은 속도보다 더 많은 배터리 용량을 제공한다.A/h 정격이 다양한 배터리를 설치하는 것은 부하 한계를 초과하지 않는 한 특정 전압에 대한 정격 장치 작동(운전 간격에 영향을 미칠 수 있지만)에 영향을 미치지 않는다.디지털 카메라와 같은 고배수 부하로 인해 알칼리성 배터리의 경우와 같이 총 용량이 감소할 수 있다.예를 들어 10시간 또는 20시간 방전 시 2A/h로 정격된 배터리는 명시된 용량에서 알 수 있듯이 2시간 동안 1A의 전류를 유지하지 못할 것이다.
C-레이트(C-레이트)는 배터리가 충전 또는 방전되는 속도의 측정값이다.이 전류는 배터리를 통과하는 전류를 이론적 전류 요구량으로 나눈 값이며, 배터리는 1시간 내에 공칭 정격 용량을 제공한다.[48]그것은 유닛−1 h를 가지고 있다.내부 저항 손실과 세포 내부의 화학적 작용 때문에 배터리는 명판 정격 용량을 단 1시간 만에 거의 제공하지 않는다.일반적으로 최대 용량은 낮은 C-레이트에서 발견되며, 높은 C-레이트에서 충전 또는 방전은 배터리의 사용 가능 수명과 용량을 감소시킨다.제조업체는 종종 용량 대 C-레이트 곡선을 보여주는 그래프가 있는 데이터시트를 발행한다.C-레이트(C-rate)는 배터리가 회로 내에서 안전하게 전달할 수 있는 최대 전류를 나타내는 배터리 정격으로도 사용된다.충전용 배터리의 표준은 일반적으로 용량과 충전 주기를 4시간(0.25C), 8시간(0.125C) 이상의 방전 시간에 걸쳐 평가한다.컴퓨터 무정전 전원 공급장치와 같이 특별한 목적을 위한 형식은 제조자가 1시간(1C) 미만의 방전 기간 동안 정격을 받을 수 있지만 제한된 사이클 수명을 겪을 수 있다.
2012년[update] 기준 리튬 철 인산염(LiFePO
4) 배터리 기술은 10~20초 만에 완전 방전돼 가장 빠른 충전/방전 속도였다.[49]
수명
배터리 수명(및 동의어 배터리 수명)은 충전용 배터리의 두 가지 의미를 가지지만, 비충전용 배터리의 의미는 하나만 가진다.충전기의 경우, 완전 충전된 배터리에서 기기가 작동할 수 있는 시간 길이 또는 셀이 만족스럽게 작동하지 않을 때까지 가능한 충전/배출 사이클의 수를 의미한다.비충전 가능의 경우, 세포가 정의상 단 한 사이클 동안만 지속되기 때문에 이 두 수명은 동일하다.(저장 수명은 배터리의 제조와 사용 간 성능을 얼마나 오래 유지하는지를 설명하는 데 사용된다.)모든 배터리의 가용 용량은 온도가 감소함에 따라 감소한다.오늘날 대부분의 배터리와는 대조적으로, 1812년에 발명된 잠보니 더미는 나노암페어에서만 전류를 공급하지만, 리퍼브나 재충전 없이 매우 긴 사용 수명을 제공한다.옥스포드 전기 벨은 잠보니 말뚝으로 생각되는 원래의 배터리로 1840년부터 거의 지속적으로 울리고 있다.[citation needed]
일회용 배터리는 일반적으로 상온(20~30°C)에서 보관할 때 원래 충전량의 8~20%가 손실된다.[50]이를 '자기방전율'이라고 하며, 하중을 가하지 않아도 세포 내에서 일어나는 비전류성 '측면' 화학반응에 기인한다.일부 배터리는 결빙에 의해 손상될 수 있지만 낮은 온도에서 보관되는 배터리의 경우 측면 반응 속도가 감소한다.오래된 충전용 배터리는 일회용 알칼리성 배터리, 특히 니켈 기반 배터리보다 더 빠르게 자가 방전된다; 새로 충전된 니켈 카드뮴(NiCd) 배터리는 처음 24시간 동안 충전량의 10%가 손실되고, 그 후 매달 약 10%의 비율로 방전된다.그러나, 신형 저방전 니켈 금속 하이드라이드(NiMH) 배터리와 현대 리튬 디자인은 낮은 자기방전율(그러나 여전히 기본 배터리보다 높은)을 나타낸다.
배터리 플레이트의 활성 물질은 각 충전 및 방전 주기에 따라 화학적 조성을 변화시킨다. 활성 물질은 부피의 물리적 변화로 인해 손실될 수 있으며, 배터리를 충전할 수 있는 횟수를 더욱 제한한다.니켈 기반 배터리는 대부분 구입 시 부분적으로 방전되며, 처음 사용하기 전에 충전해야 한다.[51]신형 NiMH 배터리는 구입 시 바로 사용할 수 있으며, 1년 내 방전이 15%에 불과하다.[52]
각 충전-배출 사이클에서 일부 열화가 발생한다.분해는 보통 전해질이 전극으로부터 멀어지거나 활성 물질이 전극으로부터 분리되기 때문에 발생한다.저용량 NiMH 배터리(1,700–2,000mA·h)는 약 1,000회 충전이 가능한 반면, 대용량 NiMH 배터리(2,500mA·h 이상)는 약 500회 지속된다.[53]NiCd 배터리는 내부 저항이 사용 가능한 값을 초과하여 영구적으로 증가하기 전에 1,000 사이클의 정격을 받는 경향이 있다.급속 충전은 부품 변화를 증가시켜 배터리 수명을 단축시킨다.[53]충전기가 배터리가 완전히 충전된 시기를 감지하지 못하면 과충전이 발생하여 배터리가 손상될 수 있다.[54]
NiCd 셀은 특정한 반복적인 방법으로 사용할 경우 "메모리 효과"[55]라고 불리는 용량이 감소할 수 있다.그 효과는 간단한 실천으로 피할 수 있다.NiMH 세포는 화학에서는 비슷하지만 기억력 효과로 인한 고통은 적다.[56]
자동차 납산 충전 배터리는 진동, 충격 및 온도 범위로 인한 스트레스를 견뎌야 한다.이러한 스트레스와 납판의 황화 때문에, 6년 이상 정기적으로 사용하는 자동차 배터리는 거의 없다.[57]자동차 시동(SLI: Starting, Lighting, Ignition) 배터리는 전류를 최대화하기 위해 얇은 플레이트를 많이 가지고 있다.일반적으로 접시가 두꺼울수록 수명이 길어진다.그것들은 일반적으로 재충전 전에 약간만 방전된다.전기 골프 카트에 사용되는 것과 같은 "딥 사이클" 납산 배터리는 수명을 연장하기 위해 훨씬 두꺼운 접시를 가지고 있다.[58]납산 배터리의 주요 이점은 낮은 비용이다. 배터리의 주요 단점은 주어진 용량과 전압에 대한 큰 크기와 무게다.납산 배터리는 재충전 시 내부 저항으로 열과 손상이 발생하므로 용량의 20% 미만으로 방전해서는 안 된다.[59]딥 사이클 리드-산소 시스템은 배터리 수명을 단축시킬 손상 유형을 방지하기 위해 저차지 경고등 또는 저차지 전원 차단 스위치를 사용하는 경우가 많다.[60]
배터리 수명은 냉장고나 냉동고처럼 낮은 온도로 배터리를 보관하면 길어지기 때문에 부작용 속도가 느려진다.이러한 저장장치는 알칼리성 배터리의 수명을 약 5% 연장할 수 있다; 충전용 배터리는 종류에 따라 충전량을 훨씬 더 오래 유지할 수 있다.[61]최대 전압에 도달하려면 배터리를 실온으로 되돌려야 한다. 알칼리성 배터리를 0°C에서 250mA로 방전하는 것은 20°C의 절반밖에 효율적이지 않다.[32]듀라셀 등 알칼리성 배터리 제조사는 냉장 배터리를 권장하지 않는다.[31]
위험
이 섹션은 검증을 위해 추가 인용구가 필요하다.할 수있음(2017년 4월 (이 템플릿 제거 및 |
배터리 폭발은 일반적으로 1차(비충전) 배터리를 재충전하려고 하거나 단락을 시도하는 등 오용이나 오작동에 의해 발생한다.
배터리를 과도한 속도로 재충전할 경우 수소와 산소의 폭발성 가스 혼합물이 배터리 내부에서 탈출할 수 있는 속도보다 더 빨리 생성되어 압력이 축적되고 배터리 케이스가 결국 파열될 수 있다.극단적인 경우 배터리 화학물질이 케이스에서 심하게 분사되어 부상을 일으킬 수 있다.이 문제의 전문가 요약에 따르면 이 유형은 양극과 음극 사이에 리튬 이온을 운반하기 위해 "액체 전해질"을 사용한다고 한다.배터리 셀이 너무 빨리 충전되면 누전을 일으켜 폭발과 화재로 이어질 수 있다."[62][63]자동차 배터리는 단락 회로가 매우 큰 전류를 발생시킬 때 폭발할 가능성이 가장 높다.그런 배터리는 과충전될 때(전해질 속의 물의 전기분해 때문에) 매우 폭발성이 높은 수소를 생산한다.정상적인 사용 중 과충전의 양은 대개 매우 적고 수소가 거의 생성되지 않아 금방 소멸된다.그러나 자동차를 "점프 시동"할 때 높은 전류로 인해 많은 양의 수소가 방출될 수 있으며, 이는 점퍼 케이블을 분리할 때와 같이 근처의 스파크에 의해 폭발적으로 점화될 수 있다.
과충전(전력을 초과하는 배터리 충전을 시도함)은 누출 또는 되돌릴 수 없는 손상 외에도 배터리 폭발로 이어질 수 있다.또한 나중에 과충전된 배터리를 사용하는 충전기나 장치에 손상을 일으킬 수 있다.
소각을 통해 배터리를 폐기하면 밀봉 케이스 내에 증기가 쌓이면서 폭발을 일으킬 수 있다.
많은 배터리 화학 물질은 부식성, 독성 또는 둘 다 있다.자연발생적이거나 사고를 통해 누출이 발생하면 방출되는 화학물질은 위험할 수 있다.예를 들어, 일회용 배터리는 종종 아연 "캔"을 반응제로서 그리고 다른 시약을 담는 용기로 사용한다.이런 종류의 배터리가 과다하게 방전되면 시약이 용기의 나머지 부분을 구성하는 마분지와 플라스틱을 통해 나올 수 있다.그러면 활성 화학 물질 누출은 배터리가 구동하는 장비를 손상시키거나 비활성화할 수 있다.이 때문에 많은 전자기기 제조사는 장시간 사용하지 않는 기기에서 배터리를 분리할 것을 권고하고 있다.
많은 종류의 배터리는 납, 수은, 카드뮴과 같은 독성 물질을 전극이나 전해질로 사용한다.각 배터리는 수명이 다하면 환경 손상을 방지하기 위해 폐기해야 한다.[64]배터리는 전자 폐기물(전자 폐기물)의 한 형태다.전자 폐기물 재활용 서비스는 독성 물질을 회수하고, 독성 물질을 새 배터리에 사용할 수 있다.[65]미국에서 연간 구매되는 거의 30억 개의 배터리 중 약 17만 9천 톤은 미국 전역의 매립지에 버려진다.[66]
배터리는 삼킬 경우 유해하거나 치명적일 수 있다.[67]작은 버튼 셀은 특히 어린 아이들이 삼킬 수 있다.소화관에 있는 동안, 배터리의 전기는 조직 손상으로 이어질 수 있다;[68] 그러한 손상은 때때로 심각하고 죽음에 이를 수 있다.섭취한 디스크 배터리는 대개 위장관에 박혀 있지 않는 한 문제를 일으키지 않는다.디스크 배터리가 박히는 가장 흔한 장소는 식도인데, 그 결과 임상적인 속편이 생겨난다.식도를 성공적으로 가로지르는 배터리는 다른 곳에 보관할 가능성이 낮다.디스크 배터리가 식도에 들어갈 가능성은 환자의 나이와 배터리 크기의 함수다.16mm의 디스크 배터리는 1년 미만 어린이 2명의 식도에 박혀 있다.[citation needed]나이 든 아이들은 21-23mm보다 작은 배터리에 문제가 없다.수산화나트륨은 배터리에 의해 생성되는 전류(보통 양극에서)에 의해 생성되기 때문에 액화 괴사가 발생할 수 있다.천공은 섭취한 지 6시간 만에 빠르게 발생했다.[69]
법률 및 규정
전기 배터리 관련 법률에는 안전한 폐기 및 재활용과 같은 주제가 포함된다.
미국에서는 1996년 '수성 함유 및 충전용 배터리 관리법'이 수은 함유 배터리의 판매를 금지하고, 충전용 배터리에 대한 균일한 라벨 부착 요건을 제정했으며, 충전용 배터리를 쉽게 분리할 수 있도록 요구하였다.[70]캘리포니아와 뉴욕시는 고체 폐기물에 재충전 가능한 배터리를 폐기하는 것을 금지하고 있다.[71][72]충전식 배터리 산업은 미국과 캐나다에서 전국적인 재활용 프로그램을 운영하고 있으며, 국내 소매점에서는 중단점을 두고 있다.[73]
유럽연합(EU)의 배터리 지침은 배터리 재활용을 늘리고 배터리 재활용 방법을 개선할 수 있는 연구를 촉진할 뿐 아니라 유사한 요건을 갖추고 있다.[74]이 지침에 따라 EU 내에서 판매되는 모든 배터리는 반드시 "수집 기호"(바퀴가 교차된 빈)로 표시해야 한다.이것은 프리즘 배터리 표면의 최소 3%와 원통형 배터리 표면의 1.5%를 포함해야 한다.모든 포장도 마찬가지로 표시해야 한다.[75]
보고된 사고와 고장, 때로는 점화 또는 폭발에 대응하여, 리튬 이온 배터리를 사용하는 장치의 리콜이 최근 몇 년 사이에 더 흔해졌다.[76][77]
참고 항목
참조
- ^ Crompton, T. R. (20 March 2000). Battery Reference Book (third ed.). Newnes. p. Glossary 3. ISBN 978-0-08-049995-6. Retrieved 18 March 2016.
- ^ Pauling, Linus (1988). "15: Oxidation-Reduction Reactions; Electrolysis". General Chemistry. New York: Dover Publications, Inc. p. 539. ISBN 978-0-486-65622-9.
- ^ a b Schmidt-Rohr, Klaus (2018). "How Batteries Store and Release Energy: Explaining Basic Electrochemistry". Journal of Chemical Education. 95 (10): 1801–1810. Bibcode:2018JChEd..95.1801S. doi:10.1021/acs.jchemed.8b00479.
- ^ Pistoia, Gianfranco (25 January 2005). Batteries for Portable Devices. Elsevier. p. 1. ISBN 978-0-08-045556-3. Retrieved 18 March 2016.
- ^ 벨리스, 메리.배터리의 발명가 알레산드로 볼타의 전기.About.com.2008년 8월 7일 검색됨
- ^ 스틴너, 아서알레산드로 볼타와 루이지 갈바니 아카이브 2008년 9월 10일 웨이백 머신(PDF)에 보관.2008년 8월 11일 회수.
- ^ 1800년 알레산드로 볼타의 전기 배터리 발명에 대한 매혹적인 사실들.위대한 아이디어 발견자.2008년 8월 11일 회수
- ^ 예를 들어, 1820년 전자석의 발견에서
- ^ 배터리 이력, 기술, 응용 프로그램 및 개발.엠파워 솔루션스 Ltd.2007년 3월 19일 검색됨
- ^ Borvon, Gérard (10 September 2012). "History of the electrical units". Association S-EAU-S.
- ^ "Columbia Dry Cell Battery". National Historic Chemical Landmarks. American Chemical Society. Archived from the original on 23 February 2013. Retrieved 25 March 2013.
- ^ a b c Brudermüller, Martin; Sobotka, Benedikt; Dominic, Waughray (September 2019). Insight Report — A Vision for a Sustainable Battery Value Chain in 2030 : Unlocking the Full Potential to Power Sustainable Development and Climate Change Mitigation (PDF) (Report). World Economic Forum & Global Battery Alliance. pp. 11, 29. Retrieved 2 June 2021.
- ^ Siano, Pierluigi (2014). "Demand response and smart grids-A survey". Renewable and Sustainable Energy Reviews. Elsevier. 30: 461–478. doi:10.1016/j.rser.2013.10.022. ISSN 1364-0321.
- ^ Pan, AQ; Li, XZ; Shang, J; Feng, JH; Tao, YB; Ye, JL; Yang, X; Li, C; Liao, QQ (2019). The applications of echelon use batteries from electric vehicles to distributed energy storage systems. 2019 International Conference on New Energy and Future Energy System (IOP Conf. Series: Earth and Environmental Science). Vol. 354. IOP Publishing Ltd. doi:10.1088/1755-1315/354/1/012012. 012012.
- ^ Leisch, Jennifer E.; Chernyakhovskiy, Ilya (September 2019). Grid-Scale Battery Storage : Frequently Asked Questions (PDF) (Report). National Renewable Energy Laboratory (NREL) & greeningthegrid.org. Retrieved 21 May 2021.
- ^ Ashcroft, N.W.; Mermin (1976). Solid State Physics. N.D. Belmont, CA: Brooks/Cole.
- ^ 딩란도 665번지.
- ^ 사슬로338번길
- ^ 딩란도 666번지.
- ^ a b 기사 943.
- ^ a b 기사 976.
- ^ 단자 전압.Tiscali 참조.원래 허친슨 백과사전 출신이다.2007년 4월 7일 검색됨
- ^ 딩란도 674호.
- ^ 딩란도 677호.
- ^ "The Lemon Battery". ushistory.org. Archived from the original on 9 May 2007. Retrieved 10 April 2007.
- ^ ZOOM 활동: 페놈 포테이토 배터리.2007년 4월 10일에 접속.
- ^ 배터리 작동 방법 "배터리 실험: 볼타이 더미."2007년 4월 10일에 접속.
- ^ 딩란도 675번지.
- ^ 핑크, 11장 "배터리 및 연료 전지"
- ^ Franklin Leonard Pope, Electric Telegraph 15번째 판, D.반 노스트랜드 컴퍼니, 1899년, 페이지 7–11.인터넷 보관소에서 사용 가능
- ^ a b 듀라셀: 배터리 관리.2008년 8월 10일 회수
- ^ a b 알칼리성 망간 이산화 핸드북 및 사용 설명서(PDF).에너자이저.2008년 8월 25일 회수.
- ^ "Spotlight on Photovoltaics & Fuel Cells: A Web-based Study & Comparison" (PDF). pp. 1–2. Retrieved 14 March 2007.
- ^ "Lithium-Ion Battery Inventor Introduces New Technology for Fast-Charging, Noncombustible Batteries". University of Texas at Austin. University of Texas. 28 February 2017. Retrieved 15 March 2017.
- ^ Hislop, Martin (1 March 2017). "Solid-state EV battery breakthrough from Li-ion battery inventor John Goodenough". North American Energy News. The American Energy News. Retrieved 15 March 2017.
But even John Goodenough’s work doesn’t change my forecast that EVs will take at least 50 years to reach 70 to 80 percent of the global vehicle market.
- ^ Sony, Wayback Machine에서 2007년 10월 11일에 Archived By Sugar에 의해 구동되는 바이오 배터리를 개발하다.2007년 8월 24일에 접속.
- ^ 2009년 2월 6일 웨이백 머신에 보관된 다이너스티 VRLA 배터리와 응용 프로그램C&D 테크놀로지스 주식회사2008년 8월 26일 회수
- ^ 아모스, J. (2008년 8월 24일) "솔라 비행기는 기록적인 비행을 한다" BBC뉴스
- ^ "Elon Musk wins $50m bet with giant battery for South Australia". Sky News. 24 November 2017. Retrieved 20 September 2018.
- ^ Dillow, Clay (21 December 2012). "China Builds the World's Largest Battery, a Building-Sized, 36-Megawatt-Hour Behemoth Popular Science". Popsci.com. Retrieved 31 July 2013.
- ^ 콘웨이, E. (2008년 9월 2일) "알래스카에서 세계 최대 배터리가 켜졌다" Telegraph.co.uk
- ^ 비엘로, D. (2008년 12월 22일) "바람을 잡아라: 새로운 배터리로 풍력발전을 더욱 신뢰할 수 있게 할 수 있다" 과학계 미국인
- ^ "Auwahi Wind Energy Solutions Sempra U.S. Gas & Power, LLC". Semprausgp.com. Archived from the original on 2 May 2014. Retrieved 31 July 2013.
- ^ "Lithium Iron Disulfide Handbook and Application Manual" (PDF). energizer.com. Retrieved 20 September 2018.
- ^ 공기 산화제의 질량을 제외한다.
- ^ a b 배터리 지식 – AA 휴대용 전력 회사. 2007년 4월 16일 검색됨2007년 5월 23일 웨이백 머신에 보관
- ^ "Battery Capacity". techlib.com.
- ^ 2008년 12월 MIT 전기차 팀의 배터리 사양 이해 지침
- ^ Kang, B.; Ceder, G. (2009). "Battery materials for ultrafast charging and discharging". Nature. 458 (7235): 190–193. Bibcode:2009Natur.458..190K. doi:10.1038/nature07853. PMID 19279634. S2CID 20592628. 1:00–6:50(최소)2012년 2월 22일 웨이백 머신에 보관
- ^ 배터리의 자체 방전.부식 의사들.2007년 9월 9일 검색됨
- ^ Energizer 충전 가능 배터리 및 충전기: 질문과 대답 2009년 2월 9일 웨이백 머신에 보관.에너자이저.2009년 2월 3일 검색됨
- ^ "eneloop, environmentally friendly and energy saving batteries Panasonic eneloop". www.panasonic-eneloop.eu. Archived from the original on 2 February 2010.
- ^ a b 충전식 배터리 팁.NIMH 기술 정보.2007년 8월 10일 회수
- ^ 배터리 신화 vs 배터리 팩트.2007년 8월 10일 회수
- ^ Filip M. Gieszczykiewicz. "Sci.Electronics FAQ: More Battery Info". repairfaq.org.
- ^ RechargheableBatteryInfo.com, ed. (28 October 2005), What does 'memory effect' mean?, archived from the original on 15 July 2007, retrieved 10 August 2007
- ^ 리치, 빈센트(1994)국제 리드 트레이드.케임브리지:목두. 129.
- ^ Deep Cycle Battery FAQ 2010년 7월 22일 웨이백 머신에 보관.노스 애리조나 윈드 앤 선2009년 2월 3일 검색됨
- ^ 차량 및 딥 사이클 배터리 FAQ.레인보우 파워 컴퍼니.2009년 2월 3일 검색됨
- ^ Deep cycle 배터리 가이드 2009년 2월 17일 웨이백 머신에 보관.에너지 문제.2009년 2월 3일 검색됨
- ^ 야후에게 물어보기: 배터리를 냉동실에 넣어 두면 수명이 더 오래 가는가?2006년 4월 27일 웨이백 머신에 보관.2007년 3월 7일 검색됨
- ^ Hislop, Martin (1 March 2017). "Solid-state EV battery breakthrough from Li-ion battery inventor John Goodenough". North American Energy News. The American Energy News. Retrieved 15 March 2017.
- ^ "battery hazards". YouTube. Retrieved 20 September 2018.
- ^ 배터리EPA, 2007년 9월 11일 회수
- ^ 배터리 재활용 » Earth 911.2007년 9월 9일 검색됨
- ^ "샌프란시스코 감독관이 유독 배터리 폐기물을 겨냥하다"환경 뉴스 네트워크 (2001년 7월 11일)
- ^ 제품 안전 데이터시트.에너자이저(2페이지)2007년 9월 9일 검색됨
- ^ "Swallowed a Button Battery? Battery in the Nose or Ear?". Poison.org. 3 March 2010. Archived from the original on 16 August 2013. Retrieved 26 July 2013.
- ^ "Disk Battery Ingestion: Background, Pathophysiology, Epidemiology". 9 June 2016 – via eMedicine.
{{cite journal}}:Cite 저널은 필요로 한다.journal=(도움말) - ^ "Mercury-Containing and Rechargeable Battery Management Act" (PDF). EPA. Retrieved 15 February 2021.
- ^ "Battery Recycling in New York... it's the law!". call2recycle.org. Retrieved 2 June 2021.
- ^ Bill No. 1125 - Rechargeable Battery Recycling Act of 2006, State of California (PDF), 2006, retrieved 2 June 2021
- ^ "Archived copy". www.rbrc.org. Archived from the original on 12 August 2008. Retrieved 15 January 2022.
{{cite web}}: CS1 maint: 타이틀로 보관된 사본(링크) - ^ 사용후 배터리 및 축전지의 폐기.유럽 연합2009년 7월 27일 검색됨
- ^ "Guidelines on Portable Batteries Marking Requirements in the European Union 2008" (PDF). EPBA-EU. Archived from the original (PDF) on 7 October 2011.
- ^ Schweber, Bill (4 August 2015). "Lithium Batteries: The Pros and Cons". GlobalSpec. GlobalSpec. Retrieved 15 March 2017.
- ^ Fowler, Suzanne (21 September 2016). "Samsung's Recall – The Problem with Lithium Ion Batteries". The New York Times. New York. Retrieved 15 March 2016.
참고 문헌 목록
- Dingrando, Laurel; et al. (2007). Chemistry: Matter and Change. New York: Glencoe/McGraw-Hill. ISBN 978-0-07-877237-5. 21장(pp. 662–695)은 전기화학에 관한 것이다.
- Fink, Donald G.; H. Wayne Beaty (1978). Standard Handbook for Electrical Engineers, Eleventh Edition. New York: McGraw-Hill. ISBN 978-0-07-020974-9.
- Knight, Randall D. (2004). Physics for Scientists and Engineers: A Strategic Approach. San Francisco: Pearson Education. ISBN 978-0-8053-8960-9. Chs. 28–31 (pp. 879–995)에는 전위에 대한 정보가 수록되어 있다.
- Linden, David; Thomas B. Reddy (2001). Handbook of Batteries. New York: McGraw-Hill. ISBN 978-0-07-135978-8.
- Saslow, Wayne M. (2002). Electricity, Magnetism, and Light. Toronto: Thomson Learning. ISBN 978-0-12-619455-5. 8–9장(pp. 336–418)은 배터리에 대한 더 많은 정보를 가지고 있다.
외부 링크
 Wikimedia Commons의 전기 배터리와 관련된 미디어
Wikimedia Commons의 전기 배터리와 관련된 미디어- 컬리의 배터리
- 비충전식 배터리
- HowStuffWorks: 배터리 작동 방식
- 기타 배터리 셀 유형
- DoITPoMS 교육 및 학습 패키지 - "배터리"
- The Physics arXiv Blog (17 August 2013). "First Atomic Level Simulation of a Whole Battery MIT Technology Review". Technologyreview.com. Retrieved 21 August 2013.












 (는) 배터리(
(는) 배터리( (는) 배터리가 지속할 수 있는 시간(시간 단위)이다.
(는) 배터리가 지속할 수 있는 시간(시간 단위)이다. 1.3 전후의 상수다.
1.3 전후의 상수다.





