플로우 배터리
Flow battery
플로우 배터리 또는 레독스 플로우 배터리는 환원 산화 후, 화학 에너지가 액체에 용해된 두 개의 화학 구성 요소에 의해 공급되는 전기 화학 셀의 한 종류입니다. 두 개의 화학 구성 요소는 [2][3]막의 다른 측면에 있는 시스템을 통해 펌핑됩니다.이온 교환(전류의 흐름을 동반)은 두 액체가 각각의 공간에서 순환하는 동안 막을 통해 발생합니다.셀 전압은 Nernst 방정식에 의해 화학적으로 결정되며 실제 적용에서는 1.0 ~ 2.43V 범위입니다.
플로우 배터리는 연료전지(사용후 연료가 추출되고 시스템에 새로운 연료가 추가되는 경우) 또는 충전전지(전원이 연료의 재생을 구동하는 경우)와 같이 사용할 수 있습니다.분리 가능한 액체 탱크와 거의 무제한 수명과 같은 기존 충전기보다 기술적 이점이 있지만, 현재 구현은 상대적으로 덜 강력하며 더 정교한 전자 장치를 필요로 합니다.
에너지 용량은 전해질 부피의 함수이며, 전력은 전극 표면적의 함수입니다.
시공원칙
플로우 배터리는 화학에너지를 가역적으로 전기로 직접 변환하는 전기화학셀을 통해 하나 이상의 용해된 전기활성소자를 포함한 전해액이 흐르는 충전식 연료전지이다.전기 활성 소자는 "전극 반응에 참여할 수 있거나 [4]전극에 흡착될 수 있는 용액 중의 원소"입니다.추가적인 전해질은 외부, 일반적으로 탱크에 저장되며, 중력 공급 시스템도 [5]알려져 있지만 일반적으로 원자로의 셀(또는 셀)을 통해 펌프된다.플로우 배터리는 전해액(내연기관의 연료 탱크를 재충전하는 것과 유사한 방식으로)을 교체하는 동시에 재충전을 위해 사용 후 물질을 회수하여 신속하게 "재충전"할 수 있습니다.많은 플로우 배터리는 저비용과 적절한 전기 전도성 때문에 탄소 펠트 전극을 사용합니다.그러나 이러한 전극은 많은 산화환원 커플에 [6][7]대한 고유 활성이 낮기 때문에 전력 밀도를 다소 제한합니다.
즉, 플로우 배터리는 이온용액(전극용해액)이 (전극 주위의 셀이 아닌) 셀 외부에 저장되는[8] 특성을 가진 전기화학 셀이며, 전기를 생성하기 위해 셀에 공급될 수 있다.발생 가능한 총 전력량은 탱크 내 전해액의 양에 따라 달라집니다.
플로우 배터리는 전기화학공학에 [9]의해 확립된 설계원칙에 의해 관리됩니다.
종류들
무기 플로우[10] 배터리, 유기 플로우 배터리 [11]등 다양한 유형의 플로우 셀(배터리)이 개발되었습니다.각 범주에서 플로우 배터리 설계는 풀 플로우 배터리, 세미 플로우 배터리 및 무막 플로우 배터리로 더욱 분류할 수 있습니다.기존 배터리와 플로우 셀의 근본적인 차이점은 에너지가 기존 배터리의 전극 재료에 저장되는 반면 플로우 셀의 경우 전해질에 저장된다는 것입니다.플로우 배터리에 대한 특허 분류는 2021년 현재 완전히 개발되지 않았습니다.협동 특허 분류는 RFB를 재생 연료 전지의 하위 등급(H01M8/18)으로 간주하지만 연료 전지를 플로우 배터리의 하위 등급으로 간주하는 것이 더 적절하다.
무기류 전지
무기계 풀플로우 RFB
산화환원세포는 산화환원활성종이 액체(액체 또는 기체) 배지에 있는 가역세포이다.레독스 플로우 배터리는 충전 가능한(2차)[12] 전지입니다.고체 확산이나 인터캘레이션보다는 이종 전자 전달을 사용하기 때문에 기존 배터리(납산 또는 리튬 이온)보다는 연료 전지와 더 유사합니다.연료 전지가 배터리로 간주되지 않는 주된 이유는 원래 (1800년대에) 연료 전지가 비연소 전기화학적 과정을 통해 연료(및 공기)로부터 직접 전기를 생산하는 수단으로 등장했기 때문이다.그 후, 특히 1960년대와 1990년대에 충전식 연료 전지(즉
2
2, NASA의 헬리오스 프로토타입의 단위화된 재생 연료 전지 등)가 개발되었습니다.
레독스 플로우 배터리의 예로는 바나듐 레독스 플로우 배터리, 폴리황화 브롬화물 배터리(Regenesys), 철 레독스 플로우 배터리([13]IRFB) 및 우라늄 레독스 플로우 배터리가 있습니다.레독스 연료 전지는 많은 시스템이 [14][15][16][17]제안되었지만 상업적으로 덜 일반적이다.
바나듐 레독스 플로우 배터리는 에너지 및 전력 밀도가 제한적임에도 불구하고 다른 화학 물질에 비해 이점을 제공하므로 현재 가장 많이 시판되는 플로우 배터리입니다.양쪽 전극에 바나듐을 사용하므로 교차 오염이 발생하지 않습니다.그러나 바나듐 소금의 용해도가 제한적이기 때문에 실제로 이러한 장점이 상쇄됩니다.VRFB의 상업적 성공을 위해 더 중요한 것은 실제로 탄소/수산 계면의 전압 윈도우와 바나듐 산화환원 커플의 작동 전압 범위가 거의 완벽하게 일치한다는 것입니다.이는 저비용 탄소 전극의 내구성과 H2 및 O2 진화와 같은 부작용의 저충격성을 보장하며, 결과적으로 기록적인 긴 달력(15,000-20,000 사이클)과 수명(15,000-20,000 사이클)을 생성하며, 이는 다시 시스템 비용을 사용 가능한 에너지 사이클로 나눈 값)을 초래한다.왕복 효율).플로우 배터리의 수명이 길기 때문에 상대적으로 높은 자본 비용을 상각할 수 있습니다(바나듐, 탄소 펠트, 양극판, 막).VRFB의 에너지 평준화 비용은 대략 kWh당 수십 달러 또는 € 센트로 솔리드 스테이트 배터리보다 훨씬 낮으며 미국과 EC 정부 [18]기관이 밝힌 목표인 0.05달러와 0.05유로를 크게 벗어나지 않는다.광범위한 구현의 주요 과제로는 VO의 낮은 풍부성과25 높은 비용(> 30/Kg), VRFB의 원료, 수소와 산소 진화를 포함한 기생충 반응, 사이클링 중 VO의25 침전 등이 있다.대체 플로우 배터리 기술을 개발하는 주요 원동력이다.
기존의 플로우 배터리 화학은 비에너지가 낮고(전기차에 비해 너무 무거워짐) 비에너지가 낮습니다(정지된 에너지 저장에는 너무 비싸짐).그러나 수소-브로민 플로우 배터리는 1.4 W/cm의2 높은 출력이, 수소-브로민 플로우[19][20][21] 배터리는 높은 비 에너지(탱크 레벨에서 530 Wh/kg)가 확인되었다.
무기 반류 RFB
하이브리드 플로우 배터리는 고체층으로 [22]퇴적된 하나 이상의 전기식 구성 요소를 사용합니다.주요 단점은 솔리드 스테이트 전극을 사용할 경우 풀플로우 배터리에서 볼 수 있는 손실 분리 에너지 및 전력입니다.셀에는 배터리 전극 1개와 연료 전지 전극 1개가 있습니다.이 유형은 전극 표면적에 의해 에너지가 제한됩니다.하이브리드 플로우 배터리에는 아연-브로민, 아연-세륨,[23] 가용성 납-산 [24]및 철-소금 플로우 배터리가 포함됩니다.Weng 등은 실험 [25]OCV가 1.93V이고 작동 전압이 1.70V인 바나듐-금속 수소화물 충전식 하이브리드 플로우 배터리를 보고했는데, 이는 수성 전해질을 가진 충전식 플로우 배터리 중에서 상대적으로 높은 값입니다.이 하이브리드 배터리는 VOSOand
4 HSO
2
4 혼합 용액에서 작동하는 흑연 펠트 양극과 KOH 수용액에서 작동하는 금속 수소화물 음극으로 구성되어 있습니다.서로 다른 pH의 두 전해질은 양극성 막에 의해 분리된다.시스템은 쿨롱(95%), 에너지(84%), 전압(88%)에서 양호한 가역성과 높은 효율성을 보였습니다.그들은 이 산화환원 커플의 추가적인 개선과 함께 전류 밀도 증가, 더 큰2 100cm 전극의 포함 및 10개의 대형 셀의 연속 작동에 대한 성과를 보고했다.변동하는 시뮬레이션 전력 입력을 사용한 예비 데이터는 kWh 스케일 스토리지에 [26]대한 실행 가능성을 테스트했습니다.2016년에는 고에너지 밀도 Mn(VI)/Mn(VI)-Zn 하이브리드 플로우 배터리가 [27]제안되었다.
프로토타입의 아연-폴리오딘 플로우 배터리는 에너지 밀도가 167 Wh/l(리터당 와트 시간)인 것으로 나타났습니다.오래된 브롬화 아연 세포는 70 Wh/l에 도달한다.비교를 위해 리튬인산철 배터리는 233Wh/l를 저장한다.아연-폴리요오드 배터리는 산성 전해질이 없고, 불연성이며, 광범위한 냉각 회로가 필요 없는 -4~122°F(-20~50°C)의 작동 범위를 고려하면 다른 흐름 배터리보다 안전하다고 주장됩니다.한 가지 해결되지 않은 문제는 막에 침투할 수 있는 음극에 아연이 축적되어 효율을 떨어뜨리는 것입니다.Zn 덴드라이트가 생성되기 때문에 Zn-할라이드 배터리는 고전류 밀도(> 20 mA/cm2)에서 작동할 수 없으므로 전력 밀도가 제한됩니다.ZnI 배터리의 전해질에 알코올을 첨가하면 [28]문제를 해결할 수 있습니다.Zn/I RFB의 단점은 요오드화염의 고비용(> $20/Kg), Zn 증착의 제한된 면적 용량 또한 분리된 에너지와 전력을 손실하고 Zn 덴드라이트 생성에 있습니다.
배터리가 완전히 방전되면 두 탱크 모두 양전하 아연 이온(Zn2+
)과 음전하 요오드화 이온(I−
)의 혼합물로 동일한 전해질 용액을 유지합니다.충전 시 한 탱크에는 또 다른 음이온인 폴리요오드화물(I−
3)이 들어 있습니다.배터리는 외부 탱크에서 액체가 혼합된 배터리 스택 영역으로 액체를 펌핑하여 전력을 생산합니다.스택 내부에서 아연 이온은 선택적 막을 통과하여 스택의 음측에서 [29]금속 아연으로 바뀝니다.요오드화 아연 플로우 배터리의 에너지 밀도를 한층 더 높이기 위해서, 착화제로서 브롬화 이온
–(Br)을 이용해 유리 요오드를 안정화해,[30] 요오드 브롬화
2−
이온(IBR)을 형성해 전하 축적용의 요오드화 이온을 해방한다.
프로톤 플로우 배터리(PFB)는 금속 수소화물 저장 전극을 가역 양성자 교환막(PEM) 연료 전지에 통합합니다.충전 중에 PFB는 물을 쪼개서 발생하는 수소이온을 연료전지의 1개의 전극에 전자 및 금속입자와 결합시킨다.에너지는 고체 금속 수소화물 형태로 저장됩니다.방전은 과정이 역전되고 양성자가 주변 산소와 결합될 때 전기와 물을 생산합니다.리튬보다 저렴한 금속을 사용할 수 있고 리튬 [31][32]전지보다 더 높은 에너지 밀도를 제공합니다.
유기 흐름 배터리
바나듐 레독스 플로우 배터리, Zn-Br2 배터리 등 무기질인 레독스 플로우 배터리에 비해 2009년에는 유기 레독스 플로우 배터리가 등장했다.유기 레독스 플로우 배터리의 주된 매력은 활성 구성 요소의 조정 가능한 레독스 특성에 있습니다.2021년 현재 유기 RFB의 내구성은 낮습니다(즉, 달력 또는 주기 수명 또는 둘 다).이러한 이유로 무기 RFB만 상업적인 [33]규모로 시연되었습니다.
유기 레독스 플로우 배터리는 수성(AORFB)과 비수성(NAORFB)[34][35]으로 더욱 분류할 수 있다.AORFB는 전해질 재료의 용매로 물을 사용하는 반면, NAORFB는 유기 용매를 사용합니다.AORFB와 NAORFB는 토탈 및 하이브리드 유기 시스템으로 더욱 나눌 수 있다.전자는 유기 전극 재료만을 사용하고, 후자는 양극이나 음극에 무기 재료를 사용한다.대규모 에너지 저장소에서 낮은 용제 비용과 높은 전도성은 AORFB에 더 큰 상업적 잠재력을 제공할 뿐만 아니라 수성 전해질로부터 안전상의 이점을 제공합니다.대신 NAORFB는 훨씬 더 큰 전압 창을 제공하며 물리적 공간을 더 적게 차지합니다.
pH 중성 AORFB
pH 중성 AORFB는 pH7 조건에서 작동하며, 일반적으로 NaCl을 지지 전해질로 사용한다.pH 중성 조건에서는 유기 및 유기 금속 분자가 부식성 산성 및 알칼리성 조건보다 안정적입니다.예를 들어, AORFB에 사용되는 일반적인 캐솔리제인 K4[Fe(CN)]는 알칼리성 용액에서는 안정적이지 않지만 pH 중성 [36]조건이다.
AORFBs는 아놀리테로서 메틸비올로겐을, pH중성조건에서 캐솔리테로서 4-히드록시-2,2,6,6-테트라메틸피페리딘-1-옥실, NaCL 및 저비용 음이온 교환막을 사용했다.이 MV/TEMPO 시스템은 셀 전압이 1.25V로 가장 높고 자본 비용(180/k달러)이 가장 낮을 수 있습니다.Wh) AORFB에 대해 보고.수성 액체 전해질은 기존 인프라를 대체하지 않고 현재 시스템을 대체하기 위해 설계되었습니다.600밀리와트 테스트 배터리는 20~100mA/cm의2 전류 밀도에서 거의 100%의 효율로 100사이클 동안 안정적이었고, 40~50mA에서 최적의 성능 정격으로 배터리 원래 전압의 약 70%가 [37][38]유지되었습니다.중성 AORFB는 산성 또는 알칼리성 AORFB보다 환경 친화적일 수 있으며 부식성 RFB에 필적하는 전기 화학적 성능을 보일 수 있습니다.MV/TEMPO AORFB의 에너지 밀도는 8.4 Wh/L이며 TEMPO 측의 제한은 있습니다.비올로겐 기반의 플로우 배터리는 주로 유타 주립 대학의 류 교수 그룹에 의해 개발되어 왔다.2019년에는 10Wh/L의 에너지 밀도에서 1000사이클 동안 안정된 초경량 술폰산 비올로겐/페로시아니드 AORFB가 보고되었으며, 이는 지금까지 가장 안정적이고 에너지 밀도가 높은 AORFB이다.[39]
산성 AORFB
퀴논과 그 유도체는 많은 유기 산화 환원 시스템의 [40][41][42]기초이다.한 연구에서는 1,2-디히드로벤조퀴논-3,5-디술폰산(BQDS) 및 1,4-디히드로벤조퀴논-2-술폰산(BQS)이 음극으로 사용되었으며, 기존 Pb/PbSO는4 하이브리드산 AORFB의 아놀리테이트였다.퀴논은 기존의 캐솔리트에 비해 두 단위의 전하를 받아들이는데, 이는 이러한 배터리가 주어진 부피에서 두 배의 에너지를 저장할 수 있다는 것을 의미합니다.
또 다른 퀴논 9,10-안트라퀴논-2,7-디술폰산(AQDS)이 [43]평가되었다.AQDS는 황산 중 유리 상태의 탄소 전극에서 가역적인 2전자/2프로톤 환원을 빠르게 거칩니다.퀴논/히드로퀴논 커플링과 Br
2/Br−
레독스 커플링을 조합한 저렴한 탄소전극이 있는 수성유량배터리는 13,000A/m에서2 6000W/m를2 넘는 피크 갈바닉 전력밀도를 산출한다.사이클링에서는 사이클당 스토리지 용량 유지율이 99%를 넘었습니다.부피 에너지 밀도는 20 Wh/[44]L 이상이었다.음의 안트라퀴논-2-술폰산 및 안트라퀴논-2,6-디술폰산, 양의 1,2-디히드로벤조퀴논-3,5-디술폰산은 유해Br의2 사용을 회피한다.배터리는 [45]열화되지 않고 1,000 사이클 동안 지속된다고 주장되었습니다.이 시스템은 견고해 보이지만 낮은 셀 전압(0.55V 정도)과 낮은 에너지 밀도(< 4 Wh/L)를 가지고 있습니다.
전해질로 사용되는 하이드로브롬산은 독성이 낮은 알칼리 용액(1MKOH)과 페로시아니드로 [46]대체되었다.pH가 높을수록 부식성이 낮아 저렴한 폴리머 탱크를 사용할 수 있습니다.막의 전기 저항이 증가하면 전압 증가가 보상됩니다.셀 전압은 1.2V였습니다.[47][48]셀의 효율은 99%를 넘었고 왕복 효율은 84%였습니다.배터리는 최소 1,000 사이클의 예상 수명을 제공했습니다.이론적인 에너지 밀도는 19 Wh/[49]L였다.Ferrocyanide는 Fe(2OH) 또는 Fe(OH)3를 형성하지 않고 고 pH KOH 용액에서 화학적 안정성을 검증한 후 스케일업을 한다.
동일한 분자에 아놀리테와 캐솔리테를 모두 통합하는 것이 검토되었습니다.이러한 2관능 분석물질[50] 또는 콤비분자는[51] 두 탱크에 동일한 물질을 사용할 수 있게 한다.한 탱크에서는 전자 공여체이고 다른 탱크에서는 전자 공여체입니다.이는 [52]크로스오버의 효과를 감소시키는 등의 관련 이점이 있습니다.따라서 퀴논 디아미노안트라퀴논[52] 및 인디고계[50] 분자 및 TEMPO/페나딘[51] 결합 분자는 대칭 레독스 플로우 배터리(SRFB) 개발의 잠재적 전해질이다.
또 다른 접근법은 기증자/수령자로 블라터 래디칼을 채택했다.수용성은 [53]아니었지만 275번의 충전 및 방전 주기를 견뎌냈다.
알칼리성 AORFB
퀴논 분자는 알칼리성 AROFB에서 고분자로 사용되어 왔다.또 다른 아놀리테 후보로는 플루오레논이 있는데, 플루오레논은 수용성을 높이도록 재설계되었다.가역성 케톤(탈수소) 시연 셀은 촉매 없이 상온에서 1,111회 충전 사이클 동안 120일간 연속 작동하며 97%의 용량을 유지합니다.이 셀은 바나듐 기반 시스템의 [54][55]두 배 이상의 에너지 밀도를 제공합니다.알칼리성 AORFB의 주요 과제는 에너지 밀도가 5 Wh/L 미만으로 유지되는 안정적인 캐솔리테가 없다는 것입니다.보고된 모든 알칼리성 AORFB는 알칼리성 용액에서 페로시안화물의 안정성 문제로 인해 과도한 페로시안화칼륨 캐솔리테이트를 사용한다.
금속-유기 흐름 배터리는 산화 환원 활성 금속의 특성을 개선하기 위해 유기 배위자를 사용합니다.배위자는 EDTA와 같은 킬레이트일 수 있으며 전해질이 금속 아쿠오 착체가 침전되는 중성 또는 알칼리 상태에 있을 수 있습니다.유기배위자는 금속에 대한 물의 배위를 차단함으로써 금속촉매의 수분분할반응을 억제할 수 있어 고전압 전수계를 얻을 수 있다.예를 들어 1,3-프로판디아민테트라아세테이트(PDTA)에 맞춰 조정된 크롬을 사용하면 세포 전위는 페로시안화물 대 1.62V, 브롬화물 [56]대 2.13V로 기록됐다.금속-유기 흐름 배터리는 조정 화학 흐름 배터리로 알려져 있으며, 이는 록히드 마틴의 Gridstar Flow [57]기술의 배후에 있는 기술을 나타냅니다.
올리고머 RFB
올리고머 레독스 종 RFB는 저비용 막을 사용하면서 전기 활성종의 교차를 줄이기 위해 제안되었다.이러한 레독스 활성 올리고머는 레독시머로 알려져 있다.한 시스템은 유기 고분자와 셀룰로오스 막이 있는 식염수를 사용한다.시제품은 상당한 용량을 유지하면서 10,000번의 충전 주기를 거쳤습니다.에너지 밀도는 10 Wh/[58]l였습니다.전류 밀도가 100밀리암페어/[59]cm에2 도달했습니다.
또 다른 올리고머 RFB는 저비용 투석막과 조합하여 비올로겐 및 TEMPO 레드록시머를 사용한다.물에 용해된 기능성 고분자(아크릴 유리 또는 스티로폼과 유사)가 활성 전극 재료이다.크기 선택성 나노공막은 여과기처럼 작동하며 기존 이온 선택막보다 훨씬 쉽고 저렴한 비용으로 생산됩니다.그것은 작은 이온들이 [60]통과할 수 있게 하면서 큰 "스파게티"와 같은 고분자 분자를 유지합니다.이 개념은 전통적인 나피온 막의 높은 비용을 해결할 수 있지만 높은 수용성을 가진 레독스 활성 폴리머의 설계와 합성은 간단하지 않습니다.지금까지 올리고머 산화환원종을 가진 RFB는 경쟁력 있는 영역 고유 파워를 보여주지 않았다.낮은 동작 전류 밀도가 큰 산화 환원 분자의 본질적인 특징인지 아닌지는 명확하지 않다.
막이 없는
막이[61] 없는 배터리는 두 액체가 채널을 통해 펌핑되는 층류(layer flow)에 의존합니다. 여기서 두 액체가 전기화학 반응을 일으켜 에너지를 저장하거나 방출합니다.솔루션은 거의 혼재하지 않고 병렬로 스트리밍됩니다.흐름은 자연스럽게 액체를 분리하여 막이 [62]필요하지 않습니다.
막은 특정 반응물에 반복적으로 노출되면 부식될 수 있기 때문에 대부분의 경우 가장 비용이 많이 들고 신뢰성이 낮은 배터리 구성 요소입니다.막의 부재는 액체 브롬 용액과 수소의 사용을 가능하게 합니다: 막이 사용될 때 이 조합은 막이 파괴될 수 있는 수소 브롬산을 형성하기 때문에 문제가 있습니다.두 재료 모두 저렴한 [63]가격에 구입할 수 있습니다.이 설계에서는 두 전극 사이에 작은 채널을 사용합니다.액체 브롬은 흑연 캐소드를 통해 채널을 통과하고, 하이드로브롬산은 다공질 양극 아래로 흐릅니다.동시에 수소 가스가 양극을 가로질러 흐릅니다.화학 반응을 반전시켜 배터리를 충전할 수 있습니다. 이는 막이 없는 [63]설계로는 처음 있는 일입니다.2013년 8월에 발표된 이러한 무막 플로우 배터리의 최대 전력 밀도는 0.795mW/cm로2 다른 무막 시스템보다 3배 더 높고 리튬 이온 [63]배터리보다 훨씬 높습니다.
2018년에는 여러 사이클 동안 동일한 전해질 스트림을 재충전 및 재순환할 수 있는 매크로 스케일 무막 레독스 플로우 배터리가 시연되었습니다.배터리는 불용성 유기 캐솔리테와 수성 아놀리테 액체를 기반으로 하며,[64] 사이클링 시 대용량 유지 및 쿨롱 효율을 발휘합니다.
나노 네트워크
나노입자 네트워크 내에 배치된 리튬-황 시스템은 전도판과 직접 접촉하는 입자를 전하가 드나들 필요가 없습니다.대신, 나노 입자 네트워크는 액체 전체에 전기가 흐르도록 한다.이것은 더 많은 에너지를 [65]추출할 수 있게 해줍니다.
기타 Redox 플로우 배터리 화학 방법
다른 흐름형 배터리에는 아연-세륨 하이브리드 흐름 배터리, 아연-브로민 하이브리드 흐름 배터리 및 수소 브롬 배터리가 있습니다.
기타 흐름형 배터리
반고체
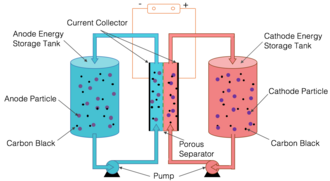
반고체 플로우 셀에서 정극과 부극이 캐리어 액체에 현탁된 입자로 구성되어 있다.양극 및 음극 서스펜션은 별도의 탱크에 저장되며 별도의 파이프를 통해 인접한 반응 챔버 스택으로 펌핑됩니다. 여기서 얇은 다공질 막과 같은 장벽에 의해 분리됩니다.이 접근법은 액체 전해액에 현탁된 전극 재료를 사용하는 수성 흐름 배터리의 기본 구조와 무탄소 서스펜션 및 전도성 탄소 네트워크와 [1][67][68]슬러리의 리튬 이온 배터리의 화학 작용을 결합합니다.카본 프리 준고체 산화 환원 플로우 배터리는 솔리드 분산 산화 환원 플로우 [69]배터리라고도 합니다.물질을 녹이면 화학적 성질이 크게 변한다.그러나 고체 재료의 비트를 현탁하면 고체의 특성이 유지됩니다.그 결과 [70]당밀처럼 흐르는 점성 현탁액입니다.
Redox-Targeted
산화 환원 표적 고체(ROTS)를 사용한 플로우 배터리도 최근에 개발된 또 다른 기술입니다.[71]
이러한 배터리에서는 양중합물 또는 네거티브 또는 둘 다(예: 산화환원액)가 전원 스택 외부의 탱크에 저장된 하나 이상의 고체 전기 활성 물질과 접촉합니다.레독스 유체는 하나 이상의 레독스 쌍으로 구성되며, 레독스 전위는 고체 전기 활성 물질의 레독스 전위 옆에 있다.이러한 고체에너지 부스터(SEB)를 탑재한 RFB는 기존 배터리(리튬 이온 등)의 높은 에너지 비장점과 플로우 배터리의 에너지 비장점을 결합합니다.SEB(ROTS) RFB는 반고체 RFB에 비해 몇 가지 장점이 있습니다. 예를 들어 비스코스 슬러리를 펌핑할 필요가 없고, 강수/폐쇄가 없으며, 영역별 전력량이 높으며, 내구성이 길고, 화학 설계 공간이 넓습니다.
화학
플로우 [2]배터리에 대한 광범위한 화학 작용이 시도되어 왔습니다.
| 커플 | 최대 셀 전압(V) | 평균 전극 전력 밀도(W/m2) | 평균 유체 에너지 밀도 | 사이클 |
|---|---|---|---|---|
| 브롬산수소-리튬 | 1.1 | 15,000 | 750 Wh/kg | |
| 염소산수소-리튬 | 1.4 | 10,000 | 1400 Wh/kg | |
| 브롬수소 | 1.07 | 7,950 | ||
| 철-주석 | 0.62 | 200 미만 | ||
| 철-티타늄 | 0.43 | 200 미만 | ||
| 철크롬 | 1.07 | 200 미만 | ||
| 아이언-아이언 | 1.21 | 1000 미만 | 20 Wh/L | 10,000 |
| 유기농 (2013) | 0.8 | 13,000 | 21.4 Wh/L | 10 |
| 유기농 (2015) | 1.2 | 7.1 Wh/L | 100 | |
| MV-TEMPO | 1.25 | 8.4 Wh/L | 100 | |
| 술폰산비올로겐(NH4)4[Fe(CN)6] | 0.9 | 500 이상 | 10 Wh/L | 1,000 |
| 금속-유기-페로시안화물[56] | 1.62 | 2,000 | 21.7 Wh/L | 75 |
| 금속-유기-브로민[56] | 2.13 | 3,000 | 35 Wh/L | 10 |
| 바나듐-바나듐(황산염) | 1.4 | ~800 | 25 Wh/L | |
| 바나듐-바나듐(브롬화물) | 50 Wh/L | 2,000[2] | ||
| 나트륨-브로민 폴리술피드 | 1.54 | ~800 | ||
| 나트륨-칼륨[72] | ||||
| 황산소염[73] | ||||
| 아연-브로민 | 1.85 | ~1,000 | 75 Wh/kg | 2,000 이상 |
| 납-산(메탄술폰산염) | 1.82 | ~1,000 | ||
| 아연-세륨(메탄술폰산염) | 2.43 | 1,200 ~ 2,500 미만 | ||
| Zn-Mn(VI)/Mn(VII) | 1.2 | 60 Wh/L[27] |
이점
redox 플로우 배터리와 하이브리드 플로우 배터리의 장점은 다음과 같습니다.
- 유연한 레이아웃(전원과 에너지 컴포넌트의 분리에 의한)
- 긴 사이클 수명(고체에서 고체로의 상전이 없기 때문에)
- 빠른 응답 시간
- "감압" 충전 필요 없음(모든 셀이 균등하게 충전되도록 배터리 과다 충전)
- 유해한 배기가스 없음.
또한 일부 유형은 충전 상태에 대한 간단한 판단(전압 의존), 유지보수가 적고 과충전/과방전에 대한 내구성을 제공합니다.
그들은 안전하다 왜냐하면
- 일반적으로 인화성 전해질을 포함하지 않는다
- 전해질은 전원 스택에서 멀리 떨어져 저장할 수 있습니다.
이러한 기술적 장점 때문에 레독스 플로우 배터리는 대규모 에너지 저장에 적합한 옵션입니다.
단점들
두 가지 주요 단점은 다음과 같습니다.
- 낮은 에너지 밀도(유용한 [citation needed]양의 에너지를 저장하기 위해 대량의 전해질 탱크가 필요함)
- 낮은 충전 및 방전 속도(다른 산업용 전극 프로세스와 비교).즉, 전극과 막 분리기가 커야 하므로 전력 [citation needed]비용이 증가합니다.
플로우 배터리는 일반적으로 연료 전지보다 에너지 효율은 높지만 리튬 이온 [74]배터리보다는 낮습니다.
적용들
플로우 배터리는 일반적으로 비교적 큰 (1 kWh – 10 MWh) 고정 애플리케이션에 [75]대해 고려됩니다.다음 용도가 있습니다.
- 부하 밸런싱 – 배터리가 전기 그리드에 연결되어 있어 사용량이 적은 시간대에 여분의 전력을 저장하고 수요가 많은 시간대에 전력을 방출합니다.이 응용 프로그램에서 대부분의 흐름 배터리 화학적 사용을 제한하는 일반적인 문제는 낮은 면적 전력(작동 전류 밀도)으로 인해 높은 전력 비용이 발생한다는 것입니다.
- 풍력이나 태양열과 같은 재생 가능한 소스에서 최대 [76]수요 기간 동안 방출되는 에너지를 저장한다.
- 피크 쉐이빙:[77][better source needed] 배터리로 수요 급증에 대응합니다.
- UPS: 주 전원이 중단되지 않는 전원 공급에 실패했을 때 배터리가 사용됩니다.
- 전력 변환 – 모든 셀이 동일한 전해질을 공유하기 때문입니다.따라서 전해질은 주어진 수의 셀을 사용하여 충전되고 다른 수의 셀로 방전될 수 있습니다.배터리의 전압은 사용된 셀 수에 비례하기 때문에 배터리는 매우 강력한 DC-DC 컨버터 역할을 할 수 있습니다.또한 셀의 수가 (입력 및/또는 출력 측에서) 지속적으로 변경되는 경우 AC/DC, AC/AC 또는 DC-AC로 변환될 수 있으며, 전환 기어의 [78]주파수에 의해 제한된다.
- 전기 자동차 – 전해질을 교체하여 플로우 배터리를 신속하게 "재충전"할 수 있기 때문에, 차량이 [79][80]연소식 차량만큼 빠르게 에너지를 소비해야 하는 용도로 사용할 수 있습니다.EV 애플리케이션의 대부분의 RFB 화학에서 흔히 볼 수 있는 문제는 짧은 주행 범위로 해석되는 낮은 에너지 밀도입니다.용해성이 높은 할로겐산염을 기반으로 하는 플로우 배터리는 주목할 만한 [81][better source needed]예외입니다.
- 독립형 전원 시스템 – 예를 들어, 그리드 전력을 사용할 수 없는 휴대 전화 기지국이 이에 해당합니다.배터리는 태양광 또는 풍력 발전원과 함께 사용되어 변동하는 전력 수준을 보상하고 발전기와 함께 사용되어 [82][83][better source needed]연료를 절약하기 위해 가장 효율적으로 사용할 수 있습니다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b Qi, Zhaoxiang; Koenig, Gary M. (12 May 2017). "Review Article: Flow battery systems with solid electroactive materials". Journal of Vacuum Science & Technology B, Nanotechnology and Microelectronics: Materials, Processing, Measurement, and Phenomena. 35 (4): 040801. Bibcode:2017JVSTB..35d0801Q. doi:10.1116/1.4983210. ISSN 2166-2746.
- ^ a b c Badwal, Sukhvinder P. S.; Giddey, Sarbjit S.; Munnings, Christopher; Bhatt, Anand I.; Hollenkamp, Anthony F. (24 September 2014). "Emerging electrochemical energy conversion and storage technologies". Frontiers in Chemistry. 2: 79. Bibcode:2014FrCh....2...79B. doi:10.3389/fchem.2014.00079. PMC 4174133. PMID 25309898.
- ^ Alotto, P.; Guarnieri, M.; Moro, F. (2014). "Redox Flow Batteries for the storage of renewable energy: a review". Renewable & Sustainable Energy Reviews. 29: 325–335. doi:10.1016/j.rser.2013.08.001.
- ^ Science-Dictionary.org 를 참조해 주세요."2013년 8월 27일 웨이백 머신에 보관된 전기 활성 물질" 2013년 5월 14일.
- ^ JP특허 S5671271A, 후지이, 도시노부, 히로세, 다카시 & 콘도, 나오키, 1981-06-13 「메탈로할로겐 2차전지」는 메이덴샤 전기 제조 주식회사에 할당.
- ^ Aaron, Douglas (2013). "In Situ Kinetics Studies in All-Vanadium Redox Flow Batteries". ECS Electrochemistry Letters. 2 (3): A29–A31. doi:10.1149/2.001303eel.
- ^ McCreery, Richard L. (July 2008). "Advanced Carbon Electrode Materials for Molecular Electrochemistry". Chemical Reviews. 108 (7): 2646–2687. doi:10.1021/cr068076m. ISSN 0009-2665. PMID 18557655.
- ^ "Researchers Drastically Reduce The Cost of Redox Flow Batteries [$25 Per kWh]". TechReportArticles. 29 January 2021.
- ^ Arenas, L.F.; Ponce de León, C.; Walsh, F.C. (June 2017). "Engineering aspects of the design, construction and performance of modular redox flow batteries for energy storage" (PDF). Journal of Energy Storage. 11: 119–153. doi:10.1016/j.est.2017.02.007.
- ^ Hu, B.; Luo, J.; DeBruler C.; Hu, M; Wu, W.; Liu, T. L. (2019). Redox Active Inorganic Materials for Redox Flow Batteries in Encyclopedia of Inorganic and Bioinorganic Chemistry: Inorganic Battery Materials. pp. 1–25.
{{cite book}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Luo, J.; Hu, B.; Hu, M.; Liu, T. L. (13 September 2019). "Status and Prospects of Organic Redox Flow Batteries towards Renewable Energy Storage". ACS Energy Lett. 2019, 4 (9): 2220–2240. doi:10.1021/acsenergylett.9b01332. S2CID 202210484.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ 린든, D.; 레디, T.B. (2002년)배터리 핸드북(Ed.)맥그로 힐.
- ^ Shiokawa, Y.; Yamana, H.; Moriyama, H. (2000). "An Application of Actinide Elements for a Redox Flow Battery". Journal of Nuclear Science and Technology. 37 (3): 253–256. doi:10.1080/18811248.2000.9714891. S2CID 97891309.
- ^ 미국 특허 567959, Borchers, William, "연료의 화학 에너지를 전기에너지로 변환하는 과정", 1896-09-22 발행
- ^ DE 특허 264026, Nernst, Walther, "Brennstoffelement mit unangreifbaren Electroden [난공불락 전극이 있는 연료전지]", 1912-06-15 출판
- ^ 미국 특허 3682704, Keefer, Richard Macay, "Redox fuel cell regenerated with sugar."는 1972-08-08 Electrocell Ltd.에 할당되었습니다.
- ^ Kummer, J. T.; Oei, D. -G. (1985). "A chemically regenerative redox fuel cell. II". Journal of Applied Electrochemistry. 15 (4): 619–629. doi:10.1007/BF01059304. S2CID 96195780.
- ^ Spagnuolo, G.; Petrone, G.; Mattavelli, P.; Guarnieri, M. (2016). "Vanadium Redox Flow Batteries: Potentials and Challenges of an Emerging Storage Technology". IEEE Industrial Electronics Magazine. 10 (4): 20–31. doi:10.1109/MIE.2016.2611760. hdl:11577/3217695. S2CID 28206437.
- ^ Cho, Kyu Taek; Tucker, Michael C.; Ding, Markus; Ridgway, Paul; Battaglia, Vincent S.; Srinivasan, Venkat; Weber, Adam Z. (2015). "Cyclic Performance Analysis of Hydrogen/Bromine Flow Batteries for Grid-Scale Energy Storage". ChemPlusChem. 80 (2): 402–411. doi:10.1002/cplu.201402043.
- ^ Yu; Tolmachev, V. (2013). "Hydrogen-halogen electrochemical cells: A review of applications and technologies". Russian Journal of Electrochemistry. 50 (4): 301–316. doi:10.1134/S1023193513120069. S2CID 97464125.
- ^ Tolmachev, Yuriy V. (2015). "Energy cycle based on a high specific energy aqueous flow battery and its potential use for fully electric vehicles and for direct solar-to-chemical energy conversion". Journal of Solid State Electrochemistry. 19 (9): 2711–2722. doi:10.1007/s10008-015-2805-z. S2CID 97853351.
- ^ Bartolozzi, M. (1989). "Development of redox flow batteries. A historical bibliography". Journal of Power Sources. 27 (3): 219–234. Bibcode:1989JPS....27..219B. doi:10.1016/0378-7753(89)80037-0.
- ^ Leung, P. K.; Ponce-De-León, C.; Low, C. T. J.; Shah, A. A.; Walsh, F. C. (2011). "Characterization of a zinc–cerium flow battery". Journal of Power Sources. 196 (11): 5174–5185. Bibcode:2011JPS...196.5174L. doi:10.1016/j.jpowsour.2011.01.095.
- ^ Krishna, M.; Fraser, E. J.; Wills, R. G. A.; Walsh, F. C. (1 February 2018). "Developments in soluble lead flow batteries and remaining challenges: An illustrated review". Journal of Energy Storage. 15: 69–90. doi:10.1016/j.est.2017.10.020. ISSN 2352-152X.
- ^ J. 전기화학Soc. 2013년 제160권, 제9호, A1384-A1389
- ^ J. 전기화학Soc. 2016년 제163권, 제1호, A5180-A5187호
- ^ a b Colli, Alejandro N.; Peljo, Pekka; Girault, Hubert H. (2016). "High energy density MnO4−/MnO42− redox couple for alkaline redox flow batteries" (PDF). Chemical Communications. 52 (97): 14039–14042. doi:10.1039/C6CC08070G. PMID 27853767.
- ^ Borghino, Dario (27 February 2015). "High-performance flow battery could rival lithium-ions for EVs and grid storage". Gizmag.
- ^ White, Frances (25 February 2015). "New flow battery to keep big cities lit, green and safe". R&D.
- ^ Weng, Guo-Ming (2017). "Unlocking the capacity of iodide for high-energy-density zinc/polyiodide and lithium/polyiodide redox flow batteries". Energy & Environmental Science. 10 (3): 735–741. doi:10.1039/C6EE03554J.
- ^ "Proton flow battery simplifies hydrogen power". Gizmag.com. 13 February 2014. Retrieved 13 February 2014.
- ^ Andrews, J.; Seif Mohammadi, S. (2014). "Towards a 'proton flow battery': Investigation of a reversible PEM fuel cell with integrated metal-hydride hydrogen storage". International Journal of Hydrogen Energy. 39 (4): 1740–1751. doi:10.1016/j.ijhydene.2013.11.010.
- ^ M.Aziz et al.수성 유기 레독스 플로우 배터리의 전해질 수명: 비판적 검토.화학 리뷰 2020, 120, 6467-6489.
- ^ Brushett, Fikile; Vaughey, John; Jansen, Andrew (2012). "An All‐Organic Non‐aqueous Lithium‐Ion Redox Flow Battery". Advanced Functional Materials. 2 (11): 1390–1396. doi:10.1002/aenm.201200322. S2CID 97300070.
- ^ Bamgbopa, Musbaudeen O.; Shao-Horn, Yang; Almheiri, Saif (2017). "The potential of non-aqueous redox flow batteries as fast-charging capable energy storage solutions: demonstration with an iron–chromium acetylacetonate chemistry". Journal of Materials Chemistry A. 5 (26): 13457–13468. doi:10.1039/c7ta02022h. ISSN 2050-7488.
- ^ Luo, J.; Sam, A.; Hu, B.; DeBruler C.; Liu, T. L. (2017). "Unraveling pH Dependent Cycling Stability of Ferricyanide / Ferrocyanide in Redox Flow Batteries". Nano Energy. 2017, 42: 215–221. doi:10.1016/j.nanoen.2017.10.057.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Moss, Richard (22 December 2015). "New flow battery projected to cost 60% less than existing standard". www.gizmag.com. Retrieved 23 December 2015.
- ^ Liu, Tianbiao; Wei, Xiaoliang; Nie, Zimin; Sprenkle, Vincent; Wang, Wei (1 November 2015). "A Total Organic Aqueous Redox Flow Battery Employing a Low Cost and Sustainable Methyl Viologen Anolyte and 4-HO-TEMPO Catholyte". Advanced Energy Materials. 6 (3): 1501449. doi:10.1002/aenm.201501449. ISSN 1614-6840. S2CID 97838438.
- ^ Luo, J.; Hu, B.; DeBruler C.; Zhao, Y., Yuan B. Hu, M. Wu, W. Liu, T. L. "Unprecedented Capacity and Stability of Ammonium Ferrocyanide Catholyte in pH Neutral Aqueous Redox Flow Batteries". Joule. 4: 149–163.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Gong, K; Fang, Q; Gu, S; Li, F.S.Y.; Yan, Y (2015). "Nonaqueous redox-flow batteries: organic solvents, supporting electrolytes, and redox pairs". Energy and Environmental Science. 8 (12): 3515–3530. doi:10.1039/C5EE02341F.
- ^ Xu, Y.; Wen, Y.; Cheng, Y.; Y., Y., Y.; Xie, Z. Cao, G. In World Non-Grid-Connected 풍력 및 에너지 컨퍼런스, 2009. WNWEC 2009 IEEE: 중국 난징, 2009, 페이지 1.
- ^ Xu, Yan; Wen, Yue-Hua; Cheng, Jie; Cao, Gao-Ping; Yang, Yu-Sheng (2010). "A study of tiron in aqueous solutions for redox flow battery application". Electrochimica Acta. 55 (3): 715–720. doi:10.1016/j.electacta.2009.09.031. ISSN 0013-4686.
- ^ WALD, MATTHEW L. (8 January 2014). "From Harvard, a Cheaper Storage Battery". New York Times. Retrieved 10 January 2014.
- ^ "Harvard team demonstrates new metal-free organic–inorganic aqueous flow battery; potential breakthrough for low-cost grid-scale storage". 11 January 2014.
- ^ Szondy, David (29 June 2014). "New water-based organic battery is cheap, rechargeable and eco-friendly". Gizmag.
- ^ "A rechargeable battery to power a home from rooftop solar panels". phys.org.
- ^ Matthew Gunther,ChemistryWorld. "Flow Battery Could Smooth Irregular Wind and Solar Energy Supply". Scientific American.
- ^ 알칼리성 퀴논 플로우 배터리 Lin 등사이언스 2015 349 (6255) 페이지 1529
- ^ Borghino, Dario (30 September 2015). "Greener, safer flow battery could store renewable energy on the cheap". www.gizmag.com. Retrieved 8 December 2015.
- ^ a b Carretero-González, Javier; Castillo-Martínez, Elizabeth; Armand, Michel (2016). "Highly water-soluble three-redox state organic dyes as bifunctional analytes". Energy & Environmental Science. 9 (11): 3521–3530. doi:10.1039/C6EE01883A. ISSN 1754-5692.
- ^ a b Winsberg, Jan; Stolze, Christian; Muench, Simon; Liedl, Ferenc; Hager, Martin D.; Schubert, Ulrich S. (11 November 2016). "TEMPO/Phenazine Combi-Molecule: A Redox-Active Material for Symmetric Aqueous Redox-Flow Batteries". ACS Energy Letters. 1 (5): 976–980. doi:10.1021/acsenergylett.6b00413. ISSN 2380-8195.
- ^ a b Potash, Rebecca A.; McKone, James R.; Conte, Sean; Abruña, Héctor D. (2016). "On the Benefits of a Symmetric Redox Flow Battery". Journal of the Electrochemical Society. 163 (3): A338–A344. doi:10.1149/2.0971602jes. ISSN 0013-4651. OSTI 1370440.
- ^ Lavars, Nick (17 March 2022). "Symmetrical flow battery may strike right balance for grid-scale storage". New Atlas. Retrieved 18 March 2022.
- ^ Lavars, Nick (21 May 2021). "Candle compound brings high density to grid-scale battery technology". New Atlas. Retrieved 26 May 2021.
- ^ Feng, Ruozhu; Zhang, Xin; Murugesan, Vijayakumar; Hollas, Aaron; Chen, Ying; Shao, Yuyan; Walter, Eric; Wellala, Nadeesha P. N.; Yan, Litao; Rosso, Kevin M.; Wang, Wei (21 May 2021). "Reversible ketone hydrogenation and dehydrogenation for aqueous organic redox flow batteries". Science. 372 (6544): 836–840. Bibcode:2021Sci...372..836F. doi:10.1126/science.abd9795. ISSN 0036-8075. PMID 34016776. S2CID 234794555.
- ^ a b c Robb, Brian H.; Farrell, Jason M.; Marshak, Michael P. (2019). "Chelated Chromium Electrolyte Enabling High-Voltage Aqueous Flow Batteries". Joule. 3 (10): 2503–2512. doi:10.1016/j.joule.2019.07.002.
- ^ "Energy Storage: GridStar Flow". Lockheed Martin. Retrieved 27 July 2020.
- ^ "Chemists present an innovative redox-flow battery based on organic polymers and water". phys.org. Phys.org. 21 October 2015. Retrieved 6 December 2015.
- ^ Janoschka, Tobias; Martin, Norbert; Martin, Udo; Friebe, Christian; Morgenstern, Sabine; Hiller, Hannes; Hager, Martin D.; Schubert, Ulrich S. (2015). "An aqueous, polymer-based redox-flow battery using non-corrosive, safe, and low-cost materials". Nature. 527 (7576): 78–81. Bibcode:2015Natur.527...78J. doi:10.1038/nature15746. PMID 26503039. S2CID 4393601.
- ^ Janoschka, Tobias; Martin, Norbert; Martin, Udo; Friebe, Christian; Morgenstern, Sabine; Hiller, Hannes; Hager, Martin D.; Schubert, Ulrich S. (2015). "An aqueous, polymer-based redox-flow battery using non-corrosive, safe, and low-cost materials". Nature. 527 (7576): 78–81. Bibcode:2015Natur.527...78J. doi:10.1038/nature15746. PMID 26503039. S2CID 4393601.
- ^ Bamgbopa, Musbaudeen O.; Almheiri, Saif; Sun, Hong (2017). "Prospects of recently developed membraneless cell designs for redox flow batteries". Renewable and Sustainable Energy Reviews. 70: 506–518. doi:10.1016/j.rser.2016.11.234. ISSN 1364-0321.
- ^ Braff, William A.; Bazant, Martin Z.; Buie, Cullen R. (2013). "New rechargeable flow battery enables cheaper, large-scale energy storage". Nature Communications. 4: 2346. arXiv:1404.0917. Bibcode:2013NatCo...4.2346B. doi:10.1038/ncomms3346. PMID 23949161. S2CID 14719469. Retrieved 20 August 2013.
- ^ a b c Braff, W. A.; Bazant, M. Z.; Buie, C. R. (2013). "Membrane-less hydrogen bromine flow battery". Nature Communications. 4: 2346. arXiv:1404.0917. Bibcode:2013NatCo...4.2346B. doi:10.1038/ncomms3346. PMID 23949161. S2CID 14719469.
- ^ Bamgbopa, Musbaudeen O.; Shao-Horn, Yang; Hashaikeh, Raed; Almheiri, Saif (2018). "Cyclable membraneless redox flow batteries based on immiscible liquid electrolytes: Demonstration with all-iron redox chemistry". Electrochimica Acta. 267: 41–50. doi:10.1016/j.electacta.2018.02.063. ISSN 0013-4686.
- ^ Kevin Bullis (24 April 2014). "Nanoparticle Networks Promise Cheaper Batteries for Storing Renewable Energy". MIT Technology Review. Retrieved 24 September 2014.
- ^ Qi, Zhaoxiang; Koenig, Gary M. (2017). "Review Article: Flow battery systems with solid electroactive materials". Journal of Vacuum Science & Technology B, Nanotechnology and Microelectronics: Materials, Processing, Measurement, and Phenomena. 35 (4): 040801. Bibcode:2017JVSTB..35d0801Q. doi:10.1116/1.4983210. ISSN 2166-2746.
- ^ Duduta, Mihai (May 2011). "Semi-Solid Lithium Rechargeable Flow Battery". Advanced Energy Materials. 1 (4): 511–516. doi:10.1002/aenm.201100152. S2CID 97634258.
- ^ Qi, Zhaoxiang; Koenig Jr., Gary M. (15 August 2016). "A carbon-free lithium-ion solid dispersion redox couple with low viscosity for redox flow batteries". Journal of Power Sources. 323: 97–106. Bibcode:2016JPS...323...97Q. doi:10.1016/j.jpowsour.2016.05.033.
- ^ Qi, Zhaoxiang; Liu, Aaron L.; Koenig Jr, Gary M. (20 February 2017). "Carbon-free Solid Dispersion LiCoO2 Redox Couple Characterization and Electrochemical Evaluation for All Solid Dispersion Redox Flow Batteries". Electrochimica Acta. 228: 91–99. doi:10.1016/j.electacta.2017.01.061.
- ^ Chandler, David L. (23 August 2011). "Go with the Flow – Cambridge Crude". Technology Review.
- ^ {{ (2) 대규모 에너지 저장용 레독스-타겟팅 기반 플로우 배터리.Advanced Materials 2018, 30, 13. (3) 타겟팅 기반 플로우 배터리.Journal of Physics 2019, 52, 17. (4) Redox Targeting은 플로우 배터리를 개선합니다.Joule 2019, 3, 2066-2067. (5) pH-Neutral 수성 유기 레독스 플로우 배터리를 위한 싱글 분자 레독스 타깃링 반응.Angewandte Chemie-International Edition 2020, 59, 14286-14291. (6) 에너지 재료의 레독스 타깃팅.전기화학 2021, 29, 7. (7) 에너지 저장 및 변환을 위한 에너지 재료의 레독스 타겟팅에 관한 현재의 의견.어드밴스드 머티리얼 2021, 2104562 (2104519)}}
- ^ Bush, Steve (20 July 2018). "Room-temperature flow battery uses liquid sodium-potassium alloy".
- ^ Li, Zheng; Sam Pan, Menghsuan; Su, Liang; Tsai, Ping-Chun; Badel, Andres F.; Valle, Joseph M.; Eiler, Stephanie L.; Xiang, Kai; Brushett, Fikile R.; Chiang, Yet-Ming (11 October 2017). "Air-Breathing Aqueous Sulfur Flow Battery for Ultralow-Cost Long-Duration Electrical Storage". Joule. 1 (2): 306–327. doi:10.1016/j.joule.2017.08.007.
- ^ Xu, Q.; Ji, Y.N.; Qin, L.Y.; Leung, P.K.; Qiao, F.; Li, Y.S.; Su, H.N. (2018). ""Evaluation of redox flow batteries goes beyond round-trip efficiency: A technical review"". Journal of Energy Storage. 16: 108–116. doi:10.1016/j.est.2018.01.005.
- ^ Service, R.F. (2 November 2018). "Advances in flow batteries promise cheap backup power". Science. 362 (6414): 508–509. Bibcode:2018Sci...362..508S. doi:10.1126/science.362.6414.508. PMID 30385552. S2CID 53218660.
- ^ REDT Energy. "Storing Renewable Energy". Archived from the original on 1 February 2014. Retrieved 27 January 2014.
- ^ [1] 2010년 2월 9일 Wayback Machine에서 아카이브 완료
- ^ WO 특허 03043170, Spaziante, Placido Maria; Kampanatsanyakorn, Krisada & Zocchi, Andrea, 2003-05-22에 의해 발행된 "가변 전압과 주파수로 에너지를 저장 및/또는 변환하는 시스템"
- ^ "Electric Vehicle Refuelling System (EVRS) used in conjunction with Vanadium Redox Flow Technology". REDT Energy Storage. Archived from the original on 10 December 2011.
{{cite web}}: CS1 유지보수: 부적합한 URL(링크) - ^ Antony Ingram. "nanoFLOWCELL-powered Quant e-Limo approved for german road trials". Fox News.
- ^ Tolmachev, Yuriy V.; Piatkivskyi, Andrii; Ryzhov, Victor V.; Konev, Dmitry V.; Vorotyntsev, Mikhail A. (2015). "Energy cycle based on a high specific energy aqueous flow battery and its potential use for fully electric vehicles and for direct solar-to-chemical energy conversion". Journal of Solid State Electrochemistry. 19 (9): 2711–2722. doi:10.1007/s10008-015-2805-z. S2CID 97853351.
- ^ Deeya energy의 John Davis가 YouTube를 통해 자사의 플로우 배터리가 텔레콤 업계에서 사용되는 것에 대해 설명합니다.
- ^ "Performance Testing of Zinc-Bromine Flow Batteries for Remote Telecom Sites" (PDF).