생장배지
Growth medium
성장 배지 또는 배양 배지는 세포 증식[1] 과정 또는 이끼 Physcomitrella patens와 같은 작은 식물을 통해 미생물 또는 세포 집단의 성장을 지원하도록 설계된 고체, 액체 또는 반고체입니다.[2] 다양한 유형의 세포를 성장시키는 데 다양한 유형의 배지가 사용됩니다.[3]
크게 두 가지 유형의 성장 배지는 식물이나 동물에서 유래한 특정 세포 유형을 사용하는 세포 배양에 사용되는 배지와 박테리아나 곰팡이와 같은 미생물을 성장시키는 데 사용되는 미생물 배양에 사용되는 배지입니다. 미생물의 가장 일반적인 성장 배지는 영양 배지와 한천 플레이트입니다. 미생물과 세포 배양 성장에 특화된 배지가 필요한 경우도 있습니다.[1] 까다로운 유기체라고 불리는 일부 유기체는 복잡한 영양 요구 사항으로 인해 전문화된 환경이 필요합니다. 예를 들어, 바이러스는 절대적인 세포 내 기생충이며 살아있는 세포를 포함하는 성장 배지를 필요로 합니다.
종류들


미생물의 가장 일반적인 성장 배지는 영양 배지(액체 영양 배지) 또는 용원 배지입니다. 액체 배지는 종종 한천과 혼합되고 멸균 배지 디스펜서를 통해 페트리 플레이트에 부어 응고됩니다. 이 한천 플레이트는 미생물을 배양할 수 있는 고체 배지를 제공합니다. 한천을 분해할 수 있는 박테리아는 거의 없기 때문에 고체 상태를 유지합니다(예를 들어 Cytophaga, Flavobacterium, Bacillus, Pseudomonas 및 Alcaligenes 속의 일부 종 제외). 액체 배양에서 자란 박테리아는 종종 콜로이드 현탁액을 형성합니다.[4][5]
세포 배양에 사용되는 성장 배지와 미생물 배양에 사용되는 성장 배지의 차이점은 전체 유기체에서 유래하고 배양에서 성장한 세포가 종종 생체 내에서 일반적으로 발생하는 호르몬 또는 성장 인자의 첨가 없이 성장할 수 없다는 것입니다.[6] 동물 세포의 경우 혈액 혈청 또는 합성 혈청 대체물을 배지에 첨가하여 이러한 어려움을 해결하는 경우가 많습니다. 미생물의 경우 단세포 생물인 경우가 많기 때문에 그러한 제한이 존재하지 않습니다. 또 다른 주요 차이점은 배양 중인 동물 세포가 그들이 부착하는 평평한 표면에서 자라는 경우가 많으며, 배지는 세포를 덮는 액체 형태로 제공된다는 것입니다. 대조적으로 대장균과 같은 박테리아는 고체 또는 액체 배지에서 성장할 수 있습니다.
성장 배지 유형 간의 중요한 차이점은 화학적으로 정의된 배지와 정의되지 않은 배지 간의 차이점입니다.[1] 정의된 배지에는 모든 성분의 알려진 양이 있습니다. 미생물의 경우 미생물이 필요로 하는 미량 원소와 비타민, 특히 정의된 탄소 및 질소 공급원을 제공하는 것으로 구성됩니다. 탄소원으로는 포도당이나 글리세롤이, 무기 질소원으로는 암모늄염이나 질산염이 많이 사용됩니다. 정의되지 않은 배지에는 효모 추출물 또는 카제인 가수분해물과 같은 일부 복잡한 성분이 있으며, 이 성분은 알려지지 않은 비율로 많은 화학 종의 혼합물로 구성됩니다. 정의되지 않은 배지는 가격을 기준으로 선택되기도 하고 필요에 따라 선택되기도 합니다. 일부 미생물은 정의된 배지에서 배양된 적이 없습니다.
성장 배지의 좋은 예는 맥주를 만드는 데 사용되는 맥아즙입니다. 맥아즙에는 효모 성장에 필요한 모든 영양소가 함유되어 있으며, 혐기성 조건에서는 알코올이 생성됩니다. 발효 과정이 완료되면 중간 미생물과 휴면 미생물, 이제 맥주의 조합이 소비 준비가 됩니다. 주요 유형은 다음과 같습니다.
- 교양 매체
- 최소한의 매체
- 선별 매체
- 차등 매체
- 수송 매체
- 지표 매체
문화매체
배양 배지에는 대부분의 세균이 성장에 필요한 모든 요소가 포함되어 있고 선택적이지 않기 때문에 실험실 배양 모음에 보관된 세균의 일반적인 배양 및 유지에 사용됩니다.

정의되지 않은 매체(기저 또는 복합 매체라고도 함)는 다음을 포함합니다.
- 포도당과 같은 탄소원
- 물.
- 각종 염류
- 아미노산과 질소의 공급원(예: 쇠고기, 효모 추출물)
아미노산 공급원에 다양한 화합물이 포함되어 있기 때문에 정확한 조성을 알 수 없기 때문에 이것은 정의되지 않은 매체입니다.
정의된 매체(화학적으로 정의된 매체 또는 합성 매체라고도 함)는 다음과 같은 매체입니다.
- 사용된 모든 화학 물질은 알려져 있습니다.
- 효모, 동물 또는 식물 조직이 없습니다.
영양 배지의 예:
최소 미디어
성장을 지원할 수 있는 충분한 성분을 가진 정의된 배지를 "최소 배지"라고 합니다. 최소 배지에 첨가해야 하는 성분의 수는 어떤 미생물을 키우느냐에 따라 엄청나게 다릅니다.[7] 최소 배지는 일반적으로 아미노산이 없는 집락 성장에 가능한 최소 영양소를 포함하는 배지이며 미생물학자와 유전학자가 "야생형" 미생물을 성장시키는 데 자주 사용합니다. 최소 배지를 사용하여 재조합 또는 접합체에 대해 선택하거나 반대할 수도 있습니다.
최소 매체는 일반적으로 다음을 포함합니다.
- 포도당과 같은 설탕이거나 석시네이트와 같은 에너지가 덜 풍부한 공급원일 수 있는 탄소 공급원
- 박테리아 종과 성장 조건에 따라 다를 수 있는 다양한 염; 이들은 일반적으로 박테리아가 단백질과 핵산을 합성할 수 있도록 마그네슘, 질소, 인 및 황과 같은 필수 요소를 제공합니다.
- 물.
보충 최소 배지는 선택된 단일 제제(일반적으로 아미노산 또는 설탕)를 포함하는 최소 배지입니다. 이 보충제를 사용하면 영양요구성 재조합의 특정 라인을 배양할 수 있습니다.
선택적 매체


선택적 배지는 선택된 미생물의 성장에만 사용됩니다. 예를 들어, 미생물이 암피실린이나 테트라사이클린과 같은 특정 항생제에 내성을 가지고 있다면, 그 항생제를 배지에 첨가하여 내성을 가지고 있지 않은 다른 세포가 자라지 않도록 할 수 있습니다. 프롤린과 같은 아미노산이 없는 배지와 이를 합성할 수 없는 대장균은 유전체학이 등장하기 전에 세균 염색체를 매핑하는 데 유전학자들이 흔히 사용했습니다.
선택적 성장 배지는 항생제 내성 또는 특정 대사산물을 합성하는 능력과 같은 특정 특성을 가진 세포의 생존 또는 증식을 보장하기 위해 세포 배양에도 사용됩니다. 일반적으로 특정 유전자 또는 유전자의 대립유전자의 존재는 세포에 선택적 배지에서 성장하는 능력을 부여합니다. 이러한 경우 유전자를 마커라고 합니다.
진핵세포의 선택적 성장 배지는 일반적으로 네오마이신 내성 유전자를 표지자로 하는 플라스미드로 성공적으로 형질감염된 세포를 선별하기 위해 네오마이신을 함유하고 있습니다. 간시클로비르는 각각의 마커인 헤르페스 심플렉스 바이러스 티미딘 키나제를 운반하는 세포를 구체적으로 죽이는 데 사용되기 때문에 이 규칙의 예외입니다.
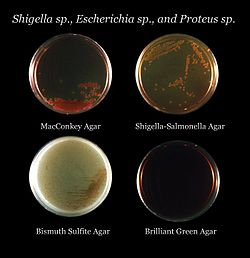
선택적 미디어의 예:
- 에오신 메틸렌 블루는 그람 양성균에 독성이 있는 염료를 함유하고 있습니다. 대장균군을 위한 선택적이고 차별적인 배지입니다.
- YM(효모 추출물 한천)은 pH가 낮아 세균 증식을 억제합니다.
- MEA(malt extract agar)는 pH가 낮아 세균 증식을 억제합니다.
- 맥콘키 한천은 그람 음성 박테리아용입니다.
- 헥토엔 장 한천은 그람 음성 박테리아에 대해 선택적입니다.
- HIS-선택 배지는 아미노산 히스티딘이 결핍된 유형의 세포 배양 배지입니다.
- 만니톨 염 한천은 그람 양성균에 대해 선택적이고 만니톨에 대해 차등적입니다.
- 자일로스 라이신 디옥시콜레이트는 그람 음성 박테리아에 대해 선택적입니다.
- 완충 숯 효모 추출물 한천은 특정 그람 음성 박테리아, 특히 레지오넬라 뉴모필라에 대해 선택적입니다.
- 베어드-파커 한천은 그람 양성 포도상구균을 위한 것입니다.
- 사보로 한천은 낮은 pH(5.6)와 높은 포도당 농도(3-4%)로 인해 특정 곰팡이에 선택적입니다.
- DRBC(dichloran rose bengl chloramphenicol agar)는 식품의 곰팡이와 효모를 열거하기 위한 선택적 배지입니다. 디클로란과 로즈벵골은 곰팡이 군체의 성장을 제한하여 호화로운 종의 과증식을 방지하고 군체의 정확한 계수를 돕습니다.[8]
- MMN(Modified Melin-Norkrans) 배지 및 BAF 배지는 외균근 진균에 사용됩니다.[9][10]
차동매체

차등 또는 지표 배지는 한 미생물 유형을 동일한 배지에서 자라는 다른 미생물 유형과 구별합니다.[11] 이러한 유형의 배지는 미생물의 정의적 특성을 가시적으로 나타내기 위해 배지에 특정 영양소 또는 지표(예: 중성 적색, 페놀 적색, 에오시니 또는 메틸렌 블루)가 첨가된 상태에서 성장하는 미생물의 생화학적 특성을 사용합니다. 이러한 배지는 미생물의 검출과 분자 생물학자가 박테리아의 재조합 균주를 검출하는 데 사용됩니다.
차등 미디어의 예:
- 혈액 한천은 스트렙토코커스 피오게네스 및 황색포도상구균과 같은 β 용혈성 유기체가 존재하는 경우 투명해지는 소 심장 혈액을 포함합니다.
- 에오신 메틸렌 블루는 유당 발효에 차별적입니다.
- 그라나다 배지는 이 배지에서 독특한 적색 집락으로 자라는 스트렙토코커스 아갈락티애(그룹 B 스트렙토코커스)에 대해 선택적이고 차등적입니다.
- 맥콘키 한천은 유당 발효에 차별적입니다.
- 만니톨 염 한천은 만니톨 발효에 차별적입니다.
- X-gal 플레이트는 lac 오페론 돌연변이에 대해 차등적입니다.
운송 매체
운송 매체는 다음 기준을 충족해야 합니다.
- 배양을 위해 시험실로 운반되는 시료의 임시 보관
- 시료 내의 모든 생물체의 농도를 변경하지 않고 생존 가능성을 유지합니다.
- 완충제와 소금만 포함합니다.
- 미생물 증식을 방지하기 위한 탄소, 질소 및 유기 성장 인자의 부족
- 혐기성 미생물의 분리에 사용되는 수송 매체는 분자 산소가 없어야 합니다.
전송 매체의 예:
- 티오글리콜레이트 육수는 엄격한 혐기성 미생물을 위한 것입니다.
- 스튜어트 수송 매체는[12][13] 산화 방지를 위한 환원제와 중화를 위한 숯이 함유된 비영양 연질 한천 겔입니다.
- 특정 박테리아 억제제는 임균에 사용되고 완충 글리세롤 식염수는 장내 간균에 사용됩니다.
- V. 콜레라에는 Venkataraman Ramakrisna(VR) 배지가 사용됩니다.
농축 매체
농축 배지에는 까다로운 일부 유기체를 포함하여 다양한 유기체의 성장을 지원하는 데 필요한 영양소가 포함되어 있습니다. 표본에 존재하는 만큼 다양한 종류의 미생물을 수확하는 데 일반적으로 사용됩니다. 혈액 한천은 영양학적으로 풍부한 전혈이 기본 영양소를 보충하는 농축 배지입니다. 초콜릿 한천은 열처리된 혈액(40–45 °C 또는 104–113 °F)이 풍부하여 갈색으로 변하고 배지에 이름이 붙은 색을 제공합니다.[14]
생리적 관련성
배양 배지의 선택은 특히 대사 연구의 경우 조직 배양 실험 결과의 생리학적 관련성에 영향을 미칠 수 있습니다.[15] 또한, 대사 유전자에 대한 세포주의 의존성은 배지 유형에 따라 영향을 받는 것으로 나타났습니다.[16] 여러 세포주를 포함하는 연구를 수행할 때 모든 세포주에 대해 균일한 배양 배지를 사용하면 생성된 데이터 세트의 편향을 줄일 수 있습니다. 영양소의 생리학적 수준을 더 잘 나타내는 성장 배지를 사용하면 시험관 내 연구의 생리학적 관련성을 향상시킬 수 있으며 최근에는 Plasmax[17] 및 인간 혈장 유사 배지(HPLM)[18]가 개발되었습니다.
참고 항목
참고문헌
- ^ a b c Madigan M, Martinko J, eds. (2005). Brock Biology of Microorganisms (11th ed.). Prentice Hall. ISBN 0-13-144329-1.
- ^ Birgit Hadeler; Sirkka Scholz; Ralf Reski (1995). "Gelrite and agar differently influence cytokinin-sensitivity of a moss". Journal of Plant Physiology (146): 369–371.
- ^ Ryan KJ, Ray CG, eds. (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. ISBN 0-8385-8529-9.
- ^ Hans Günter Schlegel (1993). General Microbiology. Cambridge University. p. 459. ISBN 978-0-521-43980-0. Retrieved 6 August 2013.
- ^ Parija, Shubhash Chandra (1 January 2009). Textbook of Microbiology & Immunology. Elsevier India. p. 45. ISBN 978-81-312-2163-1. Retrieved 6 August 2013.
- ^ Cooper, GM (2000). "Tools of Cell Biology". The Cell: A Molecular Approach. Washington, D.C: ASM Press. ISBN 0-87893-106-6.
- ^ Catherine A. Ingraham, John L. Ingraham (2000). Introduction to Microbiology.
- ^ Corry, Janet E. L.; Curtis, G. D. W.; Baird, Rosamund M., eds. (1995-01-01). "Dichloran rose bengal chloramphenicol (DRBC) agar". Progress in Industrial Microbiology. Elsevier. 34: 303–305. doi:10.1016/s0079-6352(05)80036-0. ISBN 978-0-444-81498-2. Retrieved 2020-04-20.
- ^ Islam, Ferzana; Ohga, Shoji (2013-03-12). "Effects of Media Formulation on the Growth and Morphology of Ectomycorrhizae and Their Association with Host Plant". International Scholarly Research Notices. 2013: e317903. doi:10.1155/2013/317903.
- ^ Chaitali Bhattacharya; Alok Adholeya. "Showcasing Ectomycorrhizal Culture". bookstore.teri.res.in. Retrieved 2023-02-04.
- ^ Washington, JA (1996). "Principles of Diagnosis". In Baron, S; et al. (eds.). Baron's Medical Microbiology (4th ed.). Univ of Texas Medical Branch. ISBN 0-9631172-1-1.
- ^ Mitsuhashi, Jun (2002), "Preparation of Media", Invertebrate Tissue Culture Methods, Tokyo: Springer Japan, pp. 25–32, ISBN 978-4-431-70313-6, retrieved 2023-09-07
- ^ Smriti, Saifun Nahar (2023-09-07). "Culture media: Definition, Types and Preparation Methods". GreenLeen.Com. Retrieved 2023-09-07.
- ^ "Enrichment Culture - an overview". ScienceDirect Topics. Retrieved 2023-09-07.
- ^ Lagziel S, GottliebE, Shlomi T (2020). "Mind your media". Nature Metabolism. 2 (12): 1369–1372. doi:10.1038/s42255-020-00299-y. PMID 33046912. S2CID 222319735.
{{cite journal}}: CS1 maint: 다중 이름: 작성자 목록(링크) - ^ Lagziel, S; Lee, WD; Shlomi, T (2019). "Inferring cancer dependencies on metabolic genes from large-scale genetic screens". BMC Biology. 17 (1): 37. doi:10.1186/s12915-019-0654-4. PMC 6489231. PMID 31039782.
- ^ Vande Voorde, J; Ackermann, T; Pfetzer, N; Sumpton, D; Mackay, G; Kalna, G; et al. (2019). "Improving the metabolic fidelity of cancer models with a physiological cell culture medium". Science Advances. 5 (1): eaau7314. Bibcode:2019SciA....5.7314V. doi:10.1126/sciadv.aau7314. PMC 6314821. PMID 30613774.
- ^ Cantor JR, Abu-Remaileh M, Kanarek N, Freinkman E, Gao X, Louissaint A; et al. (2017). "Physiologic Medium Rewires Cellular Metabolism and Reveals Uric Acid as an Endogenous Inhibitor of UMP Synthase". Cell. 169 (2): 258–272.e17. doi:10.1016/j.cell.2017.03.023. PMC 5421364. PMID 28388410.
{{cite journal}}: CS1 maint: 다중 이름: 작성자 목록(링크)

