노보비오신
Novobiocin | |
 | |
| 임상 데이터 | |
|---|---|
| AHFS/Drugs.com | 국제 의약품명 |
| 루트 행정부. | 정맥주사 |
| ATCvet 코드 | |
| 약동학 데이터 | |
| 바이오 어베이러빌리티 | 경구 생체 이용률 무시할 수 |
| 대사 | 변하지 않고 배설되었다 |
| 반감기 제거 | 6시간 |
| 배설물 | 신장의 |
| 식별자 | |
| |
| CAS 번호 | |
| PubChem CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 첸블 | |
| CompTox 대시보드 (EPA ) | |
| ECHA 정보 카드 | 100.005.589 |
| 화학 및 물리 데이터 | |
| 공식 | C31H36N2O11 |
| 몰 질량 | 612.624 g/120−1 |
| 3D 모델(JSmol) | |
| 녹는점 | 152 ~ 156 °C (306 ~313 °F) (12) |
| |
| |
| (표준) | |
알바마이신 또는 카토마이신으로도 알려진 노보비오신은 방선균류인 스트렙토마이세스 니베우스에 의해 생성되는 아미노쿠마린 항생물질로, 최근 방선균류인 S. spheroides의[1] 주관적인 동의어로 확인되었다.다른 아미노코마린 항생제로는 클로로비오신과 쿠메르마이신 A1이 [2]있다.노보비오신은 1950년대 중반에 처음 보고되었다.[3][4]
임상 사용
황색포도상구균 표피에 대해 활성화되며 배양 중인 노보비오신에 내성이 있는 다른 응고효소 음성 황색포도상구균 부생피질과의 분화에 사용될 수 있다.
노보비오신은 1960년대에 알바마이신(업존)이라는 상표명으로 임상 사용을 허가받았다.그 효과는 임상 전 [5][6]및 임상 시험에서 입증되었다.그 약의 경구 형태는 효능 부족으로 [7]인해 시장에서 철수되었다.업존이 파날바와 알바마이신-T와 같은 브랜드명으로 판매한 노보비오신과 테트라사이클린의 조합 제품은 특히 [8][9]FDA의 집중적인 정밀 조사 대상이 되었다.노보비오신은 MRSA [10]치료에 사용되는 효과적인 항포도상구균제이다.
작용 메커니즘
노보비오신 및 기타 관련 약물인 클로로비오신 및 쿠메르마이신 A1의 작용 분자적 기초가 [2][11][12][13][14]조사되었다.아미노코마린은 박테리아 DNA 자이라아제의 매우 강력한 억제제이며 에너지 전달에 관여하는 효소의 GyrB 서브유닛을 목표로 하여 작용한다.노보비오신 및 다른 아미노코마린 항생제는 GyrB에 의해 촉매되는 ATPase 반응의 경쟁적 억제제로 작용한다.노보비오신의 효력은 DNA 자이라아제를 표적으로 하는 플루오로퀴놀론보다 상당히 높지만 효소의 다른 부위에 있다.GyrA 서브유닛은 DNA 절단 및 결찰 활동에 관여합니다.
노보비오신은 진핵생물 Hsp90 단백질(고마이크로몰 IC50)의 C 말단을 약하게 억제하는 것으로 나타났다.노보비오신 골격의 수정은 보다 선택적인 Hsp90 [15]억제제로 이어졌다.노보비오신은 또한 그램 음성 리포다당 운반체 LptBFGC를 [16][17]결합하고 활성화하는 것으로 나타났다.
중합효소 세타의 ATP 결합 포켓은 노보바이오신에 의해 차단되어 ATP 효소 활성의 손실을 일으킨다.이는 상동 재조합 결핍 세포가 DNA 손상 물질을 우회하는 경로로서 마이크로호몰로지 매개 말단 결합의 손실을 초래한다.노보비오신의 작용은 마우스 모델에서 종양 크기를 줄이기 위한 PARP 억제제와 동기화된다.[18]
구조.
노보비오신은 아미노코마린이다.노보비오신은 벤조산유도체, 쿠마린잔기, 당노보비오스의 [11]3가지 요소로 나눌 수 있다.X선 결정학 연구는 노보비오신과 DNA 자이라제의 약물 수용체 복합체가 자이라아제 [19]분자에 ATP와 노보비오신이 겹치는 결합 부위를 가지고 있음을 보여준다.쿠마린과 ATP 결합 부위의 중복은 아미노코마린이 ATP 효소 [20]활성의 경쟁적 억제제인 것과 일치한다.
구조-활동 관계
구조 활성 관계 실험에서 노보비오스 당에 위치한 카바모일기의 제거는 노보비오신의 [20]억제 활성을 극적으로 감소시키는 것으로 나타났다.
생합성
이 아미노코마린 항생제는 3가지 주요 대체물로 구성되어 있습니다.고리 A로 알려진 3-디메틸알릴-4-히드록시벤조산 부분은 프리페네이트와 디메틸알릴 피로인산염에서 파생됩니다.고리 B로 알려진 아미노코마린 부분은 L-티로신에서 파생됩니다.노보비오신의 마지막 성분은 당 유도체 L-노비오스로, 고리 C로 알려져 있으며, 포도당 1-인산으로부터 유도된다.노보비오신에 대한 생합성 유전자 클러스터는 1999년(발표 2000년) Streptomyces spheroides NCIB 11891에서 [21]Heide와 동료들에 의해 확인되었다.그들은 23개의 추정 개방 판독 프레임(ORF)과 노보바이오신 생합성에 역할을 할 수 있는 11개 이상의 다른 ORF를 확인했다.
고리 A의 생합성(그림 1 참조)은 시키미산 생합성 경로에서 파생된 프리페네이트로 시작한다.NovF 효소는 프리페네이트의 탈탄산화를 촉매하는 동시에 니코틴아미드 아데닌디뉴클레오티드인산(NADP)+을 환원하여 NADPH를 생성한다.이 NovQ에 이어 프레닐화로 [22]알려진 디메틸알릴피로인산(DMAPP)에 의한 페닐링의 친전자 치환을 촉매한다.DMAPP는 메발론산 경로 또는 디옥시실룰로오스 생합성 경로에서 나올 수 있다.다음으로 3디메틸알릴-4-히드록시벤조산염 분자를 NovR과 [23]분자산소에 의해 2개의 산화탈탄산화한다.NovR은 독특한 2관능성 촉매 작용을 가진 비헴 철 산소화효소이다.첫 번째 단계에서는 두 개의 옥시겐이 분자 산소로부터 결합되고, 두 번째 단계에서는 동위원소 라벨링 연구에 의해 결정된 한 개만 결합된다.이것으로 링 A의 형성이 완료됩니다.
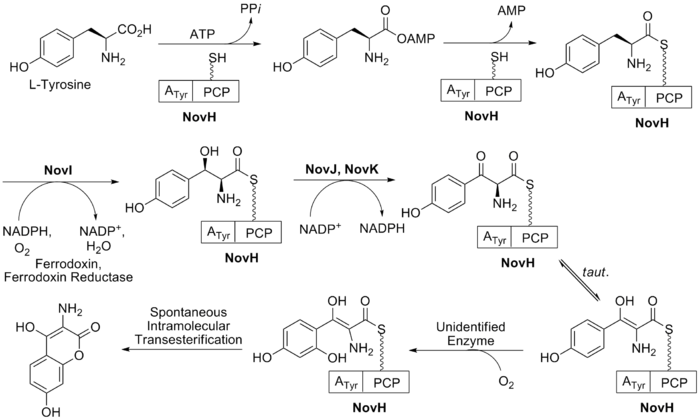
링 B(그림 2 참조)의 생합성은 천연 아미노산 L-티로신에서 시작한다.그런 다음 ATP와 NovH [24]자체에 의해 아데닐화되고 NovH의 펩티딜 캐리어 단백질(PCP)에 티오에스테르화된다.그런 다음 NovI는 NADPH와 분자산소를 사용하여 β-위치를 산화시킴으로써 이 PCP 결합 분자를 더욱 수정한다.NovJ와 NovK는 이 벤질산소화효소의 [25]활성 형태인 J2K2의 헤테로다이머를 형성한다.이 과정은 NADP를 β-알코올의 산화에 있어 수소화물 수용체로 사용한다+.이 케톤은 용액의 에놀 호변이성체 안에 존재하는 것을 선호할 것이다.다음으로 아직 확인되지 않은 단백질이 벤젠의 선택적 산화를 촉매한다(그림 2 참조).산화 시 이 중간체는 자연적으로 락톤화되어 방향족 고리 B를 형성하고 이 과정에서 NovH를 잃게 됩니다.
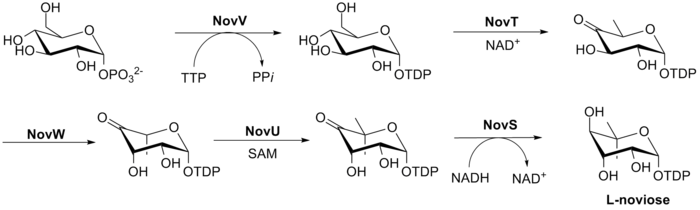
L-noviose(링 C)의 생합성은 그림 3과 같다.이 과정은 NovV가 dTTP를 취하고 인산기를 dTDP기로 대체하는 포도당 1-인산부터 시작한다.NovT는 NAD를+ 이용하여 4-히드록시기를 산화시킨다.NovT는 또한 설탕의 6위치에 대한 탈옥실화를 달성한다.그런 다음 NovW는 설탕의 [26]3가지 위치를 에피머화한다.5위치의 메틸화는 NovU와 S-아데노실메티오닌(SAM)에 의해 이루어지며, 마지막으로 NovS는 NADH를 이용하여 시작 포도당-1-인산으로부터 4위치의 에피머화를 다시 달성한다.
고리 A, B, C를 결합하여 개질하여 완성된 노보비오신 분자를 얻는다.고리 A와 B는 ATP를 이용한 효소 NovL에 의해 결합되어 고리 A의 카르본산기를 디포스포릴화함으로써 고리 B상의 아민기에 의해 카르보닐기가 공격될 수 있다.생성된 화합물은 글리코실화 [27]전에 NovO 및 SAM에 의해 메틸화된다.NovM은 dTDP의 손실과 함께 티로신 유래의 수산기에 고리 C(L-noviose)를 첨가한다.또 다른 메틸화는 NovP와 SAM에 의해 L-노비오스당의 [28]4개 위치에서 이루어진다.이 메틸화에 의해 NovN은 그림 4와 같이 당의 3위치를 카르바밀화하여 노보바이오신의 생합성을 완료한다.
레퍼런스
- ^ Lanoot B, Vancanneyt M, Cleenwerck I, Wang L, Li W, Liu Z, Swings J (May 2002). "The search for synonyms among streptomycetes by using SDS-PAGE of whole-cell proteins. Emendation of the species Streptomyces aurantiacus, Streptomyces cacaoi subsp. cacaoi, Streptomyces caeruleus and Streptomyces violaceus". International Journal of Systematic and Evolutionary Microbiology. 52 (Pt 3): 823–9. doi:10.1099/ijs.0.02008-0. PMID 12054245.
- ^ a b 알레산드라 다 실바 유스타키오(2004) 스트렙토미세스 내 아미노쿠마린 항생제 생합성:유전자 공학에 의한 구조 유사체의 생성과 항생제 생산 규제에 대한 통찰.논문
- ^ Hoeksema H.; Johnson J. L.; Hinman J. W. (1955). "Structural studies on streptonivicin, a new antibiotic". J Am Chem Soc. 77 (24): 6710–6711. doi:10.1021/ja01629a129.
- ^ Smith C. G.; Dietz A.; Sokolski W. T.; Savage G. M. (1956). "Streptonivicin, a new antibiotic. I. Discovery and biologic studies". Antibiotics & Chemotherapy. 6 (2): 135–142. PMID 24543916.
- ^ Raad I, Darouiche R, Hachem R, Sacilowski M, Bodey GP (November 1995). "Antibiotics and prevention of microbial colonization of catheters". Antimicrobial Agents and Chemotherapy. 39 (11): 2397–400. doi:10.1128/aac.39.11.2397. PMC 162954. PMID 8585715.
- ^ Raad II, Hachem RY, Abi-Said D, Rolston KV, Whimbey E, Buzaid AC, Legha S (January 1998). "A prospective crossover randomized trial of novobiocin and rifampin prophylaxis for the prevention of intravascular catheter infections in cancer patients treated with interleukin-2". Cancer. 82 (2): 403–11. doi:10.1002/(SICI)1097-0142(19980115)82:2<412::AID-CNCR22>3.0.CO;2-0. PMID 9445199.
- ^ "Determination That ALBAMYCIN (Novobiocin Sodium) Capsule, 250 Milligrams, Was Withdrawn From Sale for Reasons of Safety or Effectiveness". The Federal Register. 19 January 2011.
- ^ Mintz M (August 1969). "FDA and Panalba: A Conflict of Commercial, Therapeutic Goals?". Science. 165 (3896): 875–881. doi:10.1126/science.165.3896.875.
- ^ Mintz, Morton. "Upjohn's Shuck and Jive Routine". Mother Jones. Mother Jones and the Foundation for National Progress. Retrieved 16 February 2022.
- ^ Walsh TJ, Standiford HC, Reboli AC, John JF, Mulligan ME, Ribner BS, Montgomerie JZ, Goetz MB, Mayhall CG, Rimland D (June 1993). "Randomized double-blinded trial of rifampin with either novobiocin or trimethoprim-sulfamethoxazole against methicillin-resistant Staphylococcus aureus colonization: prevention of antimicrobial resistance and effect of host factors on outcome". Antimicrobial Agents and Chemotherapy. 37 (6): 1334–42. doi:10.1128/aac.37.6.1334. PMC 187962. PMID 8328783.
- ^ a b Maxwell A (August 1993). "The interaction between coumarin drugs and DNA gyrase". Molecular Microbiology. 9 (4): 681–6. doi:10.1111/j.1365-2958.1993.tb01728.x. PMID 8231802. S2CID 43159068.
- ^ Maxwell A (February 1999). "DNA gyrase as a drug target". Biochemical Society Transactions. 27 (2): 48–53. doi:10.1042/bst0270048. PMID 10093705.
- ^ Lewis RJ, Tsai FT, Wigley DB (August 1996). "Molecular mechanisms of drug inhibition of DNA gyrase". BioEssays. 18 (8): 661–71. doi:10.1002/bies.950180810. PMID 8760340. S2CID 9488669.
- ^ Maxwell A, Lawson DM (2003). "The ATP-binding site of type II topoisomerases as a target for antibacterial drugs". Current Topics in Medicinal Chemistry. 3 (3): 283–303. doi:10.2174/1568026033452500. PMID 12570764.
- ^ Yu XM, Shen G, Neckers L, Blake H, Holzbeierlein J, Cronk B, Blagg BS (September 2005). "Hsp90 inhibitors identified from a library of novobiocin analogues". Journal of the American Chemical Society. 127 (37): 12778–9. doi:10.1021/ja0535864. PMID 16159253.
- ^ Mandler MD, Baidin V, Lee J, Pahil KS, Owens TW, Kahne D (June 2018). "Novobiocin Enhances Polymyxin Activity by Stimulating Lipopolysaccharide Transport". Journal of the American Chemical Society. 140 (22): 6749–6753. doi:10.1021/jacs.8b02283. PMC 5990483. PMID 29746111.
- ^ May JM, Owens TW, Mandler MD, Simpson BW, Lazarus MB, Sherman DJ, Davis RM, Okuda S, Massefski W, Ruiz N, Kahne D (December 2017). "The Antibiotic Novobiocin Binds and Activates the ATPase That Powers Lipopolysaccharide Transport". Journal of the American Chemical Society. 139 (48): 17221–17224. doi:10.1021/jacs.7b07736. PMC 5735422. PMID 29135241.
- ^ Zhou J, Gelot C, Pantelidou C, Li A, Yücel H, Davis RE, Färkkilä A, Kochupurakkal B, Syed A, Shapiro GI, Tainer JA, Blagg BS, Ceccaldi R, D'Andrea AD (June 2021). "A first-in-class polymerase theta inhibitor selectively targets homologous-recombination-deficient tumors". Nature Cancer. 2 (June 2021): 598–610. doi:10.1038/s43018-021-00203-x. PMC 8224818. PMID 34179826. S2CID 235659640.
- ^ Tsai FT, Singh OM, Skarzynski T, Wonacott AJ, Weston S, Tucker A, Pauptit RA, Breeze AL, Poyser JP, O'Brien R, Ladbury JE, Wigley DB (May 1997). "The high-resolution crystal structure of a 24-kDa gyrase B fragment from E. coli complexed with one of the most potent coumarin inhibitors, clorobiocin". Proteins. 28 (1): 41–52. doi:10.1002/(sici)1097-0134(199705)28:1<41::aid-prot4>3.3.co;2-b. PMID 9144789.
- ^ a b Flatman RH, Eustaquio A, Li SM, Heide L, Maxwell A (April 2006). "Structure-activity relationships of aminocoumarin-type gyrase and topoisomerase IV inhibitors obtained by combinatorial biosynthesis". Antimicrobial Agents and Chemotherapy. 50 (4): 1136–42. doi:10.1128/AAC.50.4.1136-1142.2006. PMC 1426943. PMID 16569821.
- ^ Steffensky M, Mühlenweg A, Wang ZX, Li SM, Heide L (May 2000). "Identification of the novobiocin biosynthetic gene cluster of Streptomyces spheroides NCIB 11891". Antimicrobial Agents and Chemotherapy. 44 (5): 1214–22. doi:10.1128/AAC.44.5.1214-1222.2000. PMC 89847. PMID 10770754.
- ^ Pojer F, Wemakor E, Kammerer B, Chen H, Walsh CT, Li SM, Heide L (March 2003). "CloQ, a prenyltransferase involved in clorobiocin biosynthesis". Proceedings of the National Academy of Sciences of the United States of America. 100 (5): 2316–21. Bibcode:2003PNAS..100.2316P. doi:10.1073/pnas.0337708100. PMC 151338. PMID 12618544.
- ^ Pojer F, Kahlich R, Kammerer B, Li SM, Heide L (August 2003). "CloR, a bifunctional non-heme iron oxygenase involved in clorobiocin biosynthesis". The Journal of Biological Chemistry. 278 (33): 30661–8. doi:10.1074/jbc.M303190200. PMID 12777382.
- ^ Chen H, Walsh CT (April 2001). "Coumarin formation in novobiocin biosynthesis: beta-hydroxylation of the aminoacyl enzyme tyrosyl-S-NovH by a cytochrome P450 NovI". Chemistry & Biology. 8 (4): 301–12. doi:10.1016/S1074-5521(01)00009-6. PMID 11325587.
- ^ Pacholec M, Hillson NJ, Walsh CT (September 2005). "NovJ/NovK catalyze benzylic oxidation of a beta-hydroxyl tyrosyl-S-pantetheinyl enzyme during aminocoumarin ring formation in novobiocin biosynthesis". Biochemistry. 44 (38): 12819–26. CiteSeerX 10.1.1.569.1481. doi:10.1021/bi051297m. PMID 16171397.
- ^ Thuy TT, Lee HC, Kim CG, Heide L, Sohng JK (April 2005). "Functional characterizations of novWUS involved in novobiocin biosynthesis from Streptomyces spheroides". Archives of Biochemistry and Biophysics. 436 (1): 161–7. doi:10.1016/j.abb.2005.01.012. PMID 15752721.
- ^ Pacholec M, Tao J, Walsh CT (November 2005). "CouO and NovO: C-methyltransferases for tailoring the aminocoumarin scaffold in coumermycin and novobiocin antibiotic biosynthesis". Biochemistry. 44 (45): 14969–76. doi:10.1021/bi051599o. PMID 16274243.
- ^ Freel Meyers CL, Oberthür M, Xu H, Heide L, Kahne D, Walsh CT (January 2004). "Characterization of NovP and NovN: completion of novobiocin biosynthesis by sequential tailoring of the noviosyl ring". Angewandte Chemie. 43 (1): 67–70. doi:10.1002/anie.200352626. PMID 14694473.