신경내분비학
Neuroendocrinology신경내분비학은 신경계와 내분비계 사이의 상호작용, 즉 뇌가 [1]어떻게 신체에서 호르몬 활동을 조절하는지를 연구하는 생물학의 한 분야이다.신경계와 내분비계는 종종 신경 내분비 통합이라고 불리는 과정에서 함께 작용하여 인체의 생리학적 과정을 조절한다.신경내분비학은 뇌, 특히 시상하부가 뇌하수체 호르몬의 분비를 통제한다는 인식에서 생겨났고, 이후 내분비와 신경계의 수많은 상호연결을 조사하기 위해 확장되었다.
내분비계는 펩타이드, 스테로이드, 신경아민을 포함한 다양한 화학 구조의 호르몬을 생성하고 분비하는 몸 전체의 수많은 분비선으로 구성되어 있다.총체적으로, 호르몬은 많은 생리적 과정을 조절한다.신경내분비계는 시상하부가 항상성을 유지하고, 생식, 대사, 식사와 음주 행동, 에너지 이용, 삼투압, 혈압을 조절하는 메커니즘이다.
신경내분비계
시상하부
시상하부는 뇌의 모든 영역에서 입력을 통합하고 특정한 반응을 만들어내는 역할 때문에 일반적으로 뇌의 중계중추로 알려져 있습니다.신경내분비계에서 시상하부는 뇌의 다른 부분으로부터 전기신호를 받고 그 전기신호를 호르몬이나 방출인자의 형태로 화학신호로 변환한다.그리고 나서 이 화학물질들은 뇌하수체로 운반되고 거기서부터 전신 [2]순환으로 운반된다.
뇌하수체
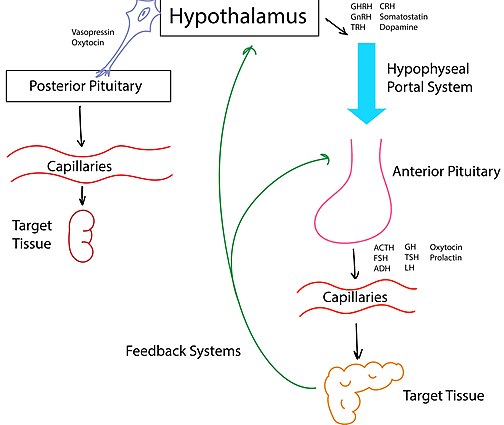
뇌하수체는 뇌하수체 전엽, 뇌하수체 중간엽, 뇌하수체 후엽의 세 개의 엽으로 나뉜다.시상하부는 뇌하수체 전엽 호르몬이라고 불리는 방출 인자를 시상하부-최고체 간문 [3]체계로 보내줌으로써 뇌하수체의 호르몬 분비를 조절합니다.예를 들어 시상하부에서 문맥계로 방출되는 티로트로핀 방출호르몬은 뇌하수체 [citation needed]전엽에 의한 갑상선 자극호르몬 분비를 촉진한다.
후뇌하수체는 시상하부에 의해 직접적으로 신경화된다; 옥시토신과 바소프레신 호르몬은 시상하부의 신경내분비세포에 의해 합성되고 후뇌하수체의 신경말단에 저장된다.그것들은 시상하부 [3]뉴런에 의해 전신순환으로 직접 분비된다.
주요 신경내분비축
후뇌하수체(신경하수체)의 두 신경하수체 호르몬인 옥시토신과 바소프레신(항이뇨호르몬이라고도 함)은 마그노세포 신경분비세포의 신경말단에서 전신순환으로 분비된다.옥시토신과 바소프레신 뉴런의 세포체는 [2]시상하부의 방실핵과 상안핵에 각각 있으며, 이들 뉴런의 전기적 활동은 다른 뇌 [4]영역으로부터의 구심성 시냅스 입력에 의해 조절된다.
이와는 대조적으로 뇌하수체 전엽(아데노하수체)의 호르몬은 포유동물에서 직접 신경화되지 않은 내분비세포에서 분비되지만 이들 호르몬(부신피질영양호르몬, 황체호르몬, 난포자극호르몬, 갑상선자극호르몬, 프로락틴 및 성장호르몬)의 분비량은 그대로 남아 있다.시상하부를 조절하는 거야시상하부는 뇌하수체 전엽을 조절하는데, 이는 시상하부 뉴런이 중앙 돌출부의 [5]혈관으로 방출하는 물질이다.시상하부-하수체 간문 혈관인 이 혈관들은 시상하부 인자를 뇌하수체 전부로 운반하고,[3] 뇌하수체 전부는 호르몬 생성 세포의 표면에 있는 특정 수용체에 결합합니다.
예를 들어 성장호르몬의 분비는 두 개의 신경내분비계, 즉 각각 [6]분비를 자극하고 억제하는 성장호르몬 방출호르몬(GHRH) 뉴런과 소마토스타틴 뉴런에 의해 제어된다.GHRH 뉴런은 시상하부의 활 모양의 핵에 위치하고 성장호르몬 조절에 관여하는 소마토스타틴 세포는 방실주위의 핵에 있습니다.이 두 개의 신경계는 축삭을 중앙 돌출부에 투영하고, 거기서 그들은 뇌하수체 전엽으로 운반하기 위해 그들의 펩타이드를 간문 혈관으로 방출합니다.성장호르몬은 GHRH와 소마토스타틴 세포 사이의 신경상호작용을 반영할 수 있는 GHRH 방출과 소마토스타틴 방출의 번갈아 일어나는 발작과 [6]성장호르몬의 음성피드백을 통해 분비된다.
기능들
신경내분비계는 결합에서 성행동에 이르기까지 모든 면에서 번식을 통제한다[7].그들은 정자 형성과 난소 주기, 분만, 수유, 모성 행동을 조절한다.그들은 스트레스와 [9]감염에[8] 대한 신체의 반응을 조절한다.그것들은 신체의 신진대사를 조절하고, 식습관과 음주 행동에 영향을 미치며, 에너지 섭취의 활용 방법, 즉 지방이 대사되는 [10]방법에 영향을 미칩니다.그들은 기분,[11] 체액과 전해질 항상성,[12] 그리고 [13]혈압에 영향을 주고 조절합니다.
신경 내분비계의 뉴런은 크다; 그들은 분비물을 생산하기 위한 작은 공장이다; 그들의 신경 말단은 크고 일관성 있는 말단 장에서 조직된다; 그들의 생산량은 종종 혈액에서 쉽게 측정될 수 있다; 그리고 이러한 뉴런들이 무엇을 하고 그들이 반응하는 자극은 가설과 실험에 쉽게 열려있다.따라서, 신경 내분비 뉴런은 "뉴런이 어떻게 제품의 합성, 포장, 분비를 조절하는가?"와 "정보가 전기 활동에서 어떻게 인코딩되는가?"와 같은 일반적인 질문을 연구하기 위한 좋은 "모델 시스템"이다.[citation needed][이것이 주요 소스 관찰인 것 같습니다]
역사
개척자
뮌헨 대학의 알버트 아인슈타인 의과대학의 [14]에른스트와 베르타 샤러는 1945년 신경펩타이드에 관한 초기 관찰과 제안으로 신경내분비학 분야의 공동 설립자로 인정받고 있다.
Geoffrey[15] Harris는 많은 사람들에게 신경내분비학의 "아버지"로 여겨진다.해리스, 닥터.옥스포드 대학의 이 교수의 해부학 교수는 포유류의 뇌하수체는 시상하부 뉴런에 의해 시상하부하수체 간문순환으로 분비되는 호르몬에 의해 조절된다는 것을 보여준 것으로 인정받고 있다.반대로 후뇌하수체의 호르몬은 시상하부 뉴런의 신경 말단에서 직접 전신순환으로 분비된다.이 중요한 작업은 룬드 대학의 [16]도라 제이콥슨과 공동으로 이루어졌다.
확인된 첫 번째 인자는 티로트로핀 방출 호르몬(TRH)과 고나도트로핀 방출 호르몬(GnRH)이다. TRH는 갑상선 자극 호르몬의 분비를 자극하는 작은 펩타이드이며, GnRH(황체 자극 호르몬 방출 호르몬이라고도 함)는 황체 자극 호르몬과 난포 자극 호르몬의 분비를 자극한다.
리옹의 Fontouré de Médecine 의대생 Roger Guillemin과 [17]툴레인 대학의 Andrew W. Schally는 양과 돼지의 시상하부에서 이러한 요인을 분리한 후 그들의 구조를 확인했습니다.길레민과 샬리는 "뇌의 [citation needed]펩타이드 호르몬 생성"을 이해하는데 기여한 공로로 1977년 노벨 생리의학상을 수상했다.
1952년, 남플로리다 대학의 안도 스젠티바니와 게자 필립은 [18]시상하부를 통해 면역의 신경 조절이 어떻게 일어나는지 보여주는 세계 최초의 연구 논문을 썼다.
최신 스코프
오늘날 신경내분비학은 신경내분비 뉴런의 핵심 개념에서 직간접적으로 생겨난 광범위한 주제를 받아들인다.신경내분비뉴런은 부신피질영양호르몬의 영향을 받아 부신에서 분비되는 코르티코스테로이드가 뇌에 영향을 미치는 생식선을 조절한다.이러한 피드백에 대한 연구는 신경내분비학자들의 영역이 되었다.시상하부 신경내분비 뉴런에 의해 혈액으로 분비되는 펩타이드는 뇌에도 방출되는 것으로 입증되었으며, 중심 작용은 종종 말초 작용을 보완하는 것으로 나타났다.그래서 이러한 중추작용을 이해하는 것도 신경내분비학자들의 영역이 되었습니다. 때로는 이 펩타이드가 내분비 조절과 무관한 기능을 하는 것처럼 보이는 뇌의 다른 부분에서 생겨났을 때도요.신경내분비 뉴런은 말초신경계에서 발견되었는데, 예를 들어 소화를 조절한다.아드레날린과 노르아드레날린을 방출하는 부신수질의 세포는 내분비세포와 뉴런 사이에 특성이 있다는 것을 증명했고, 예를 들어 세포외분자 메커니즘을 연구하기 위한 뛰어난 모델 시스템임이 증명되었다.이것들 역시 신경내분비계가 되었습니다
신경 내분비 시스템은 신경과학과 생리학에서 많은 기본 원리, 예를 들어 자극과 [19]분비 결합에 대한 우리의 이해에 중요했습니다.신경내분비에서 패턴화의 기원과 중요성은 오늘날 신경내분비학에서 여전히 지배적인 주제이다.
신경내분비학은 또한 신경생물학적 뇌장애를 이해하고 치료하는데 필수적인 부분으로 사용된다.한 가지 예는 [20]갑상선 호르몬으로 기분 증상의 치료의 증가이다.또 다른 하나는 정신분열증으로 [21]진단된 일부 환자의 뇌척수액에서 트란스티레틴(티록신 수송) 문제가 발견된 것이다.
실험 기술
시상하부와 뇌하수체 사이의 의사소통을 조사하는 제프리 해리스의 첫 번째 실험 이후, 이 상호작용의 기계적 세부 사항에 대해 많은 것을 알게 되었다.다양한 실험 기술이 사용되었습니다.초기 실험은 Hodgkin과 Huxley가 사용한 전기생리학 기술에 크게 의존했다.최근의 접근법은 이전에 식별된 메커니즘을 이해하고 다양한 [citation needed]상황에서 체계적 대응과 적응을 예측하기 위해 다양한 수학적 모델을 통합했다.
전기생리학
전기생리학 실험은 특히 시상하부와 뇌하수체 후부에서 일어나는 생리학적 현상을 확인하기 위해 신경내분비학 초기에 사용되었다.1950년, 제프리 해리스와 배리 크로스는 전기 [22]자극에 대한 반응으로 옥시토신 방출을 연구함으로써 옥시토신 경로의 개요를 설명했습니다.1974년 월터스와 해튼은 바소프레신 [22]방출을 담당하는 시상하부 중추인 상안핵을 전기적으로 자극함으로써 수분 탈수의 영향을 조사했다.글렌 해튼은 시상하부 [22]뉴런의 전기적 특성을 연구하는 신경하수체계의 생리학을 연구하는 데 그의 경력을 바쳤다.그렇게 함으로써 이러한 뉴런의 행동과 그에 따른 생리적 영향에 대한 조사가 가능해졌다.신경내분비세포의 전기적 활동을 연구함으로써 중추신경뉴런, 신경내분비뉴런,[23] 내분비뉴런을 최종적으로 구별할 수 있었다.
수학적 모델
호지킨-헉슬리 모형
Hodgkin-Huxley 모델은 특정 전압에서 시스템의 전류에 대한 데이터를 막 전위를 설명하는 시간 의존 데이터로 변환합니다.이 모형을 사용한 실험은 일반적으로 동일한 형식과 가정에 의존하지만 미분 방정식을 변경하여 특정 질문에 답합니다.이 [8]방법을 사용함으로써 바소프레신, GnRH, 체성영양소, 피질영양소, 유산영양호르몬에 대해 많은 것을 알 수 있다.
통합 및 구현 모델
적분 및 화재 모델은 생물학적 시스템을 설명할 때 수학적인 단순성을 목표로 합니다.그것은 뉴런의 역치 활동을 묘사한다.이 한 가지 측면에만 초점을 맞춤으로써, 모델은 복잡한 시스템의 복잡성을 성공적으로 감소시키지만, 실제 작용 메커니즘을 무시하고 시스템 출력이 [8]입력과 어떻게 관련되는지를 지배하는 기능으로 대체한다.이 모델은 뇌하수체 후부에 분비되는 호르몬인 옥시토신과 바소프레신을 [9]묘사하는데 사용되었습니다
기능 또는 평균 필드 모델
함수 또는 평균 필드 모델은 "심플러가 더 낫다"[8]는 전제에 의존합니다.셀의 전체 집단을 설명하기 위해 단일 변수를 사용하여 다면 시스템을 모델링하는 복잡성을 줄이기 위해 노력합니다.다른 방법은 각 모집단에 대해 서로 다른 변수 집합을 사용하는 것입니다.여러 셀 집단이 상호 작용하는 시스템을 모델링하려고 할 때 여러 세트를 사용하면 빠르게 복잡해집니다.이 모델은 특히 생식 주기(월경 주기, 황체 생성 호르몬, 프로락틴 급증)[9]와 관련된 여러 시스템을 설명하는 데 사용되어 왔다.코르티솔 분비와 성장호르몬 [9]분비를 나타내는 기능 모델도 존재한다.
「 」를 참조해 주세요.
레퍼런스
- ^ "Endocrine system and neuroendocrinology :: DNA Learning Center". www.dnalc.org. Retrieved 2018-05-12.
- ^ a b Watts, Alan G (2015-08-01). "60 Years of Neuroendocrinology: The structure of the neuroendocrine hypothalamus: the neuroanatomical legacy of Geoffrey Harris". Journal of Endocrinology. 226 (2): T25–T39. doi:10.1530/JOE-15-0157. ISSN 0022-0795. PMC 4574488. PMID 25994006.
- ^ a b c Malenka RC, Nestler EJ, Hyman SE (2009). "Chapter 10: Neural and Neuroendocrine Control of the Internal Milieu.". In Sydor A, Brown RY (ed.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 246, 248–259. ISBN 9780071481274.
- ^ Honda, Kazumasa; Zhang, William; Tomiyama, Keita (June 2014). "Oxytocin cells in the paraventricular nucleus receive excitatory synaptic inputs from the contralateral paraventricular and supraoptic nuclei in lactating rats". Neuroscience Letters. 572: 44–47. doi:10.1016/j.neulet.2014.04.040. PMID 24792395. S2CID 25107850.
- ^ Knigge, K. M.; Joseph, S. A.; Sladek, J. R.; Notter, M. F.; Morris, M.; Sundberg, D. K.; Holzwarth, M. A.; Hoffman, G. E.; O'Brien, L. (1976-01-01), Bourne, G. H.; Danielli, J. F.; Jeon, K. W. (eds.), Uptake and Transport Activity of the Median Eminence of the Hypothalamus, International Review of Cytology, vol. 45, Academic Press, pp. 383–408, doi:10.1016/s0074-7696(08)60082-0, ISBN 9780123643452, retrieved 2021-11-15
- ^ a b MacGregor, D. J.; Leng, G. (December 2005). "Modelling the Hypothalamic Control of Growth Hormone Secretion". Journal of Neuroendocrinology. 17 (12): 788–803. doi:10.1111/j.1365-2826.2005.01370.x. ISSN 0953-8194. PMID 16280026. S2CID 36712187.
- ^ Blázquez M, Bosma PT, Fraser EJ, Van Look KJ, Trudeau VL (June 1998). "Fish as models for the neuroendocrine regulation of reproduction and growth". Comparative Biochemistry and Physiology. Part C, Pharmacology, Toxicology & Endocrinology. 119 (3): 345–64. doi:10.1016/S0742-8413(98)00023-1. PMID 9827007.
- ^ a b c d Ratka A, Sutanto W, Bloemers M, de Kloet ER (August 1989). "On the role of brain mineralocorticoid (type I) and glucocorticoid (type II) receptors in neuroendocrine regulation". Neuroendocrinology. 50 (2): 117–23. doi:10.1159/000125210. PMID 2550833.
- ^ a b c d Webster JI, Tonelli L, Sternberg EM (2002). "Neuroendocrine regulation of immunity" (PDF). Annual Review of Immunology. 20: 125–63. doi:10.1146/annurev.immunol.20.082401.104914. PMID 11861600. Archived from the original (PDF) on 2013-12-12.
- ^ McMinn JE, Baskin DG, Schwartz MW (May 2000). "Neuroendocrine mechanisms regulating food intake and body weight". Obesity Reviews. 1 (1): 37–46. doi:10.1046/j.1467-789x.2000.00007.x. PMID 12119644. S2CID 33202919.
- ^ Davidson RJ, Lewis DA, Alloy LB, Amaral DG, Bush G, Cohen JD, et al. (September 2002). "Neural and behavioral substrates of mood and mood regulation". Biological Psychiatry. 52 (6): 478–502. CiteSeerX 10.1.1.558.6231. doi:10.1016/S0006-3223(02)01458-0. PMID 12361665. S2CID 39992433.
- ^ Antunes-Rodrigues J, de Castro M, Elias LL, Valença MM, McCann SM (January 2004). "Neuroendocrine control of body fluid metabolism". Physiological Reviews. 84 (1): 169–208. doi:10.1152/physrev.00017.2003. PMID 14715914.
- ^ Lenkei Z, Corvol P, Llorens-Cortes C (May 1995). "The angiotensin receptor subtype AT1A predominates in rat forebrain areas involved in blood pressure, body fluid homeostasis and neuroendocrine control". Brain Research. Molecular Brain Research. 30 (1): 53–60. doi:10.1016/0169-328X(94)00272-G. PMID 7609644.
- ^ Scharrer E, Scharrer B (1 January 1945). "Neurosecretion". Physiological Reviews. 25 (1): 171–181. doi:10.1152/physrev.1945.25.1.171. ISSN 1522-1210.
- ^ Raisman G (1997). "An urge to explain the incomprehensible: Geoffrey Harris and the discovery of the neural control of the pituitary gland" (PDF). Annual Review of Neuroscience. 20: 533–66. doi:10.1146/annurev.neuro.20.1.533. PMID 9056724. Archived from the original (PDF) on 2007-07-03. Retrieved 2006-02-10.
- ^ Breathnach CS, Moynihan JB (March 2013). "First ladies in laying the foundation of neuroendocrinology" (PDF). Irish Journal of Medical Science. 182 (1): 143–7. doi:10.1007/s11845-012-0830-9. PMID 22581099. S2CID 8177884. Archived from the original (PDF) on 2018-12-24.
- ^ Guillemin R, Schally AV, Lipscomb HS, Andersen RN, Long JM (April 1962). "On the presence in hog hypothalamus of 3-corticotropin releasing factor, alpha- and beta-melanocyte stimulating hormones, adrenocorticotropin, lysine-vasopressin and oxytocin". Endocrinology. 70 (4): 471–7. doi:10.1210/endo-70-4-471. PMID 13902822. Archived from the original on 8 July 2012.
- ^ Berczi I (2010). "Dr Andor Szentivanyi Memorial". University of Manitoba. Archived from the original on 2009-02-10. (경고: 자동 배경 음악)
- ^ Misler S (September 2009). "Unifying concepts in stimulus-secretion coupling in endocrine cells and some implications for therapeutics". Advances in Physiology Education. 33 (3): 175–86. doi:10.1152/advan.90213.2008. PMC 3747786. PMID 19745043.
- ^ Geracioti TD (2006). "Identifying Hypothyroidism's Psychiatric Presentations". Current Psychiatry. 5 (11): 98–117.
- ^ Huang JT, Leweke FM, Oxley D, Wang L, Harris N, Koethe D, et al. (November 2006). "Disease biomarkers in cerebrospinal fluid of patients with first-onset psychosis". PLOS Medicine. 3 (11): e428. doi:10.1371/journal.pmed.0030428. PMC 1630717. PMID 17090210.
- ^ a b c Leng, G.; Moos, F. C.; Armstrong, W. E. (2010-05-01). "The Adaptive Brain: Glenn Hatton and the Supraoptic Nucleus". Journal of Neuroendocrinology. 22 (5): 318–329. doi:10.1111/j.1365-2826.2010.01997.x. PMC 5713484. PMID 20298459.
- ^ Kandel, E. R. (1964-03-01). "Electrical Properties of Hypothalamic Neuroendocrine Cells". Journal of General Physiology. 47 (4): 691–717. doi:10.1085/jgp.47.4.691. ISSN 1540-7748. PMC 2195356. PMID 14127607.