Inositol-phosphate 포스 파타 아제
Inositol-phosphate phosphatase| 이노시톨-1(또는 4)-모노포스파타아제 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
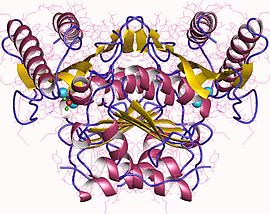 이노시톨모노포스파타아제2,이합체,인간 | |||||||||
| 식별자 | |||||||||
| EC 번호 | 3.1.3.25 | ||||||||
| CAS 번호 | 37184-63-7 | ||||||||
| 데이터베이스 | |||||||||
| 인텐츠 | IntEnz 뷰 | ||||||||
| 브렌다 | 브렌다 엔트리 | ||||||||
| ExPASy | NiceZyme 뷰 | ||||||||
| 케그 | KEGG 엔트리 | ||||||||
| 메타사이크 | 대사 경로 | ||||||||
| 프라이머리 | 프로필 | ||||||||
| PDB 구조 | RCSB PDB PDBe PDBum | ||||||||
| 진 온톨로지 | AmiGO / QuickGO | ||||||||
| |||||||||
| 이노시톨단인산가수분해효소1 | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호. | IMPA1 | ||||||
| Alt. | IMP; IMPA | ||||||
| NCBI유전자 | 3612 | ||||||
| HGNC | 6050 | ||||||
| 옴 | 602064 | ||||||
| 참조 | NP_001138350 | ||||||
| 유니프로트 | P29218 | ||||||
| 기타 데이터 | |||||||
| EC 번호 | 3.1.3.25 | ||||||
| 궤적 | 제8장 Q21.1~q21.3 | ||||||
| |||||||
| 이노시톨단인산가수분해효소2 | |||||||
|---|---|---|---|---|---|---|---|
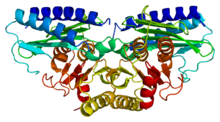 이노시톨단인산가수분해효소2의[1] X선 결정구조 | |||||||
| 식별자 | |||||||
| 기호. | IMPA2 | ||||||
| NCBI유전자 | 3613 | ||||||
| HGNC | 6051 | ||||||
| 옴 | 605922 | ||||||
| 참조 | NP_055029 | ||||||
| 유니프로트 | O14732 | ||||||
| 기타 데이터 | |||||||
| EC 번호 | 3.1.3.25 | ||||||
| 궤적 | 제18장 페이지 11.2 | ||||||
| |||||||
| 이노시톨단인산가수분해효소3 | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호. | IMPAD1 | ||||||
| Alt. | IMPA3 | ||||||
| NCBI유전자 | 54928 | ||||||
| HGNC | 26019 | ||||||
| 옴 | 614010 | ||||||
| 참조 | NP_060283 | ||||||
| 유니프로트 | Q9NX62 | ||||||
| 기타 데이터 | |||||||
| EC 번호 | 3.1.3.25 | ||||||
| 궤적 | 제8장 문제 12.1 | ||||||
| |||||||
이노시톨인산인산인산가수분해효소(EC 3.1.3.25)는 포스포디에스테라아제 계열의 [2]효소이다.포스포파티딜이노시톨 시그널링 경로에 관여하며, 포스포파티딜이노시톨 시그널링 경로는 세포 성장, 아포토시스, 분비 및 정보 [3]처리를 포함한 광범위한 세포 기능에 영향을 미칩니다.이노시톨 모노포스파타아제 억제는 조울증, 특히 조울증 [4]치료에 있어 리튬의 작용에 핵심일 수 있다.
촉매 반응:
- myo-inositol2 phosphate + HO ( \ \ myo-inositol + phosphate
명명법
이 효소는 가수분해효소, 특히 인산 모노에스테르 결합에 작용하는 효소에 속합니다.계통명은 myo-inositol-phosphohydrolase이다.일반적으로 사용되는 다른 이름은 다음과 같습니다.
- 미오이노시톨-1(또는 4)-모노포스파타아제
- 이노시톨 1-아미노사타아제
- L-묘이노시톨-1-인산인산가수분해효소
- 미오이노시톨1-아세타아제
- 이노시톨인산가수분해효소
- 이노시톨 일인산인산가수분해효소
- 이노시톨-1(또는 4)-모노포스파타아제
- myo-inositol-1(또는 4)-인산포스포히드로라아제
- 미오이노시톨단인산가수분해효소 및
- 미오이노시톨-1-아카타아제
구조.
효소는 서브유닛당 277개의 아미노산 잔류물로 구성된 이합체이다.각 이합체는 α-헬리체와 β-시트의 5개 층에 존재하며, 서브 [5]유닛당 총 9개의 α-헬리체와 β-시트를 가진다.IMPase에는 세 개의 친수성 중공 활성 부위가 있으며, 각각 물과 마그네슘 [6]분자와 결합합니다.이러한 결합 부위는 과당 1,6-비스포스파타아제([7]FBPase) 및 이노시톨 폴리인산 1-포스파타아제와 같은 다른 포스포디에스테라아제에서 보존되는 것으로 보인다.
촉매 메커니즘
앞서 이노시톨 일인산염의 가수분해가 2-마그네슘 이온 [5]메커니즘을 통해 IMPase에 의해 촉매된 것으로 보고되었다.그러나 최근의 1.4A 분해능 결정 구조에서는 2개의 이합체의 각 활성 결합 부위에서 3개의 마그네슘 이온이 배위하여 3개의 마그네슘 이온 [6]메커니즘을 지원합니다.가수분해 메커니즘은 현재 다음과 같이 진행되는 것으로 생각된다: 효소는 3개의 물 분자를 포함하는 결합 부위 I에 결합하는 마그네슘 이온에 의해 활성화되고, Glu70과 Asp90의 카르복실산염과 Ile92의 [5]카르보닐에 대한 음전하에 의해 안정화된다.이어서 또 다른 마그네슘 이온이 결합부위 2에 협동결합하고, 결합부위 1에 의해 공유되는 카르복실산염, Asp93, Asp220 및 3개의 물분자를 가진다.다음으로 물 분자 5개와 잔기 Glu70을 가진 제3결합 부위에 대해 약하고 비협조적으로 제3마그네슘을 첨가한다.3개의 마그네슘 이온이 모두 결합하면 이노시톨 단인산가수분해효소가 결합할 수 있으며, 3개의 양전하 마그네슘 이온에 의해 음전하 인산기가 안정화된다.마지막으로 활성수 분자가 친핵체를 작용시켜 기질을 가수분해하여 이노시톨 및 [8]무기인산을 얻는다.
기능.
이노시톨 모노포스파타아제는 진핵세포에서 여러 2차 전달자의 구조적 기초를 형성하는 분자인 미오이노시톨의 세포 내 수준을 유지하는 데 중요한 역할을 한다.IMPase는 이노시톨 일인산염의 이성질을 탈인산염시켜 이노시톨을 생성하는데, 주로 스테레오 이성질체인 미오이노시톨의 [9]형태로 이루어진다.이노시톨 모노포스파타아제는 이노시톨을 [10]생성하는 두 경로의 수렴에 있기 때문에 이노시톨 항상성을 조절할 수 있다.
포스파티딜이노시톨 시그널링 경로 이노시톨 모노포스파타아제
이 경로에서 G결합단백질수용체 및 티로신인산화효소수용체가 활성화되어 포스파티딜이노시톨2인산([3]PIP)2을 가수분해하는 포스폴리파아제C가 활성화되어 막관련 생성물, 디아실글리세롤 및 수용성 생성물인 이노시톨3인산이 생성된다.디아실글리세롤은 여러 단백질 키나아제를 활성화하고 확장된 다운스트림 신호를 생성하며 두 번째 전달자로 작용합니다.는 cytoplasm,[3][10][11]는 비료, 확산, 압축, 세포 대사, 소포 그리고 유체 분비, 그리고 정보 processin 조절에 참여할 수 있어 복잡한 신호 체계를 만드는 것 칼슘 이온 매장을 방출하기 위해 그 소포체의 수용을 활성화시키 이노시톨 triphosphate은 또 두번째 전령이다.neuro에 gnal [12]세포전반적으로 디아실글리세롤과 이노시톨 삼인산 시그널링은 해마 장기 증강, 스트레스 유발 인지 장애 및 신경 성장 원뿔 [11]확산에 영향을 미치는 신경 가소성에 영향을 미친다.또한 PIP는 여러2 시그널링 분자의 전구체일 뿐만 아니라 3' 위치에서 인산화되어 세포 증식, 아포토시스 및 세포 [3]이동에 관여하는 PIP3가 될 수 있다.
이 경로에서 IMPase는 IP3를 재활용하여 PIP를 생성하는2 일반적인 마지막 단계입니다.IMPase는 이노시톨 일인산을 탈인화하여 무기인산과 PIP2의 전구체인 미오이노시톨을 생성함으로써 이를 수행한다.이러한 신호 전달 경로에서 IMPase의 중요한 역할 때문에, IMPase는 억제 및 [11]변조의 잠재적 약물 대상이다.
미오이노시톨 데노보 합성 이노시톨 모노포스파타아제
포도당 6-인산으로부터 myo-inositol의 de novo 합성에 적어도 2개의 알려진 단계가 있다.제1공정에서는 포도당6-인산가수분해효소에 의해 포도당6-인산이 D-이노시톨1일인산으로 변환된다.이노시톨 모노포스파타아제는 D-이노시톨1 모노인산을 탈인화하여 미오이노시톨을 [13]형성하는 마지막 단계를 촉매한다.
임상적 의의
이노시톨 모노포스파타아제는 역사적으로 양극성 [4]장애의 주요 치료제인 리튬의 직접적인 표적으로 여겨져 왔다.리튬은 이노시톨 고갈 가설에 따라 작용한다고 생각된다. 즉, 리튬은 IMPase를 억제함으로써 치료 효과를 내고, 이에 따라 myo-inositol의 [4][14]수치를 감소시킨다.이 가설에 대한 과학적 지지는 존재하지만 제한적이다; 리튬과 이노시톨 모노포스파타아제가 양극성 장애를 치료하거나 미오이노시톨 수치를 감소시키는 완전한 역할은 잘 이해되지 않는다.
이노시톨 고갈 가설을 뒷받침하는 연구진은 리튬이 마그네슘 [15]이온 중 하나에서 정제된 소 이노시톨 모노포스파타아제에 비결정적으로 결합한다는 것을 보여 주었다.리튬을 투여한 설치류들은 [16]가설에 따라 이노시톨 수치 감소를 보였다.조울증 환자에게 투여되는 또 다른 기분 안정제인 발프로에이트도 리튬이 미오이노시톨에 [17]미치는 영향을 모방하는 것으로 나타났다.
그러나 일부 임상연구에서는 리튬을 투여한 조울증 환자들이 미오이노시톨 수치를 낮춘 반면 다른 환자들은 미오이노시톨 수치를 [18][19][20]낮춘 것으로 나타났다.게다가 리튬은 또한 포스포이노시티드 경로에 존재하는 효소인 이노시톨 폴리인산 1-포스파타아제(IPP)와 결합하고, 이[21] 메커니즘을 통해 이노시톨 수치를 낮출 수 있다. 리튬과 IMPase가 양극성 장애 [4][14]환자에서 수행하는 역할을 완전히 설명하기 위해서는 더 많은 연구가 필요하다.
리튬이 양극성 장애 치료에 효과적이라는 사실에도 불구하고, 리튬은 매우 독성이 강한 금속이며, 독성 선량은 치료 용량보다 약간 더 클 뿐이다.[2] 독성이 적은 이노시톨 모노포스파타아제의 새로운 억제제는 양극성 [22]장애에 대한 보다 바람직한 치료법이 될 수 있다.그러한 억제제는 [23]뉴런에서 이노시톨 모노포스파타아제에 도달하기 위해 혈액-뇌 장벽을 넘어야 한다.
레퍼런스
- ^ Arai R, Ito K, Ohnishi T, Ohba H, Akasaka R, Bessho Y, et al. (May 2007). "Crystal structure of human myo-inositol monophosphatase 2, the product of the putative susceptibility gene for bipolar disorder, schizophrenia, and febrile seizures". Proteins. 67 (3): 732–42. doi:10.1002/prot.21299. PMID 17340635. S2CID 46602105.
- ^ a b Can A, Schulze TG, Gould TD (August 2014). "Molecular actions and clinical pharmacogenetics of lithium therapy". Pharmacology, Biochemistry, and Behavior. 123: 3–16. doi:10.1016/j.pbb.2014.02.004. PMC 4220538. PMID 24534415.
- ^ a b c d [필요한 건]
- ^ a b c d Harwood AJ (January 2005). "Lithium and bipolar mood disorder: the inositol-depletion hypothesis revisited". Molecular Psychiatry. 10 (1): 117–26. doi:10.1038/sj.mp.4001618. PMID 15558078. S2CID 20026448.
- ^ a b c Lu S, Huang W, Li X, Huang Z, Liu X, Chen Y, et al. (September 2012). "Insights into the role of magnesium triad in myo-inositol monophosphatase: metal mechanism, substrate binding, and lithium therapy". Journal of Chemical Information and Modeling. 52 (9): 2398–409. doi:10.1021/ci300172r. PMID 22889135.
- ^ a b Gill R, Mohammed F, Badyal R, Coates L, Erskine P, Thompson D, et al. (May 2005). "High-resolution structure of myo-inositol monophosphatase, the putative target of lithium therapy". Acta Crystallographica. Section D, Biological Crystallography. 61 (Pt 5): 545–55. doi:10.1107/S0907444905004038. PMID 15858264.
- ^ Bone R, Springer JP, Atack JR (November 1992). "Structure of inositol monophosphatase, the putative target of lithium therapy". Proceedings of the National Academy of Sciences of the United States of America. 89 (21): 10031–5. Bibcode:1992PNAS...8910031B. doi:10.1073/pnas.89.21.10031. PMC 50271. PMID 1332026.
- ^ Singh, Parmvir. "Myo-inositol Monophosphatase, the Target of Lithium Therapy". Archived from the original on 2013-06-04. Retrieved 2020-01-23.
- ^ Chung; Chang (1996). "A divergent synthesis of regio-isomers of myo-inositol monophosphate". Korean Journal of Med. Chem. 6: 162–165.
- ^ a b Berridge MJ, Downes CP, Hanley MR (November 1989). "Neural and developmental actions of lithium: a unifying hypothesis". Cell. 59 (3): 411–9. doi:10.1016/0092-8674(89)90026-3. PMID 2553271. S2CID 41816045.
- ^ a b c Schloesser RJ, Huang J, Klein PS, Manji HK (January 2008). "Cellular plasticity cascades in the pathophysiology and treatment of bipolar disorder". Neuropsychopharmacology. 33 (1): 110–33. doi:10.1038/sj.npp.1301575. PMID 17912251. S2CID 2024963.
- ^ Berridge MJ (June 2009). "Inositol trisphosphate and calcium signalling mechanisms". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1793 (6): 933–40. doi:10.1016/j.bbamcr.2008.10.005. PMID 19010359.
- ^ Chen IW, Charalampous CF (May 1966). "Biochemical studies on inositol. IX. D-Inositol 1-phosphate as intermediate in the biosynthesis of inositol from glucose 6-phosphate, and characteristics of two reactions in this biosynthesis". The Journal of Biological Chemistry. 241 (10): 2194–9. doi:10.1016/S0021-9258(18)96606-8. PMID 4287852.
- ^ a b Brown KM, Tracy DK (June 2013). "Lithium: the pharmacodynamic actions of the amazing ion". Therapeutic Advances in Psychopharmacology. 3 (3): 163–76. doi:10.1177/2045125312471963. PMC 3805456. PMID 24167688.
- ^ Saudek V, Vincendon P, Do QT, Atkinson RA, Sklenar V, Pelton PD, et al. (August 1996). "7Li nuclear-magnetic-resonance study of lithium binding to myo-inositolmonophosphatase". European Journal of Biochemistry. 240 (1): 288–91. doi:10.1111/j.1432-1033.1996.0288h.x. PMID 8925839.
- ^ Allison JH, Stewart MA (October 1971). "Reduced brain inositol in lithium-treated rats". Nature. 233 (43): 267–8. doi:10.1038/newbio233267a0. PMID 5288124.
- ^ O'Donnell T, Rotzinger S, Nakashima TT, Hanstock CC, Ulrich M, Silverstone PH (October 2000). "Chronic lithium and sodium valproate both decrease the concentration of myo-inositol and increase the concentration of inositol monophosphates in rat brain". Brain Research. 880 (1–2): 84–91. doi:10.1016/s0006-8993(00)02797-9. PMID 11032992. S2CID 8823582.
- ^ Moore GJ, Bebchuk JM, Parrish JK, Faulk MW, Arfken CL, Strahl-Bevacqua J, Manji HK (December 1999). "Temporal dissociation between lithium-induced changes in frontal lobe myo-inositol and clinical response in manic-depressive illness". The American Journal of Psychiatry. 156 (12): 1902–8. doi:10.1176/ajp.156.12.1902. PMID 10588403.
- ^ Patel NC, Cecil KM, Strakowski SM, Adler CM, DelBello MP (December 2008). "Neurochemical alterations in adolescent bipolar depression: a proton magnetic resonance spectroscopy pilot study of the prefrontal cortex". Journal of Child and Adolescent Psychopharmacology. 18 (6): 623–7. doi:10.1089/cap.2007.151. PMC 2935834. PMID 19108667.
- ^ Silverstone PH, McGrath BM (2009). "Lithium and valproate and their possible effects on themyo-inositol second messenger system in healthy volunteers and bipolar patients". International Review of Psychiatry. 21 (4): 414–23. doi:10.1080/09540260902962214. PMID 20374155. S2CID 205645556.
- ^ Inhorn RC, Majerus PW (October 1988). "Properties of inositol polyphosphate 1-phosphatase". The Journal of Biological Chemistry. 263 (28): 14559–65. doi:10.1016/S0021-9258(18)68256-0. PMID 2844776.
- ^ Atack, J. (1997). "Inositol Monophosphatase Inhibitors— Lithium Mimetics?". Medicinal Research Reviews. 17 (2): 215–224. doi:10.1002/(sici)1098-1128(199703)17:2<215::aid-med3>3.0.co;2-2. PMID 9057165. S2CID 27534316.
- ^ Singh N, Halliday AC, Thomas JM, Kuznetsova OV, Baldwin R, Woon EC, et al. (2013). "A safe lithium mimetic for bipolar disorder". Nature Communications. 4: 1332. Bibcode:2013NatCo...4.1332S. doi:10.1038/ncomms2320. PMC 3605789. PMID 23299882.
추가 정보
- Parthasarathy L, Vadnal RE, Parthasarathy R, Devi CS (1994). "Biochemical and molecular properties of lithium-sensitive myo-inositol monophosphatase". Life Sciences. 54 (16): 1127–42. doi:10.1016/0024-3205(94)00835-3. PMID 8152337.
- Bradley JJ (1988). The Pitfalls of Attempted Suicide: Hazards of Lithium Carbonate Therapy. London: The Medical Protection Society.
- Fauroux CM, Freeman S (1999). "Inhibitors of inositol monophosphatase". Journal of Enzyme Inhibition. 14 (2): 97–108. doi:10.3109/14756369909036548. PMID 10445037.
- Pollack SJ, Atack JR, Knowles MR, McAllister G, Ragan CI, Baker R, et al. (June 1994). "Mechanism of inositol monophosphatase, the putative target of lithium therapy". Proceedings of the National Academy of Sciences of the United States of America. 91 (13): 5766–70. Bibcode:1994PNAS...91.5766P. doi:10.1073/pnas.91.13.5766. PMC 44077. PMID 8016062.
- Wilkie J, Cole AG, Gani D (January 1995). "3-Dimensional interactions between inositol monophosphatase and its substrates, inhibitors and metal ion cofactors". Journal of the Chemical Society, Perkin Transactions 1 (21): 2709–2727. doi:10.1039/P19950002709.
- Cole AG, Gani D (January 1995). "Active conformation of the inositol monophosphatase substrate, adenosine 2?-phosphate: role of the ribofuranosyl O-atoms in chelating a second Mg2+ ion". Journal of the Chemical Society, Perkin Transactions 1 (21): 2685–2694. doi:10.1039/P19950002685.
- Eisenberg F (April 1967). "D-myoinositol 1-phosphate as product of cyclization of glucose 6-phosphate and substrate for a specific phosphatase in rat testis". The Journal of Biological Chemistry. 242 (7): 1375–82. doi:10.1016/S0021-9258(18)96102-8. PMID 4290245.
- Gee NS, Ragan CI, Watling KJ, Aspley S, Jackson RG, Reid GG, et al. (February 1988). "The purification and properties of myo-inositol monophosphatase from bovine brain". The Biochemical Journal. 249 (3): 883–9. doi:10.1042/bj2490883. PMC 1148789. PMID 2833231.
- Hallcher LM, Sherman WR (November 1980). "The effects of lithium ion and other agents on the activity of myo-inositol-1-phosphatase from bovine brain". The Journal of Biological Chemistry. 255 (22): 10896–901. doi:10.1016/S0021-9258(19)70391-3. PMID 6253491.
- Yoshikawa T, Turner G, Esterling LE, Sanders AR, Detera-Wadleigh SD (September 1997). "A novel human myo-inositol monophosphatase gene, IMP.18p, maps to a susceptibility region for bipolar disorder". Molecular Psychiatry. 2 (5): 393–7. doi:10.1038/sj.mp.4000325. PMID 9322233. S2CID 24336959.
- Cockcroft, S. (Ed.) , 포스포이노시티드 생물학, 포스포이노시티드 생물학, 2000, 페이지 320-338.
- Ackermann KE, Gish BG, Honchar MP, Sherman WR (March 1987). "Evidence that inositol 1-phosphate in brain of lithium-treated rats results mainly from phosphatidylinositol metabolism". The Biochemical Journal. 242 (2): 517–24. doi:10.1042/bj2420517. PMC 1147736. PMID 3036092.



