메발로네이트키나아제 결핍증
Mevalonate kinase deficiency이 글은 위키백과 스타일 매뉴얼의 준수를 위해 편집이 필요하다.특히 MEDMOS(자체적인 기사/Hyper-IgD 증후군이 필요할 수 있는 부분이 있는 것 같다)를 사용하지 않는 문제가 있다.하면 개선하도록 .(2021년 10월)(이 템플릿 하는 방법 및 |
| 메발로네이트키나아제 결핍증 | |
|---|---|
| 기타 이름 | 메발론산뇨증[1] 및 하이퍼 면역글로불린D 증후군(HIDS) |
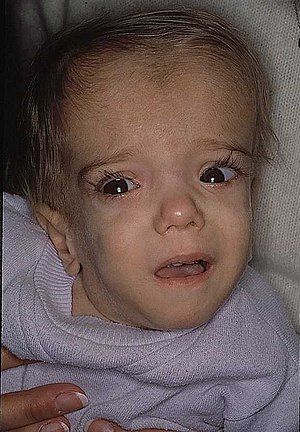 | |
| 생후 21개월의 메발론산염 키나아제 결핍증 환자로서 두개골의 특징적 특징을 보인다. | |
| 전문 | 혈액학, 신경학, 면역학, 의학 유전학, 내분비학 |
메발로네이트키나아제 결핍증(MKD)은 콜레스테롤과 이소프로노이드의 생합성을 방해하는 자가 열성[2] 대사 장애다.[3]그것은 매우 희귀한 유전병이다.null
혈액 내 면역글로불린 D 수치가 높아진 것이 특징이다.메발로네이트키나아제(MVK)는 콜레스테롤과 이소프로노이드의 생합성에 관여하는 효소로 Mg가2+ 존재하는 상태에서 메발로네이트-5인산염으로의 메발로네이트 전환에 필요한 효소다.MKD는 메발로네이트키나아제를 암호화하는 유전자의 돌연변이로 인해 이 효소의 활동성이 감소 또는 부족하게 된다.이러한 결핍 때문에 메발론산은 체내에 축적될 수 있으며, 소변에서 높은 수치가 발견된다.MKD의 심각도는 이러한 결핍의 정도에 따라 달라지는데, 고임문글로불린혈증 D 증후군(1984년 HIDS로 처음 설명)은 덜 심각하지만 더 흔하고, 메발론산뇨증(MVA)은 더 심각하지만 희귀한 형태다.null
유전학
메발로네이트키나아제 결핍증은 자가 열성적 방식으로 유전되는데, 이는 아이가 영향을 받기 위해서는 양쪽 부모로부터 유전자의 결함 있는 사본을 물려받아야 한다는 것을 의미한다.[2]기능상실 돌연변이의 예다.메발로네이트 키나아제를 암호화하는 유전자는 locus 12q14에서 10 exon으로 구성된다.[4]유전자의 약 63개의 병리학적 염기서열 변이가 특징지어졌다.[citation needed]이들 중 가장 흔한 것은 V377I, I268T, H20P/N, P167L로, 대상자의 70%에 존재한다.[4]null
면역글로불린D
면역글로불린 D(IgD)는 특정 유형의 백혈구에서 생성되는 단백질이다.면역글로불린에는 5가지 등급이 있다.IgG, IgA, IgM, IgE 및 IgD.그들은 각각 면역체계에 중요한 역할을 한다.IgD의 여러 가지 효과 중 하나가 면역체계를 활성화하는 것이지만 IgD의 기능은 여전히 불분명하다.null
생화학
MKD에서 사이토카인 인터루킨 1 베타(IL-1β)를 촉진하는 열 분비가 증가하는데, 이는 결함이 있는 단백질 태교에 의해 매개되었을 가능성이 크다.혼수성(Parenylation)은 단백질에 소수성 이소프로노이드(FPP)나 제라닐제라닐 피로인산염(GGGPP)과 같은 것을 첨가하는 것을 말한다.이와 같은 이소프로노이드들이 표적 단백질과 결합하면 이는 단백질의 세포 위치와 기능에 영향을 미친다.인간 단세포 MKD 모델에서 GGPP의 결핍은 IL-1β의 과잉생산을 초래하고 RoA의 태교에 결함이 있다는 것을 발견했다.이것은 Rac1과 PKB의 수준을 증가시켜 GTPases와 B7-glycoprotins에 영향을 미친다.앞서 Rac1/PI3K/PKB 경로가 MKD의 병원체 생성과 연계되어 있다는 사실이 밝혀졌다.RoA의 비활성화는 NLRP3- 또는 Caspase-1 활동과 무관하게 IL-1β mRNA 전사 유도자를 작용한다.RoA의 결함으로 인해 세포에 결함이 있는 미토콘드리아(긴장 및 불안정)의 형성이 있다.보통 결함이 있는 미토콘드리아는 자동포자기의 메커니즘에 의해 세포 안에서 제거된다.그러나 MKD에서는 결함이 있는 미토콘드리아를 시토솔로부터 분리하는 것이 중단된다.그 결과 미토콘드리아 DNA가 사이토솔에 축적되기 시작하여 IL-1β의 생산을 담당하는 NLRP3를 결합하고 활성화한다.활성화는 직접 또는 간접적일 수 있다.반응성 산소종(ROS)으로도 활성화할 수 있다.[5]영향을 받은 개인의 단세포와 대식세포도 IL-Iβ 이외의[5] 종양 괴사 인자 알파(TNF-α), 인터루킨 6(IL-6)를 더 높은 수준으로 생성하는 것으로 알려져 있다.열(페버) 공격 중에는 CRP(Creactive 단백질)도 증가한다.[4]CRP는 간에서 분비되어 염증을 일으킨다.null
하이퍼-IgD 증후군
재발열이 있는 고임무노글로불린혈증 D는 원래 1984년 [6]내과 의사인 조스 반 데르 미어가 레이든 대학 의학 센터에서 설명한 정기열 증후군이다.전 세계적으로 300건 이상의 사례가 설명되지 않았다.그것은 현재 MKD의 대립 변형으로 인식되고 있다.[7]
징후 및 증상
HIDS는 다수의 주기적인 발열 증후군 중 하나이다.그것은 발열, 관절염, 주기적인 구강 궤양, 그리고 설사를 포함한 피부 병변으로 특징지어진다.실험실 특성은 정상적인 IgD를 가진 사례가 설명되었지만 급성 위상 반응(이열 CRP 및 ESR)과 현저하게 상승된 IgD(그리고 종종 IgA)를 포함한다.[8]null
국제 등록에는 다른 나라의 사례가 다수 포함되어 있지만, 주로 네덜란드와 프랑스에서 기술되어 왔다.[8]null
차등 진단에는 기원을 알 수 없는 발열, 가족성 지중해열(FMF), 가족성 동면열(또는 정기증후군/TRAPs 관련 TNFα 수신이 포함된다.[8]null
원인
사실상 신드롬을 앓고 있는 모든 사람들은 메발로네이트 키나아제 유전자에 돌연변이를 가지고 있는데, 이것은 중요한 세포 대사 경로인 HMG-CoA 환원효소 경로의 일부분이다.[9][10]실제로 유사한 발열 발작(그러나 정상적인 IgD)이 메발론산뇨증 환자에게 설명되어 왔다. 이는 신진대사의 선천적인 오류로 현재 심각한 형태의 HIDS로 간주되고 있다.[8]
병리학
메발로네이트 키나아제 돌연변이가 열분화 현상을 어떻게 유발하는지는 알려지지 않았지만, 콜레스테롤 생합성 경로인 혼전사슬(제라닐제라니올과 파르네솔)의 다른 제품들이 그 역할을 할 것으로 추정되고 있다.[8]null
진단
메발로네이트키나제 결핍은 소변 속에 메발론산이 축적되어 효소 메발로네이트키나제[11](ATP:mevalonate 5-phosphotransferase; EC 2.7.1.36)의 불충분한 활성으로 야기된다.null
그 장애는 1985년에 처음 묘사되었다.[12]null
신진대사의 선천적인 오류로 분류되는 메발론산염 키나아제 결핍은 보통 발달지연, 저혈압, 빈혈, 간성플레노메날리, 다양한 이형성, 정신지체, 전반적인 성장장애, 그리고 몇 가지 다른 특징들을 초래한다.null

치료
MKD에 대한 치료는 없다.그러나 염증이나 다른 효과는 어느 정도 줄어들 수 있다.null
- IL-1 표적형 약물은 장애의 영향을 줄이는 데 사용될 수 있다.아나킨라는 IL-1 수용체에 대항한다.아나킨라는 IL-1 수용체를 결합하여 IL-1α와 IL-1β 모두의 작용을 방지하고, MKD에서 임상 및 생화학적 염증을 감소시키는 것으로 증명되었다.일상적으로 사용할 경우 염증성 공격의 심각성은 물론 빈도를 효과적으로 감소시킬 수 있다.이 약물의 사용으로 인한 단점은 고통스러운 주사부위 반응의 발생이며, 가까운 장래에 약물이 단종됨에 따라 열성 공격이 시작된다.(12세 환자에서 조사됨)
- Canakinumab은 IL-1β에 대한 장기간 작용하는 단핵항체로, 사례 보고와 관찰 사례 시리즈에서 경증 및 중증 MKD를 앓고 있는 환자의 빈도와 중증도를 모두 줄이는 데 효과가 있는 것으로 나타났다.생리적 효과를 감소시키지만 생화학적 파라미터는 여전히 상승된 상태를 유지한다(갈레오티 외 연구진은 MKD로 고통 받는 6명의 환자보다 더 효과적이라는 것을 보여주었다).
- 항TNF 치료는 MKD에 효과적일 수 있지만 그 효과는 대부분 부분적이며 치료 실패와 임상적 악화가 인플릭스맵이나 에탄셉트에 대한 환자들에게 자주 설명되어 왔다.[5]소수의 MKD 환자들에게서 인간 단클론 항 TNFα 항체 보조최소제의 유익한 효과가 나타났다.
- 대부분의 MKD 환자들은 반IL-1 치료의 혜택을 받는다.그러나, 반IL-1 내성 질환도 발생할 수 있다.예토실리주맙(인터루킨-6(IL-6) 수용체에 대한 인간화된 단클론 항체).이 약은 환자들이 아나킨라에게 반응이 없을 때 사용된다.(선디 등은 아나킨라가 효험이 없는 젊은 여성을 토실리주맙으로 치료했다.)생화학적, 임상적 염증을 줄이는 데 효과가 있는 것으로 밝혀졌다[30].스토펠스 외 연구진은 비록 이 두 환자 중 한 명이 생화학적인 염증 표지가 없는 상태에서 끈질기게 가벼운 염증 증상을 보였지만, 염증 공격의 빈도와 심각성의 감소를 관찰했다.
- 조혈모세포 이식의 유익한 효과는 심각한 메발로네이트 키나아제 결핍상태에서 사용될 수 있다(한 소녀에게서 모든 유발 줄기세포 이식이 관찰된 후 MRI에 대한 뇌골격화 개선).그러나 간 이식 수술은 이 환자의 열성 발작에는 영향을 미치지 않았다.[5]
HIDS 치료
카나키눔밥은 HIDS 치료 승인을 받아 효과가 있는 것으로 나타났다.[13][14]면역억제제인 에타너셉트와[15] 아나킨라도[16] 효과가 있는 것으로 나타났다.스타틴 약물은 메발론화 수준을 낮출 수 있으며 현재 조사 중이다.최근의 단일 사례 보고서는 비스포스포네이트를 잠재적 치료 옵션으로 부각시켰다.[17]null
역학
세계적으로 10만 명 중 1명도 안 되는 사람들이 HIDS를 앓고 있으며, 이 중 200명에 이르는 사람들이 MKD를 앓고 있다.[4]이것은 그 상태를 희귀한 유전 질환으로 분류한다.null
추가 이미지
참조
- ^ 온라인 멘델리안 상속인(OMIM): 251170
- ^ a b "Mevalonate kinase deficiency".
- ^ Mancini J, Philip N, Chabrol B, Divry P, Rolland MO, Pinsard N (May–Jun 1993). "Mevalonic aciduria in 3 siblings: a new recognizable metabolic encephalopathy". Pediatr. Neurol. 9 (3): 243–246. doi:10.1016/0887-8994(93)90095-T. PMID 8352861.
- ^ a b c d "Mevalonate Kinase Deficiency".
- ^ a b c d Mulders-Manders, CM; Simon, A (2015). "Hyper-IgD syndrome/mevalonate kinase deficiency: what is new?". Semin Immunopathol. 37 (4): 371–6. doi:10.1007/s00281-015-0492-6. PMC 4491100. PMID 25990874.
- ^ van der Meer JW, Vossen JM, Radl J, et al. (May 1984). "Hyperimmunoglobulinaemia D and periodic fever: a new syndrome". Lancet. 1 (8386): 1087–90. doi:10.1016/S0140-6736(84)92505-4. PMID 6144826.
- ^ "OMIM Entry - * 251170 - MEVALONATE KINASE; MVK". omim.org.
- ^ a b c d e Drenth JP, van der Meer JW (December 2001). "Hereditary periodic fever". N. Engl. J. Med. 345 (24): 1748–57. doi:10.1056/NEJMra010200. PMID 11742050.
- ^ Drenth JP, Cuisset L, Grateau G, et al. (June 1999). "Mutations in the gene encoding mevalonate kinase cause hyper-IgD and periodic fever syndrome. International Hyper-IgD Study Group". Nat. Genet. 22 (2): 178–81. doi:10.1038/9696. PMID 10369262.
- ^ Houten SM, Kuis W, Duran M, et al. (June 1999). "Mutations in MVK, encoding mevalonate kinase, cause hyperimmunoglobulinaemia D and periodic fever syndrome". Nat. Genet. 22 (2): 175–7. doi:10.1038/9691. PMID 10369261.
- ^ Bretón Martínez JR, Cánovas Martínez A, Casaña Pérez S, Escribá Alepuz J, Giménez Vázquez F (Oct 2007). "Mevalonic aciduria: report of two cases". J. Inherit. Metab. Dis. 30 (5): 829. doi:10.1007/s10545-007-0618-7. PMID 17578678.
- ^ Berger R, Smit GP, Schierbeek H, Bijsterveld K, le Coultre R (Oct 1985). "Mevalonic aciduria: an inborn error of cholesterol biosynthesis?". Clin. Chim. Acta. 152 (1–2): 219–222. doi:10.1016/0009-8981(85)90195-0. PMID 4053401.
- ^ Aróstegui, JI; Anton, J.; Calvo, I.; Robles, A.; Speziale, A.; Joubert, Y.; Junge, G.; Yagüe, J. (2015-01-01). "Long-term efficacy and safety of Canakinumab in active Hyper-IgD syndrome (HIDS): results from an open-label study". Pediatric Rheumatology. 13 (1): O58. doi:10.1186/1546-0096-13-S1-O58. ISSN 1546-0096. PMC 4596954.
- ^ Kozlova, A.; Mamzerova, E.; Maschan, A.; Shcherbina, A. (2014-06-01). "AB0918 Efficacy and Safety of Treatment of Children with Traps and Hids with IL1 Blocker (CANAKINUMAB)". Annals of the Rheumatic Diseases. 73 (Suppl 2): 1103–1104. doi:10.1136/annrheumdis-2014-eular.3697. ISSN 0003-4967.
- ^ Takada, Kazuki; Aksentijevich, Ivona; Mahadevan, Vijayabhanu; Dean, Jane A.; Kelley, Richard I.; Kastner, Daniel L. (2003-09-01). "Favorable preliminary experience with etanercept in two patients with the hyperimmunoglobulinemia D and periodic fever syndrome". Arthritis and Rheumatism. 48 (9): 2645–2651. doi:10.1002/art.11218. ISSN 0004-3591. PMID 13130485.
- ^ Rigante D, Ansuini V, Bertoni B, et al. (November 2006). "Treatment with anakinra in the hyperimmunoglobulinemia D/periodic fever syndrome". Rheumatol. Int. 27 (1): 97–100. doi:10.1007/s00296-006-0164-x. PMID 16871408.
- ^ Cantarini, L; Vitale, A; Magnotti, F; Lucherini, O. M.; Caso, F; Frediani, B; Galeazzi, M; Rigante, D (2013). "Weekly oral alendronate in mevalonate kinase deficiency". Orphanet Journal of Rare Diseases. 8: 196. doi:10.1186/1750-1172-8-196. PMC 3880037. PMID 24360083.





