탄산칼륨
Potassium carbonate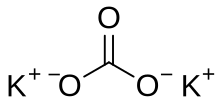 | |
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 탄산칼륨 | |
| 기타 이름 탄산칼륨, 탄산칼륨, 아탄산칼륨, 아탄산칼륨, 진주회, 칼륨, 주석염, 쑥염. | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.008.665 |
| E번호 | E501(i)(산도 조절기, ...) |
PubChem CID | |
| RTECS 번호 |
|
| 유니 |
|
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| K 2CO 3 | |
| 몰 질량 | 138.19 g/140 |
| 외모 | 흰색 흡습성 고체 |
| 밀도 | 2.43g/cm3 |
| 녹는점 | 891 °C (1,636 °F, 1,164 K) |
| 비등점 | 분해하다 |
| 110.3g/100mL(20°C) 149.2g/100mL(100°C) | |
| 용해성 | |
자화율(δ) | - 59.0·10cm−63/수직선 |
| 열화학[1] | |
열용량 (C) | 114.4 J·mol−1·K−1 |
표준 어금니 엔트로피 (S | 155.5 J·mol−1·K−1 |
표준 엔탈피/ 형성 (δHf⦵298) | - 1151.0 kJ/mol−1 |
깁스 자유 에너지 ( (Gf)) | - 1063.5kJ/mol−1 |
융해 엔탈피 (δHf⦵fus) | 27.6 kJ/mol−1 |
| 위험 요소 | |
| GHS 라벨링: | |
 | |
| 경고 | |
| H302, H315, H319, H335 | |
| P261, P305+P351+P338 | |
| NFPA 704(파이어 다이아몬드) | |
| 플래시 포인트 | 불연성 |
| 치사량 또는 농도(LD, LC): | |
LD50(중간선량) | 1870 mg/kg (구강, 쥐)[2] |
| 안전 데이터 시트(SDS) | ICSC 1588 |
| 관련 화합물 | |
기타 음이온 | 중탄산칼륨 |
기타 캐티온 | 탄산리튬 탄산나트륨 탄산 루비듐 탄산 세슘 |
관련 화합물 | 탄산암모늄 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
탄산칼륨은 KCO의23 무기화합물이다.그것은 물에 녹는 하얀 소금이다.이것은 조해성이며, 종종 축축하거나 젖은 고체로 나타납니다.탄산칼륨은 주로 비누와 [3]유리 생산에 사용된다.
역사
탄산칼륨은 칼륨의 주요 성분이며 보다 정제된 진주재 또는 주석의 소금입니다.역사적으로 진주재는 불순물을 제거하기 위해 가마에서 칼륨을 구워 만들었다.남은 고운 하얀 가루는 진주재였다.미국 특허청에 의해 발행된 첫 번째 특허는 1790년 포타쉬와 진주재를 만드는 개선된 방법으로 새뮤얼 홉킨스에게 주어졌다.
베이킹 파우더가 개발되기 전인 18세기 후반 북미에서는 펄 애쉬가 [4][5]퀵 빵의 발효제로 사용되었습니다.
생산.
탄산칼륨은 [3]수산화칼륨과 이산화탄소를 반응시켜 상업적으로 제조된다.
- 2 KOH + CO2 → KCO23 + HO2
용액에서 초수화물23 KCO를 결정화한다.3⁄2HO2('포타쉬 하이드레이트').이 고체를 200°C(392°F) 이상으로 가열하면 무수 염분이 생성됩니다.다른 방법으로는 유기 아민의 존재 하에서 염화칼륨을 이산화탄소로 처리하여 중탄산칼륨을 생성하고, 그 후 소성한다.
- 23 KHCO → KCO23 + HO + CO22
적용들
- (비누, 유리 및 식기 제조를 위해)
- 염화칼슘 및 황산마그네슘과 같은 다른 건조제가 호환되지 않을 수 있는 약한 건조제로 사용한다.산성화합물에는 적합하지 않지만 산성 불순물이 적으면 유기상 건조시 유용하다.또한 [6]증류 전에 일부 케톤, 알코올 및 아민을 건조시키는 데 사용될 수 있습니다.
- 전통 용도가 많은 요리입니다.중국 및 동남아 요리와 중국 수제면, 월병 등에서 소비되는 풀 젤리의 원재료입니다.그것은 또한 곱창을 부드럽게 하기 위해 사용된다.독일의 생강빵 레시피는 하트손과 함께 사용되기는 하지만 종종 탄산칼륨을 베이킹제로 사용한다.탄산칼륨의 사용은 해를 방지하기 위해 일정량 이내로 제한해야 하며 안내 없이 사용해서는 안 된다.
- 천연 코코아 콩의 pH(즉, 산도를 감소) 균형을 유지하여 더치 프로세스 초콜릿을 생산하기 위한 코코아 분말의 알칼리화. 또한 향을 향상시킨다.코코아 가루에 탄산칼륨을 첨가하는 과정은 네덜란드인 코엔라드 요하네스 반 후텐에 의해 1828년에 처음 개발되었기 때문에 보통 "네덜란드 가공 코코아 가루"라고 불린다.
- 메이드 또는 와인 생산 시 완충제로 사용됩니다.
- 골동품 문서에서는 [7]경수를 부드럽게 하기 위해 사용된 것으로 보고되고 있다.
- 딥 지방 프라이어 및 기타 B급 관련 화재를 진압할 때 화재 진압제로 사용됩니다.
- 질산칼륨의 부산물로써도 응축된 에어로졸 화재진압에 사용됩니다.
- 용접 플럭스의 성분으로, 아크-프로덕트 로드의 플럭스 코팅에 사용됩니다.
- 닭구이 등 가축의 칼륨 요구량을 충족시키기 위한 동물 사료 성분으로 사용됩니다.
- 스웨덴의 스너스 코담배에서 산도조절제로서
레퍼런스
- ^ CRC handbook of chemistry and physics : a ready-reference book of chemical and physical data. William M. Haynes, David R. Lide, Thomas J. Bruno (2016-2017, 97th ed.). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942.
{{cite book}}: CS1 유지보수: 기타 (링크) - ^ Chambers, Michael. "ChemIDplus - 584-08-7 - BWHMMNNQKKPAPP-UHFFFAOYSA-L - Potassium carbonate [USP] - Similar structures search, synonyms, formulas, resource links, and other chemical information". chem.sis.nlm.nih.gov. Archived from the original on 2014-08-12.
- ^ a b H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger (2005). "Potassium Compounds". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a22_039. ISBN 3527306730.
{{cite encyclopedia}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ Hartford, Hudson & Goodwin, Hartford, 1796년에 인쇄된 American Cookery의 "American Cookery"에서 "진주재"에 대한 언급을 참조하십시오.
- ^ Civitello, Linda (2017). Baking powder wars : the cutthroat food fight that revolutionized cooking. Urbana, Illinois: University of Illinois Press. pp. 18–22. ISBN 9780252041082.
- ^ Leonard, J.; Lygo, B.; Procter, G. "Advanced Practical Organic Chemistry" 1998, Stanley Thomas Publishers Ltd.
- ^ 아이, 리디아 M. "미국의 검소한 주부" 1832
참고 문헌
- 뉴욕 옥스포드 대학 출판부 과학사전, 2004
- Yu. Platonov, Andrew; Evdokimov, Andrey; Kurzin, Alexander; D. Maiyorova, Helen (29 June 2002). "Solubility of Potassium Carbonate and Potassium Hydrocarbonate in Methanol". Journal of Chemical & Engineering Data. 47 (5): 1175–1176. doi:10.1021/je020012v.



