폴리아크릴아미드겔전기영동
Polyacrylamide gel electrophoresis폴리아크릴아미드겔 전기영동(PAGE)은 생화학, 법의화학, 유전학, 분자생물학 및 생명공학에서 널리 사용되는 기술로, 전기영동 이동도에 따라 보통 단백질 또는 핵산인 생물학적 고분자를 분리한다.전기영동 이동성은 분자의 길이, 구조 및 전하의 함수이다.폴리아크릴아미드겔 전기영동은 RNA 검체를 분석하는 데 사용되는 강력한 도구입니다.전기영동 후 폴리아크릴아미드겔이 변성되면 RNA종의 [1]샘플 조성에 대한 정보를 제공합니다.
아크릴로니트릴의 수화 작용으로 아크릴아미드 분자가 생성된다.니트릴35 하이드라타아제([2]CHNO).아크릴아미드 단량체는 물을 첨가하기 전에 분말 상태에 있다.아크릴아미드는 인체 신경계에 독성이 있으므로 아크릴아미드를 사용할 때는 모든 안전 조치를 준수해야 합니다.아크릴아미드는 물에 녹으며 유리방사성 개시제를 첨가하면 중합되어 폴리아크릴아미드가 [2]형성됩니다.모공 크기를 조절할 수 있기 때문에 아크릴아미드 수화를 통해 폴리아크릴아미드 겔을 만드는 것이 유용합니다.아크릴아미드의 농도가 증가하면 중합 후 모공 크기가 감소합니다.작은 모공을 가진 폴리아크릴아미드 겔은 작은 분자가 모공으로 들어가 큰 분자가 모공 개구부에 갇히는 동안 겔을 통해 이동할 수 있기 때문에 작은 분자를 더 잘 검사하도록 도와줍니다.
모든 형태의 겔 전기영동과 마찬가지로, 분자는 본래의 상태로 작동하여 분자의 고차 구조를 보존할 수 있습니다.이 메서드는 native-PAGE라고 불립니다.또는 화학적 변성제를 첨가하여 이 구조를 제거하고 이동성이 길이에만 의존하는 비구조화 분자로 만들 수 있다(단백질-SDS 복합체는 모두 유사한 질량 대 전하 비율을 가지기 때문이다).이 순서를 SDS-PAGE라고 부릅니다.도데실황산나트륨폴리아크릴아미드겔전기영동(SDS-PAGE)은 분자량의 차이를 바탕으로 분자를 분리하는 방법이다.겔 전기영동이 이루어지는 pH에서 SDS 분자는 음전하되어 단백질에 정해진 비율로 결합되며, 아미노산 [3]: 164–79 2개당 약 1분자의 SDS를 가진다.이렇게 해서 세제는 모든 단백질에 균일한 전하 대 질량 비율을 제공한다.단백질에 결합함으로써 세제는 단백질의 2차, 3차 및/또는 4차 구조를 변성시켜 음전하를 띤 선형 폴리펩타이드 체인으로 변화시킨다.PAGE의 전계를 받으면 음전하를 띤 폴리펩타이드 체인은 이동성이 다른 양극을 향해 이동한다.그들의 이동성, 즉 분자가 이동한 거리는 분자량의 [4]대수에 반비례합니다.각 단백질이 이동한 거리의 상대적인 비율을 겔(Rf) 길이에 대해 비교함으로써 단백질의 상대적인 분자량에 대해 결론을 내릴 수 있으며, 여기서 겔의 길이는 추적 [5]염료와 같은 작은 분자가 이동한 거리에 의해 결정된다.
핵산의 경우 요소가 가장 일반적으로 사용되는 변성제입니다.단백질 들어, 나트륨 dodecyl 황산(SDS)은 음이온 세제에 위해denatured 단백질의 모든 두개의 아미노산이 2, 음극(모든 SDS분자로부터)을 가르칠 때 단백질 샘플에 피막 단백질과 신청했다.[3]:161–3 2-Mercaptoethanol은 이황화 결합은 단백질 단지, furthe을 돕는 사이에 발견을 방해하는 것을 사용할 수 있다.단백질을 변성시킨다.대부분의 단백질에서 SDS와 폴리펩타이드 사슬의 결합은 단위질량당 전하 분포를 균일하게 함으로써 전기영동 중에 대략적인 크기에 의한 분화를 일으킨다.는 예를 들면 더 큰 소수성 콘텐츠 –이 단백질은 많은 세포막 단백질과, 계면 활성제에 대한 환경에서 – 상호 작용하는 본질적으로 정확히 이 메서드를 사용하여가 묶이고, SDS.[6]Procedurally의 비율이 가변성 때문에, 둘 다 인디언과 SDS-PAGE은 함께 사용할 수 있는 치료하기가 어렵습니다.to 단백질의 다양한 서브유닛을 정제하고 분리한다.Native-PAGE는 올리고머 형태를 그대로 유지하고 겔에 활성 수준을 나타내는 밴드를 표시합니다.SDS-PAGE는 올리고머 형태를 변성 및 단량체로 분리하여 분자량을 나타내는 띠를 보여줍니다.이 밴드를 사용하여 [3]: 161–3 단백질의 순도를 확인하고 평가할 수 있습니다.
절차.
샘플 준비
샘플은 단백질 또는 핵산을 포함하는 모든 물질일 수 있습니다.이것들은 생물학적으로, 예를 들어 원핵 또는 진핵 세포, 조직, 바이러스, 환경 샘플 또는 정제된 단백질로부터 파생될 수 있다.고체 조직 또는 세포의 경우, 이들은 종종 혼합기(대량 샘플의 경우), 균질화기(소량) 또는 소닉에 의해 또는 고압 사이클링에 의해 먼저 기계적으로 분해되며, 다양한 유형의 여과와 원심 분리를 포함한 생화학 및 기계적 기술의 조합은 다음과 같을 수 있다.전기영동 전에 세포 구획과 세포 조직을 분리하는 데 사용됩니다.올리고뉴클레오티드 등의 합성 생체분자도 분석물질로 사용할 수 있다.
분석할 샘플은 원하는 경우 화학적 변성제(일반적으로 단백질의 경우 SDS, 핵산의 경우 요소)와 선택적으로 혼합된다.SDS는 음이온성 세제로서 2차 및 비이황화물 연결 3차 구조를 변성하고, 각 단백질에 질량에 비례하여 음전하를 가한다.요소는 핵산의 염기쌍 사이의 수소 결합을 파괴하여 구성 가닥을 분리시킵니다.샘플을 60°C 이상으로 가열하면 [7][8][9][10]변성이 더욱 촉진됩니다.
단백질은 SDS에 더해 디티오트레이톨(DTT) 또는 2-메르캅토에탄올(베타메르캅토에탄올/BME) 등의 환원제 존재 하에서 일시적으로 끓어오르기 직전까지 가열할 수 있으며, 이는 디술피드 결합을 감소시킴으로써 단백질을 더욱 변성시켜 단백질 4차 접힘을 극복한다.구조(중합체 서브유닛)에 있습니다.이를 SDS-PAGE 축소라고 합니다.
용액에 트래킹 염료를 첨가해도 좋다.이는 일반적으로 분석물보다 전기영동 이동성이 높기 때문에 실험자가 전기영동 실행 중에 겔을 통해 용액의 진행 상황을 추적할 수 있습니다.
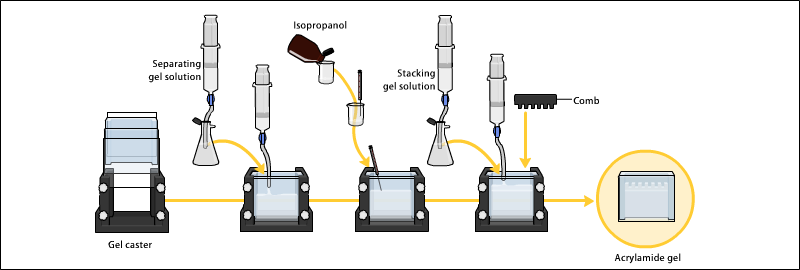
아크릴아미드겔 준비
겔은 일반적으로 아크릴아미드, 비사크릴아미드, 선택적 변성제(SDS 또는 요소) 및 pH가 조정된 완충제로 구성됩니다.용액은 중합 중에 기포가 형성되는 것을 방지하기 위해 진공 상태에서 탈기될 수 있다.또는 부탄올이 기포를 제거하여 표면을 매끄럽게 하기 때문에 부탄올을 주입한 후 분해겔(단백질용)에 첨가해도 된다.[11] 유리기의 공급원과 과황산암모늄, TEMED 등의 안정제를 첨가하여 [12]중합시킨다.중합 반응은 첨가된 비사크릴아미드 때문에 겔을 생성하며, 두 아크릴아미드 분자 사이에 가교를 형성할 수 있습니다.비사크릴아미드와 아크릴아미드의 비율은 특별한 목적에 따라 달라질 수 있지만, 일반적으로 35분의 1 수준이다.젤의 아크릴아미드 농도는 일반적으로 5%에서 25%까지 다양할 수 있습니다.낮은 비율의 젤은 매우 높은 분자량 분자를 분해하는 데 더 좋은 반면, 더 작은 단백질을 분해하기 위해 훨씬 더 높은 비율의 아크릴아미드가 필요합니다.폴리아크릴아미드겔의 평균 모공직경은 아크릴아미드의 총농도(% T with T = 아크릴아미드 및 비사크릴아미드의 총농도)와 가교제 비사크릴아미드의 농도(%C with Bisacrylamide 농도)[13]에 의해 결정된다.모공 크기가 %T와 상호 작용하여 감소합니다.%C에 대해서는 비사크릴아미드가 모공크기에 미치는 영향은 정점이 5%인 포물선형이기 때문에 농도가 5%일 때 가장 작은 모공을 생성한다.
겔은 보통 겔 캐스터의 두 유리판 사이에서 중합되며 상단에 빗을 삽입하여 샘플 웰을 만듭니다.겔이 중합된 후 빗을 제거할 수 있으며 겔은 전기영동 준비가 완료됩니다.
전기영동
PAGE에서는 시료의 성질과 실험 목적에 따라 다양한 버퍼 시스템이 사용됩니다.양극과 음극에서 사용되는 버퍼는 같거나 [9][14]다를 수 있습니다.[15]
전기장이 겔 전체에 인가되어 음전하 단백질 또는 핵산이 겔을 가로질러 음전하(이것이 갈바닉 셀이 아닌 전해질인 음극)에서 양전극(양극)으로 이동한다.각각의 생체 분자는 크기에 따라 겔 매트릭스를 통해 다르게 움직인다: 작은 분자는 겔의 모공을 통해 더 쉽게 들어가는 반면 큰 분자는 더 어렵다.겔은 보통 몇 시간 동안 작동하지만, 이는 겔 전체에 인가되는 전압에 따라 달라집니다. 이동은 높은 전압에서 더 빠르게 이루어지지만, 이러한 결과는 낮은 전압에서보다 일반적으로 정확도가 떨어집니다.정해진 시간이 지나면, 생체 분자들은 크기에 따라 다른 거리를 이동하게 된다.작은 생체 분자는 겔을 따라 더 멀리 이동하는 반면, 큰 분자는 원점에 더 가깝게 남아 있습니다.따라서 생체 분자는 크기에 따라 대략 분리될 수 있으며, 이는 주로 변성 조건에서는 분자량에 따라 달라지지만, 또한 고유 조건에서는 고차 배합에 의존한다.겔 이동도는 1V/cm의 전압 구배를 가진 이동 속도로 정의되며 단위는 cm2/sec/[3]: 161–3 V입니다.분석을 위해 생체분자의 상대적 이동성, Rf, 추적 염료의 총 이동 거리에 대한 분자의 이동 거리의 비율은 분자의 분자량(또는 MW의 로그, 더 나아가서는 M의r 분자 반지름)에 대해 표시된다.이러한 전형적인 선형 그림은 다양한 생체 분자 [3]: 161–3 크기의 정량적 추정에 널리 사용되는 표준 마커 또는 검정 곡선을 나타냅니다.
그러나 특정 당단백질은 SDS 겔에서 비정상적으로 작용합니다.또한 250,000~60,000Da 범위의 큰 단백질의 분석도 이러한 폴리펩타이드가 일반적으로 사용되는 [16]겔 시스템에서 부적절하게 이동하기 때문에 문제가 있는 것으로 보고되었다.
추가 처리
전기영동 후 겔은 (가장 일반적으로 쿠마시에 밝은 파란색 R-250 또는 오토라디오그래피로, 핵산, 브롬화 에티듐 또는 은색 염색으로) 염색되어 분리된 단백질의 가시화를 가능하게 할 수도 있고, 더 나아가서 처리될 수도 있다(예: 웨스턴 블롯).염색 후, 다른 종의 생체 분자가 겔 안에서 다른 띠로 나타납니다.알려진 분자량의 분자량 크기 마커를 겔의 별도 레인으로 실행하여 겔을 보정하고 마커와 상대적인 이동 거리를 비교하여 알려지지 않은 생체 분자의 대략적인 분자량을 결정하는 것이 일반적입니다.
단백질의 경우 SDS-PAGE는 일반적으로 신뢰성과 용이성 때문에 순도 측정으로 가장 먼저 선택됩니다.SDS의 존재와 변성 단계는 대략 크기에 따라 단백질을 분리하지만 일부 단백질의 비정상적인 이동이 발생할 수 있습니다.다른 단백질은 또한 다르게 염색될 수 있으며, 이것은 염색에 의한 정량화를 방해한다.PAGE는 단백질 정화를 위한 준비 기술로도 사용될 수 있다.예를 들어 정량적 제제 네이티브 연속 폴리아크릴아미드겔 전기영동(QPNC-PAGE)은 복잡한 생물학적 매트릭스에서 네이티브 메탈로프로틴을 분리하는 방법이다.
화학성분과 그 역할
폴리아크릴아미드겔(PAG)은 1964년부터 조직을 분할하기 위한 잠재적 매립 매체로 알려져 있었으며,[17][18] 1959년 두 개의 독립적인 그룹이 전기영동에 PAG를 사용했다.전기영동학적으로 바람직한 특징을 몇 가지 가지고 있어 다용도 매체입니다.합성, 열안정성, 투명성, 강성, 화학적으로 비교적 불활성 겔로 다양한 평균 모공 [19]크기로 제조할 수 있습니다.겔의 모공크기와 겔 모공크기의 재현성은 존재하는 아크릴아미드의 총량(%T)(T = 아크릴아미드와 비스 아크릴아미드 모노머의 총농도), 가교체(%C)(C = 비스 아크릴아미드 농도), 아크릴아미드의 중합시간(cflamide) 등 3가지 요인에 의해 결정된다.QPNC-PAGE)를 참조해 주세요.모공 크기는 %T 증가에 따라 감소합니다. 가교 시 5%C가 가장 작은 모공 크기를 제공합니다.%C에 대한 모공 크기는 정점이 5%C인 포물선 함수이므로 %C가 5%에서 증가하거나 감소하면 모공 크기가 증가한다.이는 겔 내에서 고분자 가닥의 비균질 번들링으로 인한 것으로 보인다.이 젤 재료는 또한 고전압 구배를 견딜 수 있고, 다양한 염색 및 소실 절차를 수행할 수 있으며, 소화되어 분리된 부분을 추출하거나 자동 방사선 촬영 및 영구 기록을 위해 건조될 수 있습니다.
구성 요소들
폴리아크릴아미드겔은 적층겔과 분리겔로 구성된다.겔을 쌓는 것은 분리 겔에 비해 다공성이 높고 단백질이 집중된 영역에서 이동할 수 있도록 한다.또한 중성 글리신 분자가 단백질 이동 속도를 빠르게 하기 때문에 겔 쌓기의 pH는 보통 6.8입니다.분리겔은 음이온성 글리신이 단백질의 이동 속도를 느리게 하는 pH 8.8을 가집니다.겔 분리는 단백질 분리를 가능하게 하며 상대적으로 다공성이 낮다.여기서 단백질은 크기(SDS-PAGE)와 크기/전하(Native PAGE)[20]에 따라 분리된다.
화학 버퍼는 겔 자체 및 전기영동 버퍼 내의 pH 값을 원하는 값으로 안정화시킨다.완충제의 선택은 완충제 반대편의 전기영동 이동성과 그에 따른 겔 분해능에도 영향을 미칩니다.완충제는 또한 반응하지 않아야 하며 대부분의 단백질과 수정하거나 반응해서는 안 됩니다.용도에 따라 각각 다른 버퍼를 캐소드 버퍼 및 애노드 버퍼로 사용할 수 있다.예를 들어 DISC 전기영동에서는 단일 겔 내에서 여러 pH 값을 사용할 수 있습니다.PAGE의 일반적인 버퍼에는 Tris, Bis-Tris 또는 이미다졸이 있습니다.
대항 이온은 버퍼 이온의 고유 전하 균형을 맞추고 전기영동 중에 전계 강도에 영향을 미칩니다.SDS-PAGE 캐소드 버퍼에서는 고충전 및 이동 이온이 종종 회피되지만 겔 자체에 포함되어 단백질보다 먼저 이동할 수 있습니다.DISC SDS-PAGE와 같은 애플리케이션에서 겔 내의 pH 값은 분해능을 향상시키기 위해 실행 중 대항체의 평균 전하를 변경하기 위해 달라질 수 있습니다.인기 있는 대항제는 글리신과 트리신이다.글리신은 pKa가 9.69이고 글리신산염의 이동성이 pH 범위에서 가장 느리게 알려진 단백질의 값보다 낮은 값으로 설정될 수 있기 때문에 후행 이온 또는 느린 이온의 공급원으로 사용되어 왔다.이 범위의 최소 pH는 약 8.0입니다.
아크릴아미드(CHNO35; mW: 71.08)는 물에 녹으면 아크릴아미드의 느린 자발적 자동 중합이 일어나 머리끝부터 꼬리끝까지 분자를 결합하여 긴 단일 사슬 폴리머를 형성한다.활성 래디칼 생성 시스템이 존재하면 중합이 크게 가속화됩니다.이러한 반응을 비닐 첨가 중합이라고 합니다.이러한 고분자 사슬의 용액은 점성이 되지만 겔을 형성하지 않습니다. 왜냐하면 체인은 단순히 서로 미끄러지기 때문입니다.젤 형성을 위해서는 다양한 체인을 연결해야 합니다.아크릴아미드는 발암성,[21] 신경독소 [22]및 생식독소이다.아크릴아미드는 자동 중합 및 가수 분해를 줄이기 위해 어둡고 건조한 서늘한 곳에 보관해야 합니다.
비사크릴아미드(N,N--메틸렌비스크릴아미드)(CHNO71022,mW:154.17)는 폴리아크릴아미드겔에 가장 많이 사용되는 가교제이다.화학적으로 그것은 두 개의 아크릴아미드 분자가 그들의 비반응 말단에서 머리를 맞대고 결합된 것으로 생각될 수 있다.비사크릴아미드는 2개의 폴리아크릴아미드 사슬을 서로 가교하여 겔로 할 수 있다.
도데실황산나트륨(SDS)(CHNaOS12254;mW:288.38)은 토종 단백질을 개별 폴리펩타이드로 변성시키는 데 사용되는 강력한 세제제이다.재구성 변성이라고 하는 이러한 변성은 단백질의 완전한 선형화에 의해 달성되는 것이 아니라 무작위 코일 및 α 나선 [6]2차 구조의 조합에 대한 구조 변화를 통해 달성된다.단백질 혼합물을 SDS가 있는 상태에서 100 °C까지 가열하면 세제는 폴리펩타이드 골격을 감싼다.폴리펩타이드 1.4g SDS/g의 일정 중량비로 폴리펩타이드와 결합한다.이 과정에서 폴리펩타이드의 고유전하는 SDS가 기여하는 음전하에 비해 무시할 수 있게 된다.따라서 처리 후 폴리펩타이드는 단위 중량당 동일한 순 음전하인 균일한 전하 밀도를 갖는 막대 모양의 구조가 된다.이러한 단백질의 전기영동 이동성은 분자량의 로그의 선형 함수이다.SDS가 없다면, 각각의 단백질은 1차 구조에 특정한 등전점과 분자량을 가지기 때문에 유사한 분자량을 가진 단백질들은 질량 전하비의 차이로 인해 다르게 이동할 것이다.이것은 네이티브 PAGE라고 불립니다.SDS를 추가하면 단백질이 결합 및 전개되어 폴리펩타이드 길이에 따라 거의 균일한 음전하를 제공하기 때문에 이 문제가 해결됩니다.
요소(CO(NH2);2 mW: 60.06)는 수소 결합 및 판데르발스 힘 등의 비공유력에 의해 매개되는 분자 내 상호작용에 간섭하여 시스템의 엔트로피를 증가시키는 카오트로픽제이다.고분자 구조는 이러한 힘의 순 효과에 의존하므로, 카오트로픽 용질의 증가는 고분자를 변성시킨다.
과황산암모늄(APS)(NHSO2828; mW: 228.2)은 유리기의 원천이며 종종 겔 형성의 개시제로 사용된다.유리기의 대체 공급원은 광화학 반응에서 유리기를 생성하는 리보플라빈이다.
TEMED(N, N, N,, N--테트라메틸에틸렌디아민)(CHN6162, mW: 116.21)는 유리기를 안정시켜 중합성을 향상시킨다.중합 속도와 결과 겔의 특성은 활성산소의 농도에 따라 달라집니다.유리기의 양이 증가하면 평균 폴리머 체인 길이가 감소하고 겔 혼탁도가 증가하며 겔 탄성이 감소합니다.양을 줄이면 역효과가 나타난다.적당한 시간 내에 중합이 가능한 가장 낮은 촉매 농도를 사용해야 합니다.APS와 TEMED는 일반적으로 1~10mM 범위의 약 등극성 농도로 사용된다.
처리 및 시각화를 위한 화학물질
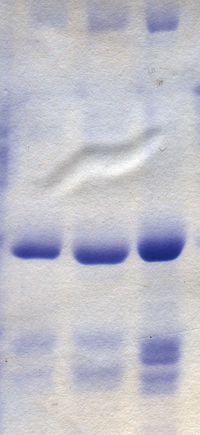
겔과 그 안에 시각화 된 단백질 검체의 가공에는 다음과 같은 화학물질과 절차가 사용됩니다.
추적 색소; 단백질과 핵산은 대부분 무색이기 때문에 전기영동 중에 겔을 통해 진행되는 과정을 쉽게 따라갈 수 없습니다.따라서 알려진 전기영동성의 음이온성 염료는 일반적으로 PAGE 샘플 버퍼에 포함된다.매우 일반적인 추적 염료는 브로모페놀 블루(BPB, 3', 3", 5', 5", 테트라브로모페놀술폰프탈레인)입니다.이 염료는 알칼리 및 중성 pH로 착색되며 양극 쪽으로 이동하는 작은 음전하 분자입니다.이동성이 매우 높은 분자이기 때문에 대부분의 단백질보다 앞서 움직인다.전기영동의 양극단에 이르면 매체 전기영동이 정지된다.그것은 일부 단백질에 약하게 결합하고 파란색을 부여할 수 있다.다른 일반적인 추적 염료로는 이동성이 낮은 자일렌시아놀과 이동성이 높은 오렌지 G가 있습니다.
로딩 보조 장치. 대부분의 PAGE 시스템은 위에서 젤 내의 웰로 로드됩니다.샘플이 겔 바닥에 가라앉도록 하기 위해 샘플 버퍼에 샘플의 밀도를 높이는 첨가제를 보충합니다.이러한 첨가물은 전기영동에 간섭하지 않도록 단백질에 대해 비이온성 및 비반응성이어야 합니다.일반적인 첨가물은 글리세롤과 수크로스이다.
쿠마시에 브릴리언트 블루 R-250(CBB)(CHNNaOS4544372; mW: 825.97)이 가장 인기 있는 단백질 염색체이다.이것은 음이온성 색소로, 단백질에 특이적으로 결합합니다.CBB의 구조는 주로 무극성으로 아세트산으로 산성화된 메타놀 용액에 사용된다.겔 중의 단백질은 아세트산으로 고정되며 동시에 착색된다.겔에 포함된 여분의 염료는 염료 없이 동일한 용액으로 제거하여 제거할 수 있습니다.단백질은 깨끗한 배경에서 파란색 띠로 검출됩니다.SDS도 음이온성이기 때문에 염색 과정을 방해할 수 있습니다.따라서 겔의 최소 10배 이상 많은 양의 염색 용액을 사용하는 것이 좋습니다.
브롬화 에티듐(EtBr)은 일반적인 핵산염색제입니다.EtBr은 자외선을 [23]받아 주황색 형광을 발해 겔에 DNA나 RNA를 쉽게 시각화할 수 있다.브롬화 에티듐은 인터칼레이션 [3]과정을 통해 핵산 사슬을 결합시킨다.브롬화 에티듐은 일반적인 착색제이지만 EtBr은 이미 알려진 발암물질이기 때문에 사용 시 주의해야 합니다.이 때문에 많은 연구자들이 [24]EtBr의 안전한 대안인 SYBR Green이나 SYBR Safe와 같은 얼룩을 사용하는 것을 선택하고 있다.EtBr은 단순히 겔 혼합물에 첨가하는 방식으로 사용됩니다.겔이 실행되면 사진 문서 [3]시스템을 사용하여 겔을 볼 수 있습니다.
은색 염색은 기존의 쿠마시 브릴리언트 블루 염색은 보통 50ng의 단백질 밴드를 검출할 수 있기 때문에 검출을 위한 보다 민감한 방법이 필요할 때 사용합니다.은색 염색은 일반적으로 민감도를 10~100배 더 높입니다.이것은 사진 현상 화학에 기초하고 있다.단백질은 묽은 메탄올 용액으로 겔에 고정시킨 다음 산성 질산은 용액으로 배양한다.은이온은 알칼리 pH에서 포름알데히드에 의해 금속 형태로 환원된다.아세트산과 같은 산성 용액은 [25]발달을 멈춘다.은염색은 [26]겔에서 미량의 단백질을 검출하는 민감한 절차로 케렌이와 갈리아스에 의해 도입되었다.이 기술은 다양한 [27]지지대에서 분리된 다른 생물학적 고분자에 대한 연구로 확장되었다.다양한 변수가 색채 강도에 영향을 미칠 수 있으며 모든 단백질에는 고유한 염색 특성이 있습니다. 깨끗한 유리 제품, 순수한 시약 및 최고 순도의 물은 [28]염색에 성공하기 위한 핵심 포인트입니다.은색 염색은 유리 표면에 색을 입히기 위해 14세기에 개발되었다.그것은 16세기부터 이러한 목적으로 널리 사용되어 왔다.초기 은색 얼룩으로 인해 생긴 색상은 연한 노란색과 오렌지색-빨간색 사이였다.카밀로 골지는 신경계 연구를 위해 은색 염색을 완벽하게 했다.Golgi의 방법은 제한된 수의 세포를 무작위로 [29]염색합니다.
겔 전기영동 후 단백질 밴드 검출에도 사용되는 오토라디오그래피는 방사성 동위원소를 이용해 단백질을 표시하고 X선 필름으로 [30]검출한다.
웨스턴 블롯은 아크릴아미드 겔에서 분리된 단백질이 니트로셀룰로오스, 나일론 또는 PVDF 막과 같이 안정적이고 조작 가능한 막으로 전기영동적으로 전달되는 과정입니다.다음으로 관심 단백질의 상대적 증감뿐만 아니라 전달된 단백질을 시각화하기 위해 면역화학적 기술을 적용할 수 있다.
「 」를 참조해 주세요.
- 아가로스겔 전기영동법
- 모세관 전기영동
- DNA전기영동
- 이스턴 블롯팅
- 일렉트로블롯팅
- 고속 병렬 단백질 분해(FASTpp)[31]
- 전기영동의 역사
- 등전초점
- 등각영동
- 네이티브 겔 전기영동
- 노던 블롯
- 단백질 전기영동
- 서던 블롯
- 2차원 SDS 페이지
- 자이모그래피
레퍼런스
- ^ Petrov A, Tsa A, Puglisi JD (2013). "Chapter Sixteen – Analysis of RNA by Analytical Polyacrylamide Gel Electrophoresis". In Lorsch J (ed.). Methods in Enzymology. Vol. 530. Academic Press. pp. 301–313. doi:10.1016/B978-0-12-420037-1.00016-6. ISBN 978-0-12-420037-1. PMID 24034328.
- ^ a b The Editors of Encyclopaedia Britannica (2017). "Polyacrylamide". Britannica Online Academic Edition. Encyclopedia Britannica, Inc.
{{cite book}}:last=범용명(도움말)이 있습니다. - ^ a b c d e f g Ninfa AJ, Ballou DP, Benore M (2010). Fundamental Laboratory Approaches for Biochemistry and Biotechnology (2nd ed.). Hoboken, NJ: John Wiley & Sons, Inc. ISBN 978-0-470-08766-4. OCLC 420027217.
- ^ Kindt T, Goldsby R, Osborne B (2007). Kuby Immunology. New York: W.H. Freeman and Company. p. 553. ISBN 978-1-4292-0211-4.
- ^ Kumar A, Awasthi A (2009). Bioseparation Engineering. New Delhi: I.K. International Publishing House. p. 137. ISBN 9789380026084.
- ^ a b Rath A, Glibowicka M, Nadeau VG, et al. (2009). "Detergent binding explains anomalous SDS-PAGE migration of membrane proteins". Proc. Natl. Acad. Sci. U.S.A. 106 (6): 1760–5. Bibcode:2009PNAS..106.1760R. doi:10.1073/pnas.0813167106. PMC 2644111. PMID 19181854.
- ^ Shapiro AL, Viñuela E, Maizel JV Jr (1967). "Molecular weight estimation of polypeptide chains by electrophoresis in SDS-polyacrylamide gels". Biochem. Biophys. Res. Commun. 28 (5): 815–20. doi:10.1016/0006-291X(67)90391-9. PMID 4861258.
- ^ Weber K, Osborn M (1969). "The reliability of molecular weight determinations by dodecyl sulfate-polyacrylamide gel electrophoresis". J Biol Chem. 244 (16): 4406–12. doi:10.1016/S0021-9258(18)94333-4. PMID 5806584.
- ^ a b Laemmli UK (1970). "Cleavage of structural proteins during the assembly of the head of bacteriophage T4". Nature. 227 (5259): 680–5. Bibcode:1970Natur.227..680L. doi:10.1038/227680a0. PMID 5432063. S2CID 3105149.
- ^ Caprette DR. "SDS-PAGE". Experimental Biosciences. Retrieved 27 September 2009.
- ^ "What is the meaning of de -gas the acrylamide gel mix?". Protocol Online. 2006. Retrieved 28 September 2009.
- ^ "SDS-PAGE". Archived from the original on 20 February 2014. Retrieved 12 September 2009.
- ^ Rüchel R, Steere RL, Erbe EF (1978). "Transmission-electron microscopic observations of freeze-etched polyacrylamide gels". J. Chromatogr. A. 166 (2): 563–575. doi:10.1016/S0021-9673(00)95641-3.
- ^ Schägger H, von Jagow G (1987). "Tricine-sodium dodecyl sulfate-polyacrylamide gel electrophoresis for the separation of proteins in the range from 1 to 100 kDa". Anal. Biochem. 166 (2): 368–379. doi:10.1016/0003-2697(87)90587-2. PMID 2449095.
- ^ Ancrews D (2007). "SDS-PAGE". Andrews Lab. Archived from the original on 2 July 2017. Retrieved 27 September 2009.
- ^ Quandt N, Stindl A, Keller U (1993). "Sodium Dodecyl Sulfate-Polyacrylamide Gel Electrophoresis for Mr Estimations of High-Molecular-Weight Polypeptides". Anal. Biochem. 214 (2): 490–494. doi:10.1006/abio.1993.1527. PMID 8109738.
- ^ Davis BJ, Ornstein L (1959). "A new high resolution electrophoresis method". Delivered at the Society for the Study of Blood at the New York Academy of Medicine.
- ^ Raymond S, Weintraub L (1959). "Acrylamide gel as a supporting medium for zone electrophoresis". Science. 130 (3377): 711. Bibcode:1959Sci...130..711R. doi:10.1126/science.130.3377.711. PMID 14436634. S2CID 7242716.
- ^ Rüchel R, Steere RL, Erbe EF (1978). "Transmission-electron microscopic observations of freeze-etched polyacrylamide gels". J. Chromatogr. A. 166 (2): 563–75. doi:10.1016/S0021-9673(00)95641-3.
- ^ Duchesne LG, Lam JS, MacDonald LA, et al. (1988). "Effect of pH and acrylamide concentration on the separation of lipopolysaccharides in polyacrylamide gels". Current Microbiology. 16 (4): 191–4. doi:10.1007/BF01568528. S2CID 932635.
- ^ Tareke E, Rydberg P, Eriksson S, et al. (2000). "Acrylamide: a cooking carcinogen?". Chem. Res. Toxicol. 13 (6): 517–22. doi:10.1021/tx9901938. PMID 10858325.
- ^ LoPachin R (2004). "The changing view of acrylamide neurotoxicity". Neurotoxicology. 25 (4): 617–30. doi:10.1016/j.neuro.2004.01.004. PMID 15183015.
- ^ Sabnis RW (2010). Handbook of biological dyes and stains: synthesis and industrial applications. Hoboken, NJ: Wiley-Blackwell. ISBN 978-0-470-40753-0. OCLC 647922579.
- ^ Singer VL, Lawlor TE, Yue S (1999). "Comparison of SYBR Green I nucleic acid gel stain mutagenicity and ethidium bromide mutagenicity in the Salmonella/mammalian microsome reverse mutation assay (Ames test)". Mutat. Res. 439 (1): 37–47. doi:10.1016/s1383-5718(98)00172-7. PMID 10029672.
- ^ Ninfa AJ, Ballou DP (2004). Fundamental laboratory approaches for biochemistry and biotechnology. Hoboken, NJ: Wiley & Sons. ISBN 978-1-891786-00-6. OCLC 633862582.
- ^ Kerenyi L, Gallyas F (1973). "Über Probleme der quantitiven Auswertung der mit physikalischer Entwicklung versilberten Agarelektrophoretogramme". Clin. Chim. Acta. 47 (3): 425–436. doi:10.1016/0009-8981(73)90276-3. PMID 4744834.
- ^ Switzer RC 3rd, Merril CR, Shifrin S (1979). "A highly sensitive silver stain for detecting proteins and peptides in polyacrylamide gels". Anal. Biochem. 98 (1): 231–7. doi:10.1016/0003-2697(79)90732-2. PMID 94518.
- ^ Hempelmann E, Schulze M, Götze O (1984). "Free SH-groups are important for the polychromatic staining of proteins with silver nitrat". In Neuhof V (ed.). Electrophoresis '84. Weinheim: Verlag Chemie. pp. 328–30.
- ^ Grant G (2007). "How the 1906 Nobel Prize in Physiology or Medicine was shared between Golgi and Cajal". Brain Res Rev. 55 (2): 490–8. doi:10.1016/j.brainresrev.2006.11.004. PMID 17306375. S2CID 24331507.
- ^ Song D, Ma S, Khor SP (2002). "Gel electrophoresis-autoradiographic image analysis of radiolabeled protein drug concentration in serum for pharmacokinetic studies". Journal of Pharmacological and Toxicological Methods. 47 (1): 59–66. doi:10.1016/s1056-8719(02)00203-4. PMID 12387940.
- ^ Minde DP (2012). "Determining biophysical protein stability in lysates by a fast proteolysis assay, FASTpp". PLOS One. 7 (10): e46147. Bibcode:2012PLoSO...746147M. doi:10.1371/journal.pone.0046147. PMC 3463568. PMID 23056252.
외부 링크
| 라이브러리 리소스 정보 폴리아크릴아미드겔전기영동 |
- SDS-PAGE: 구조
- SDS-PAGE 비디오 디스테이트화
- SDS-PAGE의 디스테이트화
- TRIS Urea 겔에 대한 맞춤형 레시피를 위한 SDS-PAGE Calculator.
- 2차원 단백질겔렉트로영동
- [1] 헴펠만 E.SDS-단백질 PAGE 및 플라스모듐 팔시파룸 단백질의 은염색 및 면역블로팅에 의한 단백질 검출.in: Moll K, Ljungström J, Perlmann H, Sherf A, Wahlgren M (eds) Methods in Malaria Research, 2008년 제5판, 263-266