수산화니켈
Nickel oxide hydroxide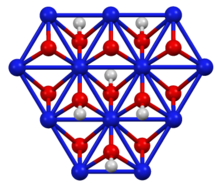 | |
 | |
| 이름 | |
|---|---|
| 기타 이름 옥시수산화니켈 | |
| 식별자 | |
3D 모델(JSmol) | |
PubChem CID | |
| |
| |
| 특성. | |
| Ni(O)(OH) | |
| 몰 질량 | 91.699 g/g |
| 외모 | 흑색 고체 |
| 녹는점 | 230 °C (446 °F, 503 K) |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
수산화니켈은 화학식이 NiO(OH)인 무기화합물이다.모든 용제에 용해되지 않지만 염기 및 산의 공격을 받는 검은색 고체입니다.이것은 니켈-금속 수소화물 배터리와 니켈-철 배터리의 구성 요소입니다.
관련 자료
산화니켈(III)은 종종 특성이 좋지 않고 비스토이코메트리 화합물로 간주됩니다.니켈(III)산화물(NiO)은23 결정학적으로 검증되지 않았다.유기화학에서의 응용에서는 니켈산화물 또는 과산화물이 제 자리에서 생성되며 결정학적 특성이 결여되어 있다.예를 들어 '과산화니켈'(CAS#12035-36-8)도 NiO(OH)[1]와 밀접하게 관련되어 있거나 동일하다.
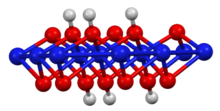
합성 및 구조
그것의 층상 구조는 니켈의 브루사이트 다형과 유사하다.II) 수산화물이지만 수소가 절반이다.니켈의 산화 상태는 3+[2]이다.니켈의 반응으로 제조할 수 있다.II) 수산화칼륨 및 브롬을 산화제로 [3]하는 수산화물:
- 2 Ni(OH)2 + 2 KOH + Br2 → 2 KBr + 22 HO + 2 NiOOH
유기화학에 사용
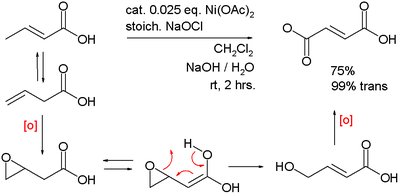
니켈(III) 산화물은 [4]표백제를 사용하여 벤질 알코올을 벤조산으로 산화시키는 촉매 역할을 합니다.
마찬가지로 3-부텐산의 푸마르산으로의 이중 산화를 촉매한다.
레퍼런스
- ^ 게리 W. 모로 "니켈"II) 과산화물"유기합성용 시약 백과사전, 2001년 John Wiley & Sons. doi: 10.1002/047084289X.rn017
- ^ Casas-Cabanas, M.; Canales-Vazquez, J.; Rodriguez Carvajal, M.R. Palacin, M.R. "니켈 배터리 재료의 특징: 베타-(NiOOH)" 재료 연구 협회 심포지엄(2009년) 1126, 페이지 131-136.p.
- ^ O. Glemser "β-니켈(II) 수산화물" (제2판).G.Braower에 의해 편집, 학술 출판, 1963년, NY. Vol. 1. p. 1549.
- ^ 알코올, 알데히드 및 불포화 카르본산 조셉 M. 그릴, 제임스 W. 오글 및 스테판 A의 촉매 산화를 위한 효율적이고 실용적인 시스템.밀러 J. 조직 화학; 2006; 71(25) 페이지 9291 - 9296; (조) doi:10.1021/jo0612574