브롬화마그네슘
Magnesium bromide | |
 | |
| 식별자 | |
|---|---|
| |
3D 모델(JSMO) | |
| 켐스파이더 | |
| ECHA 인포카드 | 100.029.246 |
펍켐 CID | |
| 유니아이 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| |
| 어금니 질량 | 184.113 g/mol (연속) 292.204 g/mol (헥사하이드레이트) |
| 외모 | 흰색 흡습성 육각 결정 (연속) 무색 단사정계 결정(헥사하이드레이트) |
| 밀도 | 3.72g/cm3(연속) 2.07 g/cm3 (헥사하이드레이트) |
| 융점 | 711°C(1,312°F; 984K) 172.4°C, 분해(헥사하이드레이트) |
| 비등점 | 1,250°C (2,280°F; 1,520K) |
| 102g/(100mL)(무수) 316g/(100mL)(0°C, 헥사하이드레이트) | |
| 용해도 | 에탄올 : 6.9g/(100mL) 메탄올 : 21.8g/(100mL) |
| -72.0·10cm−63/mol | |
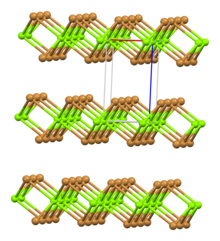
| 구조. | |
| 능면체, hP3 | |
| P-3m1, 164호 | |
| 팔면체의 | |
| 열화학 | |
열용량 (C) | 70J/(mol·K) |
어금니 엔트로피 (S⦵298) | 117.2 J·mol−1·K−1 |
스덴탈피 형성 (δh) | −524.3 kJ·mol−1 |
| 유해성 | |
| NFPA 704 (파이어다이아몬드) | |
| 안전자료(SDS) | 외부 SDS |
| 관련화합물 | |
기타 음이온 | |
기타 양이온 | |
별도의 언급이 없는 경우를 제외하고, 표준 상태(25 °C [77 °F], 100 kPa에서)의 재료에 대한 데이터가 제공됩니다. | |
마그네슘 브로마이드는 마그네슘과2 브롬의 화합물로 화학식은 MgBr입니다.그것은 하얗고 섬세한 결정성 고체입니다.그것은 종종 가벼운 진정제와 신경 [2]장애 치료를 위한 항경련제로 사용됩니다.이것은 물에 잘 녹고 알코올에 어느 정도 녹습니다.그것은 비쇼파이트와 카르날라이트와 같은 일부 광물과 [3][4]사해와 같은 바닷물에서 적은 양으로 자연적으로 발견될 수 있습니다.
합성
마그네슘 브로마이드는 산화마그네슘(및 관련된 염기성 염)을 브로마이드와 [4]함께 처리함으로써 합성될 수 있습니다.탄산마그네슘과 브로민화수소산을 반응시켜 증발 [3]후 남은 고체를 모아 만들 수도 있습니다.
무수 MgBr은2 다양한 수화물로의 용이한 전환에 의해 제시되는 바와 같이 루이스 산입니다.MgBr(dioxane)2 공식을2 갖는 배위 중합체에서, Mg는2+ 팔면체 [5]기하학을 채택합니다.
사용하다
마그네슘 브로마이드는 일부 유기 합성,[6] 예를 들어 알돌 반응에서 루이스 산 촉매로 사용됩니다.유기 규소 화학에서, 마그네슘 브로마이드는 부가물 RSiXMgBr을22 [7]형성합니다.
마그네슘 브로마이드는 [3]안정제로도 사용되어 왔습니다.
마그네슘 브로마이드는 [8]숯에 있는 팔라듐의 촉매 특성을 조절합니다.
마그네슘 브로마이드 헥사하이드레이트는 난연제로서의 특성을 가지고 있습니다.면 소재에 마그네슘 브로마이드 헥사하이드레이트 0.125 mol/L를 첨가하면 난연제 [9]역할을 하는 것으로 나타났습니다.
참고문헌
- ^ Lide, David R. (1998). Handbook of Chemistry and Physics (87 ed.). Boca Raton, Florida: CRC Press. pp. 4–67. ISBN 0-8493-0594-2.
- ^ 프레이도트 파트나익.무기 화학물질 안내서.McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ a b c Groyter, W. Concise 백과사전 화학, Walter de Groyter & Company: Berlin, 1993; 612
- ^ a b 루이스, R.J. 홀리의 축합화학사전, 15일.; John Wiley & Sons Inc.:뉴욕, 2007; 777
- ^ Fischer, Reinald; Görls, Helmar; Meisinger, Philippe R.; Suxdorf, Regina; Westerhausen, Matthias (2019). "Structure–Solubility Relationship of 1,4‐Dioxane Complexes of Di(hydrocarbyl)magnesium". Chemistry – A European Journal. 25 (55): 12830–12841. doi:10.1002/chem.201903120. PMC 7027550. PMID 31328293.
- ^ Evans, David A.; Tedrow, Jason S.; Shaw, Jared T.; Downey, C. Wade (2002). "Diastereoselective Magnesium Halide-Catalyzed anti-Aldol Reactions of Chiral N-Acyloxazolidinones". Journal of the American Chemical Society. 124 (3): 392–393. doi:10.1021/ja0119548. PMID 11792206.
- ^ Lim, Young Mook; Cho, Hyeon Mo; Lee, Myong Euy; Baeck, Kyoung Koo (2006). "A Stable Magnesium Bromosilylenoid: Transmetalation of a Lithium Bromosilylenoid by Magnesium Bromide". Organometallics. 25 (21): 4960. doi:10.1021/om060589w.
- ^ Bouzide, Abderrahim (2002). "Magnesium Bromide Mediated Highly Diastereoselective Heterogeneous Hydrogenation of Olefins". Organic Letters. 4 (8): 1347–50. doi:10.1021/ol020032m. PMID 11950359.
- ^ Mostashari, S. M.; Fayyaz, F. (2008). "XRD characterization of the ashes from a burned cellulosic fabric impregnated with magnesium bromide hexahydrate as flame-retardant". Journal of Thermal Analysis and Calorimetry. 92 (3): 845. doi:10.1007/s10973-007-8928-4. S2CID 94416902.



