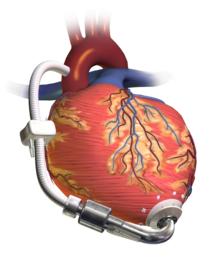
심실 보조 장치
Ventricular assist device| 심실 보조 장치 | |
|---|---|
 좌심실에서 대동맥으로 혈액을 펌핑하는 좌심실 보조 장치(LVAD)로, 외부에서 마모된 제어 장치 및 배터리 팩에 연결됩니다. | |
| Medline Plus | 007268 |
심실보조장치(VAD)는 심장순환을 보조하기 위한 전기기계장치이며, 고장난 심장의 기능을 부분적으로 또는 완전히 대체하기 위해 사용된다.VAD의 기능은 인공 심장 박동기의 기능과 다른데, VAD는 혈액을 펌프하는 반면, 심장 박동기는 심장 근육에 전기 자극을 전달합니다.일부 VAD는 일반적으로 심근경색(심근경색)에서 회복되는 환자 및 심장 수술에서 회복되는 환자를 위한 [1]단기용이며, 일부 VAD는 일반적으로 진행성 심부전 환자를 위한 장기(영구적으로 몇 개월에서 몇 년)용이다.
VAD는 우심실(RVAD) 또는 좌심실(LVAD)을 지원하거나 두 심실(BiVAD)을 모두 지원하도록 설계되었습니다.이식된 VAD의 유형은 기초 심장 질환의 유형과 우심실의 작업 부하를 결정하는 폐동맥 저항에 따라 달라집니다.좌심실 보조 장치(LVAD)는 결함이 있는 심장에 적용되는 가장 일반적인 장치입니다(대부분의 경우 충분합니다; 심장의 오른쪽은 종종 심하게 증가한 혈류를 사용할 수 있습니다). 그러나 폐동맥 저항이 높을 때, (추가) 우심실 보조 장치(RVAD)가 n일 수 있습니다.심장 순환 문제를 해결하는 데 도움이 됩니다.LVAD와 RVAD가 모두 필요한 경우 일반적으로 별도의 LVAD와 RVAD가 아닌 BiVAD가 사용됩니다.
일반적으로 장기 VAD는 이식(BTT)의 가교로 사용됩니다. 즉, 환자의 생명을 유지하고 상당히 양호한 상태를 유지하며 병원 밖에서 심장 이식을 기다릴 수 있습니다.다른 "다리"로는 후보와의 가교, 결정의 가교, 회복의 가교가 있다.경우에 따라 VAD가 목적 치료(DT)로도 사용됩니다.이 경우 환자는 심장 이식을 받지 않고 평생 [2][3]VAD에 의존하게 됩니다.
VAD는 심장 기능을 가정하도록 설계된 인공 심장과는 구별되며 일반적으로 환자의 심장을 제거해야 합니다.
설계.
펌프스
VAD에 사용되는 펌프는 두 가지 주요 범주로 나눌 수 있습니다. 즉, 심장의 자연적인 맥박 작용을 모방하는 맥동 [4]펌프와 연속 흐름 [5]펌프입니다.맥동성 VAD는 양의 치환 [6][7][8]펌프를 사용합니다.일부 맥동 펌프(압축 공기를 에너지원으로[9] 사용하는 펌프)에서 혈액이 차지하는 부피는 펌프 사이클 동안 변화합니다.펌프가 차체 내부에 있는 경우 외부 공기로의 환기 튜브가 필요합니다.
연속 흐름 VAD는 맥동 [10]VAD보다 작고 내구성이 우수하다는 것이 입증되었습니다.일반적으로 원심 펌프 또는 축류 펌프를 사용합니다.두 유형 모두 영구 자석이 포함된 중앙 로터가 있습니다.펌프 하우징에 포함된 코일에 흐르는 제어된 전류는 자석에 힘을 가하고, 자석은 로터를 회전시킵니다.원심펌프에서 로터는 혈액을 원주방향으로 가속시켜 펌프의 외연을 향해 이동하도록 형성되어 있는 반면, 축류펌프에서는 로터는 나선형 날개와 거의 원통형으로 되어 있어 혈액이 [11]회전자축방향으로 가속된다.
연속 흐름 펌프의 중요한 문제는 로터를 매달기 위해 사용되는 방법입니다.초기 버전은 솔리드 베어링을 사용했지만, EU에서 사용이 승인된 신형 펌프는 자기 부상("maglev")[12][13][14] 또는 유체 역학 서스펜션을 사용합니다.이러한 펌프에는 하나의 가동 부품(로터)[citation needed]만 포함되어 있습니다.
역사

최초의 좌심실 보조 장치(LVAD) 시스템은 1962년 휴스턴의 베일러 의과대학의 도밍고 리오타에 의해 만들어졌습니다.첫 번째 LVAD는 1963년에 Liotta와 E에 의해 이식되었습니다.스탠리 크로포드입니다LVAD의 첫 번째 성공적인 이식은 1966년 Liotta에 의해 Michael E 박사와 함께 완료되었습니다. 드베이키.환자는 37세 여성으로 수술 [16]후 10일 동안 부체(외부) 회로가 기계적 지원을 할 수 있었다.최초의 성공적인 장기 이식 인공 심폐소생술은 1988년 윌리엄 F 박사에 의해 수행되었다. 보스턴 아동병원 메디컬 센터의 베른하드와 미국 매사추세츠 주 워번의 서메딕스사는 전자 제어 보조 장치인 하트메이트(HeartMate)를 개발한 미국 국립보건연구소(NIH) 연구 계약을 체결했다.이것은 미국 국립 심장,[17] 폐, 혈액 연구소(National Heart, Lung, and Blood Institute)로부터 매사추세츠 주 보스턴에 있는 체온병원과 3년 계약으로 620만 달러를 지원받았다.초기 VAD는 좌심실에서 번갈아 혈액이 펌프로 빨려 들어가 대동맥으로 밀려나는 "펄스성" 동작을 사용하여 심장을 에뮬레이트했습니다.이러한 종류의 장치에는 1994년 10월 미국 식품의약국(FDA)에 의해 미국에서 사용이 승인된 HeartMate IP LVAS가 포함됩니다.이 장치들은 1990년대 후반 에릭 로즈, O. H. 프레이저, 메흐메트 오즈를 포함한 심장외과 의사들이 환자들이 병원 밖에서 살 수 있다는 개념을 대중화하면서 받아들여지기 시작했다.VAD를 사용한 외래환자에 대한 언론 보도는 이러한 [18]주장을 강조했다.
보다 최근의 연구는 원심 펌프 또는 축류 임펠러 구동 펌프로 크게 분류할 수 있는 연속 흐름 펌프에 집중되어 있습니다.이러한 펌프는 단순성이 향상되어 크기가 작아지고 신뢰성이 향상된다는 장점이 있습니다.이러한 디바이스를 제2세대 VAD라고 부릅니다.부작용은 사용자가 [19]펄스를 갖지 않거나 펄스 강도가 심각하게 [20]감소하는 것입니다.
3세대 VAD는 유체역학 또는 전자기 서스펜션을 사용하여 펌프의 임펠러를 매달기 때문에 베어링이 필요하지 않고 움직이는 부품의 수가 [citation needed]1개로 줄어듭니다.
임상시험 중인 또 다른 기술은 경피 케이블을 사용하는 대신 장치에 전원을 공급하고 제어하기 위해 경피 유도를 사용하는 것이다.명백한 외관상의 이점과는 별개로, 이는 감염의 위험과 그에 따른 예방 조치의 필요성을 감소시킨다.이 기술을 사용하는 맥동 펌프는 CE Mark 승인을 받았으며 미국 FDA [citation needed]승인을 위해 임상시험을 진행 중입니다.
개발 초기 단계에서 매우 다른 접근 방식은 대동맥 주위에 팽창식 측정띠를 사용하는 것이었습니다.측정띠를 팽창시키면 대동맥이 수축되고 측정띠가 수축하면 대동맥이 확장되어 대동맥이 두 번째 좌심실이 됩니다.제안된 개선 방법은 환자의 골격 근육을 사용하여 심장 박동기에 의해 구동되며, 이 장치는 진정한 자급자족형 장치를 만들 수 있습니다.그러나 1990년대에 유사한 수술(심근성형술)이 시행되었지만 실망스러운 결과를 얻었다.어떤 경우든 심장 자체를 수술할 필요가 없고 혈액과 장치 사이의 접촉을 피할 수 있는 상당한 잠재적 이점이 있습니다.이 접근법에는 맥동 [citation needed]흐름으로 되돌아가는 것이 포함됩니다.
한때 Peter Hougton은 영구적인 사용을 위해 VAD의 가장 오래 살아남은 환자였다.그는 2000년 6월에 실험용 Jarvik 2000 LVAD를 받았다.그 이후로, 그는 91마일의 자선 산책을 마치고, 두 권의 책을 출판하고, 널리 강의를 하고, 스위스 알프스와 미국 서부를 하이킹하고, 초경량 항공기를 타고 세계를 광범위하게 여행했다.그는 2007년 [21][22]69세의 나이로 급성 신장 부상으로 사망했다.이후 환자 Lidia Pluhar는 VAD에서 Hougton의 수명을 초과하여 2011년 3월 75세의 나이로 HeartMate II를 받았으며, 현재 이 장치를 계속 사용하고 있습니다.2007년 8월, ICAC(International Consortium of Circulatory Assist Clinicalians)는 간호사 개업의(NP)이자 뉴어크 주 뉴어크 베스 이스라엘 메디컬 센터의 기계 순환 지원(MCS) 프로그램의 임상 관리자인 Anthony "Tony" Martin에 의해 ICC501이 개발되었습니다.심장 이식을 위한 가교로서 또는 심장 [23]이식을 위한 기준을 충족하지 못하는 사람들의 목적 치료로서 MCS를 필요로 하는 사람들의 치료와 관련된 모범 사례와 교육의 nt.
연구 및 결과
최근의 동향
- 2007년 8월 Anthony "Tony" Martin에 의해 국제 순환 보조 의료인 컨소시엄(ICCAC)이 설립되었습니다.N.J. 뉴어크 소재 뉴어크 베스 이스라엘 메디컬 센터의 간호사(NP) 및 기계 순환 지원(MCS) 프로그램의 임상 관리자.
- 2009년 7월 영국에서 외과의사들은 그녀의 모국 심장이 회복된 후 그녀의 모국 심장 옆에 있는 유아에게 이식된 기증된 심장을 제거했다.이 기술은 LVAD와 같은 기계적 보조 장치가 기본 심장으로부터 일부 또는 모든 작업을 빼앗아 [24]치유 시간을 줄 수 있음을 시사합니다.
- 2009년 7월, HeartMate II 임상시험의 18개월 추적 결과는 연속 흐름 LVAD가 기능적 상태와 삶의 [25]질 향상과 함께 이식 대기 환자에게 최소 18개월 동안 효과적인 혈류역학적 지원을 제공한다는 결론을 내렸다.
- 하이델베르크 대학병원은 2009년 7월에 DeBakey VAD의 현대 버전으로 알려진 첫 번째 HeartAssist5가 그곳에 이식되었다고 보고했다.Heart Assist 5는 무게가 92g이고 티타늄과 플라스틱으로 만들어졌으며 좌심실에서 [26]대동맥으로 혈액을 펌프질하는 역할을 한다.
- 관상동맥 바이패스 이식 환자 및 좌심실 보조 장치를 가진 말기 심부전 환자들로 구성된 1단계 임상시험이 진행 중이다(2009년 8월 현재).이 실험은 다른 세포들이 자라도록 자극하는 호르몬과 같은 성장 인자를 분비하는 세포를 포함하는 Anginera라고 불리는 패치를 테스트하는 것을 포함한다.이 패치는 심장 근육 세포로 씨앗을 뿌린 후 심장에 이식되며 근육 세포가 규칙적인 [27][28]수축을 가능하게 하는 방식으로 토종 조직과 소통하기 시작하는 것을 목표로 한다.
- 2009년 9월 뉴질랜드 뉴스 매체 Stuff는 앞으로 18개월에서 2년 이내에 VAD에 직접 접촉하지 않고 전원을 공급하는 새로운 무선 디바이스가 임상시험을 실시할 수 있게 될 것이라고 보도했습니다.성공하면 피부를 [29]통한 전원 케이블로 인한 감염 가능성을 줄일 수 있습니다.
- 미국 국립보건원(NIH)은 마이클 드베이키와 조지 넌이 만든 마이크로메드의 두 개의 VAD를 사용하여 "맥박이 없는" 인공심장을 개발하기 위해 280만 달러의 보조금을 지급했다.보조금은 2009년 8월에 2년차 연구를 위해 갱신되었다.총 인공 심장은 두 개의 HeartAssist5 VAD를 사용하여 생성되었으며, 한 개의 VAD는 몸 전체에 혈액을 펌프하고 다른 한 개의 VAD는 폐를 [30]오가며 혈액을 순환시킵니다.
- HeartWare International은 2009년 8월 FDA 승인 IDE 연구인 ADVANCE 임상시험에서 HeartWare Ventricle Assist System 임플란트 50개를 넘어섰다고 발표했다.이 연구는 말기 심부전 환자를 위한 이식교로서 시스템을 평가하는 것이다.'진행성 심부전 치료를 위한 HeartWare LVAD 시스템 평가' 연구는 2009년 [31][32]5월에 시작된 다중 센터 연구입니다.
- 2014년 6월 27일, 독일 하노버 의과대학은 심장흉부 이식 및 혈관외과 과장 Axel Haverich M.D. 교수와 외과의사 Jan Schmitto, MD, Ph[33].D.의 지도 아래 HeartMate III의 첫 인체 임플란트를 시행하였다.
- 2015년 1월 21일, LVAD의 장기 사용이 심장 [34]재생을 유도할 수 있다는 연구 결과가 미국 심장 의학 저널에 발표되었습니다.이는 2009년 NEJM의 Yacoub 그룹이 최초로 설명한 브리지 투 리커버리 현상을 설명할 수 있습니다([citation needed]상기).
- 명예의 전당 야구 선수 로드 카레는 울혈성 심부전이 있었고 하트메이트 II를 장착했다.그는 장비를 착용하는 데 어려움을 겪었기 때문에 HeartMate II와 HeartMate [35]III를 지원하기 위해 가장 도움이 되는 착용감을 공급하기 위한 노력에 동참했다.
- 2018년 12월 카자흐스탄에서 2건의 임상 사례가 수행되었으며, Leviticus Cardio FiVAD(Fully Implantable Ventricle Assist Device)와 결합된 Jarvik 2000의 완전 무선 LVAD 시스템이 사람에게 이식되었습니다.Coplanar Energy Transfer(CET)라고 불리는 기술을 기반으로 한 무선 전력 전송 기술은 외부 전송 코일에서 인체에 내장된 소형 수신 코일로 에너지를 전달할 수 있습니다.수술 후 초기 단계에서는 CET 작동이 두 환자 모두에서 예상대로 이루어졌으며, 이를 통해 펌프에 전원을 공급하고 배터리를 충전하여 의료 및 간호 절차를 수행할 수 있게 되었습니다.Leviticus Cardio FiVAD 시스템은 드라이브라인 제거로 감염 위험을 개선하면서 LVAD를 [36]상당한 시간(약 6시간) 동안 홀리스 없이 지원할 수 있는 에너지 전송을 제공합니다.
- 2021년 6월 3일 Medtronic은 HVAD와 다른 사용 가능한 장치 대비 신경학적 사건 및 사망률이 높아 HVAD 장치를 더 이상 이식해서는 안 된다는 긴급 의료 장치 공지를 발표했다.
현재 시장에 나와 있는 대부분의 VAD는 다소 부피가 큽니다.FDA가 승인한 가장 작은 장치인 HeartMate II는 무게가 약 1파운드(0.45kg)이고 3인치(7.6cm)입니다.이것은 대안들이 너무 [38]컸을 여성과 아이들에게 특히 중요한 것으로 입증되었다.2017년 현재, HeartMate III는 FDA의 승인을 받았습니다.이전 모델인 HeartMate II보다 작고 HeartMate [39]II의 컵 앤 볼 베어링 시스템 대신 풀 자기부상 임펠러를 사용합니다.
장치 중 하나인 VentrAssist는 CE Mark의 EU 사용 승인을 받아 미국에서 임상시험을 시작했습니다.2007년 6월 현재 이 펌프는 100명이 넘는 환자에게 이식되었습니다.2009년, Ventracor는 재무상의 문제로 관리자의 손에 넘어갔고, 그 해 말에 청산되었습니다.다른 회사는 이 기술을 구매하지 않았기 때문에 VentrAssist 장치는 기본적으로 폐기되었습니다.2010년 [citation needed]1월 현재 전 세계 약 30~50명의 환자가 VentrAssist 디바이스에서 지원을 받고 있습니다.
HeartWare HVAD는 VentrAssist와 유사하게 작동하지만 훨씬 작고 복부 포켓을 이식할 필요가 없습니다.이 장치는 유럽에서는 CE Mark, 미국에서는 FDA 승인을 받았습니다.HeartWare HVAD는 흉골절제술 없이 제한된 접근을 통해 이식할 수 있었지만 2021년 Medtronic은 장치를 [40][37]중단했습니다.
소수의 사례에서 좌심실 보조 장치는 약물 치료와 결합되어 장치를 제거할 수 있을 정도로 심장이 충분히 회복될 수 있게 되었습니다.[2][3]
HeartMate II LVAD 중추적 연구
HeartMate II LVAD를 사용하는 것과 관련된 일련의 연구는 브릿지 투 이식 및 대상 치료에 LVAD를 사용하는 것의 실행 가능성과 위험을 설정하는 데 유용한 것으로 입증되었습니다.
- HeartMate II LVAD의 시범 시험은 2003년 11월에 시작되었으며 15개 센터의 46명의 연구 환자로 구성되었다.결과에는 1년 이상 지원된 11명의 환자와 2년 [citation needed]이상 지원된 3명의 환자가 포함되었습니다.
- HeartMate II 중추적 시험은 2005년에 시작되었으며, 두 가지 지표에 대한 HeartMate II의 평가가 포함되었습니다: BTT와 Destination Therapy(DT) 또는 장기적이고 영구적인 지원.Thatatec Corp.는 FDA가 두 가지 징후를 하나의 [41][42][43]프로토콜에 포함시키는 임상 실험을 승인한 것은 이번이 처음이라고 발표했다.
- 2005년부터 2007년까지 미국에서 113명의 환자를 대상으로 한 다중 기업 연구(이 중 100명의 주요 결과 보고)에 따르면 3개월 후 기능 면에서 유의한 개선이 나타났으며, [44]12개월 후 생존율은 68%였다.
- FDA는 첫 번째 임상시험에 등록된 194명의 환자의 1년 추적 데이터를 바탕으로 HeartMate II를 브리지 투 이식에 사용할 수 있도록 승인했습니다.이 실험은 광범위한 [45][46]환자의 생존율과 삶의 질 향상에 대한 임상 증거를 제공했다.
- 연구 종료점에 도달했거나 수술 후 18개월의 후속 조치를 완료한 281명의 환자에 대한 18개월 추적 데이터는 맥동 유동 장치에 비해 지속적 유동 LVADS로 생존이 향상되고, 부작용 빈도가 낮으며, 신뢰성이 더 높은 것으로 나타났다.281명의 환자 중 157명이 이식을 받았고 58명의 환자가 체내에 LVAD를 계속 투여했으며 7명의 환자가 심장이 회복돼 LVAD를 제거했으며 나머지 56명은 사망했다.결과는 LVAD 전 기준선에 비해 6개월 동안 LVAD 지원을 받은 후 환자의 NYHA 심부전 클래스가 유의하게 개선되었음을 보여주었다.이 시험에는 브릿지 투 이식 징후가 포함되었지만, 결과는 목적지 [47]치료를 위한 기계적 지원을 받는 환자에게 연속 흐름 LVAD가 내구성 및 신뢰성 측면에서 유리하다는 초기 증거를 제공합니다.
- 브리지 투 이식 목적으로 FDA가 HeartMate II LVAD를 승인한 후 상업적 환경에서 장치의 유효성을 평가하기 위한 사후 승인("등록") 연구가 수행되었다.연구 결과 다른 LVAD 치료 및 기준 환자에 비해 기기가 결과를 개선한 것으로 나타났다.구체적으로, HeartMate II 환자는 크레아티닌 수치가 낮았고, 30일 생존율은 96%로 상당히 높았으며, 93%가 성공적인 결과(이식, 심장 회복 또는 장기 LVAD)[48]에 도달했다.
하프
Harefield Recovery Protocol Study(HARPS)는 VAD 지원을 필요로 하는 고도 심부전 환자가 기기를 제거할 수 있는 충분한 심근 기능을 회복할 수 있는지 여부를 평가하기 위한 임상 시험이다.HARPS는 LVAD(HeartMate XVE)를 기존의 경구 심부전 약물과 결합한 후 새로운 β2 작용제 클렌부테롤을 사용한다.이것은 일부 고도 심부전 환자들이 심장 [49]이식을 포기할 수 있는 가능성을 열어준다.
현재까지 복합요법 요법을 받은 환자의 73%(15명 중 11명)는 이식을 허용하고 심장 이식을 피하기에 충분한 회복을 보였다. 생존 환자의 재발성 심부전으로부터의 자유도는 각각 100%, 89%였다. 평균 배출율은 59개월에서 64%였다.체내 이식; 모든 환자는 NYHA Class I이었으며 클렌부테롤 [citation needed]치료에서 유의미한 부작용은 보고되지 않았다.
재매치
REMATCH(Randomized Evaluation of Mechanical Assistance for Treating of Culestive Heart Failure) 임상시험은 1998년 5월에 시작되어 2001년 7월까지 미국 전역의 20개 심장 이식 센터에서 진행되었다.이 실험은 심장 이식을 필요로 하지만 자격이 없는 말기 심부전 환자를 위해 좌심실 보조 장치의 장기 이식 및 최적의 의료 관리를 비교하기 위해 고안되었습니다.임상 결과의 결과로 기기는 각각 [50]2001년과 2003년에 두 가지 징후 모두에 대해 FDA 승인을 받았다.
이 실험에서는 최적의 의료 관리에 비해 HeartMate XVE를 받은 환자의 2년 생존율이 81% 향상되었습니다.또한, REMATCH 시험 이후의 목적지 치료 연구에서는 VAD(HeartMate XVE)를 이식받은 환자의 1년 생존율이 17% 향상(61% 대 52%)되었으며, 이는 VAD [citation needed]이식 대상자의 적절한 선택과 시기를 암시하는 것으로 나타났다.
Eric A 박사가 2001년에 실시한 테스트. LVAD를 이식할 수 없는 울혈성 심부전 환자를 가진 Rose와 REMATCH 연구 그룹은 LVAD를 이식한 환자의 2년 생존율이 23%로 약물 치료를 받은 환자의 8%에 비해 높았다.VAD 이식의 두 가지 주요 합병증은 감염과 기계적 고장이었다[citation needed].
심장 이식을 기다리는 동안 좌심실 보조 장치로 치료된 환자들과 인트로프 치료를 비교한 소급 코호트 연구에 따르면, LVAD로 치료된 그룹은 이식 당시 더 나은 혈압, 나트륨, 혈액 요소 질소 및 크레아티닌으로 임상 및 대사 기능을 개선했다.이식 후, 이노트로프 그룹의 57.7%가 신장 기능 부전을 일으켰고, 이노트로프 그룹의 31.6%가 신장 기능 부전을 겪었고, 이노트로프 그룹의 5.6%가 신장 기능 부전을 겪었으며, 사건 없는 생존은 이노트로프 그룹의 15.8%와 LVAD [51]그룹의 55.6%였다.
합병증과 부작용
출혈은 LVAD의 이식 또는 이식 후 가장 흔한 수술 후 초기 합병증으로,[52][53] 최대 60%의 수용자에게 재수술이 필요합니다.대량 수혈의 영향은 크며 감염, 폐 기능 부전, 비용 증가, 우측 심부전, 동종감작, 바이러스 전염을 포함하며, 이들 중 일부는 치명적이거나 [53]이식을 막을 수 있다.출혈이 발생하면 1년간의 카플란-마이어 [52]사망률에 영향을 미칩니다.환자 집단의 복잡성과 출혈에 기여하는 이러한 절차의 복잡성 외에도, 장치 자체가 이러한 장치를 [54]이식할 때 발생할 수 있는 심각한 응고증의 원인이 될 수 있다.
이 장치는 일반적으로 혈액을 비생물학적 표면으로 흐르게 하여 혈액이 응고되기 쉽기 때문에 항응고 조치가 필요하다.한 장치인 HeartMate XVE는 섬유소에서 파생된 생물학적 표면으로 설계되었으며 장기적인 항응고(아스피린 제외)가 필요하지 않습니다. 불행히도 이 생물학적 표면은 또한 특정 유형의 [55]백혈구를 선택적으로 감소시킴으로써 환자가 감염될 수 있습니다.
현재 유럽 공동체에서 사용이 승인되고 FDA 승인을 위해 시험 중인 새로운 VAD 설계는 기계적 [citation needed]고장을 거의 제거했습니다.
표준 혈압 모니터링을 사용하여 LVAD 환자의 혈압을 측정하는 것은 어려우며, 현재 관행은 외래 환자의 도플러 초음파 검사와 입원 [56]환자의 침습 동맥 혈압 모니터링을 통해 측정하는 것입니다.
VAD 관련 감염은 다수의 다른 [57]유기체에 의해 발생할 수 있다.
- 그램 양성균(포도상구균, 특히 황색포도상구균, 장구균)
- 그램 음성세균(Pseudomonas aeruginosa, Enterobacter종, Klebsiella종)
- 균류, 특히 칸디다종
VAD 관련 감염의 치료는 매우 어렵고 많은 환자들이 최적의 치료에도 불구하고 감염으로 사망한다.초기 치료는 광범위한 항생제를 사용해야 하지만 배양에 적합한 샘플을 얻기 위해 모든 노력을 기울여야 한다.항생제 치료에 대한 최종 결정은 미생물 [citation needed]배양 결과에 기초해야 한다.
다른 문제로는 면역 억제, 그로 인한 뇌졸중으로 인한 응고, 항응고 이후에 발생하는 출혈 등이 있다.장치에 사용되는 폴리우레탄 성분 중 일부는 혈액이 접촉할 때 면역세포의 일부를 삭제한다.이것은 적절한 예방 치료가 [58]필요한 곰팡이 및 일부 바이러스 감염을 환자에게 유발한다.
심실 보조 장치 [59]임플란트와 관련된 다양한 위험과 생활 방식 변경을 고려할 때,[60] 의사 결정 전에 예비 환자에게 정보를 제공하는 것이 중요하다.의사 상담 외에도 [61][62]환자 교육에 도움이 되는 다양한 인터넷 기반 환자 지정 리소스를 사용할 수 있습니다.
삽입식 VAD 장치 목록
이 섹션은 업데이트해야 합니다.최신 하여 이 . (2015년 4월) |
이것은 부분 리스트이며 절대 완전하지 않을 수 있습니다.
참조된 추가를 환영합니다.
| 장치 | 제조원 | 유형 | 2010년 7월 현재 승인 현황 |
|---|---|---|---|
| 하트 어시스턴트 5 | 신뢰성 높은 하트 | 축류 로터에 의해 구동되는 연속 흐름. | 유럽연합에서 사용이 승인되었습니다.어린이 버전은 미국 FDA에 의해 어린이에게 사용이 승인되었습니다. FDA 승인을 위해 미국에서 임상시험을 진행 중입니다. |
| 노바코르 | 월드 하트 | 맥박이 뛰어요. | 북미, 유럽 연합 및 일본에서 사용이 승인되었습니다.현재는 폐지되어 제조원에 의해 지원되지 않게 되었습니다.(HeartWare는 2012년 8월에 인수를 완료) |
| 하트메이트 XVE | 타르테크 | 맥동 | 2001년 BTT에 대한 FDA 승인과 2003년 DT.CE 마크 인정신뢰성에 대한 우려 때문에 더 이상 거의 사용되지 않습니다. |
| 하트메이트 II | 타르테크 | 로터 구동식 연속 축류, 볼 및 컵 베어링 | 북미 및 EU에서의 사용이 승인되었습니다.CE 마크 인정.2008년 4월에 BTT에 대한 FDA 승인.최근 미국 FDA에 의해 목적지 치료에 대해 승인(2010년 1월 기준). |
| 하트메이트 III | 타르테크 | 자기적으로 매달린 축류 로터에 의해 구동되는 연속 흐름. | HeartMate III의 Pivotal 평가판은 2014년에 시작되었으며 CarewMedicalWear에서 지원됩니다.FDA 2017년 BTT 승인 |
| 영재하지 않다 | 베를린 심장 | 자기적으로 매달린 축류 로터에 의해 구동되는 연속 흐름. | 유럽 연합에서 사용이 승인되었습니다.미국에서는 사례별로 인도적 승인에 사용됩니다.2009년에 미국에서 임상시험에 참가. |
| Excor 소아과 | 베를린 심장 | 어린이를 위해 설계된 외부 멤브레인 펌프 장치. | 유럽 연합에서 사용이 승인되었습니다.FDA는 2011년 12월에 미국에 인도적 장치 면제를 승인했습니다. |
| 자빅 2000 | 자빅 하트 | 연속 흐름, 세라믹 베어링에 의해 지지되는 축 방향 로터. | 현재 미국에서 FDA 승인 임상 연구 하에 심장 이식을 위한 가교로 사용되고 있습니다.유럽에서는 Jarvik 2000이 브릿지 투 트랜플랜트 및 라이프타임 사용에 대해 CE Mark 인증을 취득했습니다.자 버전은 현재 개발 중입니다. |
| MicroMed DeBakey VAD | 마이크로메이드 | 세라믹 베어링에 의해 지지되는 축방향 로터에 의해 구동되는 연속 흐름. | 유럽연합에서 사용이 승인되었습니다.어린이 버전은 미국 FDA에 의해 어린이에게 사용이 승인되었습니다. FDA 승인을 위해 미국에서 임상시험을 진행 중입니다. |
| Ventr Assist(벤트 어시스턴트) | 벤트라코[63] | 유체역학적으로 매달린 원심 로터에 의해 구동되는 연속 흐름. | 유럽연합 및 호주에서 사용이 승인되었습니다.회사는 2009년 FDA 승인을 위한 임상시험이 진행 중 파산 선고를 받았다.회사는 해산되었고 지적재산은 Thatatec에 매각되었습니다. |
| MTIHeart LVAD | www.mitiheart.com | 자기적으로 매달린 원심 로터에 의해 구동되는 연속 흐름. | 현재 동물실험 중이며 최근 60일간의 종아리 이식수술이 성공적으로 완료되었습니다. |
| C-Pulse(현재는 "Aquadex") | Sunshine Heart (현재는 CHF 솔루션) | 맥박은 대동맥 주위의 부풀릴 수 있는 수갑에 의해 움직인다. | 현재 시판 중 |
| HVAD | HeartWare(현 Medtronic) | 심막 공간에 배치할 수 있는 원심 혈로와 유체 자기적으로 매달린 로터가 있는 미니어처 "3세대" 장치. | 2009년 1월, 유럽에서의 배포용으로 CE Mark 취득.2012년 11월 미국에서 FDA 승인 취득.2008년 10월 미국 BTT 시험(2010년 2월 완료), 2010년 8월 미국 DT 시험(2012년 5월 등록 완료)을 개시.2012년 BTT, 2017년 DT에 대한 FDA 승인.2021년 6월[64] 시장 철수 |
| MVAD | 하트웨어 | HeartWare의 MVAD Pump는 개발 단계의 소형 심실 보조 장치로, HeartWare의 HVAD 펌프 크기의 약 1/3입니다. | HeartWare GLP 연구 완료(2011년 9월). |
| 듀라하트 | 테루모 | 자기 부상 원심 펌프 | CE 승인, 2010년 1월 현재 미국 FDA 시험 진행 중. |
| Thatatec PVAD(패럴 심실 보조 장치) | 타르테크 | 맥동 시스템은 세 가지 주요 구성 요소로 구성됩니다.혈액 펌프, 캐뉴래 및 공압 드라이버(듀얼 드라이브 콘솔 또는 휴대용 VAD 드라이버). | CE 마크 인정1995년 BTT, 1998년 심장절개수술 후 회복(개복수술)을 위해 FDA 승인을 받았다. |
| IVAD - 이식형 심실 보조 장치 | 타르테크 | 맥동 시스템은 세 가지 주요 구성 요소로 구성됩니다.혈액 펌프, 캐뉴래 및 공압 드라이버(듀얼 드라이브 콘솔 또는 휴대용 VAD 드라이버). | CE 마크 인정2004년 BTT에 대한 FDA 승인을 받았다.안정성 문제로 인한 부상 임플란트가 아닌 내부 임플란트 전용으로 승인되었습니다. |
| FiVAD | 레비티쿠스 흉부외과 | LVAD용 범용 무선 시스템.환자에게 6시간의 자유를 부여합니다. | 조사장치, 2018년 12월 2명의 환자가 아스타나에서 Jarvik 2000 LVAD로 Pya [36]교수에 의해 시험 실시. |
「 」를 참조해 주세요.
레퍼런스
- ^ Sef, D; Mohite, P; De Robertis, F; Verzelloni Sef, A; Mahesh, B; Stock, U; Simon, A (September 2020). "Bridge to heart transplantation using the Levitronix CentriMag short-term ventricular assist device". Artificial Organs. 44 (9): 1006–1008. doi:10.1111/aor.13709. PMID 32367538. S2CID 218506853.
- ^ a b Birks, EJ; Tansley, PD; Hardy, J; et al. (2006). "Left Ventricular Assist Device and Drug Therapy for the Reversal of Heart Failure". New England Journal of Medicine. 355 (18): 1873–1884. doi:10.1056/NEJMoa053063. PMID 17079761.
- ^ a b "National TV에서 첫 Ventr Assist 심장 회복 특집Ventracor.com. 2006년 10월 19일
- ^ Fajdek, B; Krzysztof, J (2–5 September 2014). "Automatic control system for ventricular assist device". 19th International Conference on Methods and Models in Automation and Robotics (MMAR): 874–879. doi:10.1109/MMAR.2014.6957472. ISBN 978-1-4799-5081-2. S2CID 13070912.
- ^ Schulman, AR; Martens, TP; Christos, PJ; et al. (2007). "Comparisons of infection complications between continuous flow and pulsatile flow left ventricular assist devices". The Journal of Thoracic and Cardiovascular Surgery. 133 (3): 841–842. doi:10.1016/j.jtcvs.2006.09.083. PMID 17320612.
- ^ "Panel A shows a first-generation pulsatile flow left ve - Open-i". openi.nlm.nih.gov. Retrieved 23 April 2018.
- ^ "404 Page not found". ResearchGate. Retrieved 23 April 2018.
{{cite web}}:Cite는 일반 제목(도움말)을 사용합니다. - ^ "SynCardia TAH pulsatile pump components" (PDF). syncardia.com. Retrieved 23 April 2018.
- ^ "The HeartMate XVE too has a vent line, despite being battery-powered" (PDF). aldmd.com. Retrieved 23 April 2018.
- ^ Slaughter, MS; Pagani, FD; Rogers, JG; et al. (2010). "Clinical management of continuous-flow left ventricular assist devices in advanced heart failure". The Journal of Heart and Lung Transplantation. 29 (4): S1–39. doi:10.1016/j.healun.2010.01.011. PMID 20181499.
- ^ Fukamachi, Kiyo; Smedira, Nicholas (August 2005). "Smaller, Safer, Totally Implantable LVADs: Fact or Fantasy?". ACC Current Journal Review. 14 (8): 40–42. doi:10.1016/j.accreview.2005.06.001.
- ^ 똑똑해, 프랭크"미국 최초 환자에게 자기 부상 심장 펌프 이식""오늘 심장학"2008년 10월
- ^ Pai, CN; Shinshi, T; Asama, J; et al. (2008). "Development of a Compact Maglev Centrifugal Blood Pump Enclosed in a Titanium Housing". Journal of Advanced Mechanical Design, Systems, and Manufacturing. 2 (3): 343–355. Bibcode:2008JAMDS...2..343P. doi:10.1299/jamdsm.2.343.
- ^ Hoshi, H; Shinshi, T; Takatani, S (2006). "Third-generation Blood Pumps with Mechanical Noncontact Magnetic Bearings". Artificial Organs. 30 (5): 324–338. doi:10.1111/j.1525-1594.2006.00222.x. PMID 16683949.
- ^ "Dr. Denton Cooley and Dr. Michael E. DeBakey: Rock stars of Houston medicine". Houston Chronicle. 3 April 2014.
- ^ Kirklin, JK; Naftel, DC (September 2008). "Mechanical circulatory support: registering a therapy in evolution". Circulation: Heart Failure. 1 (3): 200–5. doi:10.1161/circheartfailure.108.782599. PMC 3437761. PMID 19808290.
- ^ "Heart Pump Progress Announced - A promising step in artificial heart technology". Children's Today (March): 1,5. 19 March 1988.
- ^ Electric Heart. PBS.
- ^ 댄 바움."펄스 없음: 어떻게 의사들이 인간의 심장을 재창조했는가.Popular Science, 2012년
- ^ "VAD FAQ"컬럼비아 대학 의료 센터입니다.인용문: "HeartMate II를 이식받은 환자는 보통 맥박이 약해집니다."2016-08-27 참조.
- ^ "The First Lifetime-Use Patient". Jarvik Heart. Archived from the original on 21 November 2010.
- ^ 환자가 심장 보조 장치 세계 기록을 수립했습니다.텍사스 심장 연구소.2007년 7월 6일
- ^ "Home ICCAC".
- ^ Maugh, Thomas (14 July 2009). "Transplant shows heart's reparative capabilities". Los Angeles Times.
- ^ Pagani, FD; Miller, LW; Russell, SD; et al. (2009). "Extended Mechanical Circulatory Support with a Continuous-Flow Rotary Left Ventricular Assist Device". Journal of the American College of Cardiology. 54 (4): 312–321. doi:10.1016/j.jacc.2009.03.055. PMID 19608028.
- ^ "Heidelberg Cardiac Surgeons implant world's first new DeBakey Heart Assist Device". Insciences. 17 August 2009. Archived from the original on 18 July 2011.
- ^ Quinn, Dale (4 August 2009). "VA study: heart-healing patch". Arizona Daily Star. Archived from the original on 7 August 2009.
- ^ "A Study of Anginera in Patients Undergoing Coronary Artery Bypass Graft (CABG) Surgery". ClinicalTrials.gov. U.S. National Institutes of Health. 27 March 2009. Retrieved 15 September 2009.
- ^ Hunter, Tim (13 September 2009). "Meet the Kiwi bionic man". Manawatu Standard.
- ^ "$2.8 Million Grant Renewed for Development of "Pulse-Less" Total Artificial Heart". BusinessWire. 6 August 2009.
- ^ "Evaluation of the HeartWare LVAD System for the Treatment of Advanced Heart Failure". Johns Hopkins Medical Center. May 2009.
- ^ "HeartWare International Surpasses 50 Implants in the US". Bio-Medicine. 20 August 2009.
- ^ "Thoratec Announces First HeartMate III Human Implant And Start of CE Mark Trial". Thoratec Corporation. 20 August 2009. Archived from the original on 7 October 2014.
- ^ Canseco, Diana C.; Kimura, Wataru; Garg, Sonia; Mukherjee, Shibani; Bhattacharya, Souparno; Abdisalaam, Salim; Das, Sandeep; Asaithamby, Aroumougame; Mammen, Pradeep P.A.; Sadek, Hesham A. (2015). "Human Ventricular Unloading Induces Cardiomyocyte Proliferation". Journal of the American College of Cardiology. 65 (9): 892–900. doi:10.1016/j.jacc.2014.12.027. PMC 4488905. PMID 25618530.
- ^ "LVAD Wear". carewmedicalwear.com.
- ^ a b "First human use of a wireless coplanar energy transfer coupled with a continuous-flow left ventricular assist device". Heart and Lung Transplantation. 4 February 2019.
- ^ a b Njoku, Nnamdi (3 June 2021). "Urgent Medical Device Communication: Notification Letter Medtronic HVAD™ System" (PDF). Retrieved 30 September 2021.
{{cite web}}: CS1 maint :url-status (링크) - ^ Bogaev, R; Chen, L; Russell, SD; et al. (2007). "Medical Aspects of End-Stage Heart Failure: Transplantation and Device Therapies I, Abstract 1762: An Emerging Option for Women with Advanced Heart Failure: Results of the HeartMate II Continuous Flow Left Ventricular Assist Device Bridge to Transplant Trial". Circulation. II. American Heart Association. 116: 372. Archived from the original on 8 June 2011.
- ^ "Archived copy" (PDF). Archived from the original (PDF) on 10 January 2018. Retrieved 9 January 2018.
{{cite web}}: CS1 maint: 제목으로 아카이브된 복사(링크) - ^ Popov, AF; Hosseini, MT; Zych, B; et al. (2012). "HeartWare Left Ventricular Assist Device Implantation Through Bilateral Anterior Thoracotomy". The Annals of Thoracic Surgery. 93 (2): 674–676. doi:10.1016/j.athoracsur.2011.09.055. PMID 22269746.
- ^ Benton, Susan (19 August 2008). "HeartMate II Pivotal Clinical Trial Fact Sheet" (PDF). Thoratec Corporation. Retrieved 10 September 2009.
- ^ Dewey, Todd (19 August 2008). "The HeartMate II LVAS Pivotal Trial". Cardiopulmonary Research Science and Technology Institute. Archived from the original on 13 July 2007.
- ^ Mager, Belinda (25 April 2008). "FDA Approves HeartMate II Mechanical Heart Pump for Heart-Failure Patients Waiting for Organ Transplantation". NewYork–Presbyterian Hospital. Archived from the original on 8 May 2008.
- ^ Miller, LW; Pagani, FD; Russell, SD; et al. (2007). "Use of a Continuous-Flow Device in Patients Awaiting Heart Transplantation". New England Journal of Medicine. 357 (9): 885–896. doi:10.1056/NEJMoa067758. PMID 17761592.
- ^ Gavin, Kara (23 April 2008). "Exciting times for heart-assisting devices at U-M". University of Michigan Health System. Archived from the original on 10 May 2008.
- ^ "Thoratec HeartMate II LVAS – P060040". Food and Drug Administration. 23 April 2008. Retrieved 28 August 2009.
- ^ Eisen, HJ; Hankins, SR (2009). "Continuous Flow Rotary Left Ventricular Assist Device". Journal of the American College of Cardiology. 54 (4): 322–324. doi:10.1016/j.jacc.2009.04.028. PMID 19608029.
- ^ Starling, RC; Naka, Y; Boyle, AJ; et al. (August 2009). "Initial FDA Post-Approval Study INTERMACS Registry Results with a Continuous Flow Left Ventricular Assist Device as a Bridge to Heart Transplantation". Journal of Cardiac Failure. 15 (6): S46. doi:10.1016/j.cardfail.2009.06.252.
- ^ Miller, Leslie; Aaronson and Pagani (2008). "Harefield Recovery Protocol Study for Patients With Refractory Chronic Heart Failure (HARPS)". ClinicalTrials.gov. Retrieved 3 August 2009.
- ^ Rose, EA; Moskowitz, AJ; Packer, M; et al. (1999). "The REMATCH trial: Rationale, design, and end points. Randomized Evaluation of Mechanical Assistance for the Treatment of Congestive Heart Failure". The Annals of Thoracic Surgery. 67 (3): 723–730. doi:10.1016/S0003-4975(99)00042-9. PMID 10215217.
- ^ Rogers, JG; Butler, J; Lansman, SL; et al. (2007). "Chronic Mechanical Circulatory Support for Inotrope-Dependent Heart Failure Patients Who Are Not Transplant Candidates". Journal of the American College of Cardiology. 50 (8): 741–747. doi:10.1016/j.jacc.2007.03.063. PMID 17707178.
- ^ a b Schaffer, JM; Arnaoutakis, GJ; Allen, JG; et al. (2011). "Bleeding Complications and Blood Product Utilization With Left Ventricular Assist Device Implantation". The Annals of Thoracic Surgery. 91 (3): 740–749. doi:10.1016/j.athoracsur.2010.11.007. PMID 21352991.
- ^ a b Goldstein, Daniel J.; Robert B. Beauford (2003). "Left ventricular assist devices and bleeding: adding insult to injury". The Annals of Thoracic Surgery. 75 (6): S42–7. doi:10.1016/s0003-4975(03)00478-8. PMID 12820734.
- ^ Spanier, Talia; Oz, M; Levin, H; et al. (1996). "Activation of coagulation and fibrinolytic pathways with left ventricular assist devices". Journal of Thoracic and Cardiovascular Surgery. 112 (4): 1090–1097. doi:10.1016/s0022-5223(96)70111-3. PMID 8873737.
- ^ Samuels, LE; Kohout, J; Casanova-Ghosh, E; et al. (2008). "Argatroban as a Primary or Secondary Postoperative Anticoagulant in Patients Implanted with Ventricular Assist Devices". The Annals of Thoracic Surgery. 85 (5): 1651–1655. doi:10.1016/j.athoracsur.2008.01.100. PMID 18442558.
- ^ Castagna, Francesco; Stöhr, Eric J.; Pinsino, Alberto; Cockcroft, John R.; Willey, Joshua; Reshad Garan, A.; Topkara, Veli K.; Colombo, Paolo C.; Yuzefpolskaya, Melana; McDonnell, Barry J. (2017). "The Unique Blood Pressures and Pulsatility of LVAD Patients: Current Challenges and Future Opportunities". Current Hypertension Reports. 19 (10): 85. doi:10.1007/s11906-017-0782-6. ISSN 1522-6417. PMC 5645430. PMID 29043581.
- ^ Gordon, RJ; Quagliarello, B; Lowy, FD (2006). "Ventricular assist device-related infections". The Lancet Infectious Diseases. 6 (7): 426–37. doi:10.1016/S1473-3099(06)70522-9. PMID 16790383.
- ^ Holman, WL; Rayburn, BK; McGiffin, DC; et al. (2003). "Infection in ventricular assist devices: Prevention and treatment". The Annals of Thoracic Surgery. 75 (6 Suppl): S48–S57. doi:10.1016/S0003-4975(03)00479-X. PMID 12820735.
- ^ Marcuccilli, L; Casida, J; Peters, RM (2013). "Modification of self-concept in patients with a left-ventricular assist device: an initial exploration" (PDF). Journal of Clinical Nursing. 22 (2456–64): 2456–64. doi:10.1111/j.1365-2702.2012.04332.x. hdl:2027.42/99069. PMID 23506318.
- ^ Mcillvennan, CK; Allen, LA; Nowels, C; Brieke, A; Cleveland, JC; Matlock, DD (2014). "Decision making for destination therapy left ventricular assist devices: "there was no choice" versus "I thought about it an awful lot"". Circulation: Cardiovascular Quality and Outcomes. 7 (3): 374–80. doi:10.1161/CIRCOUTCOMES.113.000729. PMC 4081474. PMID 24823949.
- ^ Iacovetto, MC; Matlock, DD; Mcillvennan, CK; et al. (2014). "Educational resources for patients considering a left ventricular assist device: a cross-sectional review of internet, print, and multimedia materials". Circulation: Cardiovascular Quality and Outcomes. 7 (6): 905–11. doi:10.1161/CIRCOUTCOMES.114.000892. PMID 25316772.
- ^ Matlock, DD; Allen, LA; Thompson, JS; Mcilvennan, CK (31 July 2014). "A decision aid for Left Ventricular Assist Device (LVAD) for Destination Therapy A device for patients with advanced heart failure" (PDF). University of Colorado School of Medicine.
- ^ Ventracor는 2009년 7월 3일에 청산되었습니다.이것에 의해, 지적 재산, 임상 시험의 데이터, 플랜트·디바이스, 및 잔여 자산을 포함한 동사의 자산은 매각에Boyd, Tony (13 July 2009). "No Heart". Business Spectator. Retrieved 15 September 2009. 부쳐집니다.
- ^ FDA (3 June 2021). "FDA Alerts Health Care Providers to Stop New Implants of Certain Ventricular Assist Device System". Food and Drug Administration. Retrieved 8 July 2021.
외부 링크
- MyLVAD.com: 다양한 LVAD 정보를 제공하는 브랜드 외 사이트