암종
Carcinoma| 암종 | |
|---|---|
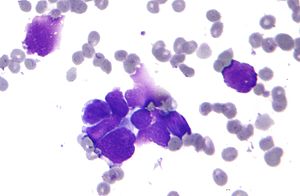 | |
| 폐 1차 소세포암의 현미경 사진, 암의 일종입니다.군집화된 암세포는 주로 핵(보라색)으로 구성되어 있으며, 세포질의 테두리가 거의 없다.주변의 창백한 얼룩, 원반상 세포는 적혈구이다.세포병리학 표본.필드 얼룩 | |
| 전문 | 종양학 |
암은 상피세포에서 [1]생기는 악성종양이다.구체적으로는 암은 체내 또는 외표면을 경계로 하는 조직에서 시작되며, 배아 [3]발생 시 내배엽, 중배엽[2] 또는 외배엽 배아층에서 유래한 세포에서 발생하는 암이다.
암종은 세포의 DNA가 손상되거나 변형되어 세포가 통제 불능으로 자라기 시작하고 악성화 될 때 발생한다.그것은 그리스어에서 유래했다: ααα δμα, 로마자: karkinoma, litt. '구토, 궤양, 암' (그 자체가 [4]게를 뜻하는 karkinos에서 유래)
분류
2004년 현재, [5]과학계에서는 간단하고 포괄적인 분류 시스템이 고안되어 받아들여지고 있지 않다.그러나 전통적으로 악성종양은 다음과 [6]같은 기준을 조합하여 다양한 유형으로 분류되어 왔다.
시작 셀 유형. 구체적으로는 다음과 같습니다.
역할을 하는 기타 기준은 다음과 같습니다.
- 악성세포가 정상적이고 변형되지 않은 세포와 비슷한 정도
- 국소 조직과 간질 구조의 출현
- 종양이 발생하는 해부학적 위치
- 유전적, 후생적, 분자적 특징
조직학적 유형
- 선암
- (아데노 = 글랜드) 현미경샘 관련 조직 세포학, 조직 구조 및/또는 글랜드 관련 분자 제품(예: 뮤신)을 특징으로 하는 암을 말한다.
- 편평상피암
- 편평상 분화(세포간 교량, 각질화, 편평상 진주)를 나타내는 특징과 특징이 관찰 가능한 암을 말한다.
- 아데노 편평암
- 선암과 편평상피암을 모두 포함하는 혼합종양을 말하며, 이들 세포타입이 종양용적의 적어도 10%를 구성한다.
- 미분화성암
- 보다 구체적으로 분화된 종양 중 어떤 것에 대한 뚜렷한 조직학적 또는 세포학적 증거가 결여된 세포를 특징으로 하는 이종 고등급 암종 그룹을 말한다.이러한 종양을 미분화암 또는 미분화암이라고 한다.
- 대세포암
- 풍부한 세포질을 가진 크고 단조로운 원형 또는 명백하게 다각형 모양의 세포로 구성됩니다.
- 소세포암
- 세포는 보통 둥글고 휴식 중인 림프구 지름의 약 3배 미만이며 뚜렷한 세포질이 거의 없다.간혹 작은 세포 악성종양 자체가 약간 다각형 및/또는 방추형 [7]세포의 중요한 성분을 가질 수 있다.
미분화성 암종에는 많은 희귀 아형이 있다.더 잘 알려진 것 중 일부는 유사 사코마티스 성분을 포함하는 병변들을 포함한다: 방추 세포 암(결합 조직 암과 유사한 긴 세포를 포함한다), 거대 세포 암(거대, 기괴, 다핵 세포를 포함한다), 그리고 육종(방추와 거대 세포 암의 혼합체)다형성암은 방추세포 및/또는 거대세포 성분을 포함하고 있으며, 또한 보다 고도로 분화된 유형의 세포(즉 선암 및/또는 편평상피세포암) 중 적어도 10%의 성분을 포함한다.매우 드물게 종양은 암육종과 폐포종을 포함하여 암종과 진육종을 [7]모두 닮은 개별 구성요소를 포함할 수 있다.흡연의 역사는 큰 세포암의 가장 흔한 원인이다.
알 수 없는 1차 부위의 암
암이라는 용어는 또한 기원이 불분명하거나 발달 계통이 불분명한 변형 세포로 구성된 악성 종양을 포함하게 되었다(원발성 암, CUP 참조). 그러나 상피세포의 전형적인 특정 분자, 세포 및 조직학적 특성을 가지고 있다.여기에는 하나 이상의 형태의 사이토케라틴 또는 다른 중간 필라멘트, 세포간 브리지 구조, 케라틴 진주 및/또는 성층화 [5][6]또는 의사 계층화와 같은 조직 구조 모티브의 생산이 포함될 수 있다.
ICD-10 코드
- (8010-8045) 상피신생물, NOS
- (8050-8080) 편평상피세포신생물
- (8090-8110) 기초세포종양
- (8120-8130) 전이세포암
- (8140-8380)선암
- (8390-8420) 부가종양 및 피부 부속종양
- (8430-8439) 무코에피더스 신생물
- (8440-8490) 낭포성, 점액성 및 장액성 종양
- (8500-8540) 관상, 엽상 및 수질 종양
- (8550-8559)아시나르세포신생물
- (8560-8580) 복합상피신생물
암종 발생 상황
위치암(또는 CIS)이라는 용어는 상당히 비정상적이지만 [8]암이 아닌 세포를 지칭하는 용어이다.그러므로 그들은 전형적인 [9]암종이 아니다.
병인 발생
암은 단일 전구 세포가 세포의 게놈을 구성하는 DNA, 히스톤, 그리고 다른 생화학적 화합물에 돌연변이와 다른 변화를 축적할 때 발생한다.세포 게놈은 세포의 생화학적 구성 요소의 구조, 세포 내에서 일어나는 생화학적 반응, 그리고 그 세포와 다른 세포와의 생물학적 상호작용을 통제한다.특정 전구 세포에서 돌연변이의 특정 조합은 궁극적으로 해당 세포(암 줄기세포라고도 함)가 여러 가지 비정상적인 악성 세포 특성을 나타내며, 함께 섭취할 경우 다음을 포함한 암의 특징으로 간주됩니다.
- 지속적으로 분열하여 기하급수적으로(또는 거의 연속적으로) 증가하는 새로운 악성 암 "딸 세포"(제어되지 않은 유사분열
- 정상적인 신체 표면과 장벽을 관통하고, 인근 신체 구조와 조직을 관통하는 능력(국소침습성)
- 림프관(국소 전이) 및/또는 혈관에 침투하거나 들어가 체내의 다른 부위로 확산하는 능력(부위 전이)[10]
면역 방어 자극과 치료 개입을 통해 지속적인 성장, 국소 침윤, 국소적·원거리 전이 과정을 중단하지 않으면 숙주는 몸 전체에 걸쳐 지속적으로 증가하는 종양 세포의 부담을 갖게 된다.결국 종양의 부담은 숙주의 장기에 의해 수행되는 정상적인 생화학적 기능을 점점 더 방해하고 결국 죽음에 이르게 된다.
암은 암의 한 형태일 뿐인데, 상피세포의 [5][6]세포학적 외관, 조직학적 구조 또는 분자적 특성을 발달시킨 세포로 구성되어 있다.전구암 줄기세포는 전능세포,[11][11] 다기능세포 또는 성숙한 분화세포에서의 [12]돌연변이의 많은 종양 유발 조합 중 하나로 형성될 수 있다.
침입과 전이
악성 종양의 특징은 국소 및 인접 구조에 침입하여 침투하는 경향이며, 결국 그 발생지점에서 신체 내 비인접 지역 및 먼 곳으로 전이되는 과정이다.선택하지 않으면 종양의 성장과 전이가 결국 종양 부담을 크게 만들어 숙주가 굴복하게 된다.암은 림프절과 혈액을 통해 전이된다.
돌연변이
전체 게놈 염기서열 분석으로 전체 인간 게놈의 돌연변이 빈도가 확립되었습니다.인간(부모 대 자녀) 세대 간 전체 게놈의 돌연변이 빈도는 [13]세대당 약 70개의 새로운 돌연변이다.
그러나 암종은 돌연변이 빈도가 훨씬 높다.특정 빈도는 조직 유형, 일치하지 않는 DNA 복구 결핍이 있는지 여부 및 담배 연기의 성분과 같은 DNA 손상 물질에 대한 노출에 따라 달라집니다.참치와 Amos는 표와 같이 일부 [14]암종에서 메가베이스(Mb)당 돌연변이 빈도를 (게놈당 돌연변이 빈도와 함께) 요약했다.
| 셀 타입 | 돌연변이 빈도 | |
|---|---|---|
| 메가베이스당 | 이배체별 게놈 | |
| 생식선 | 0.023 | 70 |
| 전립선암 | 0.9 | 5,400 |
| 대장암 | ~5 | ~30,000 |
| 마이크로위성안정(MSS)대장암 | 2.8 | 16,800 |
| 마이크로위성 불안정(MSI) 대장암(불일치 수리 부족) | 47 | 282,000 |
| 간세포암 | 4.2 | 25,200 |
| 유방암 | 1.18–1.66 | 7,080–9,960 |
| 폐암 | 17.7 | 106,200 |
| 소세포 폐암 | 7.4 | 44,400 |
| 비소세포 폐암(흡연자) | 10.5 | 63,000 |
| 비소세포 폐암(절대흡연자) | 0.6 | 3,600 |
| 폐선암(흡연자) | 9.8 | 58,500 |
| 폐선암(절대흡연자) | 1.7 | 10,200 |
돌연변이의 원인
암종 돌연변이의 가장 근본적인 원인은 DNA [citation needed]손상이다.예를 들어 폐암의 경우 외인성 유전독성 담배연기(예: 아크로레인, 포름알데히드, 아크릴로니트릴, 1,3-부타디엔, 아세트알데히드, 산화 에틸렌 및 이소프렌)[15]에 의해 DNA 손상이 발생한다.인간 세포의 게놈에서 하루에 평균 [citation needed]60,000번 이상 발생하는 내인성 DNA 손상 또한 매우 빈번하다.외적 및 내생적으로 발생한 손상은 부정확한 트랜스리온 합성 또는 부정확한 DNA 복구(예를 들어 비호몰로지 엔드 접합)에 의해 돌연변이로 변환될 수 있다.
고주파
암종 내 전체 게놈에서 높은 빈도의 돌연변이는 종종 초기 발암성 변화가 DNA 수복에 부족할 수 있음을 시사한다.예를 들어, DNA 불일치[16] 복구에서 결함이 있는 세포에서 돌연변이율은 상당히 증가한다(때로는 100배까지).
DNA 복구 자체의 결핍은 DNA 손상이 축적되도록 할 수 있으며, 그러한 손상 중 일부를 지나 오류 발생 가능성이 높은 트랜슬레이션 합성이 돌연변이를 일으킬 수 있다.또한 축적된 DNA 손상에 대한 잘못된 복구는 후생유전학적 변화 또는 후생을 일으킬 수 있습니다.DNA수복유전자 자체의 돌연변이 또는 발열은 선택적인 이점을 주지 않지만, 세포가 증식적 이점을 제공하는 추가적인 돌연변이/발열을 획득할 때 그러한 수복결손은 세포 내 승객으로 운반될 수 있다.이러한 세포는 증식적 이점과 하나 이상의 DNA 복구 결함(매우 높은 돌연변이율을 유발)을 모두 가지고 있으며, 암종에서 볼 수 있는 총 게놈 돌연변이의 높은 빈도를 야기할 가능성이 있다.
DNA복구
체세포에서, DNA 수복 유전자의 돌연변이에 의해 때때로 DNA 수복의 결핍이 발생하지만, 훨씬 더 자주 DNA 수복 유전자의 발현에서 후생유전학적 감소에 기인한다.따라서 113개의 대장암에서 DNA 복구 유전자 MGMT에 체세포 미센스 돌연변이가 발생한 반면, 이들 암의 대부분은 MGMT 프로모터 [17]영역의 메틸화로 인해 MGMT 단백질 발현을 감소시켰다.
진단.
발암은 미세침흡인(FNA), 코어 조직검사 또는 단일 노드의 [18]소계절 제거를 포함한 조직검사를 통해 최종 진단할 수 있다.병리학자에 의한 현미경 검사는 상피세포의 분자, 세포 또는 조직 구조 특성을 식별하기 위해 필요하다.
종류들
- 구강 : 대부분의 구강암은 편평상피암입니다
- 폐: 암은 전체 폐암의 98% 이상을 차지한다.
- 유방: 거의 모든 유방암은 관상암이다.
- 전립선:전립선암의 가장 흔한 형태는 선암종이다.
- 결장 및 직장:결장과 직장의 거의 모든 악성 종양은 선암이나 편평상피암이다.
- 췌장: 췌장암은 거의 항상 선암 타입이고 매우 치명적입니다.
- 난소:늦게 [19]발견되어 가장 치명적인 형태 중 하나죠
일부 암종은 또는 기원의 추정 세포(예: 간세포암, 신장세포암)로 명명된다.
스테이징
암의 병기란 신체/임상검사, 세포 및 조직의 병리학적 검토, 외과적 기법, 실험실 검사, 영상 연구를 논리적으로 결합하여 종양 크기와 그 침입 및 전이 정도에 대한 정보를 얻는 과정을 말한다.
암종은 보통 로마 숫자로 단계화된다.대부분의 분류에서 1기 및 2기 암종은 종양이 작거나 국소적인 구조에만 전이된 것으로 판명되었을 때 확인된다.제3기 암종은 일반적으로 국소 림프절, 조직 및/또는 장기 구조로 전이된 것으로 밝혀졌으며, 제4기 종양은 이미 혈액을 통해 먼 부위, 조직 또는 장기로 전이되었다.
일부 유형의 암종에서는 0기 암이 현장에서의 암과 악성 세포(폐암)에 대한 가래 검사를 통해서만 발견될 수 있는 잠재암을 묘사하기 위해 사용되어 왔다.
보다 최근의 스테이징 시스템에서는 서브제(a, b, c)가 유사한 예후 또는 치료 옵션을 가진 환자 그룹을 더 잘 정의하기 위해 더 일반적으로 사용되고 있다.
암기란 악성종양의 예후와 가장 일관되고 밀접하게 관련되어 있는 변수이다.
스테이지 기준은 종양이 발생하는 장기 시스템에 따라 크게 다를 수 있습니다.예를 들어 대장암과[20] 방광암의[21] 병기 시스템은 침입 깊이에 의존하며 유방암의 병기는 종양의 크기에 의존하며 신장암의 경우 종양의 크기와 신장동으로의 종양 침입 깊이에 기초한다.폐암은 여러 가지 크기와 [22]해부학적 변수를 고려하여 보다 복잡한 병기체계를 가지고 있다.
UICC/AJCC TNM 시스템이 가장 많이 사용됩니다.[clarification needed][23]그러나 일부 일반적인 종양에서는 여전히 고전적인 단계적 방법(대장암에 대한 Dukes 분류 등)이 사용됩니다.
채점
암종 등급 부여는 암종이 유래하는 정상적인 부모 상피 조직의 외관과 비교하여 변형된 세포에서 보이는 세포 및 조직의 성숙도를 반정량화하기 위한 기준의 적용을 의미한다.
암의 등급 부여는 치료의사 및/또는 외과의사가 외과적 절제, 바늘 또는 외과적 조직검사, 종양 조직의 직접 세척 또는 칫솔질, 가래 세포병리학 등을 사용하여 의심되는 종양 조직의 샘플을 얻은 후에 가장 자주 이루어집니다.그 후 병리학자는 염색, 면역 조직 화학, 흐름 세포 측정법 또는 다른 방법을 이용하여 종양과 그 기질을 검사합니다.마지막으로 병리학자는 반정량적으로 종양을 다음과 같은 3~4등급 중 하나로 분류합니다.
- 등급 1 또는 잘 구별되는 것: 정상 부모 조직과 매우 유사하거나 매우 유사하며, 종양 세포는 쉽게 식별되고 특정 악성 조직학적 실체로 분류된다.
- 등급 2 또는 중간 정도의 분화: 모세포와 조직과 상당히 유사하지만, 이상은 일반적으로 볼 수 있으며, 보다 복잡한 특징들은 특별히 잘 형성되어 있지 않다.
- 등급 3 또는 불충분한 분화: 악성 조직과 정상적인 부모 조직 사이에는 유사성이 거의 없고, 이상 징후가 뚜렷하며, 보다 복잡한 구조적 특징은 대개 기초적이거나 원시적입니다.
- 등급 4 또는 미분화 암종: 이러한 암종들은 대응하는 모세포와 조직과 유의한 유사성을 가지지 않으며, 선, 덕트, 브리지, 성층층, 케라틴 진주 또는 보다 고도로 분화된 종양과 일치하는 다른 주목할 만한 특징이 없다.
일부 종양 유형 및 발생 부위에 대해 암 등급과 종양 예후 사이에 확실하고 설득력 있는 통계적 상관관계가 있지만, 이 연관성의 강도는 매우 가변적일 수 있다.그러나 일반적으로 병변의 등급이 높을수록 [24][25]예후가 나빠진다고 말할 수 있다.
역학
암은 일반적으로 노년의 질병으로 여겨지지만, 어린이들도 [26]암에 걸릴 수 있다.성인들과 대조적으로, 암종은 어린이들에게서 유난히 드물다.암 진단의 1% 미만이 아이들에게 [27]있다.
난소암의 두 가지 가장 큰 위험 요인은 나이와 [28]가족력이다.
레퍼런스
- ^ Kirkham N, Lemoine NR (2001). Progress in pathology. London: Greenwich Medical Media. p. 52. ISBN 9781841100500.
- ^ Weinberg RA (24 May 2013). The biology of cancer (Second ed.). New York. ISBN 9780815345282. OCLC 841051175.
- ^ "Definition of Carcinoma". Retrieved 27 January 2014.
- ^ 옥스퍼드 영어사전 제3판s.v.
- ^ a b c Berman JJ (March 2004). "Tumor classification: molecular analysis meets Aristotle". BMC Cancer. 4 (1): 10. doi:10.1186/1471-2407-4-10. PMC 415552. PMID 15113444.
- ^ a b c Berman JJ (November 2004). "Tumor taxonomy for the developmental lineage classification of neoplasms". BMC Cancer. 4 (1): 88. doi:10.1186/1471-2407-4-88. PMC 535937. PMID 15571625.
- ^ a b Travis WD, Brambilla E, Muller-Hermelink HK, Harris CC, eds. (2004). Pathology and Genetics of Tumours of the Lung, Pleura, Thymus and Heart (PDF). World Health Organization Classification of Tumours. Lyon: IARC Press. ISBN 978-92-832-2418-1. Archived from the original (PDF) on 23 August 2009. Retrieved 27 January 2014.
- ^ Chang A (2007). Oncology: An Evidence-Based Approach. Springer. p. 162. ISBN 9780387310565.
- ^ Looijenga LH, Hersmus R, de Leeuw BH, Stoop H, Cools M, Oosterhuis JW, et al. (April 2010). "Gonadal tumours and DSD". Best Practice & Research. Clinical Endocrinology & Metabolism. 24 (2): 291–310. doi:10.1016/j.beem.2009.10.002. PMID 20541153.
- ^ "Carcinoma". Academic Press Dictionary of Science and Technology.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ a b Vassilev A, DePamphilis ML (January 2017). "Links between DNA Replication, Stem Cells and Cancer". Genes. 8 (2): 45. doi:10.3390/genes8020045. PMC 5333035. PMID 28125050.
- ^ Anandakrishnan R, Varghese RT, Kinney NA, Garner HR (March 2019). "Estimating the number of genetic mutations (hits) required for carcinogenesis based on the distribution of somatic mutations". PLOS Computational Biology. 15 (3): e1006881. Bibcode:2019PLSCB..15E6881A. doi:10.1371/journal.pcbi.1006881. PMC 6424461. PMID 30845172.
- ^ Roach JC, Glusman G, Smit AF, Huff CD, Hubley R, Shannon PT, et al. (April 2010). "Analysis of genetic inheritance in a family quartet by whole-genome sequencing". Science. 328 (5978): 636–639. Bibcode:2010Sci...328..636R. doi:10.1126/science.1186802. PMC 3037280. PMID 20220176.
- ^ Tuna M, Amos CI (November 2013). "Genomic sequencing in cancer". Cancer Letters. 340 (2): 161–170. doi:10.1016/j.canlet.2012.11.004. PMC 3622788. PMID 23178448.
- ^ Cunningham FH, Fiebelkorn S, Johnson M, Meredith C (November 2011). "A novel application of the Margin of Exposure approach: segregation of tobacco smoke toxicants". Food and Chemical Toxicology. 49 (11): 2921–2933. doi:10.1016/j.fct.2011.07.019. PMID 21802474.
- ^ Hegan DC, Narayanan L, Jirik FR, Edelmann W, Liskay RM, Glazer PM (December 2006). "Differing patterns of genetic instability in mice deficient in the mismatch repair genes Pms2, Mlh1, Msh2, Msh3 and Msh6". Carcinogenesis. 27 (12): 2402–2408. doi:10.1093/carcin/bgl079. PMC 2612936. PMID 16728433.
- ^ Halford S, Rowan A, Sawyer E, Talbot I, Tomlinson I (June 2005). "O(6)-methylguanine methyltransferase in colorectal cancers: detection of mutations, loss of expression, and weak association with G:C>A:T transitions". Gut. 54 (6): 797–802. doi:10.1136/gut.2004.059535. PMC 1774551. PMID 15888787.
- ^ Wagman LD (2008). "Principles of Surgical Oncology". In Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (eds.). Cancer Management: A Multidisciplinary Approach (11th ed.).
- ^ Boyraz G, Selcuk I, Yazıcıoğlu A, Tuncer ZS (September 2013). "Ovarian carcinoma associated with endometriosis". European Journal of Obstetrics, Gynecology, and Reproductive Biology. 170 (1): 211–213. doi:10.1016/j.ejogrb.2013.06.001. PMID 23849309.
- ^ Puppa G, Sonzogni A, Colombari R, Pelosi G (June 2010). "TNM staging system of colorectal carcinoma: a critical appraisal of challenging issues". Archives of Pathology & Laboratory Medicine. 134 (6): 837–852. doi:10.5858/134.6.837. PMID 20524862.
- ^ Sharir S (February 2006). "Update on clinical and radiological staging and surveillance of bladder cancer". The Canadian Journal of Urology. 13 (Suppl 1): 71–76. PMID 16526987.
- ^ Pepek JM, Chino JP, Marks LB, D'amico TA, Yoo DS, Onaitis MW, et al. (April 2011). "How well does the new lung cancer staging system predict for local/regional recurrence after surgery?: A comparison of the TNM 6 and 7 systems". Journal of Thoracic Oncology. 6 (4): 757–761. doi:10.1097/JTO.0b013e31821038c0. PMID 21325975. S2CID 24598745.
- ^ "What is Cancer Staging?". Archived from the original on 25 October 2007. Retrieved 27 January 2014.
- ^ Sun Z, Aubry MC, Deschamps C, Marks RS, Okuno SH, Williams BA, et al. (May 2006). "Histologic grade is an independent prognostic factor for survival in non-small cell lung cancer: an analysis of 5018 hospital- and 712 population-based cases". The Journal of Thoracic and Cardiovascular Surgery. 131 (5): 1014–1020. doi:10.1016/j.jtcvs.2005.12.057. PMID 16678584.
- ^ "Poorly differentiated cancer from an unknown primary site". Retrieved 6 June 2022.
- ^ Kuriakose MA, Hicks WL, Loree TR, Yee H (August 2001). "Risk group-based management of differentiated thyroid carcinoma". Journal of the Royal College of Surgeons of Edinburgh. 46 (4): 216–223. PMID 11523714. Archived from the original on 5 May 2010.
- ^ "Key Statistics for Childhood Cancers". www.cancer.org. Retrieved 6 May 2019.
- ^ Roett MA, Evans P (September 2009). "Ovarian cancer: an overview". American Family Physician. 80 (6): 609–16. PMID 19817326.


