베타글루쿠로니다아제
Beta-glucuronidase| 베타-프로니다아제 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| 식별자 | |||||||||
| EC 번호 | 3.2.1.31 | ||||||||
| CAS 번호. | 9001-45-0 | ||||||||
| 데이터베이스 | |||||||||
| 인텐츠 | IntEnz 뷰 | ||||||||
| 브렌다 | 브렌다 입력 | ||||||||
| 엑스퍼시 | 나이스자이메 뷰 | ||||||||
| 케그 | KEG 입력 | ||||||||
| 메타사이크 | 대사통로 | ||||||||
| 프리암 | 프로필 | ||||||||
| PDB 구조 | RCSB PDB PDBe PDBsum | ||||||||
| 진 온톨로지 | 아미고 / 퀵고 | ||||||||
| |||||||||
| 글루쿠로니다아제, 베타 | |||||||
|---|---|---|---|---|---|---|---|
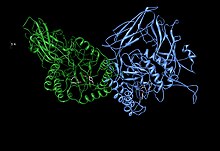 활성 사이트 잔류물 Glu451, Tyr504 및 Glu540과 잠재적으로 지원되는 Asn450 잔류물을[1] 보여주는 베타 글루쿠로니다아제 비대칭 장치 | |||||||
| 식별자 | |||||||
| 기호 | 구스비 | ||||||
| 엔씨비유전자 | 2990 | ||||||
| HGNC | 4696 | ||||||
| 오밈 | 611499 | ||||||
| RefSeq | NM_000181 | ||||||
| 유니프로트 | P08236 | ||||||
| 기타자료 | |||||||
| EC 번호 | 3.2.1.31 | ||||||
| 로커스 | 7번 씨 Q11.21 | ||||||
| |||||||
베타글루쿠로니다아제는 복합 탄수화물의 분해를 촉진하는 글리코시다아제 효소 계열의 구성원이다.[2] 인간 β-글루쿠로니다아제는 헤파란황산염과 같은 점액다당류(글리코사미노글리칸이라고도 한다)의 비절감 끝에서 β-D-글루쿠론산 잔류물의 가수분해를 촉진하는 글루쿠로니다아제의 일종이다.[2][3][4] 인간 β-글루쿠로니다아제는 리소돔에 위치한다.[5] 내장에서 브러시 테두리 β-글루쿠로니다아제는 결합 빌리루빈을 재흡수를 위해 비주선 형태로 변환한다. 모유에도 베타글루쿠로니다아제가 들어 있어 신생아 황달의 원인이 된다. 단백질은[6][7] 인간의 GUSB 유전자와 박테리아의 uidA 유전자에 의해 암호화된다.[8]
구조
인간 β-글루쿠로니다아제는 프로테롤리시스가 C-단자 끝에서 18개의 아미노산을 제거하여 78 kDa 단량체를 형성하기 전에 80 kDa 단량체로 합성된다.[9][10] 베타글루쿠로니다아제는 332 kDa 호모테트라머로 존재한다.[11] 베타글루쿠로니다아제는 젤리 롤 배럴과 TIM 배럴로 알려진 베타 배럴의 유형을 포함하여 몇 가지 주목할 만한 구조 형태를 포함하고 있다.[1]
카탈루션
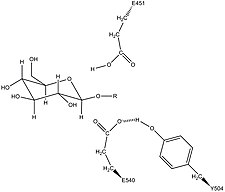
인간 β-글루쿠로니다아제는 대장균 효소 β-갈락토시다아제와 균질하다.[12][13] 이 동질적 관계는 글리코시다제가 종종 두 개의 산성 잔류물에 의해 촉매되는 가수분해를 수행한다는 지식과 함께 기계론적 가설의 개발을 가능하게 했다. 이 가설은 글루타민산 잔류물 두 개 글루540과 글루451이 각각 핵산 잔류물과 산성 잔류물이며, 티로신 잔류물 Tyr504도 촉매에 관여한다는 것을 제안한다. 이 가설을 뒷받침하기 위해, 이 세 가지 잔류물 중 어느 하나에서 실험적인 돌연변이는 효소 활성의 큰 감소를 초래한다. 아지드를 첨가한 후 E451A 돌연변이 효소(글루451을 알라닌 잔류물로 대체하는 경우)의 활성도가 증가하면 산/베이스 잔류물로 글루451과 일치한다.[14] 연구자들은 매우 안정적인 중간 단계로 진입하는 기질을 가수분해한 후 라벨이 부착된 β-글루쿠로니다아제 펩타이드의 분석을 통해 Glu540이 핵분열 잔류물임을 밝혀냈다.[15]
β-글루쿠로니다아제에 의해 채택된 핵소독성 대체의 특정 유형은 불분명하지만, 글리코시다아제 계열의 동음이의 메커니즘에 대한 증거는 이러한 반응이 질적으로 S2N 반응이라는 것을 암시한다. 반응은 옥소카르베늄 이온 특성을 가진 전이 상태를 통해 진행된다. 초기에 이러한 메커니즘은 전환 상태의 이 옥소카르베늄 특성 때문에 이산 옥소카르베늄 이온 중간을 통해 진행되는 S1N 반응으로 제안되었다. 그러나 보다 최근의 증거는 이러한 옥소카르베늄 이온 상태가 10페모초 - 0.1나노초(결합 진동 기간과 유사)의 수명을 가지고 있음을 시사한다. 이러한 수명은 반응 매개체에 할당하기에는 너무 짧다. 이러한 증거를 통해 이러한 반응은 전환 상태의 옥소카르베늄 이온 특성 때문에 S1의N 외관을 가지면서도 질적으로 S2N 반응이어야 한다는 것을 알 수 있다.[2]
촉매 메커니즘에서 Tyr504의 특정 활성도는 불분명하다.[14] 호몰로코 효소 자일라노아제의 구조적 데이터와 비교를 통해 β-글루쿠로니다아제의 Tyr504가 이탈핵생물(Glu540)을 안정화시키거나 그 활동을 조절할 수 있다는 제안이 나왔다.[16]
이러한 잔류물 외에도 보존된 아스파라긴 잔류물(Asn450)이 설탕 기질 2-하이드록실 그룹에서 수소 결합 작용을 통해 기질을 안정시킬 것을 제안했다.[11][17]
슬라이 증후군
β-글루쿠로니다아제의 결핍은 슬리 증후군 또는 뮤코폴리스다카리도스 7로 알려진 자가 열성 유전 대사 질환을 유발한다. 이 효소의 결핍은 환자에게서 무수화 점막다당체가 형성되는 결과를 초래한다. 이 질병은 환자에게 극도로 쇠약해질 수도 있고 태어나기 전에 수압 태아를 초래할 수도 있다. 또 생존 환자에서는 정신지체, 단신, 거친 얼굴 이목구비, 척수 이상, 간, 비장의 확대 등이 관찰된다.[5] 이 병은 개과뿐만 아니라 쥐의 품종에서도 본떠 만든 것이다.[19][20] 보다 최근에 연구자들은 β-글루쿠로니다아제 활동에서 결함을 보이는 고양이과 동물을 발견했다. 이러한 활동 감소의 원인은 E351K 돌연변이로 확인되었다(Glu351은 리신 잔류물로 변이된다). 글루351은 포유류 종에 보존되어 있는데, 이는 이 잔류물에 대한 중요한 기능을 시사한다. 인간 X선 결정 구조를 검사한 결과 TIM 배럴 영역 깊숙이 묻혀 있는 이 잔류물(인간 효소 내 Glu352)이 효소의 3차 구조 안정화에 중요할 수 있음을 알 수 있다.[18] 결정구조에서는 단백질의 젤리롤 영역의 멤버인 Arg216이 Glu352와 염교를 형성하는 것으로 나타나므로 Glu352는 효소의 서로 다른 3차원 영역 간의 상호작용을 안정시키는 데 관여할 가능성이 있다.[1]
분자적용: 리포터 유전자로 사용
분자생물학에서 β-글루쿠로니다아제는 포유류와 식물세포의 유전자 발현을 감시하는 리포터 유전자로 사용된다. GUS 검사를 통해 β-글루쿠로니다아제 활동을 모니터링하면 해당 유전자의 공간적, 시간적 발현을 결정할 수 있다.[21]
- 분자 그래픽 이미지는 샌프란시스코 캘리포니아 대학의 생물학 퍼팅, 시각화 및 정보학(NIH P41 RR-01081)에서 UCSF 치메라 패키지를 사용하여 제작되었다.[22]
참고 항목
참조
- ^ a b c d e f PDB: 1BHG; Jain S, Drendel WB, Chen ZW, Mathews FS, Sly WS, Grubb JH (April 1996). "Structure of human beta-glucuronidase reveals candidate lysosomal targeting and active-site motifs". Nature Structural Biology. 3 (4): 375–81. doi:10.1038/nsb0496-375. PMID 8599764. S2CID 28862883.
- ^ a b c Sinnott M, ed. (1998). Comprehensive Biological Catalysis. Vol. 1. Manchester, UK: Academic Press. pp. 119–138. ISBN 978-0-12-646864-9.
- ^ McCarter JD, Withers SG (December 1994). "Mechanisms of enzymatic glycoside hydrolysis". Current Opinion in Structural Biology. 4 (6): 885–92. doi:10.1016/0959-440X(94)90271-2. PMID 7712292.
- ^ Sinnott ML (1990). "Catalytic mechanisms of enzymic glycosyl transfer". Chem Rev. 90 (7): 1171–1202. doi:10.1021/cr00105a006.
- ^ a b Nyhan WL, Barshop B, Ozand P (2005). Atlas of Metabolic Diseases (2 ed.). London, UK: Hodder Arnold. pp. 501–503, 546–550. ISBN 978-0-340-80970-9.
- ^ Oshima A, Kyle JW, Miller RD, Hoffmann JW, Powell PP, Grubb JH, Sly WS, Tropak M, Guise KS, Gravel RA (February 1987). "Cloning, sequencing, and expression of cDNA for human beta-glucuronidase". Proceedings of the National Academy of Sciences of the United States of America. 84 (3): 685–9. Bibcode:1987PNAS...84..685O. doi:10.1073/pnas.84.3.685. PMC 304280. PMID 3468507.
- ^ "Entrez Gene: GUSB glucuronidase, beta".
- ^ Martins MT, Rivera IG, Clark DL, Stewart MH, Wolfe RL, Olson BH (July 1993). "Distribution of uidA gene sequences in Escherichia coli isolates in water sources and comparison with the expression of beta-glucuronidase activity in 4-methylumbelliferyl-beta-D-glucuronide media". Applied and Environmental Microbiology. 59 (7): 2271–6. Bibcode:1993ApEnM..59.2271M. doi:10.1128/AEM.59.7.2271-2276.1993. PMC 182268. PMID 8357258.
- ^ Islam MR, Grubb JH, Sly WS (October 1993). "C-terminal processing of human beta-glucuronidase. The propeptide is required for full expression of catalytic activity, intracellular retention, and proper phosphorylation". The Journal of Biological Chemistry. 268 (30): 22627–33. doi:10.1016/S0021-9258(18)41574-8. PMID 8226771.
- ^ Shipley JM, Grubb JH, Sly WS (June 1993). "The role of glycosylation and phosphorylation in the expression of active human beta-glucuronidase". The Journal of Biological Chemistry. 268 (16): 12193–8. doi:10.1016/S0021-9258(19)50325-8. PMID 8505339.
- ^ a b c Kim HW, Mino K, Ishikawa K (December 2008). "Crystallization and preliminary X-ray analysis of endoglucanase from Pyrococcus horikoshii". Acta Crystallographica. Section F, Structural Biology and Crystallization Communications. 64 (Pt 12): 1169–71. doi:10.1107/S1744309108036919. PMC 2593689. PMID 19052378.
- ^ Henrissat B, Bairoch A (August 1993). "New families in the classification of glycosyl hydrolases based on amino acid sequence similarities". The Biochemical Journal. 293 ( Pt 3) (3): 781–8. doi:10.1042/bj2930781. PMC 1134435. PMID 8352747.
- ^ Henrissat B (December 1991). "A classification of glycosyl hydrolases based on amino acid sequence similarities". The Biochemical Journal. 280 ( Pt 2) (2): 309–16. doi:10.1042/bj2800309. PMC 1130547. PMID 1747104.
- ^ a b Islam MR, Tomatsu S, Shah GN, Grubb JH, Jain S, Sly WS (August 1999). "Active site residues of human beta-glucuronidase. Evidence for Glu(540) as the nucleophile and Glu(451) as the acid-base residue". The Journal of Biological Chemistry. 274 (33): 23451–5. doi:10.1074/jbc.274.33.23451. PMID 10438523.
- ^ a b Wong AW, He S, Grubb JH, Sly WS, Withers SG (December 1998). "Identification of Glu-540 as the catalytic nucleophile of human beta-glucuronidase using electrospray mass spectrometry". The Journal of Biological Chemistry. 273 (51): 34057–62. doi:10.1074/jbc.273.51.34057. PMID 9852062.
- ^ a b "EzCatDB: T00066". EzCatDB: A Database of Catalytic Mechanisms. Archived from the original on 2009-06-17. Retrieved 2008-12-12.
- ^ a b Henrissat B, Callebaut I, Fabrega S, Lehn P, Mornon JP, Davies G (July 1995). "Conserved catalytic machinery and the prediction of a common fold for several families of glycosyl hydrolases". Proceedings of the National Academy of Sciences of the United States of America. 92 (15): 7090–4. Bibcode:1995PNAS...92.7090H. doi:10.1073/pnas.92.15.7090. PMC 41477. PMID 7624375.
- ^ a b Fyfe JC, Kurzhals RL, Lassaline ME, Henthorn PS, Alur PR, Wang P, Wolfe JH, Giger U, Haskins ME, Patterson DF, Sun H, Jain S, Yuhki N (June 1999). "Molecular basis of feline beta-glucuronidase deficiency: an animal model of mucopolysaccharidosis VII". Genomics. 58 (2): 121–8. doi:10.1006/geno.1999.5825. PMID 10366443.
- ^ Birkenmeier EH, Davisson MT, Beamer WG, Ganschow RE, Vogler CA, Gwynn B, Lyford KA, Maltais LM, Wawrzyniak CJ (April 1989). "Murine mucopolysaccharidosis type VII. Characterization of a mouse with beta-glucuronidase deficiency". The Journal of Clinical Investigation. 83 (4): 1258–66. doi:10.1172/JCI114010. PMC 303816. PMID 2495302.
- ^ Haskins ME, Desnick RJ, DiFerrante N, Jezyk PF, Patterson DF (October 1984). "Beta-glucuronidase deficiency in a dog: a model of human mucopolysaccharidosis VII". Pediatric Research. 18 (10): 980–4. doi:10.1203/00006450-198410000-00014. PMID 6436780.
- ^ Marathe SV, McEwen JE (February 1995). "Vectors with the gus reporter gene for identifying and quantitating promoter regions in Saccharomyces cerevisiae". Gene. 154 (1): 105–7. doi:10.1016/0378-1119(94)00845-J. PMID 7867935.
- ^ Pettersen EF, Goddard TD, Huang CC, Couch GS, Greenblatt DM, Meng EC, Ferrin TE (October 2004). "UCSF Chimera--a visualization system for exploratory research and analysis" (PDF). Journal of Computational Chemistry. 25 (13): 1605–12. doi:10.1002/jcc.20084. PMID 15264254. S2CID 8747218.
추가 읽기
- George J (June 2008). "Elevated serum beta-glucuronidase reflects hepatic lysosomal fragility following toxic liver injury in rats". Biochemistry and Cell Biology. 86 (3): 235–43. doi:10.1139/O08-038. PMID 18523484.
- Bell CE, Sly WS, Brot FE (January 1977). "Human beta-glucuronidase deficiency mucopolysaccharidosis: identification of cross-reactive antigen in cultured fibroblasts of deficient patients by enzyme immunoassay". The Journal of Clinical Investigation. 59 (1): 97–105. doi:10.1172/JCI108627. PMC 333336. PMID 401508.
- Tanaka J, Gasa S, Sakurada K, Miyazaki T, Kasai M, Makita A (January 1992). "Characterization of the subunits and sugar moiety of human placental and leukemic beta-glucuronidase". Biological Chemistry Hoppe-Seyler. 373 (1): 57–62. doi:10.1515/bchm3.1992.373.1.57. PMID 1311180.
- Wolfe JH, Sands MS, Barker JE, Gwynn B, Rowe LB, Vogler CA, Birkenmeier EH (1993). "Reversal of pathology in murine mucopolysaccharidosis type VII by somatic cell gene transfer". Nature. 360 (6406): 749–53. doi:10.1038/360749a0. PMID 1465145. S2CID 4337590.
- Tomatsu S, Fukuda S, Sukegawa K, Ikedo Y, Yamada S, Yamada Y, Sasaki T, Okamoto H, Kuwahara T, Yamaguchi S (January 1991). "Mucopolysaccharidosis type VII: characterization of mutations and molecular heterogeneity". American Journal of Human Genetics. 48 (1): 89–96. PMC 1682743. PMID 1702266.
- Shipley JM, Miller RD, Wu BM, Grubb JH, Christensen SG, Kyle JW, Sly WS (August 1991). "Analysis of the 5' flanking region of the human beta-glucuronidase gene". Genomics. 10 (4): 1009–18. doi:10.1016/0888-7543(91)90192-H. PMID 1916806.
- Ono M, Taniguchi N, Makita A, Fujita M, Sekiya C, Namiki M (April 1988). "Phosphorylation of beta-glucuronidases from human normal liver and hepatoma by cAMP-dependent protein kinase". The Journal of Biological Chemistry. 263 (12): 5884–9. doi:10.1016/S0021-9258(18)60648-9. PMID 2833520.
- Guise KS, Korneluk RG, Waye J, Lamhonwah AM, Quan F, Palmer R, Ganschow RE, Sly WS, Gravel RA (1985). "Isolation and expression in Escherichia coli of a cDNA clone encoding human beta-glucuronidase". Gene. 34 (1): 105–10. doi:10.1016/0378-1119(85)90300-2. PMID 3924735.
- Ho YC, Ho LH, Ho KJ (1985). "Human hepatic beta-glucuronidase: an enzyme kinetic study". Enzyme. 33 (1): 9–17. doi:10.1159/000469398. PMID 3987656.
- Shipley JM, Klinkenberg M, Wu BM, Bachinsky DR, Grubb JH, Sly WS (March 1993). "Mutational analysis of a patient with mucopolysaccharidosis type VII, and identification of pseudogenes". American Journal of Human Genetics. 52 (3): 517–26. PMC 1682147. PMID 7680524.
- Vervoort R, Lissens W, Liebaers I (1994). "Molecular analysis of a patient with hydrops fetalis caused by beta-glucuronidase deficiency, and evidence for additional pseudogenes". Human Mutation. 2 (6): 443–5. doi:10.1002/humu.1380020604. PMID 8111412. S2CID 46432543.
- Wu BM, Sly WS (1994). "Mutational studies in a patient with the hydrops fetalis form of mucopolysaccharidosis type VII". Human Mutation. 2 (6): 446–57. doi:10.1002/humu.1380020605. PMID 8111413. S2CID 21484555.
- Maruyama K, Sugano S (January 1994). "Oligo-capping: a simple method to replace the cap structure of eukaryotic mRNAs with oligoribonucleotides". Gene. 138 (1–2): 171–4. doi:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Moullier P, Bohl D, Heard JM, Danos O (June 1993). "Correction of lysosomal storage in the liver and spleen of MPS VII mice by implantation of genetically modified skin fibroblasts". Nature Genetics. 4 (2): 154–9. doi:10.1038/ng0693-154. PMID 8348154. S2CID 26122567.
- Shipley JM, Grubb JH, Sly WS (June 1993). "The role of glycosylation and phosphorylation in the expression of active human beta-glucuronidase". The Journal of Biological Chemistry. 268 (16): 12193–8. doi:10.1016/S0021-9258(19)50325-8. PMID 8505339.
- Nishimura Y, Kato K, Himeno M (July 1995). "Biochemical characterization of liver microsomal, Golgi, lysosomal, and serum beta-glucuronidases in dibutyl phosphate-treated rats". Journal of Biochemistry. 118 (1): 56–66. doi:10.1093/oxfordjournals.jbchem.a124892. PMID 8537326.
- Jain S, Drendel WB, Chen ZW, Mathews FS, Sly WS, Grubb JH (April 1996). "Structure of human beta-glucuronidase reveals candidate lysosomal targeting and active-site motifs". Nature Structural Biology. 3 (4): 375–81. doi:10.1038/nsb0496-375. PMID 8599764. S2CID 28862883.
- Vervoort R, Islam MR, Sly WS, Zabot MT, Kleijer WJ, Chabas A, Fensom A, Young EP, Liebaers I, Lissens W (March 1996). "Molecular analysis of patients with beta-glucuronidase deficiency presenting as hydrops fetalis or as early mucopolysaccharidosis VII". American Journal of Human Genetics. 58 (3): 457–71. PMC 1914559. PMID 8644704.
- Bonaldo MF, Lennon G, Soares MB (September 1996). "Normalization and subtraction: two approaches to facilitate gene discovery". Genome Research. 6 (9): 791–806. doi:10.1101/gr.6.9.791. PMID 8889548.
- Dentino AR, Raj PA, De Nardin E (January 1997). "Subtle differences between human and rabbit neutrophil receptors shown by the secretagogue activity of constrained formyl peptides". Archives of Biochemistry and Biophysics. 337 (2): 267–74. doi:10.1006/abbi.1996.9791. PMID 9016822.
외부 링크
- 미국 국립 의학 도서관의 글루쿠로니다아제(MSH)
- 리포지터gene의 리포터 글루쿠로니다아제 및 기타 리포터에 대한 최신 연구
- 촉매 메커니즘 연구 데이터베이스 및 베타 글루쿠로니다아제에 대한 기타 정보