계수 XIII
Factor XIII| 응고인자 XIII, A1 폴리펩타이드 | |||||||
|---|---|---|---|---|---|---|---|
 비활성 A1 펩타이드 호모디머로 모든 도메인과 주요 촉매 잔류물이 다른 색상으로 표시됨. | |||||||
| 식별자 | |||||||
| 기호. | F13A1 | ||||||
| Alt. | F13A | ||||||
| NCBI유전자 | 2162 | ||||||
| HGNC | 3531 | ||||||
| 옴 | 134570 | ||||||
| 참조 | NM_000129 | ||||||
| 유니프로트 | P00488 | ||||||
| 기타 데이터 | |||||||
| EC 번호 | 2.3.2.13 | ||||||
| 궤적 | 제6장 p24.2-p23 | ||||||
| |||||||
| 응고인자 XIII, B폴리펩타이드 | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호. | F13B | ||||||
| NCBI유전자 | 2165 | ||||||
| HGNC | 3534 | ||||||
| 옴 | 134580 | ||||||
| 참조 | NM_001994 | ||||||
| 유니프로트 | P05160 | ||||||
| 기타 데이터 | |||||||
| 궤적 | 제1장 q31-q32.1 | ||||||
| |||||||
인자 XIII 또는 섬유소 안정화 인자는 사람과 다른 동물의 혈액에서 발견되는 자이모겐이다.트롬빈에 의해 활성화되어 XIIIa 인자가 된다.인자 XIIIa는 섬유소를 가교하는 혈액응고 시스템의 효소이다.XII가 부족하면 응고 안정성이 나빠지고 출혈 경향이 [1]높아집니다.
인간 XIII는 이성질체이다.2개의 효소 A 펩타이드와 2개의 비효소 B 펩타이드로 구성되어 있다.XIIa는 활성화된 A펩타이드의 [1]이합체이다.
기능.
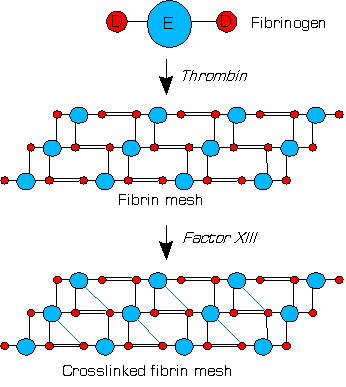
혈액 내에서 트롬빈은 응고 중에 피브리노겐을 피브린으로 분해하고 피브린 기반의 혈전을 형성한다.인자 XIII는 2개의 A와 2개의 B 서브유닛의 헤테로테트라미터로 사람의 혈액을 순환하는 트랜스글루타미나아제이다.인자 XIII는 B유닛을 통해 응고에 결합합니다.피브린의 존재 하에서 트롬빈은 XII 사량체 내에서 각 A 단위의 R37–G38 펩타이드 결합을 효율적으로 분해한다.유닛은 N-말단 활성화 펩타이드를 [1]방출합니다.
두 비공유 결합 B 단위 모두 이제 혈액 내 칼슘 이온(Ca2+)의 도움으로 4량체로부터 분리할 수 있습니다. 또한 이러한 이온은 구조 [1]변화를 통해 두 개의 A 단위의 나머지 이합체를 활성화시킵니다.
인자 XIIIa(2개의 활성 A 단위 중 조미체)는 피브린의 다양한 글루타민과 리신 사이에 이소펩티드 결합을 형성함으로써 응고 내에서 피브린을 가교한다.이러한 결합은 응고를 물리적으로 더 오래 지속하게 하고 조기 효소 분해(섬유 분해)[1]로부터 보호합니다.
사람의 경우 플라즈민, 항트롬빈 및 TFPI는 활성인자 XIIII의 가장 관련성이 높은 단백질 분해 억제제이며,[1] α2-마크로글로불린은 유의미한 비단백질 억제제이다.
유전학
인적 요인 XIII는 A와 B 서브유닛으로 구성됩니다.서브유닛 유전자는 F13A1이다.그것은 6번 염색체의 6p24-25 위치에 있다.160kbp가 넘고 14개의 인트론과 15개의 엑손이 있습니다.mRNA는 3.9kbp입니다.5' UTR은 84bp, 3' UTR은 1.6kbp입니다.F13A1 [1]엑손
B 서브유닛 유전자는 F13B이다.그것은 염색체 1의 1q31–32.1 위치에 있다.용량은 28kpb이며, 11개의 인트론 및 12개의 엑손이 있습니다.mRNA는 2.2kbp입니다.Exon 1은 5' UTR 코드입니다.Exon 2 ~ 12는 10개의 다른 [1]초밥 도메인을 코드합니다.
구조.
인간 혈액의 인자 XIII는 두 개의 A와 두 개의 B 선형 폴리펩타이드 또는 "단위"로 이루어진 헤테로테트라머이다.A 유닛은 잠재적으로 촉매제이지만 B 유닛은 촉매제가 아닙니다.단위는 이합체 중심을 형성합니다.비공유 결합 B 유닛은 중심 주위에 고리 모양의 구조를 형성합니다.B 유닛은 XII가 XIIa로 활성화되면 제거됩니다.A 단위만을 포함하는 이합체도 혈소판 등의 세포 내에서 발생합니다.다량의 단수 B 단위(단량체)도 혈액 내에서 발생한다.이러한 이합체 및 단량체는 응고에 관여하는 것으로 알려져 있지 않지만, 4량체는 [1]응고에 관여한다.
A 단위의 질량은 약 83kDa, 아미노산 잔기 731개, 단백질 도메인 5개(N 말단에서 C 말단까지 나열, 잔기 번호는 [1]괄호 안에 표시)이다.
- 활성화펩타이드(1~37)
- β-나트륨(38~184)
- 잔류물 C314, H373, D396 및 W279가 촉매 작용에 관여하는 촉매 도메인(185–515)
- β-1991 (516–628)
- β-1992(629–731)
B단위는 당단백질이다.각각의 질량은 약 80kDa(질량의 8.5%가 탄수화물), 잔기 641개, 초밥 도메인 10개이다.각 도메인은 약 60개의 잔류물과 2개의 내부 디술피드 [1]결합을 가지고 있다.
생리학
인간인자 XII의 서브유닛은 주로 혈소판 및 골수 유래의 다른 세포에 의해 만들어진다.B 서브유닛은 간세포에 의해 혈액으로 분비된다.A와 B 단위는 혈액 내에서 결합하여 2개의 A 단위와 2개의 B 단위의 헤테로트램을 형성합니다.헤테로테트라미터의 혈장 농도는 14~48mg/l이고 반감기는 9~[1]14일이다.
FX에 의해 안정화되지 않은 응고IIIa는 5 mol/L 요소에서 용해되며, 안정화된 응괴는 이러한 [2]현상에 내성이 있다.
인자 XIII 결핍증
인자 XIIIID(Factor XIIID) 결핍은 일반적으로 드물지만 발생하며, 이란은 473건으로 전 세계적으로 발병률이 가장 높다.시스탄과 발루치스탄 주에 위치한 카슈끄지는 이란에서 가장 높은 발생률을 보이며 혈연결혼 [3]비율이 높다.
진단 용도
인자 XIII는 일상적으로 측정되지 않지만 원인 불명의 출혈 경향을 가진 환자에게서 고려될 수 있다.이 효소는 단구 및 대식세포에 대해 상당히 특이적이기 때문에 인자 XIII의 존재여부를 판단하여 이들 [4]세포를 포함하는 악성질환을 식별하고 분류할 수 있다.
검출
제13인자 결핍은 1948년에 [2]처음 그 존재를 제안한 과학자들인 칼만 라키와 라즐로 로랜드의 이름을 따서 라키-로랜드 인자라고도 한다.2005년 회의에서 명명법의 [4]표준화가 권장되었습니다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b c d e f g h i j k l Muszbek L, Bereczky Z, Bagoly Z, Komáromi I, Katona É (July 2011). "Factor XIII: a coagulation factor with multiple plasmatic and cellular functions". Physiological Reviews. 91 (3): 931–72. doi:10.1152/physrev.00016.2010. PMID 21742792. S2CID 24703788.
- ^ a b Laki K, Lóránd L (September 1948). "On the Solubility of Fibrin Clots". Science. 108 (2802): 280. Bibcode:1948Sci...108..280L. doi:10.1126/science.108.2802.280. PMID 17842715.
- ^ Dorgalaleh A, Naderi M, Hosseini MS, Alizadeh S, Hosseini S, Tabibian S, et al. (2015). "Factor XIII Deficiency in Iran: A Comprehensive Review of the Literature. Seminars in thrombosis and hemostasis". 41 (3): 323–29.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ a b Muszbek L, Ariëns RA, Ichinose A (January 2007). "Factor XIII: recommended terms and abbreviations". Journal of Thrombosis and Haemostasis. 5 (1): 181–83. doi:10.1111/j.1538-7836.2006.02182.x. PMID 16938124. S2CID 20424049.