설핀산
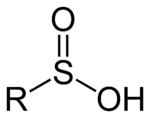
Sulfinic acid설핀산은 RSO(OH) 구조를 가진 황의 산화물이다. 이 유기황 화합물에서 유황은 피라미드형이다.[1]
구조 및 특성
설핀산 RSOH는2 해당 카르복실산 RCOH보다2 약 1000배 높은 산성이다. 유황은 피라미드형이고, 결과적으로 설핀산은 키랄이다.
준비
그들은 흔히 황산염에 대응하는 황산염의 산성화에 의해 현장에서 준비되는데, 일반적으로 황산염은 산성보다 튼튼하다. 이 염들은 황화염소화물의 감소에 의해 생성된다.[2] 다른 경로로는 그리너드 시약과 이산화황의 반응이다. 전이 금속 설핀은 또한 금속 알킬에 아황산가스를 삽입하여 생성되는데, 이 반응은 금속 아황산가스를 통해 진행될 수 있다. R이 수소원자일 때 미분해 설핀산은 둘 다 불안정한 황산염의 높은 에너지 이성질체다.
예
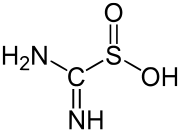
단순하고 잘 연구된 설핀산의 예는 페닐술핀산이다. 상업적으로 중요한 설핀산은 이산화 티우레아인데, 티우레아가 과산화수소로 산화되면서 만들어진다.[3]
- (NH2)2CS + 2HO22 → (NH2)CSOH2 + 2HO2
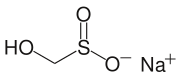
또 다른 상업적으로 중요한 설핀산은 히드록시메틸설핀산인데, 보통 나트륨염(HOCHSONa22)으로 고용된다. 롱갈라이트라고 불리는 이 음이온은 환원제로도 상업적으로 유용하다.
설피나테스
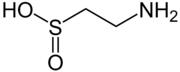
설핀산의 결합 베이스는 황산염 음이온이다. 시스테인 디옥시제나아제는 시스테인을 해당 황산염으로 변환시킨다. 이 카타볼릭 반응의 한 제품은 설핀산 하이포타우린이다. 설피나이트는 설피닌산의 에스테르를 묘사하기도 한다. 주기적인 설피나이트 에스테르는 술틴이라고 불린다.
참조
- ^ Saul Patai, ed. (1981). Sulphinic Acids, Esters and Derivatives. PATAI'S Chemistry of Functional Groups. John Wiley & Sons. doi:10.1002/9780470772270.
- ^ Whitmore, F. C.; Hamilton, F. H. (1922). "Sodium p-Toluenesulfinic Acid". 2: 89. doi:10.15227/orgsyn.002.0089.
{{cite journal}}: Cite 저널은 필요로 한다.journal=(도움말) - ^ D. Wiley-VCH, Weinheim Ulmann's 산업 화학 2012 백과사전의 슈바르트 "설핀산 및 파생상품" doi:10.1002/14356007.a25_461
외부 링크
- Sulfinic+Acids(미국 국립 의학 라이브러리 의료 과목 제목)
- 다이어그램(ucalgary.ca
- 다이어그램(acdlabs.com