치아 법랑질
Tooth enamel| 치아 법랑질 | |
|---|---|
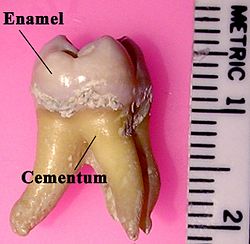 라벨링 어금니 | |
| 세부 사항 | |
| 식별자 | |
| 라틴어 | 법랑질 |
| MeSH | D003743 |
| TA98 | A05.1.03.056 |
| TA2 | 938 |
| FMA | 55629 |
| 해부학 용어 [위키데이터 편집] | |

치아 법랑질은 인간과 몇몇 물고기 종을 포함한 많은 동물들의 치아를 구성하는 4대 주요 조직 중 하나입니다. 크라운을 덮고 있는 치아의 정상적으로 보이는 부분을 구성합니다. 다른 주요 조직은 상아질, 시멘트 및 치수입니다. 치아를 보호하는 장벽 역할을 하지만 특히 음식과 음료의 산에 의해 분해되기 쉬운 매우 단단하고 백색에서 백색에 가까운 고도로 광물화된 물질입니다. 드문 경우 에나멜이 형성되지 않아 표면에 기본적인 상아질이 노출됩니다.[1]
특징들
에나멜은 인체에서 가장 단단한 물질로 가장 높은 비율의 미네랄을 함유하고 있으며(96%),[2] 물과 유기물이 나머지를 구성하고 있습니다.[3] 주요 광물은 결정질 인산칼슘인 수산화인회석입니다.[4] 치아가 입으로 분출되기 전에 턱뼈 안에서 발달하는 동안 에나멜이 치아에 형성됩니다. 에나멜은 완전히 형성되면 혈관이나 신경을 포함하지 않으며 세포로 만들어지지 않습니다. 치아의 광물화는 치아의 손상을 어느 정도 수리할 수 있지만, 그 이상의 손상은 신체가 수리할 수 없습니다. 사람의 치아 에나멜을 유지하고 수리하는 것은 치과의 주요 관심사 중 하나입니다.
사람의 경우, 에나멜은 치아 표면의 두께가 다양하며, 종종 최대 2.5 mm까지 커스프에서 가장 두껍고, 시멘트오엔멜 접합부(CEJ)에서 시멘트움과의 경계에서 가장 얇습니다.[5]
법랑질의 일반적인 색상은 밝은 노란색부터 회색(청색) 흰색까지 다양합니다. 상아질의 노란색이 보이는 얇고 반투명한 에나멜을 가진 노란 치아와 불투명한 에나멜을 가진 회색 치아의 투명도 차이에 의해 색상이 결정된다고 제안되었습니다. 반투명도는 석회화 정도의 변화와 법랑질의 균질성에 기인할 수 있습니다. 에나멜 밑에 움푹 들어간 부분이 없는 치아 가장자리에서, 이 색은 때때로 약간 파란색이거나 반투명한 오프 화이트 톤을 가지고 있으며, 이는 상부 앞니에서 쉽게 관찰할 수 있습니다. 법랑질은 반투명하기 때문에 상아질의 색과 법랑질 아래에 있는 모든 물질은 치아의 외관에 강한 영향을 미칩니다. 1차 치아의 법랑질은 결정형이 불투명하기 때문에 영구치보다 희게 보입니다.
에나멜에 다량의 미네랄이 함유되어 있는 것은 그 강도뿐만 아니라 취성도 설명해 줍니다.[6] 치아 에나멜은 모오스 경도 척도(강철과 티타늄 사이)에서 5위를 차지하며 영률은 83 GPa입니다.[4] 덴틴은 광물화가 덜 되고 덜 부서지기 쉬우며 경도가 3-4로 에나멜을 보충하며 지지체로 필요합니다.[7] 방사선 사진에서 치아와 주변 치주의 다양한 부분의 광물화 차이를 확인할 수 있습니다. 에나멜은 밀도가 높고 방사선 불투과성이 높기 때문에 상아질이나 펄프보다 더 가벼워 보입니다.[8]
에나멜은 상아질이나 뼈와 같은 다른 단단한 조직에서 발견되는 콜라겐을 포함하지 않지만, 아멜로제닌과 에나멜린의 두 가지 독특한 종류의 단백질을 포함하고 있습니다. 이 단백질들의 역할은 완전히 이해되지는 않았지만, 다른 기능들 중에서도 광물들이 형성될 수 있는 틀의 역할을 함으로써 에나멜의 발달을 돕는 것으로 여겨집니다.[6] 일단 성숙되면, 에나멜은 더 부드러운 유기물이 거의 없습니다. 에나멜은 혈관이 없고 그 안에 신경 공급이 없고 재생되지 않지만 광물화 변화를 겪을 수 있기 때문에 정적인 조직이 아닙니다.[9]
구조.

법랑질의 기본 단위는 법랑질 막대라고 불립니다.[7] 직경 4~8μm의 에나멜 막대, 공식적으로 에나멜 프리즘이라고 불리는 에나멜 막대는 조직화된 패턴으로 빽빽하게 채워진 수산화인회석 결정체 덩어리입니다.[2] 단면적으로, 그것은 열쇠 구멍과 비교할 때 가장 좋으며, 꼭대기 또는 머리는 치아의 왕관을 향하고, 바닥 또는 꼬리는 치아의 뿌리를 향합니다.
각 에나멜 막대 내의 결정체 배열은 매우 복잡합니다. 아멜로아세포(에나멜 형성을 시작하는 세포)와 톰스의 과정 모두 결정체의 패턴에 영향을 미칩니다. 에나멜 로드의 헤드에 있는 에나멜 결정체는 로드의 장축과 평행하게 배향되어 있습니다.[2][5] 에나멜 막대의 꼬리에서 발견되면 결정체의 방향이 장축에서 약간(65도) 차이가 납니다.[2]
법랑질 막대의 배열은 내부 구조보다 더 명확하게 이해됩니다. 법랑질 막대는 치아를 따라 일렬로 발견되며, 각 열 내에서 법랑질 막대의 장축은 일반적으로 아래 상아질에 수직입니다.[10] 영구치에서는 시멘토엔멜 접합부(CEJ) 근처의 에나멜 막대가 치아의 뿌리 쪽으로 약간 기울어져 있습니다. 에나멜 방향을 이해하는 것은 복원 치과에서 매우 중요한데, 그 이유는 기본적인 상아질에 의해 지지되지 않는 에나멜은 골절되기 쉽기 때문입니다.[10]

에나멜 막대 주변은 인터로드 에나멜로 알려져 있습니다. 인터로드 에나멜은 에나멜 로드와 동일한 구성을 갖지만 각각의 결정체 방향이 다르기 때문에 둘 사이에 역사학적인 차이가 있습니다.[5] 에나멜 로드의 결정체와 인터로드 에나멜의 결정체가 만나는 경계를 로드 시스라고 합니다.[10]
레치우스의 Striae는 성숙한 에나멜의 얼룩진 부분에 갈색으로 보이는 점증선입니다. 이 선들은 에나멜 막대의 띠 또는 교차 줄무늬로 구성되어 있으며, 이 선들은 세로 섹션에서 결합될 때 에나멜 막대를 가로지르는 것처럼 보입니다.[10] Tomes의 과정의 직경 변화로부터 형성된 이 증가된 선들은 에나멜의 횡단면에 있는 나무의 연간 고리와 유사한 에나멜의 성장을 보여줍니다. 이러한 라인을 생성하는 정확한 메커니즘은 여전히 논의되고 있습니다. 일부 연구자들은 이 선들이 에나멜 기질을 생성하는 아멜라아세포의 일주성(일주성), 즉 24시간 대사 리듬의 결과이며, 이는 활발한 분비 작업 기간과 치아 발달 동안의 비활성 휴식 기간으로 구성된다고 가정합니다. 따라서 에나멜 로드의 각 밴드는 일반적으로 일주일 동안 발생하는 아멜라세포의 작업/휴식 패턴을 보여줍니다.[11]
Striae와 관련된 페리키마타는 구강 내 일부 치아의 비 저작 표면에 임상적으로 관찰되는 얕은 홈입니다.[6] 근막은 일반적으로 일부 치아의 보호된 경추 부위, 특히 영구 상악 중심절개, 송곳니, 제1전몰을 제외하고는 치아 마모를 통해 손실되며 치석으로 혼동될 수 있습니다.[11] 다른 점증선보다 어두운 신생아선은 출생 전과 후에 형성된 에나멜을 분리하는 점증선입니다.[12] 신생아 라인은 출생 시 아멜라세포가 경험하는 스트레스나 트라우마를 표시하며, 에나멜 기질을 형성하는 동안 아멜라세포의 민감성을 다시 한번 보여줍니다. 예상대로 신생아 선은 모든 일차 치아와 영구적인 첫 어금니의 더 큰 치근에서 발견됩니다. 그것들은 에나멜 프리즘의 불규칙한 구조를 포함하고 있으며, 기본적으로 프리즘이 뿌리 쪽으로 갑자기 휘어짐으로써 형성된 무질서한 결정체 배열을 가지고 있습니다. 일반적으로 프리즘은 이전 방향을 되찾기 위해 점차 다시 뒤로 구부러집니다.[11]
구불구불한 법랑질은 치아 끝에서 발견됩니다.[3] 그것의 뒤틀린 모양은 에나멜 막대의 방향과 그들이 누워있는 줄에서 비롯됩니다.
발전

에나멜 형성은 치아 발달의 전반적인 과정의 일부입니다. 현미경으로 관찰하면 발달 중인 치아의 조직 내에서 다양한 세포 응집체를 확인할 수 있으며, 여기에는 에나멜 기관, 치아 라미나 및 치아 유두로 알려진 구조가 포함됩니다.[13] 일반적으로 인식되는 치아 발달 단계는 발아 단계, 캡 단계, 종 단계, 크라운 단계 또는 석회화 단계입니다. 에나멜 형성은 크라운 단계에서 처음 보입니다.}
아멜로제닉(amelogenesis) 또는 에나멜 형성은 아멜로블라스트(ameloblast)로 알려진 세포를 통해 상아질이 처음 형성된 후에 발생합니다. 인간의 법랑질은 임신 3개월 또는 4개월경에 미래의 자궁경부 위치에서 시작하여 하루에 약 4μm의 속도로 형성됩니다.[10] 인간의 모든 과정과 마찬가지로 에나멜의 생성은 복잡하지만 일반적으로 두 단계로 나눌 수 있습니다.[3] 분비 단계라고 불리는 첫 번째 단계는 단백질과 부분적으로 광물화된 에나멜을 형성하는 유기 기질이 포함됩니다. 성숙 단계라고 불리는 2단계는 에나멜 광물화를 완료합니다.
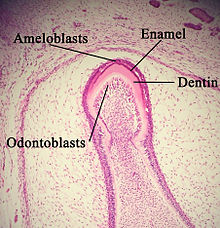
분비 단계에서 아멜라세포는 극성화된 주상 세포입니다. 이 세포의 거친 소포체에서 에나멜 단백질은 주변으로 방출되어 에나멜 기질이라고 알려진 것에 기여하고, 그 다음에 알칼리성 포스파타제 효소에 의해 부분적으로 광물화됩니다.[14] 이 첫 번째 층이 형성되면 아멜로아세포가 상아질에서 멀어져서 세포의 정점 극에서 탐스 과정이 발달할 수 있습니다. 에나멜 형성은 인접한 에나멜 세포 주위에서 계속되어 톰의 과정이 있는 벽으로 둘러싸인 영역, 즉 피트가 생성되고 또한 각각의 톰의 과정이 끝날 때쯤에 각 피트 내부에 에나멜 매트릭스가 침착됩니다.[3] 구덩이 안의 매트릭스는 결국 에나멜 막대가 될 것이고, 벽은 결국 막대 간 에나멜이 될 것입니다. 이 둘을 구별하는 유일한 요소는 인산칼슘 결정체의 방향입니다.
성숙 단계에서 아멜라세포는 에나멜 형성에 사용되는 물질을 운반합니다. 조직학적으로 이 단계의 가장 주목할 만한 측면은 이 세포들이 줄무늬가 되거나 주름진 경계를 가지고 있다는 것입니다.[14] 이러한 징후들은 아멜로아세포가 분비 단계에서와 같이 생산에서 수송으로 기능이 변화했음을 보여줍니다. 최종 광물화 과정에 사용되는 단백질은 운반되는 물질의 대부분을 구성합니다. 관련된 주목할 만한 단백질은 아멜로게닌, 아멜로플라스틴, 에나멜린 및 터프텔린입니다. 이 단백질들이 어떻게 에나멜 구조로 분비되는지는 아직 밝혀지지 않았으며, 이 과정에 Wnt 신호전달 성분인 BCL9와 피고푸스와 같은 다른 단백질들이 관련되어 있습니다.[15] 이 과정에서 사용 후 아멜로게닌과 아멜로플라스틴이 제거되어 에나멜린과 터프텔린이 에나멜에 남게 됩니다.[16] 이 단계가 끝날 때까지 에나멜은 광물화를 완료했습니다.
치아가 입으로 분출되기 전의 어느 시점에서는 성숙 단계가 지나면 아멜라세포가 분해됩니다. 결과적으로, 에나멜은 신체의 다른 많은 조직들과 달리 스스로 재생할 방법이 없습니다.[17] 부패나 부상으로 인해 에나멜이 파괴된 후에는 신체나 치과 의사가 에나멜 조직을 복구할 수 없습니다. 에나멜은 비병리적 과정에 의해 더 영향을 받을 수 있습니다.
에나멜은 치아의 발달과 관련하여 다양한 구조로 덮여 있습니다.
| 출생시 형성되는 법랑질의 양 | 에나멜 광물화 완료 | ||
|---|---|---|---|
| 기본적인 상악의 이 | 중심절치 | 5/6 | 출생 후 1.5개월 |
| 횡절치 | 2/3 | 생후 2.5개월 | |
| 개의 | 1/3 | 생후 9개월 | |
| 어금니 1번 | 교합; 교합이 완전히 석회화됨 1/2 ~ 3/4 크라운 높이 | 생후 6개월 | |
| 두 번째 어금니 | 커스프 결합; 교합이 불완전하게 석회화됨; 석회화 티슈 커버 1/5 ~ 1 ⁄4 크라운 높이 | 생후 11개월 | |
| 기본적인 하악의 이 | 중심절치 | 3/5 | 생후 2.5개월 |
| 횡절치 | 3/5 | 출생후 3개월 | |
| 개의 | 1/3 | 생후 9개월 | |
| 어금니 1번 | 교합; 교합 완전히 석회화된 | 출생 후 5.5개월 | |
| 두 번째 어금니 | 교합; 교합 불완전하게 석회화된 | 출생후 10개월 | |
법랑질 손실
이 조직을 인체에서 가장 단단하게 만드는 에나멜의 높은 미네랄 함량은 또한 충치로 알려진 치아 우식증으로 종종 발생하는 과정에서 탈광물화를 만듭니다.[13] 탈염은 여러 가지 이유로 일어나지만 충치의 가장 중요한 원인은 발효성 탄수화물의 섭취입니다.[citation needed] 충치는 산이 치아 에나멜을 녹일 때 발생합니다.[22] 치아 마모와 에나멜 골절을 통해 에나멜도 손실됩니다.[23]
- Ca10(PO4)6(OH)2(s) + 8H+(aq) → 10Ca2+(aq) + 6HPO42−(aq) + 2H2O(l)
사탕, 청량음료, 과일 주스의 설탕과 산은 충치와 결과적으로 에나멜 파괴에 중요한 역할을 합니다.[24] 입 안에는 수많은 세균과 다양한 종류의 세균이 들어 있는데, 가장 흔한 당류인 수크로스가 입 표면을 코팅하면 일부 구강 내 세균이 이와 상호작용하여 젖산을 형성하게 되어 입 안의 pH가 떨어집니다.[25] 일반적으로 치아 법랑질의 임계 pH는 pH 5.5로 인정됩니다. 산이 존재하고 임계 pH에 도달하면 법랑질의 수산화인회석 결정체가 탈염화되어 더 큰 박테리아가 치아 깊숙이 침투할 수 있습니다. 충치와 관련된 가장 중요한 세균은 스트렙토코커스 뮤탄스이지만 치아 파괴의 진행에 따라 세균의 수와 종류가 달라집니다.[25]
또한 치아 형태학은 치아 우식이 시작되는 가장 일반적인 장소가 에나멜의 깊은 홈, 구덩이 및 균열에 있음을 나타냅니다.[citation needed] 이러한 위치는 칫솔로는 도달할 수 없고 박테리아가 거주할 수 있기 때문에 예상됩니다. 에나멜의 탈회가 일어나면 치과 의사는 치과 탐험가와 같은 날카로운 기구를 사용할 수 있고, 충치가 생긴 위치에 '막대를 느낀다'고 합니다. 에나멜이 계속해서 덜 광물화되고 박테리아의 잠식을 막을 수 없게 되면서, 기본적인 상아질도 영향을 받게 됩니다. 평소 에나멜을 지지하는 상아질이 생리적인 상태나 부패로 파괴되면, 에나멜은 그 취성을 보완하지 못하고 치아에서 쉽게 이탈하게 됩니다.

우식성으로 알려진 충치의 가능성이 있는 정도는 당이 입 안에 얼마나 오래 남아 있는지와 같은 요인에 달려 있습니다. 일반적인 생각과 달리 충치의 원인이 되는 가장 중요한 요인은 섭취한 설탕의 양이 아니라 섭취한 설탕의 빈도입니다.[26] 처음에 당류 섭취로 인해 입안의 pH가 낮아지면 에나멜이 탈염되어 약 30분 동안 취약하게 방치됩니다. 한 자리에 더 많은 양의 설탕을 섭취한다고 해서 탈염 시간이 늘어나는 것은 아닙니다. 마찬가지로, 한 자리에 적은 양의 설탕을 섭취한다고 해서 탈염 시간이 줄어들지는 않습니다. 따라서 하루에 한 번에 많은 양의 설탕을 섭취하는 것은 하루 동안 여러 간격으로 섭취하는 매우 적은 양보다 덜 해롭습니다. 예를 들어 구강 건강에 있어서는 하루 종일 사탕 한 봉지를 먹고 간식을 먹는 것보다 저녁 시간에 디저트 한 개를 먹는 것이 더 좋습니다.
에나멜은 박테리아 침입 외에도 다른 파괴력에도 취약합니다. 이를 악물거나 갈기도 하는 브루시스는 에나멜을 매우 빨리 파괴합니다. 마모라고 불리는 에나멜의 마모율은 정상적인 요인으로부터 1년에 8마이크로미터입니다.[citation needed] 일반적인 오해는 에나멜이 대부분 씹는 동안 닳아 없어지지만 실제로 씹는 동안 치아가 거의 닿지 않는다는 것입니다. 또한, 정상적인 치아 접촉은 생리학적으로 치주 인대(pdl)와 치과 교합의 배열에 의해 보상됩니다. 진정으로 파괴적인 힘은 브룩시스에서 발견되는 부기능적인 움직임으로, 에나멜에 비가역적인 손상을 일으킬 수 있습니다.
에나멜 파괴의 다른 비세균적 과정에는 마모(칫솔과 같은 이물질 포함), 침식(소프트 드링크나[27] 레몬 및 기타 주스에 의해 용해되는 것과 같은 화학적 과정 포함), 그리고 아마도 마찰(압축력 및 인장력 포함)이 포함됩니다.[citation needed]
에나멜은 질긴 것으로 묘사되지만 유리와 유사한 취성을 가지고 있어 쉘이나 진주층 같은 다른 천연 균열에 강한 적층 구조와 달리 파괴에 취약합니다. 그럼에도 불구하고 씹는 동안 하루에 1,000N만큼 높은 물린 힘을 견딜 수 있습니다.[28][29] 이러한 저항성은 부분적으로 덴티노에나멜 접합부의 그러한 골절을 안정화시키는 에나멜 터프를 포함하는 에나멜의 미세 구조에 기인합니다.[30] 치아의 구성은 또한 깨물 때 골절을 일으키는 인장 스트레스를 줄이는 역할을 합니다.[30]
위식도 역류질환은 식도와 입으로 산이 역류해 밤잠을 자는 동안 가장 많이 발생하기 때문에 에나멜 소실로도 이어질 수 있습니다.
구강위생
에나멜은 탈염에 취약하기 때문에 충치를 예방하는 것이 치아의 건강을 유지하는 가장 좋은 방법입니다. 대부분의 국가에서는 칫솔을 광범위하게 사용하여 치아 생물막과 에나멜에 있는 식품 입자의 수를 줄일 수 있습니다. 칫솔을 사용할 수 없는 고립된 사회에서, 그런 사람들은 치아를 닦기 위해 막대기와 같은 다른 물체를 사용하는 것이 일반적입니다. 인접한 두 치아 사이에서는 치실을 사용하여 치태와 음식물 입자가 없는 법랑질 표면을 닦아 박테리아 성장을 억제합니다. 치실이나 칫솔 모두 에나멜의 깊은 홈과 구덩이를 관통할 수는 없지만, 좋은 일반 구강 건강 습관은 보통 충치가 시작되는 것을 막기에 충분한 박테리아 성장을 막을 수 있습니다. 에나멜의 구조적 완전성은 유전적이며, 탈염이나 박테리아로부터의 공격에 대한 경향도 마찬가지입니다.[15]
불화물 재광화
불소는 치아 표면으로 칼슘과 인산염이 확산되는 것을 촉매하고, 이는 치아 공동의 결정 구조를 재광화합니다. 재광화된 치아 표면에는 불소화된 수산화인회석과 플루오로인회석이 함유되어 있어 원래 치아보다 산 공격에 훨씬 더 잘 저항합니다.[31] 불소 요법을 사용하여 충치 예방에 도움을 줍니다.

불소 이온은 항균제로서 불소 리보스위치와 관련된 박테리아 유전자를 활성화시킬 수 있습니다.[32][unreliable medical source?] 불소 이온과 QAS(4차 암모늄염)의 조합은 S. mutans를 포함한 충치와 관련된 많은 구강 박테리아에 더 강한 항균 효과를 주는 것으로 밝혀졌습니다.
먹는물중의불화물
대부분의 치과 전문가들과 단체들은 공공수에 불소가 포함된 것이 충치의 유병률을 감소시키는 가장 효과적인 방법 중 하나였다는데 동의합니다.[33] 불소는 바다와 다른 수원과 같은 많은 장소에서 자연적으로 발견될 수 있습니다. 음용수의 불소 권장 복용량은 공기 온도에 의존하지 않습니다.[34][35]
일부 단체들은 불소의 신경 독성이나 불소가 불소증으로 할 수 있는 손상과 같은 이유로 불소화된 식수에 반대하는 목소리를 냈습니다. 불소증은 특히 6개월에서 5년 사이에 불소에 과다 노출되어 발생하는 질환으로 얼룩덜룩한 법랑질로 나타납니다.[3] 결과적으로 치아의 충치 발생률은 매우 적지만 치아가 보기 흉하게 보입니다. 불소가 고농도로 자연적으로 발견되는 곳에서는 필터를 사용하여 물 속의 불소의 양을 줄이는 경우가 많습니다. 이 때문에 치과 전문가들이 사람이 먹어야 하는 불소의 양을 제한하는 코드를 개발했습니다.[36] 이러한 코드는 미국 치과 협회와 미국 소아 치과 학회의 지원을 받고 있습니다.
또한 치약이나 구강청결제 등에서 발견되는 국소불소는 불소증을 유발하지 않지만, 현재는 불소화물을 마실 때와 같이 전신불소증보다 그 효과가 중요하게 여겨지고 있습니다.[37] 그러나 전신 불소는 불소화 물을 마실 때도 타액의 불소 농도가 증가할 때 국소적으로 작용합니다. 최근 치과 전문가들은 불소(예: 바니시) 또는 아몰퍼스 인산칼슘과 같은 다른 광물화 제품을 전문가가 하거나 자가 투여하는 국소 시술의 형태로 지역 사회에 제공할 다른 방법을 찾고 있습니다. 나중에 복원하는 대신 초기 병변을 광물화하는 것이 대부분의 치과 전문가들의 주요 목표입니다.
치과진료

치과복원
대부분의 치아 복원에는 에나멜 제거가 포함됩니다. 종종 제거의 목적은 상아질의 근본적인 부패 또는 펄프의 염증에 접근하는 것입니다. 일반적으로 아말감 복원 및 내이도 치료의 경우에 해당됩니다.
그럼에도 불구하고 에나멜은 부패가 일어나기 전에 제거될 수 있습니다. 가장 인기 있는 예는 치과용 실란트입니다. 과거에는 치아 봉합제를 넣는 과정에서 치아 깊은 틈과 홈에서 법랑질을 제거한 뒤 복원재로 교체하는 과정이 있었습니다.[38] 현재는 부패한 법랑질이 있는 경우에만 제거하는 것이 더 일반적입니다. 그럼에도 불구하고 부식을 방지하기 위해 법랑질의 깊은 틈과 홈을 제거하는 경우와 상황에 따라 실란트를 놓을 수도 있고 그렇지 않을 수도 있습니다. 밀봉제는 미래의 부패로부터 보호하기 위한 예방적 복원물이라는 점에서 독특하며, 7년 동안 부패 위험을 55% 감소시키는 것으로 나타났습니다.[39]
에나멜을 제거하는 또 다른 이유는 미학입니다. 치아의 외관을 향상시키기 위해 크라운과 베니어를 배치할 때는 법랑질 제거가 필요합니다. 이 두 경우 모두 기본적인 상아질에 의해 지지되지 않는 경우 에나멜의 해당 부분이 골절되기 쉽습니다.[40]
산에칭기법
1955년에 발명된 산성 에칭은 치과용 에칭제를 사용하며 치아 복원을 치아에 접합할 때 자주 사용됩니다.[41] 이것은 복합재 및 밀봉제와 같은 일부 재료를 장기간 사용하는 데 중요합니다.[13] 에천트는 광물질을 에나멜에 녹임으로써 에나멜 표면의 외부 10 마이크로미터를 제거하고 다공성 층을 5-50 마이크로미터 깊이로 만듭니다.[42] 이것은 에나멜을 현미경으로 거칠게 하고 결합할 표면적이 넓어집니다.
에나멜에 대한 산 식각의 영향은 다양할 수 있습니다. 중요한 변수는 식각액 도포 시간, 사용된 식각액의 종류, 법랑질의 현재 상태입니다.[42]
산에칭으로 형성되는 패턴은 세 가지 유형이 있습니다.[42] 1형은 주로 에나멜 봉이 용해된 패턴이고, 2형은 주로 에나멜 봉 주변이 용해된 패턴이고, 3형은 에나멜 봉이 전혀 남아있지 않은 패턴입니다. 유형 1이 가장 유리한 패턴이고 유형 3이 가장 덜 유리한 패턴이라는 결론을 내리는 것 외에도, 이러한 다양한 패턴에 대한 설명은 확실하게 알려지지 않았지만 가장 일반적으로 에나멜의 결정체 방향이 다르기 때문입니다.[3]
치아미백
시간이 지남에 따라 치아가 변색되는 것은 담배, 커피, 차와 같은 물질에 노출됨으로써 발생할 수 있습니다.[43] 염색은 내부적으로 에나멜에 있는 마찰간 영역에서 발생하는데, 이로 인해 치아가 전체적으로 더 어둡게 또는 더 노랗게 보입니다. 완벽한 상태에서 에나멜은 무색이지만 치아의 빛 반사 특성이 낮기 때문에 치아의 얼룩이 있는 근본적인 치아 구조를 반영합니다.
치아 미백 또는 치아 표백 시술은 화학적 또는 기계적 작용의 두 가지 방법 중 하나로 치아의 색을 밝게 하려고 시도합니다. 화학적으로 작용하는 표백제는 에나멜과 상아질에서 산화 반응을 수행하는 데 사용됩니다.[44] 치아의 색을 본질적으로 변화시키기 위해 가장 일반적으로 사용되는 약제는 과산화수소와 과산화카바미드입니다. 미백제의 과산화물에서 산소 라디칼이 에나멜 층 내의 마찰 공간에 있는 얼룩과 접촉합니다. 이런 일이 발생하면 얼룩이 탈색되고 치아의 색이 더 옅어집니다. 치아는 더 하얗게 보일 뿐만 아니라 빛을 더 많이 반사시켜 치아를 더 밝게 보이게 합니다. 연구에 따르면 미백은 치아 조직에 미세 구조적 또는 미세 경도 변화를 일으키지 않습니다.[8]
치아가 하얗게 된 환자들이 더 잘 관리한다는 연구 결과가 나왔습니다.[45] 하지만 전반적으로 낮은 pH를 가진 치아 미백 제품은 탈염에 의해 에나멜이 부패하거나 파괴될 위험에 처할 수 있습니다. 따라서 매우 산성인 제품을 선택할 때 주의하고 위험을 평가해야 합니다.[46] 치약의 치아 미백제는 기계적 작용을 통해 작동합니다. 에나멜의 얼룩을 제거하는 데 도움이 되는 가벼운 연마제가 있습니다. 이것이 효과적인 방법이 될 수 있지만 치아의 고유 색상을 변경하지는 않습니다. 미세 마모 기술은 두 가지 방법을 모두 사용합니다. 에나멜의 외부 22~27 마이크로미터를 약화시키기 위해 산을 먼저 사용하여 후속 연마력을 충분히 약화시킵니다.[47] 이를 통해 에나멜의 표면 얼룩을 제거할 수 있습니다. 만약 변색이 더 깊거나 상아질에 있다면, 이 치아 미백 방법은 성공하지 못할 것입니다.
관련병리학
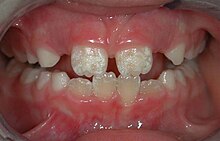
14가지 유형의 아멜 생성 불완전성이 있습니다.[3] 가장 흔한 저칼슘화형은 에나멜이 완전히 광물화되지 않은 상염색체 우성 상태입니다.[51] 결과적으로, 에나멜은 치아에서 쉽게 벗겨지는데, 이는 상아질이 드러나기 때문에 노란색으로 보입니다. 저플라스틱 타입은 X연쇄형으로 너무 적은 양으로 나타나는 정상적인 에나멜로 가장 일반적인 타입과 같은 효과를 냅니다.[51]
태아 적혈구증으로 발생할 수 있는 만성 빌리루빈 뇌증은 신생아에게 많은 영향을 미치는 질환이지만, 에나멜 저형성증과 에나멜의 녹색 염색을 유발할 수도 있습니다.[52]
에나멜 저형성증은 다양한 정도의 부재에서 정상적인 에나멜로부터의 모든 편차를 포괄하도록 광범위하게 정의됩니다.[53] 사라진 에나멜이 국소화되어 작은 구덩이를 형성하거나 완전히 없을 수 있습니다.
적혈구 생성 포르피린은 전신에 포르피린이 침착되는 유전적 질병입니다. 이 침전물은 또한 에나멜에서 발생하며 색상과 형광으로 빨간색으로 묘사되는 외관을 남깁니다.[54]
불소증은 얼룩덜룩한 법랑질로 이어지고, 불소에 과도하게 노출되면서 발생합니다.[25]
테트라사이클린 염색으로 에나멜이 발달하는 부위에 갈색 띠가 생깁니다. 8세까지의 어린이는 테트라사이클린을 복용하여 얼룩덜룩한 에나멜이 생길 수 있습니다. 그 결과 임산부에서는 테트라사이클린을 금하고 있습니다.
글루텐에 대한 자가면역반응을 특징으로 하는 질환인 셀리악병 또한 흔히 에나멜의 탈염을 초래합니다.[48][50]
다른 포유류
대부분, 연구는 동물의 치아 에나멜 형성이 인간의 형성과 거의 동일하다는 것을 보여주었습니다. 치아 유두를 포함한 법랑질 기관과 아멜라아세포는 유사한 기능을 합니다.[55] 존재하는 에나멜의 변형은 드물지만 때로는 중요합니다. 확실히 동물들 사이에 치아의 형태, 수, 종류에 차이가 있습니다.

개의 타액의 높은 pH로 인해 개는 사람보다 치아가 썩을 가능성이 적으며, 이는 산성 환경이 형성되는 것을 막고 그에 따른 에나멜의 탈염을 발생시킵니다.[56] 만약 충치가 발생한다면 (보통 외상으로 인해), 개들은 사람들이 하는 것처럼 치아 충전재를 받을 수 있습니다. 사람의 치아와 마찬가지로 개의 법랑질도 테트라사이클린 염색에 취약합니다. 따라서 어린 개에게 테트라사이클린 항생제를 투여할 때 이러한 위험을 고려해야 합니다.[56] 에나멜 저형성증은 개에게도 발생할 수 있습니다.[57]
설치류 에나멜의 미네랄 분포는 원숭이, 개, 돼지, 인간과 다릅니다.[58] 말의 치아는 에나멜층과 상아질층이 서로 얽혀 있어 치아의 강도와 내마모성이 높아집니다.[59]
기타생물
에나멜 또는 에나멜로이드는 상어와 많은 초기 척추동물의 진피 치아에서 발견되며,[60] 그것은 치골이 진화하기 전에 나타났습니다.[61] 많은 방선균들의 비늘을 덮고 있는 가노인은 아마도 에나멜에서 유래했을 것입니다.[62] 에나멜과 같은 물질은 일부 갑각류의 턱에도 코팅되지만, 이것은 척추동물의 에나멜과 상동성이 아닙니다.[63][64] 에나멜로이드는 일부 물고기 비늘을 덮습니다.
기계적 성질
에나멜의 독특한 구조로 인해 기계적 특성이 매우 흥미롭습니다. 에나멜은 신체에서 가장 단단한 물질이며 가장 내구성이 강한 하중을 받는 생물학적 물질 중 하나입니다. 에나멜의 주광물인 지질 수산화인회석보다 3배나 큰 파괴인성을 가지는 것으로 나타났습니다.[65]
에나멜의 미세구조 내에서 막대 영역과 막대 사이 영역으로 구성된 에나멜의 기계적 특성은 미세구조 내 위치에 따라 다릅니다.[66] 로드와 인터로드 구조는 두 구성 요소가 기계적 특성이 다르기 때문에 에나멜에 이방성을 유발합니다. 인터로드 에나멜은 로드 구조에 비해 경도 및 탄성 계수가 약 53% 및 74% 감소합니다. 이것은 에나멜의 계층 구조와 같은 복합물로 이어집니다.[67] 로드 축과 평행한 경도와 강성은 높은 경도와 모듈러스를 나타내는데, 모듈러스 값은 85-90 GPa이고 경도 값은 3.4-3.9 GPa입니다.[66] 로드 방향과 수직한 방향의 경도와 모듈러스는 낮은 값으로 탄성 모듈러스는 70~77 GPa이고 경도는 3.0~3.5 GPa인 것으로 나타남.[66] 두 방향 사이의 이방성은 30%[66]까지 높아질 수 있습니다. 이것은 부분적으로 재료의 구조와 c-방향의 막대의 방향성에 기인합니다.[66] 에나멜의 구조는 또한 자연적으로 인터로드와 로드 사이에 복합적으로 존재하며, 이는 또한 이방성으로 이어집니다. 미네랄 에나멜이 기반이 되는 단결정질 하이드록시아파타이트도 이방성입니다. 단결정질 수산화인회석은 경도와 영률이 더 높은데, 이는 유기물질의 존재뿐만 아니라 치환이온과 같은 에나멜에 존재하는 결함 때문일 수 있습니다.[66]
에나멜의 기계적 특성은 막대와 중간체의 구조로 인해 이방성을 가질 뿐만 아니라요. 그것들은 또한 치아 표면의 에나멜부터 외부 에나멜, 상아질과 에나멜 사이의 접합부인 DEJ까지 에나멜의 길이에 걸쳐 다양합니다. 탄성 계수는 에나멜 내에서 덴틴-에나멜 접합부(DEJ) 사이의 거리가 증가함에 따라 증가합니다.[68] 파단 인성도 이방성입니다. 파단인성은 막대의 방향성으로 인해 최대 3배까지 변화할 수 있습니다. 또한 법랑질에서도 균열이 상아질에 쉽게 침투하지 않아 파단인성이 높아질 수 있습니다.[69] 전체적으로 에나멜은 미세한 구조로 인해 매우 이방성이 강한 물질이며, 이는 우리 치아의 효과적인 사용에 필요한 특성으로 이어집니다.
참고 항목
참고문헌
- ^ "Severe Plane-Form Enamel Hypoplasia in a Dentition from Roman Britain". ResearchGate. Retrieved 9 January 2019.
- ^ a b c d Ross et al., p. 485
- ^ a b c d e f g Ten Cate's Oral Histology, Nancy, Elsevier, pp. 70–94
- ^ a b M. Staines, W. H. Robinson and J. A. A. Hood (1981). "Spherical indentation of tooth enamel". Journal of Materials Science. 16 (9): 2551–2556. Bibcode:1981JMatS..16.2551S. doi:10.1007/bf01113595. S2CID 137704231.
- ^ a b c Ten Cate's Oral Histology, Nanci, Elsevier, 2013, 페이지 122
- ^ a b c Ten Cate's Oral Histology, Nanci, Elsevier, pp. 70–94
- ^ a b 존슨
- ^ a b 치과 배아학, 조직학 및 해부학, Bath-Balogh Fehrenbach, Elsevier, 2011, p. 180
- ^ Bath-Balogh, Ferhrenbach, 179쪽
- ^ a b c d e Ten Cate's Oral Histology, Nanci, Elsevier, 2013, pp. 122–128
- ^ a b c 배스발로그, 페렌바흐, 186쪽
- ^ Ten Cate's Oral Histology, Nanci, Elsevier, 2013, p. 156
- ^ a b c Ross et al., p. 443
- ^ a b Ross et al., p. 445
- ^ a b Cantù, Claudio; Pagella, Pierfrancesco; Shajiei, Tania D.; Zimmerli, Dario; Valenta, Tomas; Hausmann, George; Basler, Konrad; Mitsiadis, Thimios A. (7 February 2017). "A cytoplasmic role of Wnt/β-catenin transcriptional cofactors Bcl9, Bcl9l, and Pygopus in tooth enamel formation". Sci. Signal. 10 (465): eaah4598. doi:10.1126/scisignal.aah4598. ISSN 1945-0877. PMID 28174279. S2CID 6845295.
- ^ Ross et al., p. 491
- ^ Ross et al., p. 3
- ^ Armstrong W.G.; Pääkkö, P; Kerttula, R; Taikina-Aho, O; Tuuponen, T; Hassi, J (1968). "Origin and nature of the acquired pellicle". Proceedings of the Royal Society of Medicine. 61 (9): 923–930. doi:10.1177/003591576806100929. PMC 1902619. PMID 5679017.
- ^ Darling A.I.; Pääkkö, P; Kerttula, R; Taikina-Aho, O; Tuuponen, T; Hassi, J (1943). "The Distribution of the Enamel Cuticle and Its Significance". Proceedings of the Royal Society of Medicine. 36 (9): 499–502. doi:10.1177/003591574303600917. PMC 1998608. PMID 19992694.
- ^ Bradway S.D.; Bergey E.J.; Scannapieco F.A.; Ramasubbu N.; Zawacki S. & Levine M.J. (1992). "Formation of salivary-mucosal pellicle: the role of transglutaminase". Biochem. J. 284 (2): 557–564. doi:10.1042/bj2840557. PMC 1132674. PMID 1376115.
- ^ 애쉬와 넬슨, 54쪽
- ^ 브라운, 688쪽
- ^ Salas, M.M.S.; Nascimento, G.G.; Huysmans, M.C.; Demarco, F.F. (1 January 2015). "Estimated prevalence of erosive tooth wear in permanent teeth of children and adolescents: An epidemiological systematic review and meta-regression analysis". Journal of Dentistry. 43 (1): 42–50. doi:10.1016/j.jdent.2014.10.012. ISSN 0300-5712. PMID 25446243.
- ^ "Tooth Enamel Defined". GogoSmile. Retrieved 4 August 2018.
- ^ a b c Ross et al., p. 453
- ^ 영국영양재단
- ^ Larsen MJ, Nyvad (1999). "Enamel erosion by some soft drinks and orange juices relative to their pH, buffering effect and contents of calcium phosphate". Caries Res. 33 (1): 81–87. CiteSeerX 10.1.1.464.7695. doi:10.1159/000016499. PMID 9831784. S2CID 28664016.
- ^ Braun, S; Bantleon, HP; Hnat, WP; Freudenthaler, JW; Marcotte, MR; Johnson, BE (1995). "A study of bite force, part 1: Relationship to various physical characteristics". The Angle Orthodontist. 65 (5): 367–72. ISSN 0003-3219. PMID 8526296.
- ^ Xu, H. H.; Smith, D. T.; Jahanmir, S.; Romberg, E; Kelly, J. R.; Thompson, V. P.; Rekow, E. D. (1998). "Indentation damage and mechanical properties of human enamel and dentin". Journal of Dental Research. 77 (3): 472–480. doi:10.1177/00220345980770030601. PMID 9496920. S2CID 21928580.
- ^ a b Chai, H.; Lee, J. J.; Constantino, P. J.; Lucas, P. W.; Lawn, B. R. (2009). "Remarkable resilience of teeth". PNAS. 106 (18): 7289–7293. Bibcode:2009PNAS..106.7289C. doi:10.1073/pnas.0902466106. PMC 2678632. PMID 19365079.
- ^ Selwitz RH, Ismail AI, Pitts NB (2007). "Dental caries". Lancet. 369 (9555): 51–59. doi:10.1016/S0140-6736(07)60031-2. PMID 17208642. S2CID 204616785.
- ^ Breaker, R.R. (2012). "New Insight on the Response of Bacteria to Fluoride". Caries Research. 46 (1): 78–81. doi:10.1159/000336397. PMC 3331882. PMID 22327376.
- ^ "20세기 10대 공중보건 업적 중 하나": 지역사회 물 불소화 – 구강보건; 20세기 10대 공중보건 업적 – CDC
- ^ "U.S. Public Health Service Recommendation for Fluoride Concentration in Drinking Water for the Prevention of Dental Caries". Public Health Reports. U.S. Department of Health and Human Services Federal Panel on Community Water Fluoridation. 130 (4): 318–331. 2015. doi:10.1177/003335491513000408. PMC 4547570. PMID 26346489.
- ^ "Fluoride in Drinking Water". EPA.gov. Environmental Protection Agency. 12 August 2015.
- ^ "Caries diagnosis and risk assessment. A review of preventive strategies and management". J Am Dent Assoc. 126 (Suppl): 1S–24S. 1995. doi:10.14219/jada.archive.1995.0371. PMID 7790681.
- ^ Twetman S (September 2009). "Caries prevention with fluoride toothpaste in children: an update". Eur Arch Paediatr Dent. 10 (3): 162–167. doi:10.1007/bf03262678. PMID 19772846. S2CID 22227878.
- ^ Summit et al., p. 273
- ^ Summit et al., p. 274
- ^ Summit et al., p. 7
- ^ Summit et al., p. 191.
- ^ a b c Summit et al., p. 193
- ^ 미국 치과 위생사 협회
- ^ Summit et al., p. 402
- ^ 배스발로그, 페렌바흐, 189쪽
- ^ Summit et al., p. 404
- ^ Summit et al., p. 420
- ^ a b c "Diagnosis of Celiac Disease". National Institute of Health (NIH). Archived from the original on 15 May 2017. Retrieved 6 June 2017.
- ^ 2016년 3월 5일 웨이백 머신 국립 보건원(NIH)에서 보관된 치아 에나멜 결함 및 셀리악 질환
- ^ a b Pastore L, Carroccio A, Compilato D, Panzarella V, Serpico R, Lo Muzio L (2008). "Oral manifestations of celiac disease" (PDF). J Clin Gastroenterol (Review). 42 (3): 224–32. doi:10.1097/MCG.0b013e318074dd98. hdl:10447/1671. PMID 18223505. S2CID 205776755.
- ^ a b 해리스, 페이지 7: "X-연동 상속"이라는 제목의 섹션을 참조하십시오.
- ^ eMedicine: 케르니테루스
- ^ 애쉬와 넬슨, 31쪽
- ^ e-메디신: 에리트로포이에틱 포르피리아
- ^ Frandson and Spurgeon, 305쪽
- ^ a b 피니, 187쪽
- ^ 피니, 186쪽
- ^ 페예스코프
- ^ 마틴; 랜달 보우먼
- ^ Mondéjar-Fernández, Jorge; Meunier, François J.; Cloutier, Richard; Clément, Gaël; Laurin, Michel (2021). "A microanatomical and histological study of the scales of the Devonian sarcopterygian Miguashaia bureaui and the evolution of the squamation in coelacanths". Journal of Anatomy. 239 (2): 451–478. doi:10.1111/joa.13428. ISSN 1469-7580. PMC 8273612. PMID 33748974.
- ^ Mondéjar-Fernández, Jorge; Janvier, Philippe (2021). "Finned Vertebrates". Vertebrate Skeletal Histology and Paleohistology. CRC Press: 294–324. doi:10.1201/9781351189590-15. ISBN 978-1-351-18959-0. S2CID 241700775.
- ^ Zylberberg, Louise; Meunier, François; Laurin, Michel (2015). "A microanatomical and histological study of the postcranial dermal skeleton of the Devonian actinopterygian Cheirolepis canadensis". Acta Palaeontologica Polonica. doi:10.4202/app.00161.2015. ISSN 0567-7920. S2CID 55113048.
- ^ "Evolution: Tooth-enamel similarities". Nature. 485 (7399): 419. 2012. Bibcode:2012Natur.485Q.419.. doi:10.1038/485419a. S2CID 52798363.
- ^ Bentov, S.; Zaslansky, P.; Al-Sawalmih, A.; Masic, A.; Fratzl, P.; Sagi, A.; Berman, A.; Aichmayer, B. (2012). "Enamel-like apatite crown covering amorphous mineral in a crayfish mandible". Nature Communications. 3 (5): 839. Bibcode:2012NatCo...3..839B. doi:10.1038/ncomms1839. PMC 3382302. PMID 22588301.
- ^ White, S.N. (2001). "Biological organization of hydroxyapatite crystallites into a fibrous continuum toughens and controls anisotropy in human enamel". J. Dent. Res. 80 (1): 321–326. doi:10.1177/00220345010800010501. PMID 11269723. S2CID 25482660.
- ^ a b c d e f Habelitz, S (2001). "Mechanical properties of human dental enamel on the nanometre scale". Archives of Oral Biology. 46 (2): 173–183. doi:10.1016/S0003-9969(00)00089-3. PMID 11163325.
- ^ Ge, J (2005). "Property variations in the prism and the organic sheath within enamel by nanoindentation". Biomaterials. 26 (16): 3333–3339. doi:10.1016/j.biomaterials.2004.07.059. PMID 15603829.
- ^ Park, S (2008). "Mechanical properties of human enamel as a function of age and location in the tooth". J Mater Sci: Mater Med. 19 (6): 2317–2324. doi:10.1007/s10856-007-3340-y. PMID 18157510. S2CID 25159868.
- ^ Xu, H (1998). "Indentation Damage and Mechanical Properties of Human Enamel and Dentin". Journal of Dental Research. 77 (3): 472–480. doi:10.1177/00220345980770030601. PMID 9496920. S2CID 21928580.
인용된 작품
- Ash, Jr., Major; Nelson, S.J. (2003). Dental anatomy, physiology, and occlusion (8th ed.). Philadelphia: W.B. Saunders. ISBN 0-7216-9382-2.
- Bath-Balogh, M.; Fehrenbach, M.J. (2011). Illustrated Dental Embryology, Histology, Anatomy (3rd ed.). Philadelphia: W.B. Saunders. ISBN 978-1-4377-1730-3.
- Brown, Theodore L. (2003). Chemistry: The central science (9th, paperback ed.). Upper Saddle River, NJ [Great Britain]: Prentice Hall. ISBN 0-13-049140-3. ISBN 0-13-047038-4; ISBN 0-13-038165-9 (CD-ROM)
- Nanci, Antonio, ed. (27 December 2016). Ten Cate's Oral Histology: Development, structure, and function (9th ed.). Elsevier. ISBN 9780323485241.
- Fejerskov, O. (March 1979). "Human dentition and experimental animals". Journal of Dental Research. 58 (Spec Issue B): 725–734. doi:10.1177/002203457905800224011. PMID 105027. S2CID 9282056. 특별호 B.
- Frandson, R.D.; Spurgeon, T.L. (1992). Anatomy and Physiology of Farm Animals (5th ed.). Philadelphia: Lea & Febiger. ISBN 0-8121-1435-3.
- Harris, Edward F. (2002). Craniofacial Growth and Development.
- Johnson, Clarke (1999). "Biology of the Human Dentition". dentistry.uic.edu.
- Pinney, Chris C. (1992). The illustrated veterinary guide for dogs, cats, birds & exotic pets (1st ed.). Blue Ridge Summit, PA: Tab Books. ISBN 0-8306-1986-0.
- Randall-Bowman (2004). "Gummed Out: Young Horses Lose Many Teeth, Vet Says". tamu.edu. Archived from the original on 3 March 2005. Retrieved 8 October 2007.
- Ross, Michael H.; Kaye, G.I.; Pawlina, W. (2006). Histology: a text and atlas (5th ed.). Philadelphia; London: Lippincott Williams & Wilkins. ISBN 0-7817-7221-4.
- Summitt, James B.; Robbins, William; Schwartz, J.; Schwartz, R.S. (2001). Fundamentals of Operative Dentistry: A Contemporary Approach (2nd ed.). Chicago, IL; London: Quintessence Publishing. ISBN 0-86715-382-2.


