요오드화 카드뮴
Cadmium iodide | |
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 카드뮴(II) 요오드화합물 | |
| 기타 이름 카드뮴 다이오다이오드 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.029.294 |
| EC 번호 |
|
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| CdI2 | |
| 어금질량 | 366.22 g/190 |
| 외관 | 백색에서 연한 황색 결정체 |
| 밀도 | 5.18 g/cm3, 솔리드 |
| 녹는점 | 387°C(729°F, 660K) |
| 비등점 | 742°C(1,368°F, 1,015K) |
| 787 g/L(0°C) 847 g/L(20°C) 1250 g/L(100 °C) | |
| 용해성 | 에탄올, 아세톤, 에테르, 암모니아에 녹는다. |
자기 감수성(magnetic susibility) | -1987.2·10cm−63/190cm |
| 구조 | |
| 삼각, hP3, 우주군 P3m1, 번호 164 | |
| 팔면체의 | |
| 위험 | |
| GHS 라벨 표시: | |
   | |
| 위험 | |
| H301, H331, H351, H373, H410 | |
| P260, P280, P301+P330+P331, P304+P340, P310, P311, P403+P233 | |
| NFPA 704(화재 다이아몬드) | |
| NIOSH(미국 건강 노출 제한): | |
PEL(허용) | [1910.1027] TWA 0.005 mg/m3 (Cd)[1] |
REL(권장) | CA[1] |
IDLH(즉시 위험) | Ca [9 mg/m3 (Cd)로)][1] |
| 관련 화합물 | |
기타 음이온 | 불화 카드뮴 염화 카드뮴 브롬화 카드뮴 |
기타 양이온 | 요오드화아연 수은(mercury)II) 요오드화합물 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
요오드화 카드뮴은 CdI라는2 공식을 가진 무기 화합물이다. 그것은 백색 발광 고체다. 그것은 또한 단수화물과 사수화물로 얻을 수 있다.[2] 응용 프로그램이 거의 없다. 양극화 효과가 강한 MX2 형태의 복합체에 전형적으로 나타나는 결정구조가 눈에 띈다.
준비
요오드화 카드뮴은 카드뮴 금속, 또는 그 산화물, 수산화물 또는 탄산염을 수산화산에 첨가하여 제조된다. 또한, 이 화합물은 카드뮴을 요오드로 가열하여 만들 수 있다.[2]
결정구조
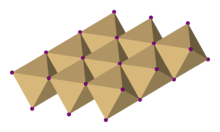
요오드화 카드뮴에서 요오드 음이온은 육각형의 촘촘한 포장을 형성하고 카드뮴 양이 모든 팔면체를 번갈아 채운다. 결과물 구조는 층층이 쌓인 격자로 구성된다. 이와 같은 기본적인 구조는 다른 많은 소금과 미네랄에서 발견된다. 요오드화 카드뮴은 대부분 이온적으로 결합되어 있지만 부분적인 공동발효 특성을 가지고 있다.[3]
요오드화 카드뮴의 결정 구조는 그 결정 구조가 많은 다른 화합물들의 기초가 되는 것으로 간주될 수 있는 시제품이다. 다음 특성을 가진 화합물은 CdI2 구조를 채택하는 경향이 있다.[citation needed]
- 적당히 편광된 양이온의 요오드화합물; 강한 편광 양이온의 브로미이드와 염소화합물
- 디커뮤니케이션의 수산화물, 즉 일반 공식 M(OH)2을 포함한 화합물
- 황화물, 셀레니드 및 텔루라이드(chalcogenides)의 사차화합물, 즉2 일반 공식 MX와의 화합물, 여기서 X = S, Se, Te
참조
- ^ a b c NIOSH Pocket Guide to Chemical Hazards. "#0087". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b F. Wagenknecht; R. Juza (1963). "Cadmium iodide". In G. Brauer (ed.). Handbook of Preparative Inorganic Chemistry, 2nd Ed. Vol. 2. NY, NY: Academic Press. p. 1096.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. pp. 1211–1212. ISBN 978-0-08-037941-8.




