아세테이트 카드뮴
Cadmium acetate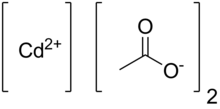 | |
| 이름 | |
|---|---|
| IUPAC 이름 아세테이트 카드뮴 | |
| 기타 이름 디아세트산 카드뮴 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.008.049 |
| EC 번호 |
|
펍켐 CID | |
| RTECS 번호 |
|
| 유니 |
|
| UN 번호 | 2570 |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| Cd(CHCOO3)(2무수) Cd(CHCOO3)/22HO2(수화물) | |
| 어금질량 | 230.500 g/㎥(무수) 266.529 g/diwidrate (dihydrate) |
| 외관 | 무색 결정(무수) 백색 결정(디하이드레이트) |
| 냄새 | 아세트산 |
| 밀도 | 2.341 g/cm3(무수) 2.01 g/cm3(수화물) |
| 녹는점 | 255 °C(491 °F; 528 K) (무수) 이수화물은 130 °C에서 분해된다. |
| 가용성(무수), 매우 가용성(수소) | |
| 용해성 | 메탄올, 에탄올(무수)에 용해성 에탄올에 용해되는 (디히드레이트) |
자기 감수성(magnetic susibility) | -83.7·10cm−63/190cm |
| 구조 | |
| 단색의 | |
| 위험 | |
| GHS 라벨 표시: | |
  | |
| 경고 | |
| H302, H312, H332, H410 | |
| P261, P264, P270, P271, P273, P280, P301+P312, P302+P352, P304+P312, P304+P340, P312, P322, P330, P363, P391, P501 | |
| NFPA 704(화재 다이아몬드) | |
| NIOSH(미국 건강 노출 제한): | |
PEL(허용) | [1910.1027] TWA 0.005 mg/m3 (Cd)[2] |
REL(권장) | CA[2] |
IDLH(즉시 위험) | Ca [9 mg/m3 (Cd)로)][2] |
| 관련 화합물 | |
기타 음이온 | 불화 카드뮴 염화 카드뮴 브롬화 카드뮴 요오드화 카드뮴 |
기타 양이온 | 아세테이트 아연 수성(Mercury)II) 아세테이트 아세테이트 은 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
아세트산 카드뮴은 Cd(CHCO32)라는 공식을 가진 화학 화합물이다.2 이 무색 고체는 카드뮴 센터를 상호 연결하는 아세테이트 리간즈(acetate ligands)를 특징으로 하는 분류된 조정 중합체다. 그 화합물은 무수형태로 다이하이드레이트로 존재한다. 산화카드뮴을 아세트산으로 처리하여 형성된다.[3][4]
사용하다
아세트산 카드뮴은 유리 세라믹과 도자기, 전기 도금 욕조, 염색 및 인쇄 직물, 그리고 유황, 셀레늄, 텔루륨의 분석 시약에 사용된다.[4]
준비
아세트산 카드뮴은 산화카드뮴을 아세트산으로 처리해 제조한다. 이 화합물은 또한 카드뮴 질산염을 아세트산 무수화물로 처리함으로써 준비될 수 있다.[5]
안전
카드뮴 화합물은 IARC에 의해 그룹 1 발암물질로 간주된다.
참조
- ^ Lide, David R. (1998). Handbook of Chemistry and Physics (87 ed.). Boca Raton, Florida: CRC Press. p. 447. ISBN 0-8493-0594-2.
- ^ a b c NIOSH Pocket Guide to Chemical Hazards. "#0087". National Institute for Occupational Safety and Health (NIOSH).
- ^ Gangolli, S. (1999). The Dictionary of Substances and Their Effects. London: Royal Society of Chemistry. pp. 12–13. Retrieved 2009-03-29.
- ^ a b Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill Professional. pp. 143–144. ISBN 0-07-049439-8. Retrieved 2009-03-29.
- ^ F. Wagenknecht; R. Juza (1963). "Cadmium acetate". In G. Brauer (ed.). Handbook of Preparative Inorganic Chemistry, 2nd Ed. Vol. 2. NY, NY: Academic Press. p. 1105.



