면역 체크포인트
Immune checkpoint면역 체크포인트는 면역체계의 규제기관이다.이러한 경로는 면역체계가 세포를 무차별적으로 공격하지 못하도록 하는 자기강도에 매우 중요하다.그러나 일부 암은 면역체크포인트 대상을 자극해 공격으로부터 자신을 보호할 수 있다.[1]
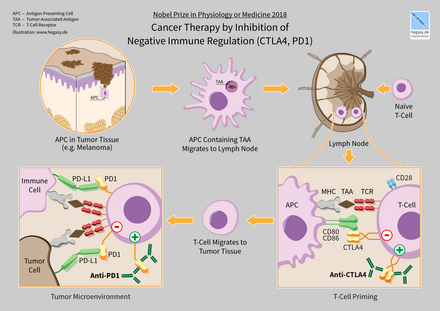
억제 체크포인트 분자는 여러 종류의 암에 사용될 가능성이 있기 때문에 암 면역 요법의 대상이다.현재 승인된 체크포인트 억제제는 CTLA4와 PD-1, PD-L1을 차단한다.관련 기초과학발견에 대해서는 제임스 P. 앨리슨과 혼조 타수쿠는 2018년 당상, 노벨 생리의학상을 각각 수상했다.[2][3]
자극성 체크포인트 분자
4개의 자극성 체크포인트 분자는 종양 괴사 인자(TNF) 수용체 슈퍼 패밀리의 구성원이다.CD27, CD40, OX40, GITR 및 CD137.B7-CD28 슈퍼 패밀리에 속하는 또 다른 두 개의 자극성 체크포인트 분자CD28 자체와 ICOS.
- CD27: 이 분자는 항원 특유의 순종 T세포 확장을 지지하며 T세포 기억력 생성을 위해 필수적이다.[4]CD27은 B세포의 기억표기도 하다.[5]CD27의 활동은 리간드 CD70이 림프구와 덴드리트 세포에서 일시적으로 사용할 수 있는지의 여부에 따라 결정된다.[6]CD27 비용 시뮬레이션은 Th17 이펙터 셀 기능을 억제하는 것으로 알려져 있다.[7]미국 생명공학 회사 셀덱스 테라피틱스는 동물 모델에서 T세포 수용체 자극의 맥락에서 효과가 있는 것으로 밝혀진 작용제 항체[8] CDX-1127을 연구하고 있다.[9]
- CD28: 이 분자는 거의 모든 인간 CD4+T 세포와 모든 CD8 T 세포의 약 절반에 구성적으로 표현된다.두 개의 리간드로 결합하면 CD80과 CD86으로 덴드리트 셀에 표현되며 T 셀 확장이 촉진된다.CD28은 2006년 3월 런던에서의 1인 연구에서의 심한 염증 반응을 일으킨 TGN1412 '수퍼 길항제'의 표적이었습니다.[10]
- CD40: 항원 표시 세포를 포함한 다양한 면역 체계 세포에서 발견되는 이 분자는 CD40L를 가지고 있는데, CD154라고도 하며 활성 CD4+T 세포 표면에 일시적으로 그 리간드로 표현된다.CD40 신호는 수지상세포가 성숙하도록 '라이센스'하여 T세포 활성화와 분화를 유발하는 것으로 알려져 있다.[11]지금은 없어진 시애틀에 본사를 둔 생명공학 회사인 VLST는 2012년 화이저로부터 항CD40 작용제 단클론 항체를 허가했다.스위스 제약사 로슈는 2013년 VLST가 폐쇄되면서 이 프로젝트를 인수했다.[12]
- CD122: 인터루킨-2 수용체 베타 서브 유닛인 이 분자는 CD8+이펙터 T 세포의 증식을 증가시키는 것으로 알려져 있다.[13]미국 생명공학회사 네카르 테라피틱스는 2016년 11월 발표한 CD122 편향 면역억제 사이토카인[14] 1단계 결과물인 NKTR-214를 개발 중이다.[15]
- CD137: 4-1BB라고도 불리는 이 분자가 CD137 리간드로 묶여 있을 때 그 결과는 T세포 증식이다.CD137 매개 신호는 T세포도 보호하는 것으로 알려져 있으며, 특히 CD8+T세포는 활성화에 의한 세포사망으로부터 보호된다.[16]독일 바이오기업 피에리스제약은 CD137과 HER2용 바이오 전용 리포칼린을 개발했다.[17]
- OX40: CD134라고도 불리는 이 분자는 OX40L, 즉 CD252를 리간드로 가지고 있다.OX40은 CD27과 마찬가지로 이펙터와 메모리 T세포의 확장을 촉진하지만, T-규제세포의 분화와 활동을 억제하는 능력, 사이토카인 생산의 규제로도 주목받는다.[18]OX40의 약물 표적으로서의 가치는 주로 T-세포 수용체 결합 후 과도적으로 표현되어 염증성 병변 내에서 가장 최근에 항원으로 활성화된 T세포에서만 상향 조절된다는 사실에 있다.[19]항-OX40 단클론 항체는 고도암에 임상 효용이 있는 것으로 나타났다.[20]제약회사 아스트라제네카는 OX40을 겨냥한 3가지 약을 개발 중에 있다. MEDI0562는 인간화된 OX40 작용제, MEDI6469, 뮤린 OX4 작용제, MEDI6383은 OX40 작용제다[21].
- GITR: 글루코르티코이드 유도 TNFR 계열 관련 유전자의 줄임말로 Treg 확장을 포함한 T세포 확장을 촉진한다.[22]GITR을 위한 리간드는 주로 항원을 나타내는 세포에 표현된다.[23]GITR에 대한 항체는 Treg 혈통 안정성의 상실을 통해 항투석 반응을 촉진하는 것으로 나타났다.[24]생명공학 회사 TG Therapeutics는 항-GITR 항체를[25] 연구하고 있다.
- ICOS: 인덕터블 T세포 코스트모뮬레이터의 약자로 CD278이라고도 불리는 이 분자는 활성 T세포에 표현된다.리간드는 ICOSL로 주로 B세포와 덴드리트세포에 표현된다.이 분자는 T세포 이펙터 기능에서 중요한 것 같다.[26]미국의 생명공학 회사인 Jounce Therapeutics는 ICOS 작용제를 개발하고 있다.
억제 체크포인트 분자
- A2AR: 아데노신 A2A 수용체는 A2a 수용체 활성화로 이어지는 면역 미세 환경의 아데노신이 음의 면역 피드백 루프이며 종양 미세 환경은 상대적으로 아데노신 농도가 높기 때문에 암 치료에서 중요한 체크포인트로 간주된다.[27]
- B7-H3: CD276이라고도 불리는데, 처음에는 공동 자극 분자로[28] 이해되었으나 현재는 공동 억제 분자로 간주되고 있다.[29]미국 생명공학회사 매크로제닉스가 MGA271을 연구하고 있는 것은 B7-H3를 대상으로 하는 fc에 최적화된 단핵항체다.[30]b7-H3의 수용체는 아직 확인되지 않았다.[31]
- B7-H4: VTCN1이라고도 하며, 종양 세포와 종양 관련 대식세포에 의해 발현되어 종양 탈출의 역할을 한다.[32]
- BTLA: B와 T 림프구 감쇠기의 줄임말이며 CD272라고도 불리는 이 분자는 HVEM(Herpesvirus Entry Medicator)을 리간드로 한다.BTLA의 표면 표현은 인간 CD8+T 세포를 순진하고 이펙터 세포 표현형에서 분화하는 동안 점차적으로 하향 조절되지만, 종양 특유의 인간 CD8+T 세포는 높은 수준의 BTLA를 표현한다.[33]
- CTLA-4: 세포독성 T-림포시세포 연관 단백질 4의 줄임말이며 CD152로도 불리는 브리스톨-마이어스 스퀴브의 흑색종 치료제 예르보이가 2011년 3월 FDA 승인을 받은 대상이다.Treg 세포에 CTLA-4를 발현하면 T세포 증식을 억제하는 역할을 한다.[34][35]
- IDO: 인도레아민 2,3-다이옥시제나아제의 줄임말로, 면역 억제 성질을 가진 트립토판 카타볼릭 효소다.또 다른 중요한 분자는 TDO, 트립토판 2,3-다이옥시제네제다.IDO는 T세포와 NK세포를 억제하고, Tregs와 몰로이드 유래 억제세포를 생성·활성화하며, 종양 혈관신생을 촉진하는 것으로 알려져 있다.[36][35]
- KIR: 킬러 세포 면역글로불린 유사 수용체의 줄임말로, 내추럴 킬러 세포의 MHC Class I 분자를 위한 수용체다.브리스톨마이어스 스퀴브는 KIR에 대한 단핵항체인 리릴루맵을 연구하고 있다.
- LAG3: 림프구 활성화 유전자-3의 줄임말로서, CD8+T세포에 대한 직접적인 영향뿐만 아니라 트레그스에[37] 대한 작용에 의한 면역 반응을 억제하는 작용을 한다.[38][35]Bristol-Myers Squibb는 BMS-986016이라는 항 LAG3 단클로널 항체를 가지고 1단계에 있다.[39]
- NOX2: 니코틴아미드 아데닌 디뉴클레오티드 인산염 NADPH 산화효소 이소폼 2의 줄임말로 면역억제 활성산소종을 생성하는 골수세포의 효소다.골수세포에서 NOX2의 유전적, 약리학적 억제는 인접한 NK세포와 T세포의 투석방지 기능을 향상시키고 인간과 실험동물의 자가면역성을 유발한다.NOX2는 EU 내에서 급성 골수성 백혈병에 대한 사용 승인을 얻은 세플렌의 대상이다.
- PD-1: Programed Death 1(PD-1) 수용체의 줄임말이며, PD-L1과 PD-L2라는 두 개의 리간드가 있다.이 검문소는 2014년 9월 FDA 승인을 받은 머크앤코의 흑색종 치료제 키트루다의 표적이다.이 검문소는 2017년 FDA 승인을 받은 EMD 세로노(메르크 KGAA)의 마약 바벤시오의 표적이기도 하다.대상 PD-1의 장점은 종양 미세환경에서 면역 기능을 회복할 수 있다는 점이다.[41][35]
- TIM-3: T-cell Immunoglobulin 도메인과 Mucin 도메인 3의 줄임말로, 활성화된 인간 CD4+ T세포에 표현하고 Th1과 Th17 사이토카인을 조절한다.[42]TIM-3는 리간드, 갈락틴-9와 상호작용할 때 세포 사멸을 유발하여 Th1/Tc1 함수의 음의 조절기 역할을 한다.[43][35]
- VISTA: T세포 활성화의 V-domain Ig 억제기의 약자로, VISTA는 종양 내 백혈구에 대한 VISTA의 일관된 표현이 광범위한 고형종 종양에 걸쳐 VISTA 봉쇄를 효과적으로 수행할 수 있도록 조혈세포에[44] 주로 표현된다.[45][35]
- SIGLEC7 (Sialic acid-binding immunoglobulin-type lectin 7, also designated as CD328) and SIGLEC9 (Sialic acid-binding immunoglobulin-type lectin 9, also designated as CD329) are proteins found on the surface of various immune cells, including natural killer cells and macrophages (SIGLEC7) and neutrophils, macrophages, dendritic cells and activatedT-세포([46]SIGLEC9)SIGLECs 7과 9는 세포 표면을 덮고 있는 글리칸의 단자 시알산에 결합하여 이들 세포의 면역 기능을 억제한다.[47][48]
면역 체크포인트 억제제
억제 체크포인트 분자를 억제/차단하는 약물 또는 약물 후보자들은 때때로 체크포인트 억제제라고 알려져 있다; 이 생각은 종종 면역 체크포인트 봉쇄 또는 단순히 체크포인트 봉쇄라고 불린다.[49][35]체크포인트 억제제는 브리스톨마이어스스스퀴브, 머크, 머크KGA, 로슈, 아스트라제네카 등 기업의 암 관련 제약 연구가 성장세를 보이고 있다.[50]
참조
- ^ Pardoll DM (March 2012). "The blockade of immune checkpoints in cancer immunotherapy". Nature Reviews. Cancer. 12 (4): 252–64. doi:10.1038/nrc3239. PMC 4856023. PMID 22437870.
- ^ "2014 Tang Prize in Biopharmaceutical Science". Archived from the original on 2017-10-20. Retrieved 2016-06-18.
- ^ Devlin, Hannah (2018-10-01). "James P Allison and Tasuku Honjo win Nobel prize for medicine". the Guardian. Retrieved 2018-10-01.
- ^ Hendriks J; Gravestein LA; Tesselaar K; van Lier RA; Schumacher TN; Borst J. (November 1, 2000). "CD27 is required for generation and long-term maintenance of T cell immunity". Nat Immunol. 1 (5): 433–40. doi:10.1038/80877. PMID 11062504.
- ^ Agematsu K (April 1, 2000). "Memory B cells and CD27". Histology and Histopathology. 15 (2): 573–6. PMID 10809378.
- ^ Borst J, Hendriks J, Xiao Y (June 1, 2005). "CD27 and CD70 in T cell and B cell activation". Curr Opin Immunol. 17 (3): 275–81. doi:10.1016/j.coi.2005.04.004. PMID 15886117.
- ^ Coquet JM, Middendorp S, van der Horst G, Kind J, Veraar EA, Xiao Y, Jacobs H, Borst J (January 24, 2013). "The CD27 and CD70 costimulatory pathway inhibits effector function of T helper 17 cells and attenuates associated autoimmunity". Immunity. 38 (1): 53–65. doi:10.1016/j.immuni.2012.09.009. PMID 23159439.
- ^ "CDX-1127 – Monoclonal Antibody Targeting CD27". Celldex Therapeutics.
- ^ He LZ, Prostak N, Thomas LJ, Vitale L, Weidlick J, Crocker A, Pilsmaker CD, Round SM, Tutt A, Glennie MJ, Marsh H, Keler T (October 15, 2013). "Agonist anti-human CD27 monoclonal antibody induces T cell activation and tumor immunity in human CD27-transgenic mice". J Immunol. 191 (8): 4174–83. doi:10.4049/jimmunol.1300409. PMID 24026078.
- ^ Eastwood D, Findlay L, Poole S, Bird C, Wadhwa M, Moore M, Burns C, Thorpe R, Stebbings R (October 1, 2010). "Monoclonal antibody TGN1412 trial failure explained by species differences in CD28 expression on CD4+ effector memory T-cells". Br J Pharmacol. 161 (3): 512–526. doi:10.1111/j.1476-5381.2010.00922.x. PMC 2990151. PMID 20880392.
- ^ O'Sullivan B, Thomas R (January 1, 2003). "CD40 and dendritic cell function". Crit Rev Immunol. 23 (1): 83–107. doi:10.1615/critrevimmunol.v23.i12.50. PMID 12906261.
- ^ Zimm, Angela (April 12, 2014). "Cancer 'Miracle' Patients Studied Anew for Disease Clues". Bloomberg. Retrieved 25 June 2015.
- ^ Boyman O, Sprent J (February 17, 2012). "The role of interleukin-2 during homeostasis and activation of the immune system". Nat Rev Immunol. 12 (3): 180–190. doi:10.1038/nri3156. PMID 22343569.
- ^ "Nektar and MD Anderson Cancer Center Announce Phase 1/2 Clinical Research Collaboration for NKTR-214, a CD122-Biased Immuno-Stimulatory Cytokine". Nektar Therapeutics. June 2, 2015. Archived from the original on 19 December 2017. Retrieved 25 June 2015.
- ^ 면역치료, NKTR-214, 임상시험에서 고형종양에 대한 활동 표시
- ^ Mittler RS, Foell J, McCausland M, Strahotin S, Niu L, Bapat A, Hewes LB (June 1, 2004). "Anti-CD137 antibodies in the treatment of autoimmune disease and cancer". Immunol Res. 29 (1): 197–208. doi:10.1385/ir:29:1-3:197. PMID 15181282.
- ^ "Pieris Pharmaceuticals to present data on novel anti-CD137 and HER2 bispecific immuno-oncology program at UBS Global Healthcare Conference". Pieris Pharmaceuticals. 19 May 2015. Retrieved 5 June 2015.
- ^ Croft M, So T, Duan W, Soroosh P (May 1, 2009). "The significance of OX40 and OX40L to T-cell biology and immune disease". Immunol Rev. 229 (1): 173–91. doi:10.1111/j.1600-065x.2009.00766.x. PMC 2729757. PMID 19426222.
- ^ Weinberg AD, Morris NP, Kovacsovics-Bankowski M, Urba WJ, Curti BD (November 1, 2011). "Science gone translational: the OX40 agonist story". Immunol Rev. 244 (1): 218–31. doi:10.1111/j.1600-065x.2011.01069.x. PMC 3622727. PMID 22017441.
- ^ Curti BD; Kovacsovics-Bankowski M; Morris N; Walker E; Chisholm L; Floyd K; Walker J; Gonzalez I; Meeuwsen T; Fox BA; Moudgil T; Miller W; Haley D; Coffey T; Fisher B; Delanty-Miller L; Rymarchyk N; Kelly T; Crocenzi T; Bernstein E; Sanborn R; Urba WJ; Weinberg AD. (December 15, 2013). "OX40 is a potent immune-stimulating target in late-stage cancer patients". Cancer Res. 73 (24): 7189–98. doi:10.1158/0008-5472.can-12-4174. PMC 3922072. PMID 24177180.
- ^ "Q1 2015 Result". AstraZeneca. 24 April 2015. Retrieved 5 June 2015.
- ^ Ronchetti S, Zollo O, Bruscoli S, Agostini M, Bianchini R, Nocentini G, Ayroldi E, Riccardi C (March 1, 2004). "GITR, a member of the TNF receptor superfamily, is costimulatory to mouse T lymphocyte subpopulations". Eur J Immunol. 34 (3): 613–22. doi:10.1002/eji.200324804. PMID 14991590.
- ^ Nocentini G, Ronchetti S, Cuzzocrea S, Riccardi C (May 1, 2007). "GITR/GITRL: more than an effector T cell co-stimulatory system". Eur J Immunol. 37 (5): 1165–9. doi:10.1002/eji.200636933. PMID 17407102.
- ^ Schaer DA, Budhu S, Liu C, Bryson C, Malandro N, Cohen A, Zhong H, Yang X, Houghton AN, Merghoub T, Wolchok JD (November 1, 2013). "GITR pathway activation abrogates tumor immune suppression through loss of regulatory T cell lineage stability". Cancer Immunol Res. 1 (5): 320–31. doi:10.1158/2326-6066.cir-13-0086. PMC 3885345. PMID 24416730.
- ^ "TG Therapeutics Enters Into a Global Collaboration With Checkpoint Therapeutics to Develop and Commercialize Novel Immuno-Oncology Targeted Antibodies". TG Therapeutics. 4 March 2015. Retrieved 5 June 2015.
- ^ Burmeister Y, Lischke T, Dahler AC, Mages HW, Lam KP, Coyle AJ, Kroczek RA, Hutloff A (January 15, 2008). "ICOS controls the pool size of effector-memory and regulatory T cells". J Immunol. 180 (2): 774–782. doi:10.4049/jimmunol.180.2.774. PMID 18178815.
- ^ Leone RD, Lo YC, Powell JD (April 8, 2015). "A2aR antagonists: Next generation checkpoint blockade for cancer immunotherapy". Comput Struct Biotechnol J. 13: 265–72. doi:10.1016/j.csbj.2015.03.008. PMC 4415113. PMID 25941561.
- ^ Chapoval AI, Ni J, Lau JS, Wilcox RA, Flies DB, Liu D, Dong H, Sica GL, Zhu G, Tamada K, Chen L (March 1, 2001). "B7-H3: a costimulatory molecule for T cell activation and IFN-gamma production". Nat Immunol. 2 (3): 269–74. doi:10.1038/85339. PMID 11224528.
- ^ Leitner J, Klauser C, Pickl WF, Stöckl J, Majdic O, Bardet AF, Kreil DP, Dong C, Yamazaki T, Zlabinger G, Pfistershammer K, Steinberger P (July 1, 2009). "B7-H3 is a potent inhibitor of human T-cell activation: No evidence for B7-H3 and TREML2 interaction". Eur J Immunol. 39 (7): 1754–64. doi:10.1002/eji.200839028. PMC 2978551. PMID 19544488.
- ^ "MacroGenics Provides Update on Corporate Progress and First Quarter 2015 Financial Results". MacroGenics. 6 May 2015. Retrieved 5 June 2015.
- ^ Mao Y, Li W, Chen K, Xie Y, Liu Q, Yao M, Duan W, Zhou X, Liang R, Tao M (February 20, 2015). "B7-H1 and B7-H3 are independent predictors of poor prognosis in patients with non-small cell lung cancer". Oncotarget. 6 (5): 3452–61. doi:10.18632/oncotarget.3097. PMC 4413666. PMID 25609202.
- ^ Dangaj D, Lanitis E, Zhao A, Joshi S, Cheng Y, Sandaltzopoulos R, Ra HJ, Danet-Desnoyers G, Powell DJ Jr, Scholler N (August 1, 2013). "Novel recombinant human b7-h4 antibodies overcome tumoral immune escape to potentiate T-cell antitumor responses". Cancer Res. 73 (15): 4820–9. doi:10.1158/0008-5472.can-12-3457. PMC 3732560. PMID 23722540.
- ^ Derré L, Rivals JP, Jandus C, Pastor S, Rimoldi D, Romero P, Michielin O, Olive D, Speiser DE (January 1, 2010). "BTLA mediates inhibition of human tumor-specific CD8+ T cells that can be partially reversed by vaccination". J Clin Invest. 120 (1): 157–67. doi:10.1172/jci40070. PMC 2799219. PMID 20038811.

- ^ Kolar P, Knieke K, Hegel JK, Quandt D, Burmester GR, Hoff H, Brunner-Weinzierl MC (January 1, 2009). "CTLA-4 (CD152) controls homeostasis and suppressive capacity of regulatory T cells in mice". Arthritis Rheum. 60 (1): 123–32. doi:10.1002/art.24181. PMID 19116935.
- ^ a b c d e f g h Syn, Nicholas L; Teng, Michele W L; Mok, Tony S K; Soo, Ross A (2017). "De-novo and acquired resistance to immune checkpoint targeting". The Lancet Oncology. 18 (12): e731–e741. doi:10.1016/s1470-2045(17)30607-1. PMID 29208439.
- ^ Prendergast GC, Smith C, Thomas S, Mandik-Nayak L, Laury-Kleintop L, Metz R, Muller AJ (July 1, 2014). "Indoleamine 2,3-dioxygenase pathways of pathogenic inflammation and immune escape in cancer". Cancer Immunol Immunother. 63 (7): 721–35. doi:10.1007/s00262-014-1549-4. PMC 4384696. PMID 24711084.
- ^ Huang CT; Workman CJ; Flies D; Pan X; Marson AL; Zhou G; Hipkiss EL; Ravi S; Kowalski J; Levitsky HI; Powell JD; Pardoll DM; Drake CG; Vignali DA. (October 1, 2004). "Role of LAG-3 in regulatory T cells". Immunity. 21 (4): :503–13. doi:10.1016/j.immuni.2004.08.010. PMID 15485628.
- ^ Grosso JF, Kelleher CC, Harris TJ, Maris CH, Hipkiss EL, De Marzo A, Anders R, Netto G, Getnet D, Bruno TC, Goldberg MV, Pardoll DM, Drake CG (November 1, 2007). "LAG-3 regulates CD8+ T cell accumulation and effector function in murine self- and tumor-tolerance systems". J Clin Invest. 117 (11): 3383–92. doi:10.1172/jci31184. PMC 2000807. PMID 17932562.
- ^ ClinicalTrials.gov의 "고형종양 치료에 있어 Anti-PD-1이 있는 경우와 없는 경우의 안전성 연구"에 대한 임상 시험 번호 NCT01968109
- ^ Martner A, Aydin E, Hellstrand K (October 1, 2018). "NOX2 in autoimmunity, tumor growth and metastasis". J Pathol. 247 (2): 151–154. doi:10.1002/path.5175. PMC 6587556. PMID 30270440.
- ^ Philips GK, Atkins M (January 1, 2015). "Therapeutic uses of anti-PD-1 and anti-PD-L1 antibodies". Int Immunol. 27 (1): 39–46. doi:10.1093/intimm/dxu095. PMID 25323844.
- ^ Hastings WD, Anderson DE, Kassam N, Koguchi K, Greenfield EA, Kent SC, Zheng XX, Strom TB, Hafler DA, Kuchroo VK (September 1, 2009). "TIM-3 is expressed on activated human CD4+ T cells and regulates Th1 and Th17 cytokines". Eur J Immunol. 39 (9): 2492–501. doi:10.1002/eji.200939274. PMC 2759376. PMID 19676072.
- ^ Zhu C, Anderson AC, Kuchroo VK (August 11, 2010). TIM-3 and its regulatory role in immune responses. Curr Top Microbiol Immunol. Current Topics in Microbiology and Immunology. Vol. 350. pp. 1–15. doi:10.1007/82_2010_84. ISBN 978-3-642-19544-0. PMID 20700701.
- ^ Wang L, Rubinstein R, Lines JL, Wasiuk A, Ahonen C, Guo Y, Lu LF, Gondek D, Wang Y, Fava RA, Fiser A, Almo S, Noelle RJ (March 14, 2011). "VISTA, a novel mouse Ig superfamily ligand that negatively regulates T cell responses". J Exp Med. 208 (3): 577–92. doi:10.1084/jem.20100619. PMC 3058578. PMID 21383057.
- ^ Lines JL, Pantazi E, Mak J, Sempere LF, Wang L, O'Connell S, Ceeraz S, Suriawinata AA, Yan S, Ernstoff MS, Noelle R (April 1, 2014). "VISTA is an immune checkpoint molecule for human T cells". Cancer Res. 74 (7): 1924–32. doi:10.1158/0008-5472.CAN-13-1504. PMC 3979527. PMID 24691993.
- ^ Läubli, Heinz; Zippelius, Alfred; Varki, Ajit; Speiser, Daniel E.; Stenner, Frank; Egli, Adrian; Syedbasha, Mohammedyaseen; Amos, Christopher I.; Han, Younghun (2018-11-01). "Self-associated molecular patterns mediate cancer immune evasion by engaging Siglecs on T cells". The Journal of Clinical Investigation. 128 (11): 4912–4923. doi:10.1172/JCI120612. ISSN 0021-9738. PMC 6205408. PMID 30130255.
- ^ Varki, Ajit; Paulson, James C.; Crocker, Paul R. (2007). "Siglecs and their roles in the immune system". Nature Reviews Immunology. 7 (4): 255–266. doi:10.1038/nri2056. ISSN 1474-1741. PMID 17380156.
- ^ Paulson, James C.; Crocker, Paul R.; Macauley, Matthew S. (2014). "Siglec-mediated regulation of immune cell function in disease". Nature Reviews Immunology. 14 (10): 653–666. doi:10.1038/nri3737. ISSN 1474-1741. PMC 4191907. PMID 25234143.
- ^ Pardoll, Drew M. (22 March 2012). "The blockade of immune checkpoints in cancer immunotherapy". Nature Reviews Cancer. 12 (4): 252–264. doi:10.1038/nrc3239. PMC 4856023. PMID 22437870.
- ^ "Cancer drugs are getting better and dearer". The Economist. 2017-05-04. Retrieved 2017-05-19.