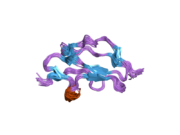인자 H
Factor H| 보계수 H | |
|---|---|
 보완 H 사량체, 인간 | |
| 식별자 | |
| 기호. | ? |
| CFH | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||
| 에일리어스 | CFH, AHUS1, AMBP1, ARMD4, ARM1, CFHL3, FH, FHL1, HF1, HF2, HUS, 보완인자 H | ||||||||||||||||||||||||
| 외부 ID | OMIM: 134370 MGI: 88385 HomoloGene: 20086 GeneCard: CFH | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 맞춤법 | |||||||||||||||||||||||||
| 종. | 인간 | 마우스 | |||||||||||||||||||||||
| 엔트레즈 | |||||||||||||||||||||||||
| 앙상블 | |||||||||||||||||||||||||
| 유니프로트 | |||||||||||||||||||||||||
| RefSeq(mRNA) | |||||||||||||||||||||||||
| RefSeq(단백질) | |||||||||||||||||||||||||
| 장소(UCSC) | Chr 1: 196.65 ~196.75 Mb | Chr 1 : 140.01 ~140.11 Mb | |||||||||||||||||||||||
| PubMed 검색 | [3] | [4] | |||||||||||||||||||||||
| 위키데이터 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
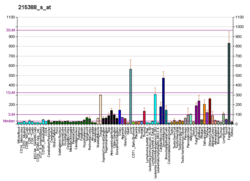
인자 H는 보체 활성화 패밀리의 조절제이며 보체 제어 단백질이다.이것은 사람 혈장 내에서 순환하는 (일반적으로 밀리리터당[5][6][7] 200~300 마이크로그램의 농도로) 큰 (155 킬로달톤) 용해성 당단백질이다.주요 기능은 보체 시스템의 대체 경로를 조절하여 보체 시스템이 병원체 또는 다른 위험한 물질로 향하도록 하고 숙주 조직을 손상시키지 않도록 하는 것이다.인자 H는 인자 I 매개 C3b 분열을 위한 보조인자 활성과 대체 경로 C3-변환효소 C3bb에 대한 붕괴 촉진 활성을 모두 보유함으로써 자기 세포 및 표면에서의 보체 활성화를 조절한다.인자 H는 자가 세포와 자가 표면에는 보호 작용을 하지만 박테리아나 바이러스의 표면에는 그렇지 않습니다.이는 인자 H가 C3 분해 또는 붕괴 가속 [8]활성의 보조 인자로서 더 낮거나 더 높은 활성에 대한 적합성을 채택할 수 있는 능력을 가진 결과로 생각된다.하부 활성 구성은 용액에서 지배적인 형태이며 유체 위상 증폭을 제어하기에 충분합니다.보다 능동적인 배치는 인자 H가 일반적으로 숙주 세포에 존재하지만 일반적으로 병원체 표면에는 존재하지 않는 글리코사미노글리칸(GAG) 및/또는 시알산에 결합할 때 유도되는 것으로 생각되며, 외부 [9][10]표면에서는 보체가 수그러들지 않고 진행되는 동안 자가 표면이 보호된다.
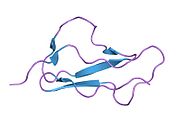
구조.
분자는 20개의 보체제어단백질(CCP) 모듈(3~8개의 아미노산 잔류물)로 서로 연결되어 있으며 머리부터 꼬리까지 확장된 방식으로 배열되어 있습니다.각 CCP 모듈은 약 60개의 아미노산과 1-3-2-4 배열로 결합된 4개의 시스테인 잔기 디술피드와 거의 불변한 트립토판 잔기 주위에 구축된 소수성 코어로 구성됩니다.CCP 모듈은 (단백질의 N 말단에서) 1~20의 번호가 매겨집니다.CCP 1~4 및 CCP 19~20은 C3b에, CCP 7 및 CCP 19~20은 GAG 및 시알산에 [11]결합합니다.현재까지 CCP 1~3,[12] CCP [13]5, CCP [14]7, CCP 10-11 및 CCP 11~[15]12, CCP 12~[16]13, CCP 15, [17]CCP 16, CCP 15~[18]16, CCP 18~20,[19][20][21] CCP 19~20S에 대해 원자구조가 결정되었다.수크로스 옥타황산염과 결합한 CCPs 6~8의 원자구조,[22] C3b와[23] 복합체 CCPs 1~4 및 C3d(C3b의 [24][25]티오스터 도메인에 해당)와 복합체 CCPs 19~20도 결정되었다.온전한 인자 H에 대한 원자 분해능 구조는 아직 결정되지 않았지만,[26] 저해상도 기술은 용액에서 다시 구부러질 수 있음을 나타냅니다.현재까지 이용 가능한 정보에 따르면 CCP 모듈 1~4는 인자 H의 보조인자 및 붕괴촉진 활성에 책임이 있는 반면, 자기/비자기 식별은 주로 CCP 모듈 7 및/또는 GAG 또는 19~[26][27]20에 결합하는 시알산에 의해 발생한다.
임상적 의의
보체의 조절에서 인자 H가 수행하는 중심적인 역할 때문에, 이상 인자 H의 활성에서 발생하는 많은 임상적 영향이 있다.과잉 활성 인자 H는 병원성 세포에서 보체 활성을 감소시켜 미생물 감염에 대한 민감도를 높일 수 있다.저활성인자 H는 건강한 숙주 세포에서 보체 활성을 증가시켜 자가면역질환을 일으킬 수 있다.따라서 보체인자 H유전자(CFH)의 희귀 돌연변이 또는 공통 단일 뉴클레오티드 다형(SNP)이 종종 병리학을 초래하는 것은 놀라운 일이 아니다.게다가 인자 H의 보체 억제 활성과 다른 보체 조절제는 종종 병원균에 의해 독성을 증가시키기 위해 사용된다.
2005년에 여러 독립 연구 그룹이 CFH에서 SNP를 식별하여 단백질 변화 p를 유발하였다.유럽인의 약 3분의 1이 AMD의 리스크 [28]요인으로서 Y402H에 대응하고 있습니다.대립 유전자의 빈도는 모집단에 따라 상당히 다르지만 Y402H는 AMD의 발병과 [28]진행과 일관되게 관련되어 있습니다.호모 접합성 개인은 AMD와 연관될 확률이 약 7배 높은 반면 헤테로 접합성 개인은 AMD와 연관될 확률이 약 2~3배 더 높습니다.[28]인자 H의 CCP 모듈 7에 위치한 이 SNP는 인자 H 단백질이 망막 조직의 염증 부위(예: 폴리아니온과 펜트락신)에 위치하는 능력과 보체와 면역 [28]세포의 활성화를 조절하는 능력에 영향을 미치는 것으로 나타났다.SNP는 또한 CCPs 1~7로만 구성된 인자 H의 대체 스플라이스 버전인 인자 H 유사 단백질 1의 기능에 영향을 미치는 것으로 나타났으며, 이는 안구 보체 조절에서 [28]더 큰 역할을 하는 것으로 생각된다.그러나, 개인의 AMD 위험에 가장 큰 영향을 미치는 CFH의 유전자 변이는 [28]보체의 대체 경로의 영향을 감소시키는 데 관여하는 CCP 1~4에 영향을 미치는 것으로 나타났다.드문 함수 코드 변경, p.CFH의 R1210C는 인자 H의 기능적 결핍을 초래하고 황반변성 및 보체 매개 신장 질환의 [28][29]상당히 높은 위험을 초래한다.
보체 인자 H 관련 유전자뿐만 아니라 다른 보체 단백질(예: 인자 I, C2/인자 B 및 C3)과 같은 보체 활성화 궤적의 다른 유전자 변화도 더 큰 AMD [28]위험과 관련이 있다.현재의 이론은 AMD의 [28]만성 염증의 주요 동인이 보체 규제 장애라는 것이다.
비정형 용혈성 요독증후군
용혈성 요독증후군은 미세혈관성 용혈성 빈혈, 혈소판 감소증, 급성 신부전과 관련된 질병이다.이는 후천성(예: 시가톡스성 대장균 감염 후) 또는 유전될 수 있다(일명 비정형 용혈성 요독증후군, aHUS). aHUS는 보체 시스템, 특히 인자 [28]H의 유전자 돌연변이와 강하게 관련되어 있다.AMD와 하는 N-말단(CCPs 14)간에 다양성과 관련된 C3신사 구체 병증( 다른complement-mediated 신장 병), 인자 H에서 발생하기 쉬운 돌연변이로 대조적으로 주로 시말단은 신장 조직과 레의 준수 여부에 대해 책임을 지는 반면 단백질(임계 채널 출력 모듈 19,20일)[28]의 영향을 미친다.장미.보체 구성요소 및 그 다운스트림 이펙터의 이온화.[28][30][31]
정신분열증
면역반응의 변화는 정신분열증을 포함한 많은 신경정신질환의 병인과 관련이 있다.최근 연구에 따르면 대체 보체 경로의 과활성화를 초래할 수 있는 보체 시스템의 변화가 정신분열증에 걸리기 쉬운 것으로 나타났다.예를 들어 CFH SNP rs424535(2783-526T>A)는 [32]정신분열증과 긍정적으로 관련되어 있습니다.
허혈성 뇌졸중
rs800292(184G >A) SNP는 뇌졸중과 양성으로 관련되었으며 CFH 유전자의 rs800912 마이너 대립 유전자는 허혈성 [32]뇌졸중의 위험 인자로 간주될 수 있다.
병원균에 의한 모집
보체로부터 세포를 보호하는 데 있어 인자 H의 중심 역할을 고려할 때, 몇몇 중요한 인간 병원균이 인자 H를 모집하기 위한 메커니즘을 발전시킨 것은 놀라운 일이 아니다.병원균에 의한 인자 H의 모집은 보체 공격에 대한 상당한 저항력을 제공하고, 따라서 독성을 증가시킨다.H 인자를 모집하는 것으로 나타난 병원체는 다음과 같다.아스페르길루스 spp.;Borrelia burgdorferi, B. duttonii, 재발성, 칸디다 알비칸스,[33] 프랜시셀라 툴라렌시스, 헤모필루스 인플루엔자, Neisseria meningitidis, Streptoccus pyogenees.[8]그램 음성 박테리아 B.burgdorferi는 5가지 인자 H 결합 단백질, 즉 CRASP-1, CRASP-2, CRASP-3, CRASP-4 및 CRASP-5를 [34]가지고 있다.각 CRASP 단백질은 또한 플라스미노겐과 [34]결합합니다.전 세계 CFH 변이체의 대립 유전자 빈도는 전염병의 [28]선택적 압력을 반영할 수 있다.
상호 작용
인자 H는 다른 보체 단백질 및 인자 중 보체 성분 3과 상호작용하는 것으로 나타나 [28][35][36]보체의 대체 경로의 조절로 이어졌다.
재조합생산
생물학적으로 활성인자 H는 랄프 레스키와 이끼 생물반응기의 [37]동료들에 의해 분자농이라고 불리는 과정에서 생성되었습니다.효모 발현 호스트인 Pichia pastoris에서 [38]발현되는 합성 코돈 최적화 유전자를 사용하여 잠재적으로 치료 목적에 적합한 다량의 생물학적 활성 인간 인자 H가 생성되었다.
치료약으로서의 잠재적 사용
연령 관련 황반 변성
Gemini Therapeutics Inc.는 매사추세츠에 본사를 둔 정밀 의학 회사로서 질병에 대한 보다 깊은 이해를 통해 새로운 치료법 개발에 주력하고 있습니다.인간 인자 H의 생물학적 활동을 바탕으로 제미니는 건조 AMD의 치료를 위해 재조합 인간 인자 H 단백질 GEM103을 개발하고 있다. 제미니는 최근 유전자 위험이 높은 변종에서 건조 연령 관련 황반변성(AMD) 환자의 GEM103에 대한 2a 임상시험의 등록을 완료했다고 발표했다.최고 라인 데이터는 2021년 1H에 예상됩니다.
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG000000971 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000026365 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Sofat R, Mangione PP, Gallimore JR, Hakobyan S, Hughes TR, Shah T, et al. (April 2013). "Distribution and determinants of circulating complement factor H concentration determined by a high-throughput immunonephelometric assay". Journal of Immunological Methods. 390 (1–2): 63–73. doi:10.1016/j.jim.2013.01.009. PMID 23376722.
- ^ Hakobyan S, Harris CL, Tortajada A, Goicochea de Jorge E, García-Layana A, Fernández-Robredo P, et al. (May 2008). "Measurement of factor H variants in plasma using variant-specific monoclonal antibodies: application to assessing risk of age-related macular degeneration". Investigative Ophthalmology & Visual Science. 49 (5): 1983–90. doi:10.1167/iovs.07-1523. PMID 18436830.
- ^ Scholl HP, Charbel Issa P, Walier M, Janzer S, Pollok-Kopp B, Börncke F, et al. (July 2008). "Systemic complement activation in age-related macular degeneration". PLOS ONE. 3 (7): e2593. Bibcode:2008PLoSO...3.2593S. doi:10.1371/journal.pone.0002593. PMC 2440421. PMID 18596911.
- ^ a b Herbert AP, Makou E, Chen ZA, Kerr H, Richards A, Rappsilber J, Barlow PN (November 2015). "Complement Evasion Mediated by Enhancement of Captured Factor H: Implications for Protection of Self-Surfaces from Complement". Journal of Immunology. 195 (10): 4986–98. doi:10.4049/jimmunol.1501388. PMC 4635569. PMID 26459349.
- ^ Pangburn MK (August 2000). "Host recognition and target differentiation by factor H, a regulator of the alternative pathway of complement". Immunopharmacology. 49 (1–2): 149–57. doi:10.1016/S0162-3109(00)80300-8. PMID 10904114.
- ^ Rodríguez de Córdoba S, Esparza-Gordillo J, Goicoechea de Jorge E, Lopez-Trascasa M, Sánchez-Corral P (June 2004). "The human complement factor H: functional roles, genetic variations and disease associations". Molecular Immunology. 41 (4): 355–67. doi:10.1016/j.molimm.2004.02.005. PMID 15163532.
- ^ Schmidt CQ, Herbert AP, Kavanagh D, Gandy C, Fenton CJ, Blaum BS, et al. (August 2008). "A new map of glycosaminoglycan and C3b binding sites on factor H". Journal of Immunology. 181 (4): 2610–9. doi:10.4049/jimmunol.181.4.2610. PMID 18684951.
- ^ Hocking HG, Herbert AP, Kavanagh D, Soares DC, Ferreira VP, Pangburn MK, et al. (April 2008). "Structure of the N-terminal region of complement factor H and conformational implications of disease-linked sequence variations". The Journal of Biological Chemistry. 283 (14): 9475–87. doi:10.1074/jbc.M709587200. PMC 2276370. PMID 18252712.
- ^ Barlow PN, Norman DG, Steinkasserer A, Horne TJ, Pearce J, Driscoll PC, et al. (April 1992). "Solution structure of the fifth repeat of factor H: a second example of the complement control protein module". Biochemistry. 31 (14): 3626–34. doi:10.1021/bi00129a011. PMID 1533152.
- ^ Herbert AP, Deakin JA, Schmidt CQ, Blaum BS, Egan C, Ferreira VP, et al. (June 2007). "Structure shows that a glycosaminoglycan and protein recognition site in factor H is perturbed by age-related macular degeneration-linked single nucleotide polymorphism". The Journal of Biological Chemistry. 282 (26): 18960–8. doi:10.1074/jbc.M609636200. PMID 17360715.
- ^ Makou E, Mertens HD, Maciejewski M, Soares DC, Matis I, Schmidt CQ, et al. (December 2012). "Solution structure of CCP modules 10-12 illuminates functional architecture of the complement regulator, factor H". Journal of Molecular Biology. 424 (5): 295–312. doi:10.1016/j.jmb.2012.09.013. PMC 4068365. PMID 23017427.
- ^ Schmidt CQ, Herbert AP, Mertens HD, Guariento M, Soares DC, Uhrin D, et al. (January 2010). "The central portion of factor H (modules 10-15) is compact and contains a structurally deviant CCP module". Journal of Molecular Biology. 395 (1): 105–22. doi:10.1016/j.jmb.2009.10.010. PMC 2806952. PMID 19835885.
- ^ Norman DG, Barlow PN, Baron M, Day AJ, Sim RB, Campbell ID (June 1991). "Three-dimensional structure of a complement control protein module in solution". Journal of Molecular Biology. 219 (4): 717–25. doi:10.1016/0022-2836(91)90666-T. PMID 1829116.
- ^ Barlow PN, Steinkasserer A, Norman DG, Kieffer B, Wiles AP, Sim RB, Campbell ID (July 1993). "Solution structure of a pair of complement modules by nuclear magnetic resonance". Journal of Molecular Biology. 232 (1): 268–84. doi:10.1006/jmbi.1993.1381. PMID 8331663.
- ^ Morgan HP, Mertens HD, Guariento M, Schmidt CQ, Soares DC, Svergun DI, et al. (2012). "Structural analysis of the C-terminal region (modules 18-20) of complement regulator factor H (FH)". PLOS ONE. 7 (2): e32187. Bibcode:2012PLoSO...732187M. doi:10.1371/journal.pone.0032187. PMC 3289644. PMID 22389686.
- ^ Herbert AP, Uhrín D, Lyon M, Pangburn MK, Barlow PN (June 2006). "Disease-associated sequence variations congregate in a polyanion recognition patch on human factor H revealed in three-dimensional structure". The Journal of Biological Chemistry. 281 (24): 16512–20. doi:10.1074/jbc.M513611200. PMID 16533809.
- ^ Jokiranta TS, Jaakola VP, Lehtinen MJ, Pärepalo M, Meri S, Goldman A (April 2006). "Structure of complement factor H carboxyl-terminus reveals molecular basis of atypical haemolytic uremic syndrome". The EMBO Journal. 25 (8): 1784–94. doi:10.1038/sj.emboj.7601052. PMC 1440827. PMID 16601698.
- ^ Prosser BE, Johnson S, Roversi P, Herbert AP, Blaum BS, Tyrrell J, et al. (October 2007). "Structural basis for complement factor H linked age-related macular degeneration". The Journal of Experimental Medicine. 204 (10): 2277–83. doi:10.1084/jem.20071069. PMC 2118454. PMID 17893204.
- ^ Wu J, Wu YQ, Ricklin D, Janssen BJ, Lambris JD, Gros P (July 2009). "Structure of complement fragment C3b-factor H and implications for host protection by complement regulators". Nature Immunology. 10 (7): 728–33. doi:10.1038/ni.1755. PMC 2713992. PMID 19503104.
- ^ Morgan HP, Schmidt CQ, Guariento M, Blaum BS, Gillespie D, Herbert AP, et al. (April 2011). "Structural basis for engagement by complement factor H of C3b on a self surface". Nature Structural & Molecular Biology. 18 (4): 463–70. doi:10.1038/nsmb.2018. PMC 3512577. PMID 21317894.
- ^ Kajander T, Lehtinen MJ, Hyvärinen S, Bhattacharjee A, Leung E, Isenman DE, et al. (February 2011). "Dual interaction of factor H with C3d and glycosaminoglycans in host-nonhost discrimination by complement". Proceedings of the National Academy of Sciences of the United States of America. 108 (7): 2897–902. Bibcode:2011PNAS..108.2897K. doi:10.1073/pnas.1017087108. PMC 3041134. PMID 21285368.
- ^ a b Aslam M, Perkins SJ (June 2001). "Folded-back solution structure of monomeric factor H of human complement by synchrotron X-ray and neutron scattering, analytical ultracentrifugation and constrained molecular modelling". Journal of Molecular Biology. 309 (5): 1117–38. doi:10.1006/jmbi.2001.4720. PMID 11399083.
- ^ Kirkitadze MD, Barlow PN (April 2001). "Structure and flexibility of the multiple domain proteins that regulate complement activation". Immunological Reviews. 180: 146–61. doi:10.1034/j.1600-065X.2001.1800113.x. PMID 11414356. S2CID 25095717.
- ^ a b c d e f g h i j k l m n Tzoumas, Nikolaos; Hallam, Dean; Harris, Claire L.; Lako, Majlinda; Kavanagh, David; Steel, David H.W. (November 2020). "Revisiting the role of factor H in age-related macular degeneration: Insights from complement-mediated renal disease and rare genetic variants". Survey of Ophthalmology. 66 (2): 378–401. doi:10.1016/j.survophthal.2020.10.008. ISSN 0039-6257. PMID 33157112. S2CID 226274874.
- ^ Raychaudhuri S, Iartchouk O, Chin K, Tan PL, Tai AK, Ripke S, et al. (October 2011). "A rare penetrant mutation in CFH confers high risk of age-related macular degeneration". Nature Genetics. 43 (12): 1232–6. doi:10.1038/ng.976. PMC 3225644. PMID 22019782.
- ^ Atkinson JP, Goodship TH (June 2007). "Complement factor H and the hemolytic uremic syndrome". The Journal of Experimental Medicine. 204 (6): 1245–8. doi:10.1084/jem.20070664. PMC 2118604. PMID 17548524.
- ^ de Jorge EG, Macor P, Paixão-Cavalcante D, Rose KL, Tedesco F, Cook HT, et al. (January 2011). "The development of atypical hemolytic uremic syndrome depends on complement C5". Journal of the American Society of Nephrology. 22 (1): 137–45. doi:10.1681/ASN.2010050451. PMC 3014042. PMID 21148255.
- ^ a b Boyajyan A, Ghazaryan H, Stepanyan A, Zakharyan R (December 2013). "Genetic polymorphisms of complement factor H in schizophrenia and ischemic stroke". Mol. Immunol. 56 (3): 294. doi:10.1016/j.molimm.2013.05.154.
- ^ Luo S, Poltermann S, Kunert A, Rupp S, Zipfel PF (December 2009). "Immune evasion of the human pathogenic yeast Candida albicans: Pra1 is a Factor H, FHL-1 and plasminogen binding surface protein". Molecular Immunology. 47 (2–3): 541–50. doi:10.1016/j.molimm.2009.07.017. PMID 19850343.
- ^ a b Zipfel PF, Hallström T, Riesbeck K (December 2013). "Human complement control and complement evasion by pathogenic microbes--tipping the balance". Molecular Immunology. 56 (3): 152–60. doi:10.1016/j.molimm.2013.05.222. PMID 23810413.
- ^ Soames CJ, Sim RB (September 1997). "Interactions between human complement components factor H, factor I and C3b". The Biochemical Journal. 326 ( Pt 2) (Pt 2): 553–61. doi:10.1042/bj3260553. PMC 1218704. PMID 9291131.
- ^ Jokiranta TS, Westin J, Nilsson UR, Nilsson B, Hellwage J, Löfås S, et al. (March 2001). "Complement C3b interactions studied with surface plasmon resonance technique". International Immunopharmacology. 1 (3): 495–506. doi:10.1016/S1567-5769(00)00042-4. PMID 11367533.
- ^ Büttner-Mainik A, Parsons J, Jérôme H, Hartmann A, Lamer S, Schaaf A, et al. (April 2011). "Production of biologically active recombinant human factor H in Physcomitrella". Plant Biotechnology Journal. 9 (3): 373–83. doi:10.1111/j.1467-7652.2010.00552.x. PMID 20723134.
- ^ Schmidt CQ, Slingsby FC, Richards A, Barlow PN (April 2011). "Production of biologically active complement factor H in therapeutically useful quantities". Protein Expression and Purification. 76 (2): 254–63. doi:10.1016/j.pep.2010.12.002. PMC 4067574. PMID 21146613.
추가 정보
- Bradley DT, Zipfel PF, Hughes AE (June 2011). "Complement in age-related macular degeneration: a focus on function". Eye. 25 (6): 683–93. doi:10.1038/eye.2011.37. PMC 3178140. PMID 21394116.
- Kardys I, Klaver CC, Despriet DD, Bergen AA, Uitterlinden AG, Hofman A, et al. (April 2006). "A common polymorphism in the complement factor H gene is associated with increased risk of myocardial infarction: the Rotterdam Study". Journal of the American College of Cardiology. 47 (8): 1568–75. doi:10.1016/j.jacc.2005.11.076. PMID 16630992.
- Pío R, Elsasser TH, Martínez A, Cuttitta F (April 2002). "Identification, characterization, and physiological actions of factor H as an adrenomedullin binding protein present in human plasma". Microscopy Research and Technique. 57 (1): 23–7. doi:10.1002/jemt.10047. PMID 11921353. S2CID 37608883.
- Walport MJ (April 2001). "Complement. First of two parts". The New England Journal of Medicine. 344 (14): 1058–66. doi:10.1056/NEJM200104053441406. PMID 11287977.
- Walport MJ (April 2001). "Complement. Second of two parts". The New England Journal of Medicine. 344 (15): 1140–4. doi:10.1056/NEJM200104123441506. PMID 11297706.