클로로디페닐포스핀
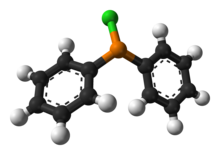
Chlorodiphenylphosphine | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 염화디페닐포스핀[1] | |
| 기타 이름 클로로디페닐포스핀 p-클로로디페닐포스핀 염화디페닐포스핀 디페닐클로로포스핀 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.012.813 |
| EC 번호 |
|
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| CHCP1210 | |
| 몰 질량 | 220.63776 g mol−1 |
| 외모 | 맑고 밝은 노란색 액체 |
| 밀도 | 1.229gcm−3 |
| 비등점 | 320°C |
| 반응 | |
| 용해성 | 알코올과 반응하다 벤젠, THF 및 에테르에 고도로 용해되는 |
| 위험 요소 | |
| GHS 라벨링: | |
  | |
| 위험. | |
| H290, H302, H314, H412 | |
| P234, , , , , , , , , , , , , ,, | |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
클로로디페닐포스핀은 (CH)라는 식에 해당하는65 2유기인 화합물이다.PCl(PhPCl2 약어).이것은 마늘과 비슷하며 ppb 범위에서도 검출 가능한 자극적인 냄새를 가진 무채색 유성 액체입니다.많은 리간드를 포함하는 분자에 PhP기를2 도입하는 데 유용한 시약이다.[2]다른 할로포스핀과 마찬가지로 PhPCl은2 물과 같은 많은 핵 친성과 반응하며 공기에 의해서도 쉽게 산화된다.
합성 및 반응
클로로디페닐포스핀은 벤젠과 삼염화인(PCL3)에서 상업적으로 생산된다.벤젠은 약 600°C의 극한 온도에서 삼염화 인과 반응하여 디클로로페닐포스핀(PhPCl2)과 HCl을 생성합니다.고온에서 기상에서 PhPCl의2 재배포는 클로로디페닐포스핀을 [2][3]발생시킨다.
- 22 PhPCL → PhPCL2 + PCL3
또는 트리페닐포스핀 및 삼염화인에서 시작하는 재배포 반응에 의해 이러한 화합물을 제조한다.
- PCl3 + 2 PPh3 → 3 PhPCl2
클로로디페닐포스핀은 가수분해되어 디페닐포스핀산화물을 얻는다.나트륨으로 환원하면 테트라페닐디포스핀이 생성됩니다.
- PhPCL2 2개 + Na 2개 → [PhP2]2 + NaCl 2개
암모니아와 원소 황에서는 티오포스폴아미드로 [4]전환됩니다.
- PhPCl2 + 2 NH3 + S → PhP2(S)NH2 + NHCl4
사용하다
클로로디페닐포스핀은 다른 클로로포스핀과 함께 다양한 포스핀의 합성에 사용된다.일반적인 경로에서는 그리냐드 [3]시약을 사용합니다.
- PhPCL2 + MgRX → PhPR2 + MgClX
그 phosphines Ph2PCl과 반응으로 생산 더 나아 가, 예로는 살충제,(Sandostab P-EPQ), Ph2PCl 중요한 intermedia를 만들고(치과 재료에 사용되) 들어 있는 플라스틱 안전 장치 다양한 할로겐 화합물의 기폭제가 불꽃 retardants(순환phosphinocarboxylic 무수), 뿐만 아니라UV-hardening 회화 시스템(EPN 같은)사용되는 개발된다.기산업계에서요.[2][3]
디페닐포스피도 유도체 전구체
클로로디페닐포스핀은 역류 다이옥산에서의 [5]디페닐포스핀화나트륨과의 반응을 통해 디페닐포스핀화나트륨의 합성에 사용된다.
- PhPCL2 + 2 Na → PhPNa2 + NaCl
디페닐포스핀은 PhPCl과2 LiAlH의4 반응에서 합성될 수 있으며,[6] PhPCl과 LiAlH는 일반적으로 과도하게 사용된다.
- 42 PhPCL + LiAlH4 → 4 PhPH2 + LiCl + AlCl3
또한2 PhPNa와2 PhPH는 유기포스핀 배위자의 합성에 사용된다.
특성화
클로로디페닐포스핀의 품질은 31P NMR [7]분광법에 의해 종종 확인된다.
| 컴파운드 | 31P 화학 이동 (ppm vs 85% H3PO4) |
|---|---|
| PPh3 | -6 |
| PPh2Cl | 81.5 |
| PPhCl2 | 165 |
| PCl3 | 218 |
레퍼런스
- ^ International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. p. 926. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ a b c Quin, L. D. 유기인 화학 가이드; Wiley IEEE: New York, 2000; 페이지 44-69.ISBN 0-471-31824-8
- ^ a b c 스바라, J., 웨퍼링, 호프만, T. "인화합물, 유기", 울만의 산업화학 백과사전 제7판;Wiley-VCH: 2008, doi: 10.1002/14356007.a19_545.pub2;접근처:2008년 2월 18일
- ^ Lin, Shaoquan; Otsuka, Yasunari; Yin, Liang; Kumagai, Naoya; Shibasaki, Masakatsu (2017). "Catalytic Enantioselective Addition of Diethyl Phosphite to N-Thiophosphinoyl Ketimines: Preparation of (R)-Diethyl (1-Amino-1-phenylethyl)phosphonate". Organic Syntheses. 94: 313–331. doi:10.15227/orgsyn.094.0313.
- ^ Roy, Jackson W; Thomson, RJ; MacKay, M.F. (1985). "The Stereochemistry of Organometallic Compounds. XXV. The Stereochemistry of Displacements of Secondary Methanesulfonate and p-Toluene-sulfonate esters by Diphenylphosphide Ions. X-ray Crystal Structure of (5α-Cholestan-3α-yl)diphenylphosphine Oxide". Australian Journal of Chemistry. 38 (1): 111–18. doi:10.1071/CH9850111.
- ^ Stepanova, Valeria A.; Dunina, Valery V.; Smoliakova, Irina P. (2009). "Reactions of Cyclopalladated Complexes with Lithium Diphenylphosphide". Organometallics. 28 (22): 6546–6558. doi:10.1021/om9005615.
- ^ O. Kühl "인-31 NMR 분광학" 스프링어, 베를린, 2008.ISBN 978-3-540-79118-8


