카르복실화
Carboxylation카르복실화는 기질을 이산화탄소로 처리해 카르복실산군이 생성되는 화학반응이다.[1] 반대 반응은 데카복시화다. 화학에서 탄산화라는 용어는 때때로 탄복제와 동의어로 사용되기도 하는데, 특히 CO와2 함께 카르바니온 시약의 반응에 적용될 때 더욱 그러하다. 보다 일반적으로 탄산화는 보통 탄산수의 생산을 설명한다.[2]
유기 화학
카르복실화는 유기화학에서 표준변환이다.[3] 특히 그리니드 시약과 오르가늄 화합물의 탄산화(즉, 카르복시화)는 유기 할로겐화물을 카르복시산으로 변환하는 고전적인 방법이다.[4]
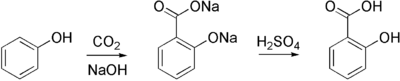
아스피린의 전구체인 살리실산 나트륨은 콜베-슈미트 반응으로 알려진 방법인 페놀산나트륨(페놀의 나트륨 소금)을 이산화탄소와 함께 고압(100 atm)과 고온(390 K)으로 처리해 상업적으로 준비한다. 그 결과로 생긴 살리실산염의 산화는 살리실산을 준다.
많은 세부 절차들이 학술지 Organic Synthes에 설명되어 있다.[5][6][7]
카르복실화 촉매에는 N-헤테로사이클릭 카베네와 은을 기반으로 한 촉매가 포함된다.[9]
생화학에서의 카르복시화
탄소 기반 생명은 대기 중의 이산화탄소를 설탕에 결합시키는 탄복제에서 비롯된다. 그 과정은 보통 루비스코라는 효소에 의해 촉매된다. 이 카르복실화를 촉진하는 효소인 리불로스-1,5-비스인산염 카르복실라제/옥시제나아제는 아마도 지구상에서 가장 풍부한 단일 단백질일 것이다.[10][11][12]

아세틸-코아 카복실라제, 메틸크로토닐-코아 카복실라제, 프로피오닐-코아 카복실라제, 피루바이트 카복실라제 등 많은 카복실라제는 공동작용제로 바이오틴이 필요하다. 이 효소들은 다양한 생물학적 경로에 관여한다.[13] EC 방식에서, 그러한 카복실라제는 EC 6.3.4, "기타 탄소—니트로겐 리가스"에 따라 분류된다.
또 다른 예로는 글루탐산염 잔류물의 변환 후 단백질 내 car-카복시글루탐산염에 대한 수정이다. 주로 혈액 응고 폭포와 관련된 단백질, 특히 인자 II, VII, IX, X, 단백질 C, 단백질 S에서 발생하며, 일부 뼈 단백질에서도 발생한다. 이러한 단백질들이 기능하기 위해서는 이러한 개조가 필요하다. 카르복실화는 간에서 발생하며 γ-글루타밀 카르복실라제(GGCX)에 의해 수행된다.[14] GGCX는 공동 인자로서 비타민 K를 필요로 하며, 그 반응을 과정적으로 수행한다.[15] γ-carboxyglutamate는 칼슘을 결합하는데, 칼슘은 그 활동에 필수적이다.[16] 예를 들어 프로트롬빈에서 칼슘 결합은 단백질이 혈소판의 혈장막과 연관되도록 하여, 프로트롬빈을 상처 후 활성 트롬빈으로 분리한 단백질과 근접하게 한다.[17]
참고 항목
참조
- ^ "카르복실화: 카복실 그룹이 분자나 화합물에 유입되어 카복실산이나 카복실산을 형성하는 것, 이것의 한 예."Oxford English Dictionary. Oxford University Press. 2018.
- ^ "탄산화: 이산화탄소로 침공 또는 처리, 탄산염으로의 전환."Oxford English Dictionary. Oxford University Press. 2018.
- ^ Braunstein, Pierre; Matt, Dominique; Nobel, Dominique (August 1988). "Reactions of Carbon Dioxide with Carbon-Carbon Bond Formation Catalyzed by Transition-Metal Complexes". Chemical Reviews. 88 (5): 747–764. doi:10.1021/cr00087a003.
- ^ A. M. Appel; et al. (2013). "Frontiers, Opportunities, and Challenges in Biochemical and Chemical Catalysis of CO2 Fixation". Chem. Rev. 113 (8): 6621–6658. doi:10.1021/cr300463y. PMC 3895110. PMID 23767781.
- ^ Akira Yanagisawa; Katsutaka Yasue; Hisashi Yamamoto (1997). "Regio- and Stereoselective Carboxylation of Allylic Barium Reagents: (E)-4,8-Dimethyl-3,7-Nonadienoic Acid". Organic Syntheses. 74: 178. doi:10.15227/orgsyn.074.0178.
- ^ H. Koch; W. Haaf (1964). "1-Adamantanecarboxylic Acid". Organic Syntheses. 44: 1. doi:10.15227/orgsyn.044.0001.
- ^ W. Haaf (1966). "1-Methylcyclohexanecarboxylic Acid". Organic Syntheses. 46: 72. doi:10.15227/orgsyn.046.0072.
- ^ Zhang Liang (2013). "N-Heterocyclic carbene (NHC)–copper-catalysed transformations of carbon dioxide". Chemical Science. 4 (9): 3395. doi:10.1039/C3SC51070K.
- ^ K. Sekine; T. Yamada (2016). "Silver-catalyzed carboxylation". Chem. Soc. Rev. 45 (16): 4524–4532. doi:10.1039/C5CS00895F. PMID 26888406.
- ^ Dhingra A, Portis AR, Daniell H (April 2004). "Enhanced translation of a chloroplast-expressed RbcS gene restores small subunit levels and photosynthesis in nuclear RbcS antisense plants". Proc. Natl. Acad. Sci. U.S.A. 101 (16): 6315–20. Bibcode:2004PNAS..101.6315D. doi:10.1073/pnas.0400981101. PMC 395966. PMID 15067115.
(Rubisco) is the most prevalent enzyme on this planet, accounting for 30–50% of total soluble protein in the chloroplast;
- ^ Feller U, Anders I, Mae T (2008). "Rubiscolytics: fate of Rubisco after its enzymatic function in a cell is terminated" (PDF). J. Exp. Bot. 59 (7): 1615–24. doi:10.1093/jxb/erm242. PMID 17975207.
- ^ Raven, John A. (April 2013). "Rubisco: still the most abundant protein of Earth?". New Phytologist. 198 (1): 1–3. doi:10.1111/nph.12197. PMID 23432200.
- ^ "Biotin – Fact Sheet for Health Professionals". Office of Dietary Supplements, US National Institutes of Health. 8 December 2017. Retrieved 25 February 2018.
- ^ OMIM - 감마 글루타밀 카복실라아제, McKusick VA에 의해 기여, 2004년 10월 마지막 업데이트 [1]
- ^ Morris DP, Stevens RD, Wright DJ, Stafford DW (1995). "Processive post-translational modification. Vitamin K-dependent carboxylation of a peptide substrate". J. Biol. Chem. 270 (51): 30491–8. doi:10.1074/jbc.270.51.30491. PMID 8530480.
- ^ Hauschka PV, Lian JB, Gallop PM (1975). "Direct identification of the calcium-binding amino acid, gamma-carboxyglutamate, in mineralized tissue". Proc. Natl. Acad. Sci. U.S.A. 72 (10): 3925–9. Bibcode:1975PNAS...72.3925H. doi:10.1073/pnas.72.10.3925. PMC 433109. PMID 1060074.
- ^ Berg JM, Tymoczko JL, Stryer L. 생화학, 5부작. 뉴욕: W. H. Freeman and Company, 2002.