아세틸 플루오르화
Acetyl fluoride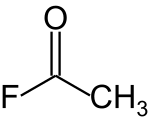 | |
 | |
| 이름 | |
|---|---|
| 선호 IUPAC 이름 아세틸 플루오르화 | |
| 체계적 IUPAC 이름 에다노일 플루오르화 | |
| 기타 이름 메틸카르보닐 플루오르화물 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.008.354 |
펍켐 CID | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C2H3FO | |
| 어금질량 | 62.043 g·192−1 |
| 밀도 | 1.032 g/cm3 |
| 녹는점 | -84°C(-119°F, 189K) |
| 비등점 | 21°C(70°F, 294K)[1] |
| 위험 | |
| GHS 라벨 표시: | |
 | |
| 위험 | |
| H314 | |
| P260, P264, P280, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P363, P405, P501 | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
아세틸 플루오르화물은 화학적 공식 CHCOF와3 함께 아킬 할로겐화물이다.[2] 이 공식은 일반적으로 AcF로 약칭된다.
합성
아세틸 플루오르화물은 플루오르화 수소 및 무수 아세트산을 사용하여 합성된다. 아세트산은 부산물로 생산된다.[3]
- HF + (CH
3CO)
2O → CH
3CO
2H + CH
3COF
참고 항목
참조
- ^ "Acetyl fluoride". Archived from the original on 2014-03-28. Retrieved 2012-03-07.
- ^ "Acetyl Fluoride". NIST. Archived from the original on 21 February 2019. Retrieved 7 March 2012.
- ^ Tanaka, Mutsuo; Fujiwara, Masahiro; Ando, Hisanori (1995). "Dual Reactivity of the Formyl Cation as an Electrophile and a Bransted Acid in Superacids". Journal of Organic Chemistry. 60 (12): 3846–3850. doi:10.1021/jo00117a041.


