이산화나트륨
Sodium diacetate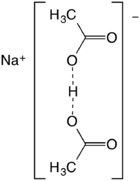 이산화나트륨 | |
| 이름 | |
|---|---|
| IUPAC 이름 이산화나트륨 | |
| 기타 이름 이산화나트륨(무수); 아세트산 나트륨; 아세트산 나트륨 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.004.378 |
| 메슈 | 디아세트산나트륨 디아세트산 |
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C4H7나O4 | |
| 어금질량 | 142.086 g·192−1 |
| 외관 | 화이트 파우더 |
| 냄새 | 아세트산(소) 냄새 |
| 1g/mL | |
| 알코올 용해성 | 살짝 |
| 에테르 내 용해성 | 불용성 |
| 위험 | |
| 산업안전보건(OHS/OSH): | |
흡입 위험 | 자극성[1] |
눈 위험 | 자극성[1] |
| GHS 라벨 표시:[1] | |
  | |
| 위험 | |
| H318, H319 | |
| P264, P280, P305+P351+P338, P310, P337+P313 | |
| 플래시 포인트 | 150°C(302°F)[1] 이상 |
| 치사량 또는 농도(LD, LC): | |
LD50(중간 선량) | >2,000mg/kg (랫드, 피부), 5,600mg/kg (랫드, 구강) |
| 안전 데이터 시트(SDS) | PubChem sodium diacetate LCSS |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
디아세트산 나트륨은 NaH(CHO
2
3
2) 공식을 가진 화합물이다.
2 그것은 아세트산의 소금이다. 무색 고체로 양념에 쓰이며 항균제로 쓰인다.
준비 및 구조
소금은 아세트산의 반중립화 후에 용액의 증발로 형성된다. 이는 농축 용액에서 아세트산의 산도를 높이는 효과인 호모 연관성의 결과로 볼 수 있다.
- 2 CHCOH32 + NaOH → Na+[(CHCO32)2H]− + HO2
아세트산의 나트륨산염으로도 설명되며, 수소결합 음이온(CHCO32)2H의− 나트륨염으로 가장 잘 설명된다. O··O 거리는 약 2.47 앙스트롬이다.[2] 그 종은 용액에 있어서 유의미한 존재는 없지만 안정된 결정체를 형성한다.
적용들
식품첨가물로서 E번호 E262를 가지고 있으며 소금과 식초향을 전달하는 데 사용된다.[3]
참고 항목
참조
- ^ a b c d PubChem. "Sodium diacetate". PubChem. Retrieved 2019-10-24.
- ^ 바로우, 마이클 J; 커리, 머독; 뮤어, 케네스 W.; 스피크맨, J. 클레어; 화이트, 데이비드 N, J. "단조산 산염의 결정 구조. XII. 수소 이산화나트륨의 구조, 중성자 회절에 의해 재결정" 화학회지, 퍼킨트랜잭션 2: 물리유기화학 1975, 페이지 15-18. 도이:10.1039/P29750000015
- ^ Peter J. Taormina "미생물 식품 안전성에 대한 소금과 나트륨 감소의 시사점, 2010, vol. 50, 209-227. doi:10.1080/10408391003626207