순환 이분법
Circular dichroism원편광(circular dichroism, CD)은 원편광, 즉 왼손과 오른손 빛의 [1][2]차동 흡수를 포함하는 이분법이다.왼쪽 원형(LHC)과 오른쪽 원형(RHC) 편광은 광자에 대해 두 가지 가능한 스핀각 운동량 상태를 나타내므로 원형 이색성은 스핀각 운동량에 [3]대한 이분법이라고도 합니다.이 현상은 19세기 [4]전반 장밥티스트 비오, 오귀스틴 프레넬, 아이메 코튼에 의해 발견되었다.원형 이색성과 원형 복굴절은 광학 활동의 징후이다.그것은 광학적으로 활성화된 키랄 분자의 흡수 대역에 나타난다.CD 분광법은 다양한 분야에서 광범위하게 응용되고 있다.특히 UV CD는 단백질의 [5]2차 구조를 조사하는데 사용된다.UV/Vis CD는 전하 전달 [6]전이를 조사하는 데 사용됩니다.근적외선 CD는 금속 d→d [2]전이를 프로빙하여 기하학적 및 전자적 구조를 조사하는 데 사용됩니다.적외선 에너지 영역의 빛을 사용하는 진동 원형의 이분법은 작은 유기 분자와 가장 최근에는 단백질과 [5]DNA의 구조 연구에 사용됩니다.
물리 원리
빛의 원형 편광
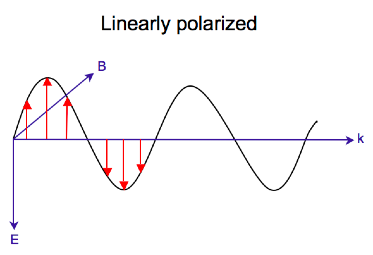
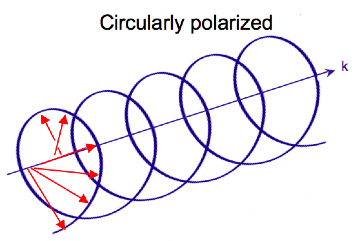
전자기 복사는 서로 수직 및 전파 [7]방향에 대해 진동하는 전기 style 및 B\display\ 장으로 구성됩니다.전계 벡터가 한 면에서만 진동할 때 직선 편광이 발생하는 반면, 원편광은 벡터가 일정한 크기를 유지한 상태에서 전계 벡터의 방향이 전파 방향으로 회전할 때 발생한다.공간의 한 지점에서 원형 편광 벡터는 파동 주파수의 한 주기에 걸쳐 원을 추적합니다. 따라서 이름은 다음과 같습니다.아래 두 그림은 일정한 위치에 대해 한 순간에 직선 및 원편광의 전계 벡터를 보여줍니다. 원편광된 전기 벡터의 플롯은 방향을 따라 나선을 형성합니다 style \ bold 。프로파(left circular pariplymbol {k} 。관찰자를 향한 회전, 전기 벡터는 시계 [2]반대 방향으로 회전합니다.우측 원편광(RCP)의 경우 전기 벡터는 시계 방향으로 회전합니다.
원편광과 물질의 상호작용
원편광은 흡수광학적 활성매체를 통과할 때 오른쪽 편광과 왼쪽 편광 사이의 속도( L R \ c{ \ mathrm L } 와 파장( L \ \ { L 이 .) 및 흡수 범위( 「 R\ \ _ { \ {} } \ \ _ { \ { ) 。원형 이색성은 차이 L- R \_{\{L_{\[5]입니다.광빔의 전기장은 분자(전기 쌍극자)와 상호작용할 때 전하의 선형 변위를 일으키는 반면, 자기장은 전하 순환(자기 쌍극자)을 일으킵니다.이 두 가지 운동이 결합하면 나선 운동에서 전자가 들뜨게 되며, 여기에는 변환과 회전 및 관련 연산자가 포함된다.시료의 R R과 사이의 실험적으로 결정된 관계는 다음과 같다.
회전 강도 또한 이론적으로 결정되었다.
이 2개의 방정식에서 0이 아닌 를 가지기 위해 전기 및 자기 쌍극자 모멘트 (M^ ( c . i { { \ { ( . dipole ) } } } m m m ( m( m^ ) ( ) 。_{(은(는) 동일한 축소 불가능한 표현으로 변환해야 합니다. \C} _ 및 (\은 키랄 분자 CD만 활성 상태로 만들 수 있는 점 그룹입니다.
간단히 말해서, 원형 편광 자체가 "키랄"이기 때문에, 그것은 키랄 분자와 다르게 상호작용합니다.즉, 두 종류의 원편광은 서로 다른 범위로 흡수됩니다.CD 실험에서 선택된 파장의 동일한 양의 좌우 원편광을 교대로 (키랄) 시료에 조사한다.두 편파 중 하나가 다른 편파보다 더 많이 흡수되고, 이 파장의존 흡수차가 측정되어 시료의 CD 스펙트럼이 된다.분자와의 상호작용에 의해 빛의 전계 벡터는 시료를 통과한 후 타원 경로를 추적한다.
분자의 키랄리티가 구조적인 것이 아니라 입체구조적인 것일 수 있다는 것이 중요하다.즉, 예를 들어 나선형 2차 구조를 가진 단백질 분자는 배열의 변화에 따라 변화하는 CD를 가질 수 있다.
델타 흡광도
정의상
여기서 A는 왼쪽 원편광(LCP)과 오른쪽 원편광(RCP) 빛의 흡광도 차이(일반적으로 측정)입니다.A)는 파장의 함수이므로 측정의 의미가 있으려면 수행한 파장을 알아야 .
몰 원형 이색성
맥주의 법칙을 적용하여 다음과 같이 나타낼 수도 있습니다.
어디에
- \ displaystyle \ _ { \ { L and r R \displaystyle \ _ { \ { R } the 、 LCP 및 RCP 빛의 몰 소광계수이다.
- C는 몰 농도입니다.
- l은 센티미터(cm) 단위의 경로 길이입니다.
그리고나서
어금니 원형의 이색성이죠이 본질적인 특성은 보통 물질의 원형 이색성이 의미하는 것이다. { \ \은 파장의 함수이므로 몰 원형 이색성 값({\ \ \\ 은 유효한 파장을 지정해야 합니다.
원형 이색성에 대한 외인성 효과
아래에서 논의된 것처럼, 원형 이색성(CD)의 많은 실제 적용에서, 측정된 CD는 단순히 분자의 고유 특성이 아니라 분자 구조에 의존한다.이러한 경우 CD는 온도, 농도 및 용제를 포함한 화학적 환경의 함수일 수도 있습니다.이 경우 CD 값이 의미를 가지려면 다른 관련 요소도 지정해야 합니다.
2중 회전대칭이 결여된 질서 있는 구조에서는 원편파의 차동전달[10](및[11] 반사)을 포함한 광학활동도 [8][9]재료를 통한 전파방향에 따라 달라진다.이 경우, 이른바 외인성 3d 키랄리티는 광빔과 구조의 상호 방향과 관련이 있습니다.
몰 타원율
으로 A \ A가 측정되지만, 과거 이유로 대부분의 측정은 타원도로 보고됩니다.몰 타원율은 농도에 대해 보정된 원형 이색성이다.몰 원형 이색성과 몰 타원성 [\theta은 다음 방정식으로 쉽게 상호 변환됩니다.
이 관계는 편광의 타원성을 다음과 같이 정의함으로써 도출됩니다.
어디에
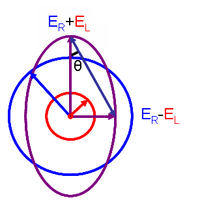
- 및 L은 각각 우원 편광의 전계 벡터의 크기이다.
R{\ 이E L {\E_{\{L과 같을 때(좌측 원편광의 흡광도에 차이가 없을 때) {\은 0°이고 직선으로 편광한다. EL(\E_{ 중 가 0일 때(원편광의 한 방향 흡수가 완전히 이루어졌을 때)(\})는 45°이고 원편광은 원편광이다.
일반적으로 원형 이색 효과가 작기 에 tan { \\}는 작으며 라디안에서는 { \}로 근사할 수 있습니다.빛의 강도 또는 조사 강도( I는 전계 벡터의 제곱에 비례하므로 타원은 다음과 같습니다.
그런 다음 자연 로그 형식의 맥주의 법칙을 I로 대체하면 다음과 같습니다.
이제 타원률은 다음과 같이 쓸 수 있습니다.
A1 \ \ A \ 1, ≪ 、 Taylor 시리즈의 지수를 1차까지 확장한 후 통일성과 비교하여 A \ \A의 항을 삭제하고 라디안에서 도수로 변환함으로써 이 식을 근사화할 수 있습니다.
용질 농도와 경로 길이의 선형 의존성은 몰 타원성을 다음과 같이 정의함으로써 제거된다.
그런 다음 마지막 두 식을 Beer의 법칙과 결합하면 몰 타원율은 다음과 같이 됩니다.
몰 타원의 단위는 과거(deg·cm2/dmol)입니다.몰 타원도를 계산하기 위해서는 시료농도(g/L), 세포경로(cm), 분자량(g/mol)을 알아야 한다.
샘플이 단백질인 경우 분자량 대신 평균잔기량(이 샘플에 포함된 아미노산잔기의 평균 분자량)이 사용되는 경우가 많아 기본적으로 해당 단백질을 아미노산 용액으로 취급한다.평균 잔기 타원성을 사용하면 분자량이 다른 단백질의 CD를 쉽게 비교할 수 있습니다. 이 표준화 CD의 사용은 단백질 구조에 대한 연구에서 중요합니다.
평균잔차타원성
특히 고분자, 단백질 및 폴리펩타이드에서 2차 구조를 추정하는 방법은 종종 측정된 몰 타원성 스펙트럼을 정규화된 값, 특히 고분자 길이에 독립적인 값으로 변환해야 한다.평균 잔기 타원성은 단순히 분자의 측정된 몰 타원성을 분자의 단량체 단위(잔기) 수로 나눈 것이다.
생물학적 분자에 대한 응용
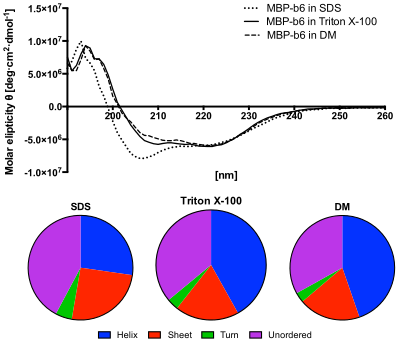
하부 패널:CDSTR 알고리즘을 사용하여 CD 스펙트럼에서 예측된 이차 구조의 함량.SDS 용액에 포함된 단백질은 무질서한 구조의 함량이 증가하고 헬리컬 [12]함량이 감소하는 것을 보여준다.
일반적으로 이 현상은 광학적으로 활성화된 분자의 흡수 대역에서 나타난다.그 결과 생물학적 분자는 덱스트로로타리와 레보로타리 성분을 가지기 때문에 원형 이색성을 보인다.더욱 중요한 것은 2차 구조가 각각의 분자에 독특한 CD를 제공한다는 것이다.따라서 단백질의 알파나선과 핵산의 이중나선은 그 구조를 대표하는 CD 스펙트럼 시그니처를 가진다.CD의 대표적인 구조적 특징을 제공하는 능력은 CD를 거의 모든 연구 분야에서 찾을 수 있는 응용 분야와 함께 현대 생화학에서 강력한 도구로 만듭니다.
CD는 광학회전분산(ORD) 기술과 밀접하게 관련되어 있으며 일반적으로 더 진보된 것으로 간주됩니다.CD는 관심 분자의 흡수 대역 또는 그 근처에서 측정되며, ORD는 이러한 대역에서 멀리 측정될 수 있다.CD의 장점은 데이터 분석에서 명백합니다.구조 요소는 기록된 대역이 ORD에서처럼 특정 파장에서 광범위하게 겹치지 않기 때문에 더 명확하게 구별됩니다.원칙적으로 모든 흡수가 측정에 포함되는 경우 이 두 스펙트럼 측정은 적분 변환(Kramers-Kronig 관계)을 통해 상호 변환될 수 있다.
단백질의 원 UV (자외선) CD 스펙트럼은 그들의 2차 구조의 중요한 특징을 드러낼 수 있다.CD 스펙트럼은 알파 나선 형태, 베타 시트 형태, 베타-턴 형태 또는 기타 (예: 랜덤 코일) [13][14][15][16]형태에 있는 분자의 분율을 추정하는 데 쉽게 사용할 수 있다.이러한 부분 할당은 단백질이 있을 수 있는 가능한 2차 구조에 중요한 제약을 가합니다.CD는 일반적으로 검출된 알파 나선이 분자 내에서 어디에 있는지 말할 수도 없고 심지어 얼마나 많은 나선이 있는지 완전히 예측할 수도 없다.그럼에도 불구하고 CD는 특히 구성의 변화를 보여주는 귀중한 도구입니다.예를 들어 온도 또는 변성제(예: 염화구아니디늄 또는 요소) 농도의 함수로서 분자의 2차 구조가 어떻게 변화하는지를 연구하는 데 사용될 수 있다.이러한 방법으로 분자에 대한 중요한 열역학 정보(엔탈피 및 깁스 변성의 자유 에너지 등)를 쉽게 얻을 수 없다.단백질을 연구하려는 사람은 CD가 광범위하고/또는 비용이 많이 드는 실험을 하기 전에 단백질이 본래의 형태인지 검증하는 귀중한 도구라는 것을 알게 될 것이다.또한 단백질 화학에서는 α-나선율 추정과 관련되지 않은 CD분광법에는 다른 많은 용도가 있다.게다가 CD분광학은 생물유기계면 연구에 사용되어 왔다.구체적으로는 공학적 단백질의 2차 구조 차이를 [17]시약으로 분석하기 위해 사용되어 왔다.
단백질의 근UV CD 스펙트럼(>250 nm)은 3차 구조에 대한 정보를 제공한다.250~300nm 영역에서 얻은 신호는 페닐알라닌, 티로신, 시스테인(또는 S-S 이황화물 브리지) 및 트립토판 아미노산의 흡수, 다이폴 배향 및 주변 환경의 특성 때문이다.원 UV CD와 달리 근 UV CD 스펙트럼은 특정 3D 구조에 할당할 수 없습니다.오히려 근UV CD 스펙트럼은 단백질, 예를 들어 헤모글로빈과 시토크롬 c의 헴 그룹에 대한 구조 정보를 제공한다.
가시 CD 분광법은 금속-단백질 상호작용을 연구하는 매우 강력한 기술이며 개별 d-d 전자 전이를 별도의 대역으로 해결할 수 있다.가시광선 영역의 CD 스펙트럼은 금속 이온이 키랄 환경에 있을 때만 생성되므로 용액 중의 유리 금속 이온은 검출되지 않는다.이것은 단백질 결합 금속만을 관찰할 수 있는 장점이 있기 때문에 pH의존성과 화학량계를 쉽게 얻을 수 있다.전이 금속 이온 복합체에서의 광학 활동은 구성, 배향 및 부차 효과에 기인한다.Klewpatinond와 Viles(2007)는 히스티딘 및 주쇄 배열을 포함하는2+ Cu 및 Ni 사각 평면 복합체에2+ 대한 가시 CD 스펙트럼의 출현을 예측하기 위한 경험적 규칙 세트를 작성했다.
예를 들어 CD는 X선 결정학 및 단백질 NMR 분광학보다 덜 구체적인 구조 정보를 제공하며, 둘 다 원자 분해능 데이터를 제공한다.그러나 CD 분광법은 많은 양의 단백질이나 광범위한 데이터 처리를 필요로 하지 않는 빠른 방법이다.따라서 CD를 사용하여 많은 용매 조건, 다양한 온도, pH, 염도, 다양한 보조 인자의 존재를 조사할 수 있습니다.
CD 분광법은 보통 용액 속의 단백질을 연구하는 데 사용되며, 따라서 고체 상태를 연구하는 방법을 보완합니다.이것은 또한 많은 단백질이 본래의 상태에서 막에 내장되어 있고 막 구조를 포함하는 용액이 종종 강하게 산란된다는 점에서 한계이다.CD는 박막으로 측정되기도 한다.
CD 분광법은 또한 생체 분자의 전자적 전환이 종종 일어나는 [18]UV 파장의 큰 신호들을 얻기 위해 TiO와2 같은 반도체 물질을 사용해 행해졌다.
실험 한계
CD는 탄수화물에서도 연구되었지만, 스펙트럼(100-200nm)의 진공 자외선(VUV) 영역에서의 CD 스펙트럼 측정과 관련된 실험 어려움 때문에 제한적인 성공을 거두었다.VUV 영역 이상의 밴드를 가진 치환 탄수화물이 성공적으로 측정되었습니다.
CD의 측정은 또한 전형적인 수성 버퍼 시스템이 원형 편광의 구조적 특징이 차등 흡수를 보이는 범위에서 종종 흡수하기 때문에 복잡합니다.인산염, 황산염, 탄산염 및 아세테이트 완충제는 예를 들어 10~50 mM 범위에서 극도로 희석되지 않는 한 일반적으로 CD와 호환되지 않는다.원UV CD를 실행할 때는 TRIS 버퍼 시스템을 완전히 피해야 합니다.붕산염과 오늄 화합물은 CD 실험에 적합한 pH 범위를 설정하기 위해 종종 사용된다.일부 실험자들은 먼 자외선에서 불소가 덜 흡수되기 때문에 염화물 이온 대신 불소를 대체했고, 다른 실험자들은 순수한 물에서 작용했다.거의 보편적인 또 다른 기법은 먼 UV에서 작업할 때 더 짧은 경로 길이 셀을 사용하여 용매 흡수를 최소화하는 것입니다. 이 작업에서는 0.1mm 경로 길이가 드물지 않습니다.
CD, 특히 원UV CD는 수계 측정뿐만 아니라 에탄올, 메탄올, 트리플루오로에탄올(TFE)과 같은 유기 용매에서도 측정할 수 있습니다.후자는 단백질의 구조 형성을 유도하여 일부에서는 베타 시트를 유도하고 다른 곳에서는 알파 헬리스를 유도하는 장점이 있는데, 정상적인 수성 조건에서는 나타나지 않는다.그러나 아세토니트릴, THF, 클로로포름, 디클로로메탄과 같은 대부분의 일반적인 유기 용제는 원UV CD와 호환되지 않습니다.
2차 구조 추정에 사용되는 단백질 CD 스펙트럼은 아미노산을 연결하는 아미드 결합의 δ ~ δ* 안와 흡수와 관련이 있을 수 있다.이러한 흡수 대역은 부분적으로 소위 진공 자외선(약 200 nm 미만의 파장)에 있습니다.관심 파장 영역은 실제로 공기 중에서 접근할 수 없습니다. 왜냐하면 이러한 파장에서 산소에 의한 빛의 강한 흡수 때문입니다.실제로 이러한 스펙트럼은 진공이 아니라 (순수 질소 가스로 채워진) 산소가 없는 기구에서 측정된다.
산소가 제거되면, 아마도 200 nm 이하에서 작업할 때 두 번째로 중요한 기술적 요소는 이 영역에서 손실을 줄이도록 나머지 광학 시스템을 설계하는 것입니다.이와 관련하여 중요한 것은 스펙트럼의 이 영역에서 낮은 손실을 위해 코팅이 최적화된 알루미늄 도금 미러의 사용이다.
이러한 계측기의 일반적인 광원은 고압의 짧은 아크 크세논 램프입니다.일반적인 제논 아크 램프는 낮은 UV에서 사용하기에 적합하지 않습니다.대신 고순도 합성 실리카로 만든 봉투가 있는 특수 제작된 램프를 사용해야 합니다.
싱크로트론 광원의 빛은 짧은 파장에서 훨씬 높은 플럭스를 가지며 CD를 160nm까지 기록하는 데 사용되어 왔습니다.2010년 덴마크 오르후스 대학의 전자 저장 링 시설 ISA의 CD 분광 광도계를 사용하여 120 [19]nm 이하의 고체 CD 스펙트럼을 기록했다.양자역학적 수준에서 원형 이색성과 광학회전의 특징밀도는 동일하다.광회전분산 및 원형이색성은 동일한 양자정보 내용을 공유한다.
「 」를 참조해 주세요.
레퍼런스
- ^ P. Atkins; J. de Paula (2005). Elements of Physical Chemistry (4th ed.). Oxford University Press. ISBN 978-0-7167-7329-0.
- ^ a b c Edward I. Solomon; A. B. P. Lever (3 February 2006). Inorganic electronic structure and spectroscopy. Wiley-Interscience. p. 78. ISBN 978-0-471-97124-5. Retrieved 29 April 2011.
- ^ 양자 이론 소개 2ED 데이비드 박 섹 2.2 페이지32 "빛의 편광은 전자 빔의 회전과 정확히 같은 종류이며, 역사적 발견 순서의 사고만을 반영하는 용어의 차이입니다."
- ^ Gerald D. Fasman (1996). Circular dichroism and the conformational analysis of biomolecules. Springer. pp. 3–. ISBN 978-0-306-45142-3. Retrieved 29 April 2011.
- ^ a b c Kōji Nakanishi; Nina Berova; Robert Woody (1994). Circular dichroism: principles and applications. VCH. p. 473. ISBN 978-1-56081-618-8. Retrieved 29 April 2011.
- ^ Solomon, Neidig; A. T. Wecksler; G. Schenk; T. R. Holman (2007). "Kinetic and Spectroscopic Studies of N694C Lipoxygenase: A Probe of the Substrate Activation Mechanism of a Non-Heme Ferric Enzyme". J. Am. Chem. Soc. 129 (24): 7531–7537. doi:10.1021/ja068503d. PMC 2896304. PMID 17523638.
- ^ Alison Rodger; Bengt Nordén (1997). Circular dichroism and linear dichroism. Oxford University Press. ISBN 978-0-19-855897-2. Retrieved 29 April 2011.
- ^ R. Williams (1968). "Optical Rotatory Effect in the Nematic Liquid Phase of p-Azoxyanisole". Physical Review Letters. 21 (6): 342. Bibcode:1968PhRvL..21..342W. doi:10.1103/PhysRevLett.21.342.
- ^ R. Williams (1969). "Optical-rotary power and linear electro-optic effect in nematic liquid crystals of p-azoxyanisole". Journal of Chemical Physics. 50 (3): 1324. Bibcode:1969JChPh..50.1324W. doi:10.1063/1.1671194.
- ^ Plum, E.; Fedotov, V. A.; Zheludev, N. I. (2008). "Optical activity in extrinsically chiral metamaterial" (PDF). Applied Physics Letters. 93 (19): 191911. arXiv:0807.0523. Bibcode:2008ApPhL..93s1911P. doi:10.1063/1.3021082. S2CID 117891131.
- ^ Plum, E.; Fedotov, V. A.; Zheludev, N. I. (2016). "Specular optical activity of achiral metasurfaces" (PDF). Applied Physics Letters. 108 (14): 141905. Bibcode:2016ApPhL.108n1905P. doi:10.1063/1.4944775.
- ^ Surma M.A.; Szczepaniak A.; Króliczewski J. (2014). "Comparative Studies on Detergent-Assisted Apocytochrome b6 Reconstitution into Liposomal Bilayers Monitored by Zetasizer Instruments". PLOS ONE. 9 (11): e111341. Bibcode:2014PLoSO...9k1341S. doi:10.1371/journal.pone.0111341. ISSN 1932-6203. PMC 4244035. PMID 25423011.
- ^ Hall V, Nash A, Rodger A (2014). "SSNN, a method for neural network protein secondary structure fitting using circular dichroism data" (PDF). Analytical Methods. 6 (17): 6721–26. doi:10.1039/C3AY41831F.
- ^ Hall V, Nash A, Hines E, Rodger A (2013). "Elucidating protein secondary structure with circular dichroism and a neural network". Journal of Computational Chemistry. 34 (32): 2774–86. doi:10.1002/jcc.23456. PMID 24122928. S2CID 19685126.
- ^ Whitmore L, Wallace BA (2008). "Protein secondary structure analyses from circular dichroism spectroscopy: methods and reference databases". Biopolymers. 89 (5): 392–400. doi:10.1002/bip.20853. PMID 17896349.
- ^ Greenfield NJ (2006). "Using circular dichroism spectra to estimate protein secondary structure". Nature Protocols. 1 (6): 2876–90. doi:10.1038/nprot.2006.202. PMC 2728378. PMID 17406547.
- ^ 바이오 무기 인터페이스:단백질 지향 나노물질 합성에 대한 역학적 연구(2016년 5월 5일).https://pubs.acs.org/doi/pdf/10.1021/acs.jpcc.6b02569에서 2019년 3월 1일 취득
- ^ Sarkar, Sumant, Ryan Behunin, 그리고 John G. Gibbs."모양 의존성, UV 활성 나노헬릭스 메타물질의 카이로 광학 반응"나노 레터(2019).https://pubs.acs.org/doi/10.1021/acs.nanolett.9b03274
- ^ U. Meierhenrich; J.J. Filippi; C. Meinert; J. H. Bredehöft; J. Takahashi; L. Nahon; N. C. Jones; S. V. Hoffmann (2010). "Circular Dichroism of Amino Acids in the Vacuum-Ultraviolet Region". Angew. Chem. Int. Ed. 49 (42): 7799–7802. doi:10.1002/anie.201003877. PMID 20845349.
외부 링크
- 상용 서비스 제공업체인 Alliance Protein Laboratories에 의한 원형 이색성 분광법
- 장비공급업체 Applied Photophysics에 의한 원형이색성분광학개론
- Valev 교수의 원형의 이색성과 광학 회전에 관한 단계별 애니메이션 튜토리얼.














 키랄 분자 CD만 활성
키랄 분자 CD만 활성 




 몰
몰

![{\displaystyle [\theta ]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e1456b03b038385e3bc52344dbf1a9bfbc41b4cf)
![[\theta] = 3298.2\,\Delta \varepsilon.\,](https://wikimedia.org/api/rest_v1/media/math/render/svg/c66e42a40570e3d3cb312c0eadd95d59170dc258)


 각각 우원 편광의
각각 우원 편광의  0°이고
0°이고  작으며
작으며 





![{\displaystyle [\theta ]={\frac {100\theta }{Cl}}\,}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ec21d26e0b12e81313ef0b42bbb5ec4f63369c3d)
![[\theta]= 100 \,\Delta \varepsilon \left( \frac {\ln 10}{4} \right) \left( \frac {180}{\pi} \right) = 3298.2\,\Delta \varepsilon \,](https://wikimedia.org/api/rest_v1/media/math/render/svg/88756c2cb3877d28ff0932ef432b0a5e4861ab58)

