전기화학적 경사
Electrochemical gradient전기화학적 구배는 전기화학적 전위의 구배이며, 일반적으로 막을 가로질러 이동할 수 있는 이온에 대한 것입니다.구배는 화학적 구배 또는 막 전체의 용질 농도 차이와 전기 구배 또는 막 전체의 전하 차이 두 부분으로 구성됩니다.투과성 막을 가로질러 이온 농도가 일정하지 않을 경우 이온은 단순한 확산을 통해 고농도 영역에서 저농도 영역으로 막 위를 이동한다.이온은 또한 막을 가로질러 전위를 형성하는 전하를 운반합니다.전하가 막 전체에 불균등하게 분포되어 있는 경우, 전위의 차이는 전하가 막의 양쪽에서 평형을 이룰 때까지 이온 확산을 촉진하는 힘을 발생시킵니다.
전기화학적 구배는 배터리와 다른 전기화학적 세포의 작동, 광합성과 세포 호흡, 그리고 특정한 다른 생물학적 과정에 필수적이다.
개요
전기화학적 에너지는 에너지를 보존할 수 있는 교환 가능한 많은 형태의 위치 에너지 중 하나입니다.전기 분석 화학에 나타나며 배터리 및 연료 전지 같은 산업적 응용 분야를 가지고 있습니다.생물학에서, 전기화학적 구배는 세포들이 이온이 막을 가로질러 이동하는 방향을 제어할 수 있게 한다.미토콘드리아와 엽록체에서, 양성자 구배는 ATP를 [1]합성하는데 사용되는 화학 삼투압 전위를 생성하고, 나트륨-칼륨 구배는 신경 시냅스가 정보를 빠르게 전달하는 것을 돕는다.
전기화학적 구배는 두 가지 요소로 구성되어 있습니다.막 전체의 전하 농도 차이와 동일한 막 전체의 화학종 농도 차이입니다.전자의 효과에서는, 집중된 전하가 반대 부호의 전하를 끌어당기고, 후자의 경우, 집중된 종은 균일한 농도로 막을 가로질러 확산되는 경향이 있다.이 두 현상의 조합에 의해 [2]: 403 [3]막을 가로지르는 이온의 움직임에 대해 열역학적으로 선호하는 방향이 결정됩니다.
결합된 효과는 열역학 전기화학 퍼텐셜의 구배로서 정량화할 수 있다: i i ( r ) + i ( ), { \ displaystyle \ \ } {} _ { i \ { } + z } { } .
때때로 "전기화학 퍼텐셜"이라는 용어는 이온 농도 구배에 의해 발생하는 전위, 즉 δ를 설명하기 위해 남용된다.이 기사는 그 관례를 따르지 않을 것이다.
전기화학적 구배는 수력발전 댐을 가로지르는 수압과 유사합니다.막에 의해 차단되지 않은 경로(예: 막 수송 단백질 또는 전극)는 물의 잠재적 에너지를 다른 형태의 물리적 또는 화학적 에너지로 변환하는 터빈에 해당하며, 막을 통과하는 이온은 하류 강으로 흐르는 물에 해당합니다.반대로, 댐 위의 호수에 물을 퍼 올리는 데 에너지를 사용할 수 있고, 전기 화학적 구배를 [4][5]만드는 데 화학 에너지를 사용할 수 있습니다.
화학
일반적으로 전기화학에서 이 용어는 화학반응의 열역학적 호감을 조절하기 위해 인가 전압 형태의 전기 에너지가 사용되는 경우에 적용됩니다.이온의 이동에 의해 발생하는 전기화학전위가 전극의 반응에너지를 평형화한다.배터리 반응이 생성할 수 있는 최대 전압을 해당 반응의 표준 전기화학적 전위라고 부르기도 합니다.
생물학적 맥락
세포막을 가로지르는 이온 이동을 통한 막 통과 전위의 생성은 신경 전도, 근육 수축, 호르몬 분비, 감각과 같은 생물학적 과정을 촉진합니다.관례상 생리전압은 세포외영역d에 대해 측정되며, 일반적인 동물세포는 내부전위가 (-70)–(-50)mV이다.[2]: 464
전기화학적 구배는 미토콘드리아 산화인산화에서 필수적이다.세포 호흡의 마지막 단계는 미토콘드리아 내부의 막에 내장된 4개의 복합체로 구성된 전자 전달 사슬이다.복합 I, III 및 IV는 매트릭스에서 막간 공간(IMS)으로 양성자를 펌프한다. 사슬에 들어가는 전자 쌍마다 10개의 양성자가 IMS로 이동한다.그 결과 200mV 이상의 전위가 발생합니다.기질로 돌아오는 양성자의 플럭스는 무기 인산염과 ADP를 [6][2]: 743–745 결합하기 위한 ATP 합성효소의 노력에 힘을 실어준다.
전자 전달 사슬과 유사하게, 광합성의 광의존적 반응은 ATP의 합성을 촉진하기 위해 엽록체의 틸라코이드 내강에 양성자를 펌프한다.양성자 구배는 비순환적 또는 순환적 광인산화를 통해 생성될 수 있다.비순환형 광인산에 관여하는 단백질 중 광계 II(PSII), 플라스티퀴논 및 시토크롬 bf6 복합체는 양성자 구배를 발생시키는 데 직접 기여한다.PSII에 의해 흡수된 4개의 광자에 대해 8개의 양성자가 내강에 [2]: 769–770 주입됩니다.
몇몇 다른 트랜스포터와 이온 채널은 양성자 전기화학적 구배를 발생시키는 역할을 한다.하나는3 TPK로, Ca에2+ 의해 활성화되어 전장 확립에 도움이 되는 틸라코이드 내강에서 스트로마까지 K를 전도합니다+.한편, 전기중립+ K배출방지장치(KEA3)는 K를 태엽내강으로, H를+ 스트로마로 운반하여+ pH구배를 [7]확립하는 데 도움이 된다.
이온 구배
이온은 대전되어 있기 때문에 단순한 확산으로는 세포막을 통과할 수 없습니다.두 가지 다른 메커니즘이 이온을 막을 가로질러 운반할 수 있습니다: 능동적 또는 수동적 운송.
이온의 활성 수송의 예로는 Na-K-ATPase(NKA)가 있습니다.NKA는 ATP를 ADP와 무기 인산염으로 가수분해함으로써 구동된다. 가수분해된 ATP의 분자당 3Na는+ 외부로 운반되고+ 2K는 세포 안으로 운반된다.이것은 세포 내부를 외부보다 더 음성으로 만들고 더 구체적으로 약 -60mV의 [5]막 전위membrane V를 생성한다.
수동 수송의 예로는 Na, K+, Ca2+ 및 Cl 채널을− 통과하는+ 이온 플럭스가 있습니다.능동수송과는 달리 수동수송은 삼투압(농도구배)과 전기장(막 통과전위)의 산술합에 의해 구동된다.형식적으로 성공적인 운송과 관련된 몰 깁스 자유 에너지 변화는
Na의+ 예에서 두 항 모두 수송을 지원하는 경향이 있는데, 세포 내부의 음전위가 양이온을 끌어당기고 Na가 세포 외부에 집중되기 때문에+ 삼투압은 Na 채널을+ 통해 세포 안으로 확산되는 것을 지원한다.K의 경우+, 외부 이온은 음의 세포내 전위에 의해 끌어당겨지지만, 엔트로피는 세포내에 이미 농축된 이온을 확산시키려 한다.역현상(삼투압은 수송을 지원하고 전위는 반대)은 비정상적인 막 통과 전위를 가진 세포에서 Na에 대해+ 달성될 수 있다. 즉, +70 mV에서는 Na 유입이+ 멈춘다. 높은 전위에서는 유출이 된다.
| 이온 | 포유동물 | 오징어 축삭 | 세레비시아에 | 대장균 | 바닷물 | ||
|---|---|---|---|---|---|---|---|
| 감방 | 피 | 감방 | 피 | ||||
| K+. | 100 - 140 | 4-5 | 400 | 10 - 20 | 300 | 30 - 300 | 10 |
| 나+ | 5-15 | 145 | 50 | 440 | 30 | 10 | 500 |
| Mg2+ | 10개 0.5~0.8 | 1 - 1.5 | 50 | 30 ~ 100 0.01 - 1 [b] | 50 | ||
| Ca2+ | 10개−4 | 2.2~2.6 1.3~1.5 | 10−4 - 3 × 10−4 | 10 | 2 | 3개 10개−4[b] | 10 |
| 클론− | 4 | 110 | 40 - 150 | 560 | 10 ~ 200 | 500 | |
| X−(음전하단백질) | 138 | 9 | 300 - 400 | 5-10 | |||
| HCO3− | 12 | 29 | |||||
| pH | 7.1~7[12].3 | 7.35 ~ 7.45 (정상 동맥혈 pH) 6.9 ~ 7.8 (표준 범위) | 7.2~7[13].8 | 8.1~8[14].2 | |||
양성자 구배
특히 양성자 구배는 에너지 저장의 한 형태로 많은 유형의 세포에서 중요하다.구배는 보통 ATP 합성효소, 편모 회전 또는 대사물 [15]수송을 촉진하는 데 사용됩니다.이 절에서는 각각의 세포에서 양성자 구배를 확립하는 데 도움이 되는 세 가지 과정에 초점을 맞출 것이다: 박테리올호돕신, 비순환형 광인산화, 산화적 인산화.
박테리어호돕신
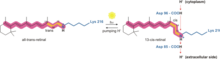
박테리어호돕신이 고고학에서 양성자 구배를 생성하는 방법은 양성자 펌프를 통해서이다.양성자 펌프는 양성자 운반체에 의존하여 H 농도가 낮은+ 막의 측면에서 H 농도가 높은+ 막의 측면으로 양성자를 이동시킵니다.568 nm 파장의 광자의 흡수에 의해 양성자 펌프가 활성화되어 K 상태를 형성하는 망막에서 쉬프 염기(SB)의 이성화를 일으킨다.그러면 SB가 Asp85 및 Asp212에서 멀어져 SB에서 Asp85로 H 전송되어+ M1 상태가 됩니다.그 후 단백질은 글루204와 글루194를 분리하여 M2 상태로 전환하고, 글루204에서 외부 배지로 양성자를 방출한다.SB는 N 상태를 형성하는 Asp96에 의해 재톤화됩니다.두 번째 양성자는 탈양성자 상태가 불안정하고 세포질의 양성자와 빠르게 재양성자되기 때문에 Asp96에서 나오는 것이 중요하다.Asp85와 Asp96의 양성자화는 O 상태를 형성하는 SB의 재이성화를 일으킨다.마지막으로, 박테리올호돕신은 Asp85가 양성자를 글루204로 [15][16]방출할 때 정지 상태로 돌아간다.
광인산화
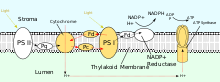
PSII는 또한 엽록체에서 양성자 구배를 형성하기 위해 빛에 의존하지만, PSII는 이 목표를 달성하기 위해 벡터 산화 환원 화학을 사용한다.단백질을 통해 양성자를 물리적으로 운반하는 대신, 양성자의 결합을 필요로 하는 반응은 세포 외 쪽에서 일어나는 반면 양성자의 방출을 필요로 하는 반응은 세포 내 쪽에서 일어날 것이다.680 nm 파장의 광자의 흡수는 P의680 두 전자를 더 높은 에너지 수준으로 자극하기 위해 사용된다.이러한 높은 에너지 전자는 단백질 결합 플라스토키논으로A 전달되고 그 후 결합 플라스토키논으로B 전달된다.이것은 플라스토퀴논(PQ)을 플라스토퀴놀(PQH2)로 환원시키고, 플라스토퀴놀(PQH)은 스트로마에서 두 개의 양성자를 얻은 후 PSII에서 방출된다.P의680 전자는 산소진화복합체(OEC)를 통해 물을 산화시킴으로써 보충된다.이것은 O와+ H를2 내강으로 방출하여 총 반응을[15] 일으킨다.
PSII에서 방출된 후2 PQH는 시토크롬 bf6 복합체로 이동하며, 시토크롬 bf 복합체는 PQH에서2 플라스토시아닌으로 두 개의 전자를 두 개의 개별 반응으로 전달합니다.발생하는 과정은 전자전달계의 복합체 III의 Q-사이클과 유사하다.첫 번째 반응에서 PQH는2 내강측 착체에 결합하고, 1개의 전자는 철황중심으로 전달되어 시토크롬 f로 전달되고, 그 후 플라스토시아닌으로 전달된다.두 번째 전자는 헴L b로 전달되고, 헴H b는 헴 b로 전달되며, 헴 b는 PQ로 전달된다.두 번째 반응에서는 두 번째 PQH가2 산화되어 다른 플라스토시아닌 및 PQ에 전자를 첨가한다.두 반응이 함께 4개의 양성자를 [2]: 782–783 [17]내강으로 전달합니다.
산화적 인산화
복합체 I(CI)는 환원 니코틴아미드 아데닌 디뉴클레오티드(NADH)로부터 2개의 전자가 전달됨으로써 유비퀴논(UQ)에서 유비퀴놀(UQH2)로의 환원을 촉매하고, 미토콘드리아 매트릭스에서 IMS로 [18]4개의 양성자를 이동시킨다.
복합 III(CII)는 Q 사이클을 촉매합니다.첫 번째 단계는 CI에 의해 감소된 UQH에서2 두 개의 전자가 Qo 부위에서 산화 시토크롬 c의 두 분자로 전달되는 것을 포함한다.두 번째 단계에서는 두 개의 전자가 Q 부위에서i UQ를 UQH로2 환원한다.전체 반응은 다음과 같습니다.[18]
복합 IV(CIV)는 CII로 환원된 시토크롬c에서 2개의 전자의 전이를 완전 산소의 절반으로 촉매한다.산화적 인산화에서 하나의 완전한 산소를 이용하려면 4개의 전자가 전달되어야 한다.산소는 매트릭스에서 4개의 양성자를 소비하여 물을 형성하고, 다른 4개의 양성자는 IMS로 펌핑하여 총 반응을[18] 일으킨다.
「 」를 참조해 주세요.
레퍼런스
- ^ Nath, Sunil; Villadsen, John (2015-03-01). "Oxidative phosphorylation revisited". Biotechnology and Bioengineering. 112 (3): 429–437. doi:10.1002/bit.25492. ISSN 1097-0290. PMID 25384602. S2CID 2598635.
- ^ a b c d e f Nelson, David; Cox, Michael (2013). Lehninger Principles of Biochemistry. New York: W.H. Freeman. ISBN 978-1-4292-3414-6.
- ^ Yang, Huanghe; Zhang, Guohui; Cui, Jianmin (2015-01-01). "BK channels: multiple sensors, one activation gate". Frontiers in Physiology. 6: 29. doi:10.3389/fphys.2015.00029. PMC 4319557. PMID 25705194.
- ^ Shattock, Michael J.; Ottolia, Michela; Bers, Donald M.; Blaustein, Mordecai P.; Boguslavskyi, Andrii; Bossuyt, Julie; Bridge, John H. B.; Chen-Izu, Ye; Clancy, Colleen E. (2015-03-15). "Na+/Ca2+ exchange and Na+/K+-ATPase in the heart". The Journal of Physiology. 593 (6): 1361–1382. doi:10.1113/jphysiol.2014.282319. ISSN 1469-7793. PMC 4376416. PMID 25772291.
- ^ a b Aperia, Anita; Akkuratov, Evgeny E.; Fontana, Jacopo Maria; Brismar, Hjalmar (2016-04-01). "Na+-K+-ATPase, a new class of plasma membrane receptors". American Journal of Physiology. Cell Physiology. 310 (7): C491–C495. doi:10.1152/ajpcell.00359.2015. ISSN 0363-6143. PMID 26791490.
- ^ Poburko, Damon; Demaurex, Nicolas (2012-04-24). "Regulation of the mitochondrial proton gradient by cytosolic Ca2+ signals" (PDF). Pflügers Archiv: European Journal of Physiology. 464 (1): 19–26. doi:10.1007/s00424-012-1106-y. ISSN 0031-6768. PMID 22526460. S2CID 18133149.
- ^ Höhner, Ricarda; Aboukila, Ali; Kunz, Hans-Henning; Venema, Kees (2016-01-01). "Proton Gradients and Proton-Dependent Transport Processes in the Chloroplast". Frontiers in Plant Science. 7: 218. doi:10.3389/fpls.2016.00218. PMC 4770017. PMID 26973667.
- ^ Philips, Ron Milo & Ron. "» What are the concentrations of different ions in cells?". Retrieved 2019-06-07.
- ^ Lodish, Harvey; Berk, Arnold; Zipursky, S. Lawrence; Matsudaira, Paul; Baltimore, David; Darnell, James (2000). "Table 15-1, Typical Ion Concentrations in Invertebrates and Vertebrates". www.ncbi.nlm.nih.gov. Retrieved 2019-06-07.
- ^ "The following table gives an idea of the intra and extra cellular ion concentrations in a squid axon and a mammalian cell". www.chm.bris.ac.uk. Retrieved 2019-06-07.
- ^ Diem K, Lenter C. Scientific Tables. Vol. 565 (Seventh ed.). Basel: Ciba-Geigy Limited. pp. 653–654. ISBN 978-3-9801244-0-9.
- ^ a b c Spitzer, Kenneth W.; Vaughan-Jones, Richard D. (2003), Karmazyn, Morris; Avkiran, Metin; Fliegel, Larry (eds.), "Regulation of Intracellular pH in Mammalian Cells", The Sodium-Hydrogen Exchanger: From Molecule to its Role in Disease, Springer US, pp. 1–15, doi:10.1007/978-1-4615-0427-6_1, ISBN 9781461504276
- ^ Slonczewski, Joan L.; Wilks, Jessica C. (2007-08-01). "pH of the Cytoplasm and Periplasm of Escherichia coli: Rapid Measurement by Green Fluorescent Protein Fluorimetry". Journal of Bacteriology. 189 (15): 5601–5607. doi:10.1128/JB.00615-07. ISSN 0021-9193. PMC 1951819. PMID 17545292.
- ^ Brewer, Peter G. (September 1, 2008). "Rising Acidity in the Ocean: The Other CO2 Problem". doi:10.1038/scientificamericanearth0908-22.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ a b c Gunner, M. R.; Amin, Muhamed; Zhu, Xuyu; Lu, Jianxun (2013-08-01). "Molecular mechanisms for generating transmembrane proton gradients". Biochimica et Biophysica Acta (BBA) - Bioenergetics. Metals in Bioenergetics and Biomimetics Systems. 1827 (8–9): 892–913. doi:10.1016/j.bbabio.2013.03.001. PMC 3714358. PMID 23507617.
- ^ Wickstrand, Cecilia; Dods, Robert; Royant, Antoine; Neutze, Richard (2015-03-01). "Bacteriorhodopsin: Would the real structural intermediates please stand up?". Biochimica et Biophysica Acta (BBA) - General Subjects. Structural biochemistry and biophysics of membrane proteins. 1850 (3): 536–553. doi:10.1016/j.bbagen.2014.05.021. PMID 24918316.
- ^ Schöttler, Mark Aurel; Tóth, Szilvia Z.; Boulouis, Alix; Kahlau, Sabine (2015-05-01). "Photosynthetic complex stoichiometry dynamics in higher plants: biogenesis, function, and turnover of ATP synthase and the cytochrome b 6 f complex". Journal of Experimental Botany. 66 (9): 2373–2400. doi:10.1093/jxb/eru495. ISSN 0022-0957. PMID 25540437.
- ^ a b c Sun, Fei; Zhou, Qiangjun; Pang, Xiaoyun; Xu, Yingzhi; Rao, Zihe (2013-08-01). "Revealing various coupling of electron transfer and proton pumping in mitochondrial respiratory chain". Current Opinion in Structural Biology. 23 (4): 526–538. doi:10.1016/j.sbi.2013.06.013. PMID 23867107.
- Campbell & Reece (2005). Biology. Pearson Benjamin Cummings. ISBN 978-0-8053-7146-8.
- Stephen T. Abedon, 오하이오 주립대학교 생물113의 "Campbell & Rece, 2002년 (1/14/2005) 제8장의 중요한 단어와 개념"