라이슈마니아
Leishmania| 라이슈마니아 | |
|---|---|
 | |
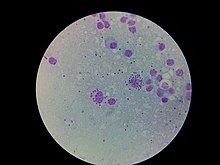
| 골수세포의 L. 도노바니 | |
| 과학적 분류 | |
| 도메인: | 진핵생물 |
| 문: | 유글레노조아목 |
| 클래스: | 키네토플라스테아목 |
| 주문: | 트리파노소마티다 |
| 속: | 라이슈마니아 보롭스키[1] 1898(Ross1903) |
| 종. | |
| 아에티오피카 | |
Leishmania /liːmeɪmeəni,, -æmén-/[2]는 기생충 원생동물이며, 트리파노솜속 단세포 유기체로 Leishmanias증을 [3][4][5]일으킨다.구세계에서는 Phlebotomus속, 신대륙에서는 Lutzomia속 모래파리에 의해 전파된다.전 [6]세계적으로 최소 93종의 모래파리들이 입증되었거나 추정된 벡터들이다.그들의 주요 숙주는 척추동물이다; 라이슈마니아는 보통 히락스, 개과, 설치류, 그리고 인간을 감염시킨다.
역사
피부 라이슈마니아증의 두드러진 증상에 대한 최초의 언급은 기원전 7세기 동양의 문헌들(기원전 1500년에서 2000년[7] 사이에 수백 년 더 오래된 출처에서 옮겨진 것으로 추정됨)에서 고생물학에서 나타났다.다양한 증상들이 나타나는 신비로운 질병으로 고대 내내 광범위하고 지속적인 유행으로 인해, 리슈마니아증은 "백색 나병"에서 "흑열"까지 다양한 이름으로 불려왔다.이 이름들 중 일부는 부정적인 문화적 신념이나 신화와의 연관성을 암시하는데,[8] 이는 오늘날에도 여전히 리슈마니아증이라는 사회적 오명을 낳고 있다.
리슈마니아 기생충의 고대 속인 고생레슈마니아는 백악기 [9]초의 화석화된 모래 파리에서 발견되었지만, 이 질병의 원인 물질은 1901년에 윌리엄 부그 리슈만과 찰스 도노반에 의해 동시 발견으로 발견되었다.그들은 감염된 인간 장기의 세포 내에 살고 있는 미세한 단세포 기생충(나중에 레이시만-도노반 몸체라고 불림)을 독립적으로 시각화했다.이 기생속은 나중에 계통학 명칭인 Leishmania donovani로 트리파노소마과 원생동물로 분류될 것이다.그 이후 몇몇 종들은 두 개의 주요 아속으로 분류되고 분류되었다.Leishmania Viannia(일반적으로 신트로픽스에 위치) 또는 Leishmania Leishmania(일반적으로 고생물군에 위치하지만 L. mexicana 하위군은 제외).
역학
라이슈마니아는 현재 98개국의 6백만 명의 사람들에게 영향을 미치고 있다.매년 약 90만-160만 건의 새로운 사례가 발생하며 21종의 질병이 인간에게 발생하는 것으로 알려져 있다: 그것은 동물병으로 여겨진다.
구조.
라이슈마니아종은 명확한 핵과 키네토플라스 및 편모를 포함한 다른 세포소기관을 가진 단세포 진핵생물이다.라이프 사이클의 단계에 따라 다음과 같은 [10][11]두 가지 구조적 변형이 존재합니다.
- 아마스티고테 형태는 인간의 단핵 식세포와 순환계에서 발견된다.그것은 세포 내 및 비운동성 형태이며, 외부 편모가 없다.짧은 편모는 돌출되지 않고 앞쪽 끝에 박혀 있다.그것은 타원형이고 길이는 3~6 µm, 폭은 1~3 µm이다.운동체와 기초체는 앞쪽 끝을 향해 놓여있다.
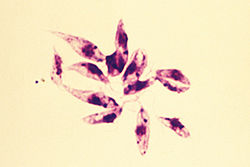
- 프로마스티고테의 형태는 모래파리의 소화관에서 발견된다.그것은 세포외의 운동성 형태이다.그것은 상당히 크고 매우 길며, 길이는 15-30 µm, 폭은 5 µm이다.방추형이며 양끝이 가늘어집니다.전단에 긴 편모(몸길이 정도)가 외부로 돌출되어 있다.핵은 중심에 있고, 그 앞에는 운동체와 기초체가 있다.
진화
이 속들의 진화에 대한 자세한 내용은 논의되고 있지만, 라이슈마니아는 명백히 조상들의 트리파노솜 혈통에서 진화한 것으로 보인다.가장 오래된 혈통은 보도나과의 혈통이며, 그 다음은 트리파노소마 브루시이며, 후자는 아프리카 대륙에 한정되어 있다.박쥐, 남미 포유류, 캥거루의 트리파노솜을 가진 트리파노소마 크루지 그룹은 남반구에서 유래한 것으로 보인다.이 군락들은 먼 친척일 뿐이다.
이 나무의 나머지 군락은 블라스토크리티디아, 허페토모나스, 피토모나스입니다.렙토모나스속, 크리티디아속, 레이슈마니아속, 엔도트리파눔속의 4개 속은 말단 가지를 형성하고 있어 비교적 최근의 기원을 짐작할 수 있다.이 속들 중 몇 개는 다계통일 수 있으며 더 많은 [12]분열을 필요로 할 수 있다.
라이슈마니아속의 기원은 불명확하다.[13][14]한 이론은 아메리카 대륙으로의 이주와 함께 아프리카 기원을 제안한다.다른 하나는 약 1500만년 전에 베링 해협 육교를 통해 아메리카 대륙에서 구세계로 이주할 것을 제안한다.세 번째 이론은 북극의 [15]기원을 제시한다.이러한 이동에는 벡터와 저장소의 후속 이동 또는 그 과정에서 연속적인 적응이 수반될 것이다.좀 더 최근의 이민은 유럽의 신대륙 식민지화 이후 지중해 국가에서 라틴 아메리카(L. chagasi로 알려져 있음)로의 L. inpantum의 이주이다.그곳에서 기생충들은 각각의 [16]생태계에서 현재의 신대륙 벡터를 얻었다.이것이 현재 명백한 전염병의 원인이다.최근 한 가지 신대륙 전염병은 [17]미국의 여우 사냥개에 관한 것이다.
라이슈마니아가 신생물학에서 [18]진화했을지도 모른다는 설이 제기되긴 했지만.이것은 아마도 비안니아 아속과 엔도트리파넘 아속에 속하는 종들에게 해당될 것이다.하지만, 라이슈마니아와 사우로라이슈마니아 하위의 일차적인 진화는 구세계라는 증거가 있다.반면 문디니아 종은 진화에 있어 더 보편적인 것으로 보인다.한 가지 이론은 다른 시기 동안 다른 혈통이 지리적으로 고립되었고 이것이 이러한 진화적 모자이즘을 낳았다는 것이다.그러나 Leishmaniinae가 단일통군이라는 것에는 의심의 여지가 없다.
대규모 데이터 세트 분석에 따르면 레이슈마니아는 9천만 [19]년에서 1억 년 전에 곤드와나에서 진화했다고 합니다.파충류를 감염시키는 종은 포유동물 군락에서 유래했다.
사우를레슈마니아 종은 원래 포유류가 아닌 파충류(라이저드)에 감염되었다는 것을 근거로 정의되었다.분자 증거에 근거해, 라이슈마니아내의 아속(亞種)으로 이동했다.이 아속은 아마도 원래 [20]포유류를 감염시킨 집단에서 진화했을 것이다.
분류법
53종이 알려져 있다.이들 중 몇 가지는 문제가 있기 때문에 최종 수치는 다를 수 있습니다.적어도 20종이 인간에게 감염된다.좀 더 복잡한 것은, 브라질에서 Leishmania (V.) Guyanensis (V.)와 Leishmania (V.) Shawi [21]shawi (V.)의 잡종과 함께 보고되었기 때문에 잡종이 관련되었을 수 있다.
이 속은 현재 라이슈마니아, 사우라이슈마니아, 문디니아, 비아니아 등 4개의 아속으로 분류되고 있다.두 아속(레이슈마니아와 비니아)으로 나눈 것은 1987년 Lainson과 Shaw가 곤충의 내장에 위치하는 것에 기초해 만들었다.비안니아 아속 종들은 뒷장에서 발달한다: L. (V.) braziliensis는 이 아속 종으로 제안되었다.이 구분은 이후의 모든 연구에서 확인되었습니다.쇼, 카마르고, 테이세이라는 2016년 [22]Leishmaniinae를 개정하면서 문디니아 아속(Mundinia)을 만들었다.
엔도트리파눔은 라이슈마니아와 밀접한 관련이 있다.일부 종들은 숙주(나무늘보)의 적혈구를 감염시킨다는 점에서 독특하다.모든 종은 중앙아메리카와 남아메리카에 [23]한정되어 있다.사람에게서 E.colombiensis 감염이 발견되었습니다.
Sauroleishmania는 원래 Ranquein 1973에 의해 별도의 속이라고 기술되었지만, 분자 연구는 이것이 사실 별도의 속이라기 보다는 하위 속이라는 것을 암시한다.
2000년에 제안된 레이슈마니아를 에를레슈마니아와 파랄레슈마니아 그룹으로 나누는 것은 기생충 사이의 깊은 계통 발생 거리를 강조했으며, 그 중 일부는 레이슈마니아 [24]종으로 명명되었다.Euleishmania는 현재 Leishmania, Sauroleishmania, Mundinia 및 Viannia 아속에 속하는 종을 포함하고 있다.제안된 Paraleyshmania에는 Endotypanum, Leishmamnia-L. colomubensis, L. herrei, L. hertigiand L. deani 및 L. equatorensis의 종이 포함되었다.최근 개정판에서는 이 종들은 서로 다른 일반적 지위를 부여받았다.
라이슈마니아의 4가지 아속(Leishmania, Sauroleishmania, Viannia 및 Mundinia, L. enriettii 복합체)이 현재 인식되고 있다.Endotrypanum과 Porcisia는 Paraleyshmania에 속합니다.
문디니아에는 4종류의 문디니아가 있다. - L. (Mundinia) 엔리엣티, L. (Mundinia) 마티니쿠엔시스, L. (Mundinia) 마크로포덤, 그리고 [25]태국에서 발견되는 L. (Mundinia) 오리엔탈리스.
L. Archibaldi의 구체적인 지위는 불확실하지만 L. donovani와 밀접한 관련이 있다.
L. herreri는 Leishmania가 아닌 Endotypanum속에 속합니다.
L. donovani와 L. inpantum은 밀접한 관련이 있다.
메모들
셀레노엔자임 셀트립은 이 [26]순서에 고유한 것으로 보입니다.그것은 비아니아아강에서 제거되었다.
고슴도치에 감염된 고슴도치는 모두 고슴도치속(Porcisia)으로 옮겨졌다.
분류
서브제너스 라이슈마니아 로스, 1903년 센수 사피아노바, 1982년
- 라이슈마니아에티오피카 Bray, Ashford & Bray, 1973년
- Leishmania amazonensis Lainson & Shaw, 1972년(가른하미 스콜자 외, 1979년 포함)
- 라이슈마니아 아라비카 피터스, 엘비하리 & 에반스, 1986년
- 라이슈마니아 아리스티데시 Lainson & Shaw, 1979년
- 라이슈마니아도노바니(라베란 & 메스닐, 1903년
- 레이슈마니아포라티니요시다, 쿠바, 파체코, 큐폴릴로, 타바레스, 마차도, 호멘 & 그리말디, 1993년
- 라이슈마니아저빌리왕취관, 1964년
- 1908년 라이슈마니아 인판텀 니콜레(차가시 쿠냐와 샤가스의 아종)
- 라이슈마니아 킬리키 Rioux, Lamotte & Pratlong, 1986년
- 큰라이슈마니아 야키모프 & 쇼호르, 1914년
- 라이슈마니아멕시카나 비아기, 1953년
- 라이슈마니아피파노이 메디나 & 로메로, 1959년
- 라이슈마니아 트로피카 (작가, 1903년
- 라이슈마니아투라니카 Strelkova, Shurkhal, Kellina, Eliseev, Evans, Peters, Chapman, Le Blancq & van Eys, 1990
- 라이슈마니아베네즐렌시스 본판테가리도, 1980년
- 라이슈마니아 월토니 Show, Pratlong & Dedet 2015
하위속 문디니아 쇼, 카마르고, 테세이라 2016
- 라이슈마니아엔리에티Muniz & Medina, 1948년
- 라이슈마니아 마크로포덤 Barratt, Kaufer, Peters, Craig, Lawrence, Roberts, Lee, McAulife, Stark, Ellis, 2017
- 라이슈마니아 마티니켄시스 데부아, 프랫롱, 퀴스트 및 디데, 2014[27]
- 리슈마니아 오리엔탈리스자리야판, 다룬툼, 자웅, 찬몰.인탁한, 소르수완, 시리야사티엔, 솜분, 베이츠, 2018년
서브제너스 사우를레슈마니아 랑케, 1973 sensu Saf'janova, 1982
- 라이슈마니아 아들레리 하이슈, 1958년
- 라이슈마니아 아가마에 1929년 데이비드
- 라이슈마니아 세라마닥틸리 아들러 & 테오도르, 1929년
- 라이슈마니아굴리카에 오베즈무카메도프 & 사피아노바, 1987년
- Leishmania nymodactyli kh Hodukin & Sofiev, 1940년
- 라이슈마니아 헬리오스코피 ch Chodukin & Sofiev, 1940년
- 라이슈마니아 반달팽이 Mackie, Gupta & Swaminath, 1923년
- 라이슈마니아후그스트랄리 맥밀런, 1965년
- 라이슈마니아니콜레이 Chodukin & Soffieff, 1940년
- 라이슈마니아 평판화살라 Telford, 2009
- 라이슈마니아인두증 Chodukin & Soffieff, 1940년
- 라이슈마니아 세네갈렌시스 랑케, 1973년
- 라이슈마니아 소피피 ↑ 마르코프, 루키나 & 마르코바, 1964년
- 라이슈마니아타렌톨레 1921년 원연
- 라이슈마니아 zmeevi ↑ 안드루치코 & 마르코프 1955
- 라이슈마니아 주커마니 Paperna, Boulard, Hering-Hagenbeck & Landau, 2001
↑ Sauroleishmania라고 하는 종.그들의 발달은 다른 아속 종들과 달라서 그들의 분류학적 위치가 의심스럽다.
서브제너스 비니아 레인슨 & 쇼 1987
- 라이슈마니아브라질렌시스 비안나, 1911년
- 라이슈마니아가야넨시스 플로치, 1954년
- 라이슈마니아린소니 실베이라, 쇼, 브라가 & 이시카와, 1987년
- 라이슈마니아린덴베르기 실베이라, 이시카와, 데소자 & 레이슨, 2002
- 라이슈마니아나이피 Lainson & Shaw, 1989년
- 라이슈마니아 파나멘시스 Lainson & Shaw, 1972년
- 라이슈마니아페루비아나 벨레스, 1913
- 라이슈마니아샤위 Lainson, Braga & de Souza, 1989년
- 라이슈마니아우팅엔시스 브라가, 레이슨, 이시카와 & 쇼 2003
관련속
이들 속과 라이슈마니아 간의 관계는 현재 불분명하지만 밀접하게 관련되어 있다.
엔도트리파넘속
- 콜롬비엔시스속 (Kreutzer, Corredor, Grimaldi, Grogl, Rowton, Young, Morales, McMahon-Pratt, Guzman & Tesh, 1991년)
- 내연균류 (그리말디, 크로이처, 하시구치, 고메트, 미모리 & 테쉬, 1992년)
- 내분지헤레리 (Zeledon, Ponce & Murillo, 1979년)
- 몬테로게이 내분비 쇼, 1969년
- 쵸우디니 메스닐과 브리몬트, 1908년
2016년 노비모나스 코스티고프 유르첸코속
- 노비모나스 에스메랄다스 보테프카, 코스티고프, 마슬로프, 루케시 2016
포르시시아쇼속, 카마르고속, 테이세이라속 2016
- 포르시시아데아네이 (레인슨 & 쇼 1977)
- 포치시아헤르티기 (1971년 양수인)
젤로니아쇼속, 카마르고속, 테이세이라속 2016
- 쯔로니아오스트랄리엔시스 Barratt, Kaufer, Peters, Craig, Lawrence, Roberts, Lee, McAulife, Stark, Ellis 2017
- 느티나무코스타리센시스 (유르첸코, 루케스, 지르쿠, 젤든, 마슬로프 2006)
생화학 및 세포생물학
라이슈마니아의 생화학 및 세포생물학은 다른 키네토플라스티드의 그것과 유사하다.그들은 동일한 형태학적 특징들을 공유한다: 기부에 침입자-편모 주머니-를 가진 단일 편모, 단일 미토콘드리아에서 발견되는 키네토플라스, 그리고 세포 골격의 주요 부분을 구성하는 미세관들의 아피질 배열.
리포포스포글리칸 코트
라이슈마니아는 세포 바깥쪽에 지방인산(liphosphopoglycan) 피막을 가지고 있다.리포포스포스포글리칸은 포유동물에서 선천적인 면역반응을 유발하는데 관여하는 신호수용체인 톨라이크 수용체2의 트리거이다.
리포포스포스포글리칸의 정확한 구조는 기생충의 종류와 라이프사이클 단계에 따라 다르다.글리칸 성분은 특히 가변적이며, 다양한 라이프사이클 단계에 대한 분자 마커로 다른 리포포스포스포글리칸 변형을 사용할 수 있다.서로 다른 글리칸과 결합하는 단백질의 그룹인 렉틴은 종종 이러한 리포포스포스포글리칸 변형을 검출하는데 사용된다.예를 들어, 땅콩 응집소는 L. major의 감염 형태 표면에서 발견되는 특정 리포포스포스포글리칸과 결합한다.
리포포스포글리칸은 기생충에 의해 숙주에서의 생존을 촉진하기 위해 사용되며 기생충이 숙주의 면역반응을 조절하는 것을 중심으로 하는 메커니즘에 의해 사용됩니다.라이슈마니아 기생충은 대식세포 내에 살고 대식세포가 그들을 죽이는 것을 막을 필요가 있기 때문에 이것은 매우 중요하다.리포포스포스포글리칸은 대식세포가 라이슈마니아 기생충에 감염되었음을 인식하는 보체계에 저항하여 산화폭발반응을 억제하고 염증반응을 유도하며 자연살해T세포를 방지하는 역할을 한다.
| 유형 | 병원체 | 위치 |
|---|---|---|
| 피부 리슈마니아증(국소적 및 확산성) 감염은 명백한 피부 반응으로 나타납니다. | 가장 흔한 것은 Oriental Sore입니다(구세계의 L. major, L. tropica, L. aethiopica에 의해 발생).신세계에서 가장 흔한 범인은 L. 멕시카나입니다. | 피부 감염은 아프가니스탄, 브라질, 이란, 페루, 사우디아라비아, 시리아에서 가장 흔하다. |
| 무코피부 리슈마니아 감염은 물린 곳의 반응으로 시작되어 점막으로의 전이에 의해 치명적일 수 있다. | 라오브라질리엔시스 | 무코피부 감염은 볼리비아, 브라질, 페루에서 가장 흔하다.중국 신장위구르자치구 카라메이에서도 무코피부 감염이 발견되고 있다. |
| 내장 리슈마니아증 감염은 발열, 간과 비장의 붓기, 빈혈 등으로 인식되는 경우가 많습니다.그들은 많은 지역 이름으로 알려져 있고, 그 중 가장 흔한 것은 아마 칼라 [28][29]아자르일 것이다. | L. donovani complex(L. donovani, L. inpantum syn)의 종에 의해서만 발생합니다.L. chagasi)[3] | 호주를 제외한 모든 대륙의 열대 및 아열대 지역에서 발견되는 내장 감염은 방글라데시, 브라질, 인도, 네팔, 그리고 [3]수단에서 가장 흔하다.내장 리슈마니아증은 쓰촨성, 간쑤성, 신장위구르자치구와 같은 중국의 일부 지역에서도 발견된다. |
감염의 세포내 메커니즘
면역 체계에 의한 파괴를 피하고 번영하기 위해, 라이슈마니아는 숙주의 세포 안에 숨는다.이 위치는 그것이 체액 면역 반응의 작용을 피할 수 있게 하고, 게다가 그것은 면역 시스템이 세포 자멸을 억제하는 비위험 표면 신호를 통해 숙주를 파괴하는 것을 막을 수 있습니다.라이슈마니아가 침투하는 1차 세포는 호중구와 [30]대식세포와 같은 식세포 세포이다.
보통, 대식세포와 같은 식세포 면역 세포는 밀폐된 엔도솜 안에 있는 병원체를 섭취하고 이 엔도솜을 병원체를 소화시키는 효소로 채울 것이다.그러나 라이슈마니아의 경우 이들 효소가 효과가 없어 기생충이 빠르게 증식할 수 있다.기생충의 이 억제되지 않은 성장은 결국 숙주 대식세포나 다른 면역세포를 압도하여 [31]죽게 만든다.
모래파리에 의해 전염되는 L. major 원생동물 기생충은 첫 번째 면역 방어 전략을 먹는 것/염증/죽이는 것/염증 없는 것/숙주 식세포를 죽이지 않는 것으로 전환하여 그들 [citation needed]자신의 이익을 위해 부패시킬 수 있다.그들은 자발적으로 식세포화하는 다형핵 호중구 과립구(PMNs)를 까다로운 은신처로 엄격하게 사용하며, 그곳에서 면역 체계에서 인식되지 않은 채 증식하고 "숨겨진" [citation needed]감염을 확립하기 위해 장수 대식세포에 들어갑니다.
흡수 및 생존
미생물 감염 시 PMN은 혈류에서 혈관 내피층을 통해 감염된 조직 부위(파리에 물린 후 피부 조직)로 이동합니다.그들은 즉시 첫 번째 면역 반응을 시작하고 기생충의 이물질과 활성 표면을 인식함으로써 침입자를 식세포화한다.활성화된 PMN은 특히 IL-8을 분비하여 과립구를 더 유인하고 식세포증을 자극합니다.또한 L. major는 PMN에 의한 IL-8의 분비를 증가시킨다.이 메커니즘은 다른 필수 세포내 기생충과의 감염 시에도 관찰된다.이러한 미생물의 경우, 여러 세포 내 생존 메커니즘이 존재합니다.놀랍게도, 아포토시스적이고 생존 가능한 병원균의 주입은 생존 가능한 기생충의 주입보다 훨씬 더 심각한 질병 과정을 야기한다.L. major는 아포토시스 세포에서 흔히 볼 수 있는 항염증 신호인 포스파티딜세린이 죽은 기생충의 표면에 노출되면 산화성 버스트를 꺼서 생균의 살상 및 열화를 방지한다.
라이슈마니아의 경우, 자손은 PMN에서 생성되지 않지만, 이러한 방법으로 그들은 살아남아 감염의 1차 부위에서 지속할 수 있다.프로마스티고테는 또한 라이슈마니아 화학요인(LCF)을 방출하여 단구나 NK 세포와 같은 다른 백혈구가 아닌 호중구를 활발하게 모집한다.또한 NK 및 Th1 세포 모집에 의한 염증 및 보호면역반응의 셧다운을 수반하는 라이슈마니아에 의해 PMNs에 의한 간섭 감마(IFN)) 유도단백질(IP10)의 생산이 차단된다.병원균은 그들의 일차 숙주인 PMN이 "병원체가 없다"는 신호를 보내는 아포토시스 세포 관련 분자 패턴(ACAMP)을 노출시키기 때문에 식세포증 동안 생존할 수 있다.
지속성과 매력
호중구 과립구의 수명은 매우 짧다.그들은 골수를 떠난 후 약 6시간에서 10시간 동안 혈류를 순환하며, 그 후 그들은 자발적인 아포토시스를 겪는다.미생물 병원균은 다른 전략으로 세포자멸에 영향을 미치는 것으로 보고되었다.분명히 caspase3-활성화의 억제 때문에 L. major는 호중구 아포토시스의 지연을 유도하고 최소 2~3일 동안 수명을 연장할 수 있다.이러한 기생충의 최종 숙주 세포가 대식세포이기 때문에 수명이 길어진다는 사실은 감염의 발달에 매우 유익하다. 대식세포는 보통 2, 3일 이내에 감염 현장으로 이동한다.그 병원균들은 단조롭지 않다; 대신에 그들은 1차 감염 부위에서 지휘권을 넘겨받는다.이들은 대식세포를 [32]모집하기 위해 케모카인 MIP-1α 및 MIP-1β(대식세포 염증 단백질)의 PMN에 의한 생성을 유도한다.
감염을 연장하는 중요한 요인은 적응 면역 시스템의 억제이다.이것은 특히 아마스티고테가 감염시킬 새로운 대식세포를 찾고 면역 반응에 더 민감할 때 세포간 단계에서 발생한다.거의 모든 종류의 식세포가 [33]대상이다.예를 들어 mincle은 L. major의 표적이 되는 것으로 나타났습니다.이 기생충에 의해 방출된 단백질과 민물과의 상호작용은 수상세포에서 [34]면역반응을 약화시킨다.
무성 식세포설
호중구에 포함된 독성 세포 성분 및 단백질 분해 효소로부터 주변 조직의 무결성을 구하기 위해 대식세포에 의해 아포토시스 PMN을 묵묵히 클리어한다.죽는 PMN은 아포토시스 동안 혈장막의 외부 리플릿으로 전달되는 "나를 먹어" 신호 포스파티딜세린을 노출시킨다.지연된 아포토시스 때문에 PMN에 잔류하는 기생충은 대식세포에 흡수되어 절대적으로 생리적, 비현상적 과정을 사용한다.이 "침묵적인 식세포증"의 전략은 기생충에게 다음과 같은 이점이 있습니다.
- 아포토시스 세포를 흡수하는 것은 대식세포 살상 활동을 억제하고 병원균의 생존을 이끈다.
- PMN 내부의 병원균은 아포토시스 세포 내부의 기생충을 볼 수 없기 때문에 대식세포 표면 수용체와 직접 접촉하지 않는다.그렇기 때문에 면역 활성화를 위한 식세포의 활성화는 일어나지 않습니다.
그러나 병원균이 아포토픽 세포를 떠나는 것으로 보여지고 이 방법에 의한 대식세포 흡수에 대한 증거가 알려져 있지 않기 때문에 연구는 이것이 가능성이 낮다는 것을 보여주었다.
분자생물학
라이슈마니아 원생동물의 중요한 측면은 리포포스포스포글리칸(LPG) 당결합층이다.이것은 포스포이노시티드막 앵커와 함께 유지되며, 지질 도메인, 중성 헥사당 및 인산화 갈락토오스-만노스로 구성된 삼원구조를 가지며 중성 캡에 종단된다.이들 기생충은 인두종 후 소화작용을 일으킬 뿐만 아니라 산화폭발에 필수적인 것으로 여겨져 감염 통로를 허용한다.세포 내 소화의 특징은 리소좀과 융합하여 DNA, RNA, 단백질 및 탄수화물을 분해하는 산성 가수분해효소 방출을 포함한다.
유전체학
라이슈마니아 4종(L. major, L. inpantum, L. donovani, L. braziliensis)의 게놈 배열을 분석하여 8300개 이상의 단백질 코드와 900개 이상의 RNA 유전자를 밝혀냈다.단백질 코드 유전자의 거의 40%는 2개에서 500개 사이의 구성원을 포함하는 662개 과로 분류된다.대부분의 작은 유전자 패밀리는 1개에서 3개의 유전자의 연속 배열이지만, 큰 유전자 패밀리는 종종 게놈 전체의 다른 위치에 연속 배열로 분산됩니다.35 또는 36개의 염색체 각각은 동일한 DNA 가닥에 있는 수십에서 수백 개의 유전자로 이루어진 소수의 유전자 클러스터로 구성되어 있다.이러한 클러스터는 tRNA, rRNA 및/또는 snRNA 유전자에 의해 종종 분리되는 머리 대 머리(분산) 또는 꼬리 대 꼬리(융합) 방식으로 구성될 수 있다.단백질 부호화 유전자의 전사는 유전자 클러스터 간의 발산 가닥 스위치 영역에서 양방향으로 개시되어 수렴 클러스터를 분리하는 가닥 스위치 영역에서 종료되기 전에 각 유전자 클러스터를 통해 다원적으로 확장된다.라이슈마니아 텔로미어는 보통 몇 가지 다른 유형의 반복 시퀀스로 구성되어 비교적 작습니다.텔로미어의 여러 다른 그룹들 사이의 재조합에 대한 증거를 찾을 수 있다.L. major 및 L. inpantum 게놈에는 비활성 변성 Ingi/L1Tc 관련 요소(DIRE) 약 50개만 들어 있으며, L. braziliensis는 또한 여러 텔로미어 관련 트랜스포저블 요소 및 스플라이스 리더 관련 레트로 요소도 포함되어 있다.라이슈마니아 게놈은 약 6200개의 유전자가 보존된 핵심 프로테옴을 관련 트리파노소마 브루스이, 트리파노소마 크루지와 공유하고 있지만 1000개 정도의 라이슈마니아 특이 유전자가 알려져 있어 대부분 게놈 전체에 랜덤하게 분포하고 있다.세 개의 배열된 라이슈마니아 게놈 사이에 유전자 함량에서 비교적 적은 종 고유의 차이가 존재하지만, 약 8%의 유전자가 세 종 사이에서 다른 속도로 진화하고 있는 것으로 보이며, 이는 질병과 관련될 수 있는 다른 선택압을 나타낸다.단백질 코드 유전자의 약 65%는 현재 기능적 [4]할당이 부족하다.
라이슈마니아 종은 몇 가지 다른 열충격 단백질을 생산한다.여기에는 Hsp90의 상동어인 Hsp83이 포함됩니다.Hsp83의 3' UTR 내의 조절 요소는 Hsp83의 변환을 온도에 민감하게 제어한다.이 영역은 높은 [35]온도에서 녹는 안정적인 RNA 구조를 형성합니다.
성적 생식
미생물 병원체의 생식 체계는 미생물의 생태와 질병 [36]확산을 조절하는 기본적인 생물학적 과정 중 하나이다.2009년 아코피안트 [37]외 연구진은 L. 메이저가 감수분열 과정을 포함한 성적 주기를 가지고 있다는 것을 입증했다.잡종 자손은 양쪽 부모로부터 완전한 게놈 보체를 가진 형태로 형성된다.짝짓기는 모래파리 벡터에서만 일어나며 잡종은 모래파리 물림에 의해 포유동물 숙주로 전염될 수 있다.L. braziliensis의 자연에서 성충은 주로 근친교배를 [38]초래하는 관련 개체들 사이에 있다.모래파리 벡터에서 다른 라이슈마니아 변종 간의 교잡 속도는 공동 감염 빈도에 따라 달라집니다.L. major와 [39]L. donovani에서는 이러한 교배 현상이 드문 것으로 보입니다.
L. inpantum은 상동 재조합 [40]수복을 촉진하기 위해 서로 상호작용하는 단백질 BRCA1과 RAD51을 생산한다.이 단백질들은 감수분열에서 중요한 역할을 한다.따라서 감수성 이벤트는 DNA[41] 손상의 효율적인 재조합 수복의 적응적 이점을 제공한다.
「 」를 참조해 주세요.
레퍼런스
- ^ Schnur, L. F (1989). "On the Clinical Manifestations and Parasites of Old World Leishmaniases and Leishmania Tropica Causing Visceral Leishmaniasis". In Hart, D. T. (ed.). Leishmaniasis. pp. 939–43. doi:10.1007/978-1-4613-1575-9_119. ISBN 978-1-4612-8862-6.
- ^ "leishmania". The Chambers Dictionary (9th ed.). Chambers. 2003. ISBN 0-550-10105-5.
- ^ a b c Ryan KJ; Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 749–54. ISBN 0-8385-8529-9.
{{cite book}}:author=범용명(도움말)이 있습니다.CS1 유지: 여러 이름: 작성자 목록(링크) - ^ a b Myler P; Fasel N (editors) (2008). Leishmania: After The Genome. Caister Academic Press. ISBN 978-1-904455-28-8.
{{cite book}}:author=범용명(도움말)이 있습니다.CS1 유지: 여러 이름: 작성자 목록(링크) - ^ Ansari MY, Equbal A, Dikhit MR, Mansuri R, Rana S, Ali V, Sahoo GC, Das P (Nov 2015). "Establishment of Correlation between In-Silico &In-Vitro Test Analysis against Leishmania HGPRT to inhibitors". International Journal of Biological Macromolecules. 83: 78–96. doi:10.1016/j.ijbiomac.2015.11.051. PMID 26616453.
- ^ WHO(2010) 연차 보고서.제네바
- ^ Cox, F. E. G (2002). "History of Human Parasitology". Clinical Microbiology Reviews. 15 (4): 595–612. doi:10.1128/CMR.15.4.595-612.2002. PMC 126866. PMID 12364371.
- ^ Yanik, M.; et al. (2004). "The psychological impact of cutaneous leishmaniasis". Clinical and Experimental Dermatology. 29 (5): 464–467. doi:10.1111/j.1365-2230.2004.01605.x. PMID 15347324. S2CID 11543741.
- ^ Poinar, G (2008). "Lutzomyia adiketis sp. n. (Diptera: Phlebotomidae), a vector of Paleoleishmania neotropicum sp. n. (Kinetoplastida: Trypanosomatidae) in Dominican amber". Parasit Vectors. 1 (1): 2. doi:10.1186/1756-3305-1-22. PMC 2491605. PMID 18627624.
- ^ "Morphology and Life Cycle". UCLA. Retrieved 24 January 2014.
- ^ Pulvertaft, RJ; Hoyle, GF (1960). "Stages in the life-cycle of Leishmania donovani". Transactions of the Royal Society of Tropical Medicine and Hygiene. 54 (2): 191–6. doi:10.1016/0035-9203(60)90057-2. PMID 14435316.
- ^ Hughes, AL; Piontkivska, H (2003). "Phylogeny of Trypanosomatidae and Bodonidae (Kinetoplastida) based on 18S rRNA: evidence for paraphyly of Trypanosoma and six other genera". Mol Biol Evol. 20 (4): 644–652. doi:10.1093/molbev/msg062. PMID 12679543.
- ^ Momen H, Cupolillo E (2000). "Speculations on the origin and evolution of the genus Leishmania". Mem. Inst. Oswaldo Cruz. 95 (4): 583–8. doi:10.1590/S0074-02762000000400023. PMID 10904419.
- ^ Noyes HA, Morrison DA, Chance ML, Ellis JT (2000). "Evidence for a neotropical origin of Leishmania". Mem. Inst. Oswaldo Cruz. 95 (4): 575–8. doi:10.1590/S0074-02762000000400021. PMID 10904417.
- ^ Kerr SF (2000). "Palaearctic origin of Leishmania". Mem. Inst. Oswaldo Cruz. 95 (1): 75–80. doi:10.1590/S0074-02762000000100011. PMID 10656708.
- ^ Kuhls, Katrin; Alam, Mohammad Zahangir; Cupolillo, Elisa; Ferreira, Gabriel Eduardo M.; Mauricio, Isabel L.; Oddone, Rolando; Feliciangeli, M. Dora; Wirth, Thierry; Miles, Michael A.; Schönian, Gabriele; Kamhawi, Shaden (7 June 2011). "Comparative Microsatellite Typing of New World Leishmania infantum Reveals Low Heterogeneity among Populations and Its Recent Old World Origin". PLOS Neglected Tropical Diseases. 5 (6): e1155. doi:10.1371/journal.pntd.0001155. PMC 3110170. PMID 21666787.
- ^ Duprey, Z. H.; Steurer, F. J.; Rooney, J. A.; Kirchhoff, L. V.; Jackson, J. E.; Rowton, E. D.; Schantz, P. M. (2006). "Canine Visceral Leishmaniasis, United States and Canada, 2000–2003". Emerging Infectious Diseases. 12 (3): 440–446. doi:10.3201/eid1203.050811. PMC 3291440. PMID 16704782.
- ^ Noyes, HA; Arana, BA; Chance, ML; Maingon, R (1997). "The Leishmania hertigi (Kinetoplastida; Trypanosomatidae) complex and the lizard Leishmania: their classification and evidence for a neotropical origin of the Leishmania-Endotrypanum clade". J Eukaryot Microbiol. 44 (5): 511–557. doi:10.1111/j.1550-7408.1997.tb05732.x. PMID 9304821. S2CID 27460253.
- ^ Harkins, Kelly M; Schwartz, Rachel S; Cartwright, Reed A; Stone, Anne C (2016). "Phylogenomic reconstruction supports supercontinent origins for Leishmania". Infection, Genetics and Evolution. 38: 101–9. doi:10.1016/j.meegid.2015.11.030. PMID 26708057.
- ^ Croan, David G; Morrison, David A; Ellis, John T (1997). "Evolution of the genus Leishmania revealed by comparison of DNA and RNA polymerase gene sequences". Molecular and Biochemical Parasitology. 89 (2): 149–59. doi:10.1016/S0166-6851(97)00111-4. PMID 9364962.
- ^ Jennings, Y. L.; de Souza, A. A. A.; Ishikawa, E. A.; Shaw, J.; Lainson, R.; Silveira, F. (2014). "Phenotypic characterization of Leishmania spp. causing cutaneous leishmaniasis in the lower Amazon region, western Pará state, Brazil, reveals a putative hybrid parasite, Leishmania (Viannia) guyanensis × Leishmania (Viannia) shawi shawi". Parasite. 21: 39. doi:10.1051/parasite/2014039. PMC 4118625. PMID 25083790.
- ^ Espinosa, O.A.; Serrano, M.G.; Camargo, E.P.; M.M.G., Teixeira; J.J., Shaw (2016). "An appraisal of the taxonomy and nomenclature of trypanosomatids presently classified as Leishmania' 'and' 'Endotrypanum". Parasitology. 145 (4): 430–442. doi:10.1017/S0031182016002092. PMID 27976601. S2CID 41544524.
- ^ Franco, AM; Grimaldi, G Jr (1999). "Characterization of Endotrypanum (Kinetoplastida: Trypanosomatidae), a unique parasite infecting the neotropical tree sloths (Edentata)". Mem Inst Oswaldo Cruz. 94 (2): 261–268. doi:10.1590/s0074-02761999000200026. PMID 10224540.
- ^ Momen, H; Cupolillo, E (2000). "Speculations on the origin and evolution of the genus Leishmania". Mem Inst Oswaldo Cruz. 95 (4): 583–588. doi:10.1590/s0074-02762000000400023. PMID 10904419.
- ^ Jariyapan, N; Daroontum, T; Jaiwong, K; Chanmol, W; Intakhan, N; Sor-Suwan, S; Siriyasatien, P; Somboon, P; Bates, MD; Bates, PA (2018). "Leishmania (Mundinia) orientalis n. sp. (Trypanosomatidae), a parasite from Thailand responsible for localised cutaneous leishmaniasis". Parasit Vectors. 11 (1): 351. doi:10.1186/s13071-018-2908-3. PMC 6006788. PMID 29914526.
- ^ Bonilla, Mariana; Krull, Erika; Irigoín, Florencia; Salinas, Gustavo; Comini, Marcelo A. (2016). "Selenoproteins of African trypanosomes are dispensable for parasite survival in a mammalian host". Molecular and Biochemical Parasitology. 206 (1–2): 13–19. doi:10.1016/j.molbiopara.2016.03.002. PMID 26975431.
- ^ Desbois, Nicole; Pratlong, Francine; Quist, Danièle; Dedet, Jean-Pierre (2014). "Leishmania (Leishmania) martiniquensis n. sp. (Kinetoplastida: Trypanosomatidae), description of the parasite responsible for cutaneous leishmaniasis in Martinique Island (French West Indies)". Parasite. 21: 12. doi:10.1051/parasite/2014011. ISSN 1776-1042. PMC 3952653. PMID 24626346.

- ^ 내장 리슈마니아증: 2005-04-28 Wayback Machine에서 아카이브된 질병
- ^ Kala-azar 2009-02-10 Wayback Machine에서 아카이브 완료.미국 유산 영어 사전
- ^ Vannier-Santos, MA; Martiny A; de Souza W. (August 2002). "Cell biology of Leishmania spp.: invading and evading". Current Pharmaceutical Design. 8 (4): 297–318. doi:10.2174/1381612023396230. PMID 11860368.
- ^ Paul, William E. (September 1993). "Infectious Diseases and the Immune System". Scientific American. 269 (3): 94–95. Bibcode:1993SciAm.269c..90P. doi:10.1038/scientificamerican0993-90. PMID 8211095.
- ^ Laskay T, et al. (2003). "Neutrophil granulocytes – Trojan horses for Leishmania major and other intracellular microbes?". Trends in Microbiology. 11 (5): 210–4. doi:10.1016/S0966-842X(03)00075-1. PMID 12781523.
- ^ Martínez-López M, et al. (2018). "Leishmania Hijacks Myeloid Cells for Immune Escape". Frontiers in Microbiology. 9: 883. doi:10.3389/fmicb.2018.00883. PMC 5949370. PMID 29867798.
- ^ Iborra S, et al. (2016). "Leishmania uses Mincle to target an inhibitory ITAM signaling pathway in dendritic cells that dampens adaptive immunity to infection". Immunity. 45 (4): 788–801. doi:10.1016/j.immuni.2016.09.012. PMC 5074365. PMID 27742545.
- ^ David, M; Gabdank, I; Ben-David, M; Zilka, A; Orr, I; Barash, D; Shapira, M (February 2010). "Preferential translation of Hsp83 in Leishmania requires a thermosensitive polypyrimidine-rich element in the 3' UTR and involves scanning of the 5' UTR". RNA. 16 (2): 364–74. doi:10.1261/rna.1874710. PMC 2811665. PMID 20040590.
- ^ Rougeron V, De Meeûs T, Kako Ouraga S, Hide M, Bañuls AL (2010). ""Everything you always wanted to know about sex (but were afraid to ask)" in Leishmania after two decades of laboratory and field analyses". PLOS Pathog. 6 (8): e1001004. doi:10.1371/journal.ppat.1001004. PMC 2924324. PMID 20808896.
- ^ a b Akopyants NS, Kimblin N, Secundino N, Patrick R, Peters N, Lawyer P, Dobson DE, Beverley SM, Sacks DL (April 2009). "Demonstration of genetic exchange during cyclical development of Leishmania in the sand fly vector". Science. 324 (5924): 265–8. Bibcode:2009Sci...324..265A. doi:10.1126/science.1169464. PMC 2729066. PMID 19359589.
- ^ Rougeron V, De Meeûs T, Hide M, Waleckx E, Bermudez H, Arevalo J, Llanos-Cuentas A, Dujardin JC, De Doncker S, Le Ray D, Ayala FJ, Bañuls AL (June 2009). "Extreme inbreeding in Leishmania braziliensis". Proc. Natl. Acad. Sci. U.S.A. 106 (25): 10224–9. Bibcode:2009PNAS..10610224R. doi:10.1073/pnas.0904420106. PMC 2700931. PMID 19497885.
- ^ Rogers MB, Downing T, Smith BA, Imamura H, Sanders M, Svobodova M, Volf P, Berriman M, Cotton JA, Smith DF (January 2014). "Genomic confirmation of hybridisation and recent inbreeding in a vector-isolated Leishmania population". PLOS Genet. 10 (1): e1004092. doi:10.1371/journal.pgen.1004092. PMC 3894156. PMID 24453988.
- ^ Genois MM, Mukherjee A, Ubeda JM, Buisson R, Paquet E, Roy G, Plourde M, Coulombe Y, Ouellette M, Masson JY (August 2012). "Interactions between BRCA2 and RAD51 for promoting homologous recombination in Leishmania infantum". Nucleic Acids Res. 40 (14): 6570–84. doi:10.1093/nar/gks306. PMC 3413117. PMID 22505581.
- ^ 번스타인 H, 버일리 HC, 홉프 FA, 미쇼드 RE유전적 손상, 돌연변이, 그리고 성의 진화.과학. 1985년 9월 20일;229(4719):1277-81. doi:10.1126/과학.3898363.PMID: 3898363
추가 정보
- Van Zandbergen, G; Bollinger, A; Wenzel, A; Kamhawi, S; Voll, R; Klinger, M; Muller, A; Holscher, C; Herrmann, M; Sacks, D; Solbach, W; Laskay, T (2006). "Leishmania disease development depends on the presence of apoptotic promastigotes in the virulent inoculum". Proceedings of the National Academy of Sciences. 103 (37): 13837–42. Bibcode:2006PNAS..10313837V. doi:10.1073/pnas.0600843103. PMC 1564231. PMID 16945916.
- 쇼, 제프리 존(1969년).나무늘보의 헤모플라겔라테스. H. K. 루이스: 런던.
- Ansari MY, Dikhit MR, Sahoo GC, Das P (2012). "Comparative modeling of HGPRT enzyme of L. donovani and binding affinities of different analogs of GMP". Int J Biol Macromol. 50 (3): 637–49. doi:10.1016/j.ijbiomac.2012.01.010. PMID 22327112.
외부 링크
- International Leishmania Network(ILN)는 질병에 대한 기본적인 정보를 가지고 있으며 질병의 많은 측면과 그 벡터에 연결되어 있다.
- 토론 목록(Leish-L)은 또한 분자 생물학자부터 공중 보건 종사자까지 국내외 많은 국가에서 600명 이상의 가입자가 이용할 수 있다.코멘트나 질문을 환영합니다.
- KBD: 키네토플라스티드 생물학과 질병은 리슈마니아증, 수면병, 샤가스병(미국 트리파노소마증)에 대한 전문 사이트입니다.이 문서에는 이러한 주제에 대한 전문 동료 검토 기사에 대한 무료 액세스가 포함되어 있습니다.이 사이트에는 독특한 키네토플라스티드 오가넬과 그 안에 있는 유전 물질에 관한 많은 기사가 있다.
- 리슈마니아 기생충의 성적 번식, "과학" 논문의 짧은 리뷰
- 라이슈마니아증 약물 검색 월드 커뮤니티 그리드