생체 재료
Biomaterial
생체 재료는 치료(신체의 조직 기능을 치료, 증강, 복구 또는 대체) 또는 진단 목적으로 생물학적 시스템과 상호작용하도록 설계된 물질입니다.과학적으로, 생체 재료는 50년 정도 되었다.생체 재료에 대한 연구는 생체 재료 과학 또는 생체 재료 공학이라고 불립니다.많은 기업들이 신제품 개발에 많은 돈을 투자하면서, 그 역사를 통해 꾸준하고 강력한 성장을 경험해 왔다.생체재료과학은 의학, 생물학, 화학, 조직공학 및 재료과학의 요소를 포함한다.
생체물질은 생체시스템에 의해 생성되는 뼈와 같은 생물학적 물질과는 다르다는 점에 유의하십시오.또한 생체소재는 용도에 따라 다르므로 생체적합성을 정의할 때 주의를 기울여야 한다.생체적합성이거나 한 용도에 적합한 생체소재는 다른 [1]용도에서는 생체적합성이 없을 수 있다.
서론
생체 재료는 자연에서 추출하거나 금속 성분, 폴리머, 세라믹 또는 복합 재료를 이용한 다양한 화학적 접근방식을 사용하여 실험실에서 합성할 수 있습니다.그것들은 종종 의료 애플리케이션에 사용 및/또는 적응되며, 따라서 자연 기능을 수행, 증강 또는 대체하는 생체 구조 또는 생물의학 장치의 전체 또는 일부를 구성한다.이러한 기능은 심장 판막에 사용되는 것과 같이 비교적 수동적일 수도 있고, 히드록시 아파타이트 코팅 고관절 삽입물과 같은 보다 상호작용적인 기능을 가진 생물 활성일 수도 있습니다.생체 재료는 또한 치과 응용, 수술, 약물 전달에 매일 사용된다.예를 들어 약품을 함침한 구조물을 체내에 넣을 수 있어 장기간 약물을 방출할 수 있다.생체소재는 자가이식재료로 사용되는 자가이식,[citation needed] 동종이식 또는 이종이식일 수도 있다.
생물 활동
생체물질의 기능과 성능을 뒷받침하는 생리적 반응을 유도하는 공학적 생체물질의 능력은 생체활동으로 알려져 있다.가장 일반적으로, 생체 활성 안경과 생체 활성 세라믹스에서 이 용어는 골전도성 또는 오서 생산적 [4]역할에서 주변 조직과 잘 결합하는 이식 물질의 능력을 의미한다.뼈 임플란트 재료는 종종 주변의 [5]체액에 녹으면서 뼈의 성장을 촉진하도록 설계된다.따라서 많은 생체 재료의 경우 우수한 강도 및 용해율과 함께 우수한 생체적합성이 바람직하다.일반적으로 생체물질의 생체활성은 표면에 히드록시아파타이트의 천연층이 형성된 표면 생물미네랄화에 의해 측정된다.오늘날, 임상적으로 유용한 생체 재료의 개발은 제한된 체외 [6]실험을 기반으로 치료 환경에서 생체 재료의 분자 효과를 예측할 수 있는 계산 루틴의 등장으로 크게 강화되고 있다.
자가 조립
자가조립은 외부 힘의 영향 없이 입자(atom, 분자, 콜로이드, 미셀 등)의 자발적 집단을 설명하기 위해 현대 과학계에서 가장 일반적으로 사용되는 용어이다.이러한 입자의 큰 그룹은 열역학적으로 안정적이고 구조적으로 잘 정의된 배열로 조립되는 것으로 알려져 있으며, 이는 야금학 및 광물학에서 발견되는 7가지 결정계 중 하나를 상당히 연상시킨다(예: 얼굴 중심 입방체, 체 중심 입방체 등).평형 구조의 근본적인 차이는 각각의 특정한 경우에 단위 셀의 공간적 스케일(latice parameter)에 있다.
분자 자가 조립은 생물학적 시스템에서 널리 발견되며 매우 다양한 복잡한 생물학적 구조의 기초를 제공합니다.여기에는 자연에서 발견된 미세구조적 특징과 디자인을 기반으로 하는 기계적으로 우수한 생체 소재의 새로운 클래스가 포함됩니다.이에 따라 자가조립도 화학합성 및 나노기술의 새로운 전략으로 부상하고 있다.분자 결정, 액정, 콜로이드, 미셀, 유화, 상분리 폴리머, 박막 및 자가조립 단분자층은 모두 이러한 기술을 사용하여 얻은 고순서 구조의 예를 나타냅니다.이러한 방법의 구별되는 특징은 자기 [7][8][9]조직화입니다.
구조 계층
공간적 규모의 변화는 변형과 손상의 다른 메커니즘을 야기하기 때문에 거의 모든 재료는 계층적으로 구조화된 것으로 볼 수 있다.그러나 생물학적 재료에서 이러한 계층적 구성은 미세 구조에 내재되어 있습니다.구조생물학의 역사에서 이것의 첫 번째 예 중 하나는 애스트버리와 [10]우즈의 머리카락과 모직의 계층 구조에 대한 초기 X선 산란 연구입니다.예를 들어 뼈에서 콜라겐은 직경 1.5nm의 삼중나선인 유기 매트릭스의 구성 요소이다.이러한 트로포콜라겐 분자는 섬유소를 형성하는 광물상(히드록시아파타이트, 인산칼슘)과 상호 작용하여 교대로 나선형으로 구부러집니다.이러한 "돌기"는 뼈의 기본 구성 요소이며, 유기물과 광물상 사이의 체적 비율 분포는 약 60/40입니다.
또 다른 복잡도 수준에서 히드록시아파타이트 결정은 직경이 약 70~100nm이고 두께가 1nm인 광물 혈소판이다.그들은 원래 콜라겐 [11]섬유 사이의 틈새에서 핵을 형성한다.
마찬가지로 전복 껍데기의 계층은 나노 수준에서 시작되며, 두께가 20~30nm인 유기층이다.이 층은 치수가 0.5인 "브릭스"로 구성되고 약 0.3mm(메소구조)[12] 층으로 마감되는 아라곤나이트(CaCO의3 다형)의 단결정으로 진행됩니다.
게는 절지동물로, 갑각류는 광물화된 단단한 성분(취약성 골절을 나타냄)과 주로 키틴으로 이루어진 부드러운 유기 성분으로 이루어져 있다.메짐성 구성 요소는 나선형 패턴으로 배열됩니다.이들 미네랄 '로드'(직경 1μm) 각각에는 약 60nm 직경의 키틴-단백질 섬유소가 함유되어 있다.이러한 섬유는 셸의 내부와 외부를 연결하는 3nm 직경의 관으로 구성되어 있습니다.
적용들
생체 재료는 다음 용도로 사용됩니다.
- 조인트 교환
- 골판
- 눈 수술용 안구내 렌즈(IOL)
- 본 시멘트
- 인공 인대 및 힘줄
- 치아 고정용 임플란트
- 혈관 보형물
- 심장 판막
- 피부수복장치(인공조직)
- 달팽이관 치환
- 콘택트 렌즈
- 가슴 이식
- 약물 전달 메커니즘
- 지속 가능한 재료
- 혈관 이식
- 스텐트
- 신경 도관
- 상처[14][15] 봉합용 외과적 봉합, 클립 및 스테이플
- 파단[16] 안정화용 핀 및 나사
- 외과용 메쉬[17][18]
생체 재료는 신체와 호환되어야 하며, 종종 생물학적 적합성의 문제가 있는데, 이는 제품이 시장에 출시되고 임상 환경에서 사용되기 전에 해결되어야 한다.이 때문에 생체 재료는 신약 [19][20]치료와 동일한 요구 조건을 받는다.또, 모든 제조회사는, 불량품이 발견되었을 경우, 같은 배치내의 다른 제품을 추적할 수 있도록, 모든 제품의 트레이서빌리티를 확보할 필요가 있습니다.
골이식
황산칼슘(α 및 β-반수화물)은 잘 알려진 생체적합성 물질로 치과에서 뼈 이식편 대체제 [21][22]또는 결합제로 널리 사용된다.
심장 판막
미국에서는 연간 250,000회의 밸브 교체 시술 중 49%가 기계식 밸브 임플란트와 관련되어 있습니다.가장 널리 사용되는 밸브는 담낭 디스크 심장 밸브 또는 St.주드 밸브이 기계장치에는 두 개의 반원형 디스크가 앞뒤로 움직이며, 혈액의 흐름을 허용하고 역류에 대한 봉인을 형성할 수 있는 능력이 있습니다.밸브는 열분해 탄소로 코팅되고 데이크론(Dacron, 폴리에틸렌 테레프탈레이트의 상표명)이라는 직물 메시로 주변 조직에 고정됩니다.메쉬를 통해 밸브와 [23][verification needed]함께 신체 조직이 성장할 수 있습니다.
피부 복구
대부분의 경우 인공조직은 환자 자신의 세포에서 배양된다.그러나 손상이 너무 심해 환자 자신의 세포를 사용할 수 없을 때는 인공 조직 세포를 배양한다.어려운 점은 세포가 성장하고 조직할 수 있는 골격을 찾는 것이다.비계의 특징은 생체적합성이 있어야 하며 세포는 비계에 부착할 수 있고 기계적으로 강하고 생분해성이 있어야 합니다.성공적인 골격 중 하나는 젖산과 글리콜산의 [23]공중합체이다.
생체 재료의 특성
앞서 논의한 바와 같이 생체 재료는 인체 내의 기능을 치료, 보조 또는 대체하기 위해 의료 기기에 사용됩니다.특정 생체 소재의 적용은 원하는 기능을 수행하기 위해 필요한 구성, 재료 특성, 구조 및 원하는 생체 내 반응을 결합해야 한다.기능적 [24][25]결과를 최대화하기 위해 다양한 원하는 속성의 분류가 정의됩니다.
호스트 응답
숙주 반응은 "임플란트 물질 또는 장치에 대한 숙주 유기체(국소 및 전신)의 반응"으로 정의됩니다.대부분의 물질은 인체에 닿으면 반응을 일으킨다.생체 물질의 성공은 숙주 조직이 이물질과 반응하는 것에 달려 있다.재료의 [25][26]생체적합성을 통해 숙주조직과 생체재료 간의 특이적 반응을 발생시킬 수 있다.
생체 물질과 조직의 상호 작용
이식 가능한 의료기기의 생체 내 기능 및 수명은 이물질에 [27]대한 신체의 반응에 영향을 받습니다.신체는 이물질로부터 호스트를 보호하기 위해 이물질 반응(FBR)에 따라 정의된 일련의 프로세스를 거칩니다.합병증 및 장치 고장을 방지하기 위해 호스트 조직/혈액뿐만 아니라 호스트 조직/혈액에 있는 장치 간의 상호 작용을 이해해야 합니다.
장치 삽입으로 인한 조직 손상은 FBR 중에 염증 및 치유 반응을 일으킵니다.염증반응은 급성기와 만성기의 두 가지 기간 내에 발생한다.급성 단계는 이식 초기 몇 시간에서 며칠 동안 발생하며 호중구 [28]반응과 함께 유체 및 단백질 삼출로 식별됩니다.급성기 동안, 몸은 과다한 혈액, 단백질, 그리고 단구들을 [29]전달함으로써 상처를 깨끗하게 하고 치유하려고 시도합니다.염증이 계속되면 단구, 대식세포,[28] 림프구의 존재로 분류할 수 있는 만성적인 단계로 이어진다.또한 상처 부위를 [30]치료하기 위해 혈관과 결합 조직이 형성된다.
호환성.
생체적합성(biocompatibility)은 다양한 화학적, 물리적 조건 하에서 다양한 환경에서 생체물질의 거동과 관련이 있다.이 용어는 소재의 사용 장소 또는 방법을 지정하지 않고 소재의 특정 특성을 나타낼 수 있습니다.예를 들어 물질은 특정 생물에서 면역반응을 거의 또는 전혀 유도하지 않을 수 있으며 특정 세포형 또는 조직과 통합될 수 있다.이 과정을 회피하기 보다는 면역 반응을 지시하는 면역 정보를 가진 생체 재료는 [31]가능성을 보여주는 한 가지 접근법이다.이 용어의 모호성은 "바이오소재가 인체와 상호작용하는 방법"에 대한 통찰력의 지속적인 발전을 반영하며, 결국 "그 상호작용이 (심박조율기 또는 고관절 치환과 같은) 의료 기기의 임상적 성공을 어떻게 결정하는지"를 나타낸다.현대의 의료 기기와 보형물은 종종 둘 이상의 재료로 만들어지기 때문에 특정 [32]재료의 생체 적합성에 대해 설명하는 것만으로는 충분하지 않을 수 있다.생체물질을 체내에 외과적으로 이식하는 것은 손상된 조직의 치유와 함께 유기 염증 반응을 일으킨다.이식된 재료의 구성, 임플란트 표면, 피로 메커니즘 및 화학적 분해에 따라 몇 가지 다른 반응이 가능합니다.이것들은 시스템뿐만 아니라 로컬일 수도 있습니다.여기에는 면역 반응, 혈관 결합 조직으로 임플란트를 분리한 이물질 반응, 감염 가능성 및 임플란트 수명에 미치는 영향이 포함됩니다.이식편 대 숙주 질환은 자가면역 및 동종면역 질환으로 다양한 임상 과정을 나타낸다.급성 또는 만성 형태로 나타날 수 있으며, 여러 장기 및 조직에 영향을 미치고 생체적합물질의 [33]이식 및 구현 중에 임상 실무에 심각한 합병증을 일으킬 수 있습니다.
독성
생체 소재는 다른 신체 조직과 장기에 부정적인 영향을 미치지 않고 생체 내에서 의도된 기능을 수행해야 한다.원치 않는 장기 및 조직의 상호작용을 방지하기 위해 생체 소재는 무독성이어야 합니다.생체물질의 독성은 생체내 물질에서 방출되는 물질을 말한다.생체 소재는 의도하지 않는 한 환경에 어떤 것도 방출해서는 안 된다.무독성은 생체물질이 비암생성, 비발열성, 비알레르기성, 혈액적합성, [34]비염증성이라는 것을 의미한다.그러나 생체물질은 의도된 목적을 위해 독성을 포함하도록 설계될 수 있다.예를 들어 독성 생체물질의 적용은 생체내 및 생체외 암 면역치료 테스트 중에 연구된다.독성 생체 재료는 암세포를 [35]조작하고 제어할 수 있는 기회를 제공한다.최근의 한 연구는 다음과 같이 말한다: "리포좀, 폴리머, 실리카를 포함한 첨단 나노 생물 물질은 약물과 면역 조절제의 공동 전달에 중요한 역할을 한다.이러한 나노 물질 기반의 전달 시스템은 항종양 면역 반응을 효과적으로 촉진하는 동시에 독성 부작용을 [36]줄일 수 있습니다."이것은 생체물질의 생체적합성이 원하는 기능을 생성하기 위해 어떻게 바뀔 수 있는지를 보여주는 좋은 예입니다.
생분해성 생체재료
생분해성 생체재료란 자연효소 반응을 통해 분해되는 물질을 말한다.생분해성 합성 고분자의 적용은 1960년대 [37]후반에 시작되었다.생분해성 물질은 장기적으로 유해한 영향을 미칠 위험이 낮기 때문에 다른 물질보다 유리합니다.생분해성 재료를 사용한 윤리적 진보와 더불어,[37] 이식 시 사용되는 재료의 생체적합성을 개선합니다.서로 다른 생분해성 생체소재를 고려할 때 생체적합성을 포함한 몇 가지 특성이 중요합니다.생분해성 생체 재료는 세포외 매트릭스(ECM)[38]의 소스 및 유형에 따라 합성 또는 천연이 될 수 있습니다.
생체 적합성 플라스틱
가장 일반적으로 사용되는 생체적합물질(또는 생체재료) 중 일부는 고유의 유연성과 조정 가능한 기계적 특성으로 인해 폴리머입니다.플라스틱으로 만들어진 의료 기기는 종종 고리형 올레핀 공중합체(COC), 폴리카보네이트(PC), 폴리에테르이미드(PEI), 의료용 폴리염화비닐(PVC), 폴리에틸렌(PEK), 폴리에테르술폰(PEK) 및 심지어 폴리프로필렌(PP)을 포함한 선택된 몇 개로 만들어진다.생체적합성을 보장하기 위해 재료 사용 인증을 통과해야 하는 일련의 규제 테스트가 있습니다.여기에는 미국 약사 IV(USP Class IV) 생물학적 반응성 테스트와 국제 표준 기구 10993(ISO 10993) 의료 기기의 생물학적 평가가 포함된다.생체적합성 시험의 주요 목적은 물질의 급성 및 만성 독성을 정량화하고 사용 조건 중 잠재적인 부작용을 결정하는 것이다. 따라서 해당 물질에 필요한 시험은 최종 사용(즉, 혈액, 중추신경계 등)[39]에 따라 달라진다.
지표면 및 벌크 속성
생체 재료의 기능에 큰 영향을 미치는 두 가지 특성은 표면 특성과 부피 [40]특성입니다.
벌크 특성은 생체 물질을 구성하는 물리적 및 화학적 특성을 말합니다.그것들은 물질이 대체하고 있는 조직의 물리화학적 특성을 모방하기 위해 특별히 생성될 수 있다.그것들은 물질의 원자 및 분자 구조에서 발생하는 기계적 특성입니다.
중요한 대량 속성:[41]
표면 특성은 숙주의 혈액/[42]조직과 직접적인 상호작용을 하는 생체물질 표면의 화학적 및 지형적 특징을 말합니다.표면 공학과 수정을 통해 임상의는 생체 물질과 숙주의 생체 시스템의 상호작용을 더 잘 제어할 수 있습니다.
중요한 지표면 특성:[43]
기계적 특성
생체재료는 생체적합성을 인증받을 뿐만 아니라 의료기기 내에서 대상 용도에 맞게 설계되어야 합니다.이것은 주어진 생체 물질이 작용하는 방식을 지배하는 기계적 특성 측면에서 특히 중요합니다.가장 관련성이 높은 재료 매개 변수 중 하나는 응력에 대한 재료의 탄성 반응을 설명하는 영 계수, E입니다.조직의 영 모듈리(Young's Moduli)와 결합되어 있는 장치는 장치를 이식하거나 외부에 장착하든 장치와 신체 간의 최적의 호환성을 위해 밀접하게 일치해야 합니다.탄성계수를 일치시키면 임플란트와 조직 사이의 생체 인터페이스에서의 움직임과 박리를 제한할 수 있을 뿐만 아니라 기계적 고장을 초래할 수 있는 응력 집중을 방지할 수 있습니다.다른 중요한 특성은 재료가 파손되기 전에 견딜 수 있는 최대 응력을 정량화하는 인장 및 압축 강도이며, 장치가 신체 내부 또는 외부에 적용될 수 있는 응력 한계를 설정하는 데 사용될 수 있다.용도에 따라서는 부하가 걸렸을 때 고장에도 견딜 수 있도록 높은 강도를 갖는 것이 바람직할 수 있지만, 다른 용도에서는 강도가 낮은 것이 유리할 수 있다.강도와 강성 사이에는 생체 재료 장치가 얼마나 강력한지 결정하는 신중한 균형이 있습니다.일반적으로 생체 소재의 탄성이 증가함에 따라 최종 인장 강도는 감소하며 그 반대도 마찬가지입니다.고강도 물질이 바람직하지 않은 한 가지 애플리케이션은 신경 프로브입니다. 이러한 용도에 고강도 물질이 사용되는 경우 경막 및 뇌 조직의 영 계수(Young's Modulus)가 약 500Pa이기 때문에 장치가 작동하기 전에 항상 조직이 고장납니다(부하 적용 시).이 경우 뇌에 돌이킬 수 없는 손상이 발생할 수 있으므로 생체물질은 뇌조직 이하의 탄성계수를 가져야 하며 가해지는 부하가 [45][46]예상될 경우 낮은 인장강도를 가져야 한다.
치과 임플란트와 같이 온도 변동을 겪을 수 있는 임플란트 생체 재료의 경우 연성이 중요합니다.재료는 인장 강도가 너무 높을 수 없는 유사한 이유로 연성이어야 하며, 연성은 재료가 파손 없이 구부러질 수 있도록 하며, 또한 온도 변화 시 조직의 응력 집중을 방지해야 합니다.인성의 재료 특성은 치과 임플란트뿐만 아니라 고관절 교체와 같은 단단하고 하중을 견디는 임플란트에도 중요합니다.인성(toughness)은 소재가 골절되지 않고 적용된 스트레스 하에서 변형될 수 있는 능력과 높은 인성을 갖는 것으로 생체 재료 임플란트가 신체 내에서 더 오래 지속될 수 있음을 나타냅니다. 특히 달리기 [45]중 고관절에 가해지는 스트레스와 같이 큰 스트레스나 주기적인 부하가 가해지는 스트레스에 시달릴 때 그렇습니다.
피부에 이식되거나 부착되는 의료기기의 경우 고려해야 할 또 다른 중요한 특성은 굽힘 강성 D이다.굽힘 강성은 장치 표면이 조직 표면과 얼마나 잘 일치하는지 결정합니다. 이는 특히 조직의 움직임(스트레인), 전기 신호(임피던스)를 측정하거나 표피 전자제품과 같이 박리 없이 피부에 부착되도록 설계된 장치에 중요합니다.굽힘 강성은 재료의 두께 h의 3제곱 h에3 따라 달라지기 때문에 앞에서 언급한 적합성이 [47]가장 중요한 용도에서는 생체소재를 얇은 층으로 형성할 수 있는 것이 매우 중요하다.
구조.
생체물질의 분자조성은 생체물질의 물리적, 화학적 특성을 결정한다.이러한 구성들은 생체 물질이 기능할 수 있도록 하는 복잡한 구조를 만들어내고, 따라서 생체 물질을 개발하기 위해 정의하고 이해하는 것이 필요하다. 생체 재료는 생체 [48]모방으로 알려진 과정인 자연 유기체를 복제하도록 설계될 수 있다.생체 재료의 구조는 재료의 특성과 기능을 더 잘 이해하기 위해 다양한 수준에서 관찰될 수 있습니다.
원자 구조
물질 내에서 원자와 이온의 배열은 생체 물질의 가장 중요한 구조적 특성 중 하나이다.물질의 원자 구조는 원자와 분자에 의해 만들어진 초구조뿐만 아니라 하위 원자 수준, 원자 수준 또는 분자 수준에서 볼 수 있습니다.물질을 구성하는 원자와 분자 사이의 분자간 힘이 물질의 물질과 화학적 [49]특성을 결정할 것이다.
하위 원자 수준은 개별 원자의 전기 구조를 관찰하여 다른 원자 및 분자와의 상호작용을 정의합니다.분자 구조는 물질 내 원자의 배치를 관찰한다.마지막으로 초구조는 물질의 원자 및 분자 구조에서 생성된 3차원 구조를 관찰합니다.물질의 고체 상태는 물질을 구성하는 원자와 분자 사이의 분자 내 결합에 의해 특징지어진다.분자 내 결합의 종류는 이온 결합, 공유 결합 및 금속 결합을 포함한다.이러한 결합은 재료의 물리적 및 화학적 특성과 재료의 유형(세라믹, 금속 또는 폴리머)을 결정합니다.
미세 구조
물질의 미세구조는 25배 [50]이상의 배율로 볼 때 물체, 생물 또는 물질의 구조를 말한다.곡류, 모공, 침전물 등의 형태, 크기, 분포의 다양한 단계로 구성되어 있습니다.대부분의 고체 미세구조는 결정성이지만, 특정 폴리머와 같은 일부 물질은 고체 [51]상태일 때 결정화되지 않습니다.
결정 구조
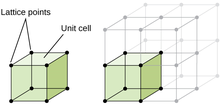
결정구조는 이온, 원자, 분자가 3D 형태로 결합되어 정렬된 구성이다.결정구조와 비정질구조 간의 주요 차이점은 구성 요소의 순서이다.결정체는 비정질 구조가 주문 [52]패턴의 요철로 이루어진 재료에서 가능한 한 높은 수준의 순서를 가진다.결정구조를 기술하는 한 가지 방법은 [53]격자로 표시된 구조에서 반복인자(단위세포)의 위치를 3차원으로 표현한 결정격자를 통과하는 것이다.결정 구조에는 14개의 서로 다른 원자 배열 구성이 있으며, 모두 Bravais Ratices로 [54]표현됩니다.
결정구조 결함
결정구조를 형성하는 동안 다른 불순물, 요철 및 기타 결함이 형성될 수 있습니다.이러한 결함은 고체, 급속 냉각 또는 고에너지 [55]방사선의 변형을 통해 형성될 수 있습니다.결점 유형에는 점 결점, 선 결점 및 모서리 이탈이 포함됩니다.
매크로 구조
매크로 구조는 파괴 시 힘, 강성, 굽힘, 응력 분포 및 재료의 무게에 영향을 미치는 전체적인 기하학적 특성을 말합니다.재료의 거시구조를 드러내는 데는 거의 또는 전혀 배율이 필요하지 않습니다.거시구조를 관찰하면 캐비티, 다공성, 가스 거품, 층화[disambiguation needed],[56] 균열 등의 특성이[disambiguation needed] 드러납니다.재료의 강도와 탄성률은 모두 매크로 구조와는 무관합니다.
천연 생체 재료
생체 재료는 인체 조직/오르간을 변경, 대체 또는 수리하기 위해 식물과 동물에서 공급되는 재료만을 사용하여 구성할 수 있습니다.천연 생체 재료의 사용은 고대 이집트부터 사용되었는데, 고대 이집트에서는 원주민들이 동물의 가죽을 봉합사로 사용했다.보다 현대적인 예는 1891년 독일에서 [57]최초로 기록된 상아 소재를 사용한 고관절 치환이다.
실행 가능한 천연 생체 재료의 중요한 기준:
천연 생체 재료의 예:
생체 고분자
생체 고분자는 생물에 의해 생성되는 중합체이다.셀룰로오스와 녹말, 단백질과 펩타이드, DNA와 RNA는 모두 생체고분자의 예이며, 단량체 단위는 각각 당, 아미노산, 뉴클레오티드이다.[60]셀룰로오스는 지구상에서 가장 흔한 생체 고분자이면서 가장 흔한 유기 화합물이다.식물성 물질의 약 33%가 [61][62]셀룰로오스이다.마찬가지로, 실크(단백질 생체 고분자)는 조직 공학 및 재생 의학, 미세 유체학, 약물 전달 [63][64]등 무수한 분야에서 엄청난 연구 관심을 얻고 있습니다.
「 」를 참조해 주세요.
각주
레퍼런스
- ^ Schmalz, G.; Arenholdt-Bindslev, D. (2008). "Chapter 1: Basic Aspects". Biocompatibility of Dental Materials. Berlin: Springer-Verlag. pp. 1–12. ISBN 9783540777823. Archived from the original on 9 December 2017. Retrieved 29 February 2016.
- ^ a b c d Vert, M.; Doi, Y.; Hellwich, K. H.; Hess, M.; Hodge, P.; Kubisa, P.; Rinaudo, M.; Schué, F. O. (2012). "Terminology for biorelated polymers and applications (IUPAC Recommendations 2012)". Pure and Applied Chemistry. 84 (2): 377. doi:10.1351/PAC-REC-10-12-04. S2CID 98107080.
- ^ Williams, D. F., ed. (2004). Definitions in Biomaterials, Proceedings of a Consensus Conference of the European Society for Biomaterials. Amsterdam: Elsevier.
- ^ Cao, Wanpeng; Hench, Larry (1996). "Bioactive Materials". Ceramics International. 22 (6): 493–507. doi:10.1016/0272-8842(95)00126-3.
- ^ Zhu, H.; et al. (2018). "Nanostructural insights into the dissolution behavior of Sr-doped hydroxyapatite". Journal of the European Ceramic Society. 38 (16): 5554–5562. arXiv:1910.10610. doi:10.1016/j.jeurceramsoc.2018.07.056. S2CID 105932012.
- ^ Ferreira, Marcel; Milano, Renato; Rangel, Elidiano; Peppelenbosch, Maikel; Zambuzzi, Willian (2020). "OsteoBLAST: Computational Routine of Global Molecular Analysis Applied to Biomaterials Development". Frontiers in Bioengineering and Biotechnology. 8: 565901. doi:10.3389/fbioe.2020.565901. PMC 7578266. PMID 33117780.
- ^ Whitesides, G.; Mathias, J.; Seto, C. (1991). "Molecular self-assembly and nanochemistry: A chemical strategy for the synthesis of nanostructures". Science. 254 (5036): 1312–9. Bibcode:1991Sci...254.1312W. doi:10.1126/science.1962191. PMID 1962191.
- ^ Dabbs, D. M.; Aksay, I. A. (2000). "Self-Assembledceramicsproduced Bycomplex-Fluidtemplation". Annual Review of Physical Chemistry. 51: 601–22. Bibcode:2000ARPC...51..601D. doi:10.1146/annurev.physchem.51.1.601. PMID 11031294.
- ^ Ariga, K.; Hill, J. P.; Lee, M. V.; Vinu, A.; Charvet, R.; Acharya, S. (2008). "Challenges and breakthroughs in recent research on self-assembly". Science and Technology of Advanced Materials. 9 (1): 014109. Bibcode:2008STAdM...9a4109A. doi:10.1088/1468-6996/9/1/014109. PMC 5099804. PMID 27877935.
- ^ Stroud, R. M. (2006). "Present at the flood: How structural biology came about, by Richard E. Dickerson". Protein Science. 16 (1): 135–136. doi:10.1110/ps.062627807. PMC 2222831.
- ^ Meyers, Marc A. (2014-07-31). Biological materials science : biological materials, bioinspired materials, and biomaterials. Chen, Po-Yu. New York. ISBN 978-1-107-01045-1. OCLC 869269337.
- ^ Pal, Subrata (2013-08-31). Design of Artificial Human Joints & Organs. Springer Science & Business Media. ISBN 978-1-4614-6255-2.
- ^ Ibrahim, H.; Esfahani, S. N.; Poorganji, B.; Dean, D.; Elahinia, M. (January 2017). "Resorbable bone fixation alloys, forming, and post-fabrication treatments". Materials Science and Engineering: C. 70 (1): 870–888. doi:10.1016/j.msec.2016.09.069. PMID 27770965.
- ^ Pillai, C. K. S.; Sharma, C. P. (2010). "Review Paper: Absorbable Polymeric Surgical Sutures: Chemistry, Production, Properties, Biodegradability, and Performance". Journal of Biomaterials Applications. 25 (4): 291–366. CiteSeerX 10.1.1.1013.5873. doi:10.1177/0885328210384890. PMID 20971780. S2CID 20278355.
- ^ Pillai CK, Sharma CP (Nov 2010). "Review paper: absorbable polymeric surgical sutures: chemistry, production, properties, biodegradability, and performance". J Biomater Appl. 25 (4): 291–366. CiteSeerX 10.1.1.1013.5873. doi:10.1177/0885328210384890. PMID 20971780. S2CID 20278355.
- ^ Waris, E; Ashammakhi, N; Kaarela, O; Raatikainen, T; Vasenius, J (December 2004). "Use of bioabsorbable osteofixation devices in the hand". Journal of Hand Surgery (Edinburgh, Scotland). 29 (6): 590–8. doi:10.1016/j.jhsb.2004.02.005. PMID 15542222. S2CID 24385943.
- ^ Deasis, F. J.; Lapin, B; Gitelis, M. E.; Ujiki, M. B. (2015). "Current state of laparoscopic parastomal hernia repair: A meta-analysis". World Journal of Gastroenterology. 21 (28): 8670–7. doi:10.3748/wjg.v21.i28.8670. PMC 4524825. PMID 26229409.
- ^ Banyard, D. A.; Bourgeois, J. M.; Widgerow, A. D.; Evans, G. R. (2015). "Regenerative biomaterials: A review". Plastic and Reconstructive Surgery. 135 (6): 1740–8. doi:10.1097/PRS.0000000000001272. PMID 26017603. S2CID 33728690.
- ^ Meyers, M. A.; Chen, P. Y.; Lin, A. Y. M.; Seki, Y. (2008). "Biological materials: Structure and mechanical properties". Progress in Materials Science. 53: 1–206. CiteSeerX 10.1.1.466.3753. doi:10.1016/j.pmatsci.2007.05.002.
- ^ Espinosa, H. D.; Rim, J. E.; Barthelat, F.; Buehler, M. J. (2009). "Merger of structure and material in nacre and bone – Perspectives on de novo biomimetic materials". Progress in Materials Science. 54 (8): 1059–1100. doi:10.1016/j.pmatsci.2009.05.001.
- ^ Zhao, Rusin; Yang, Ruijia; Cooper, Paul R.; Khurshid, Zohaib; Shavandi, Amin; Ratnayake, Jithendra (2021-05-18). "Bone Grafts and Substitutes in Dentistry: A Review of Current Trends and Developments". Molecules. 26 (10): 3007. doi:10.3390/molecules26103007. ISSN 1420-3049. PMC 8158510. PMID 34070157.
- ^ Thomas, Mark V.; Puleo, David A.; Al-Sabbagh, Mohanad (2005). "Calcium sulfate: a review". Journal of Long-Term Effects of Medical Implants. 15 (6): 599–607. doi:10.1615/jlongtermeffmedimplants.v15.i6.30. ISSN 1050-6934. PMID 16393128.
- ^ a b Brown, Theodore L.; LeMay, H. Eugene; Bursten, Bruce E. (2000). Chemistry The Central Science. Prentice-Hall, Inc. pp. 451–452. ISBN 978-0-13-084090-5.
- ^ "Chapter 4: Biomaterials: Basic principles". An Introduction to Biomaterials Science and Engineering. WORLD SCIENTIFIC. May 2021. pp. 82–93. doi:10.1142/9789811228186_0004. ISBN 978-981-12-2817-9. S2CID 240851982.
- ^ a b Badylak, Stephen F. (2015-05-08). Host Response to Biomaterials: The Impact of Host Response on Biomaterial Selection. Academic Press. ISBN 978-0-12-800500-2.
- ^ Williams, David F. (2008-07-01). "On the mechanisms of biocompatibility". Biomaterials. 29 (20): 2941–2953. doi:10.1016/j.biomaterials.2008.04.023. ISSN 0142-9612. PMID 18440630.
- ^ Morais, Jacqueline (2010). "Biomaterials/Tissue Interactions: Possible Solutions to Overcome Foreign Body Response". The AAPS Journal. 12 (2): 188–196. doi:10.1208/s12248-010-9175-3. PMC 2844517. PMID 20143194.
- ^ a b Rn, Mitchell (2003). "Acute and chronic inflammation". Robbins Basic Pathology.
- ^ Johnston, R. B. (1988-03-24). "Current concepts: immunology. Monocytes and macrophages". The New England Journal of Medicine. 318 (12): 747–752. doi:10.1056/NEJM198803243181205. ISSN 0028-4793. PMID 3279314.
- ^ Kovacs, E. J. (January 1991). "Fibrogenic cytokines: the role of immune mediators in the development of scar tissue". Immunology Today. 12 (1): 17–23. doi:10.1016/0167-5699(91)90107-5. ISSN 0167-5699. PMID 2015044.
- ^ Sridharan, Rukmani; Cavanagh, Brenton; Cameron, Andrew R.; Kelly, Daniel J.; O'Brien, Fergal J. (February 2019). "Material stiffness influences the polarization state, function and migration mode of macrophages". Acta Biomaterialia. 89: 47–59. doi:10.1016/j.actbio.2019.02.048. PMID 30826478. S2CID 73489194.
- ^ Kammula, Raju G.; Morris, Janine M. (May 1, 2001). "Considerations for the Biocompatibility Evaluation of Medical Devices". Medical Device & Diagnostic Industry.
- ^ Velnar, Tomaz; Bunc, Gorazd; Klobucar, Robert; Gradisnik, Lidija (2016). "Biomaterials and host versus graft response: a short review". Bosnian Journal of Basic Medical Sciences. 16 (2): 82–90. doi:10.17305/bjbms.2016.525. ISSN 1840-4812. PMC 4853000. PMID 26894284.
- ^ "Nanotechnology Applications for Tissue Engineering". ScienceDirect. Retrieved 2022-05-06.
- ^ Gu, Luo; Mooney, David J (January 2016). "Biomaterials and emerging anticancer therapeutics: engineering the microenvironment". Nature Reviews. Cancer. 16 (1): 56–66. doi:10.1038/nrc.2015.3. ISSN 1474-1768. PMC 4790726. PMID 26694936.
- ^ Yang, Fan; Shi, Kun; Jia, Yan-peng; Hao, Ying; Peng, Jin-rong; Qian, Zhi-yong (July 2020). "Advanced biomaterials for cancer immunotherapy". Acta Pharmacologica Sinica. 41 (7): 911–927. doi:10.1038/s41401-020-0372-z. ISSN 1745-7254. PMC 7468530. PMID 32123302.
- ^ a b Song, Richard; Murphy, Maxwell; Li, Chenshuang; Ting, Kang; Soo, Chia; Zheng, Zhong (2018-09-24). "Current development of biodegradable polymeric materials for biomedical applications". Drug Design, Development and Therapy. 12: 3117–3145. doi:10.2147/DDDT.S165440. ISSN 1177-8881. PMC 6161720. PMID 30288019.
- ^ Song, Richard; Murphy, Maxwell; Li, Chenshuang; Ting, Kang; Soo, Chia; Zheng, Zhong (2018-09-24). "Current development of biodegradable polymeric materials for biomedical applications". Drug Design, Development and Therapy. 12: 3117–3145. doi:10.2147/DDDT.S165440. ISSN 1177-8881. PMC 6161720. PMID 30288019.
- ^ Gad, Shayne Cox; Gad-McDonald, Samantha (2015-12-01). Biomaterials, Medical Devices, and Combination Products: Biocompatibility Testing and Safety Assessment. CRC Press. ISBN 978-1-4822-4838-8.
- ^ "what is a surface, why is surface analysis important". www.kratos.com. Retrieved 2022-05-06.
- ^ Zhang, Guigen; Viney, Christopher (2020-01-01), Wagner, William R.; Sakiyama-Elbert, Shelly E.; Zhang, Guigen; Yaszemski, Michael J. (eds.), "1.2.3 - Bulk Properties of Materials", Biomaterials Science (Fourth Edition), Academic Press, pp. 41–51, ISBN 978-0-12-816137-1, retrieved 2022-07-26
- ^ Roach, Paul; Eglin, David; Rohde, Kirsty; Perry, Carole C. (2007). "Modern biomaterials: A review—Bulk properties and implications of surface modifications". ResearchGate. 18 (7): 1263–1277. doi:10.1007/s10856-006-0064-3. PMID 17443395. S2CID 46254118.
- ^ Vogler, Erwin A. (2013). "Chapter 8 - Surface Modification for Biocompatibility". In Lakhtakia, Akhlesh; Martín-Palma, Raúl J. (eds.). Engineered Biomimicry. Boston: Elsevier. pp. 189–220. ISBN 978-0-12-415995-2.
- ^ "How surface roughness and wettability affects biocompatibility". www.biolinscientific.com. Retrieved 2022-05-06.
- ^ a b Saini, Monika; Singh, Yashpal; Arora, Pooja; Arora, Vipin; Jain, Krati (January 2015). "Implant biomaterials: A comprehensive review". World Journal of Clinical Cases. 3 (1): 52–7. doi:10.12998/wjcc.v3.i1.52. ISSN 2307-8960. PMC 4295219. PMID 25610850.
- ^ Lacour, Stéphanie P.; Courtine, Grégoire; Guck, Jochen (2016). "Materials and technologies for soft implantable neuroprostheses" (PDF). Nature Reviews Materials. 1 (10): 16063. Bibcode:2016NatRM...116063L. doi:10.1038/natrevmats.2016.63. ISSN 2058-8437.
- ^ Choi, Suji; Lee, Hyunjae; Ghaffari, Roozbeh; Hyeon, Taeghwan; Kim, Dae-Hyeong (June 2016). "Recent Advances in Flexible and Stretchable Bio-Electronic Devices Integrated with Nanomaterials". Advanced Materials. 28 (22): 4203–4218. doi:10.1002/adma.201504150. ISSN 0935-9648. PMID 26779680. S2CID 205264592.
- ^ Kuhn, Liisa T. (2005-01-01). "Chapter 6 - BIOMATERIALS". In Enderle, John D.; Blanchard, Susan M.; Bronzino, Joseph D. (eds.). Introduction to Biomedical Engineering. Biomedical Engineering (2nd ed.). Boston: Academic Press. pp. 255–312. ISBN 978-0-12-238662-6.
- ^ Partlow, William (2022-03-13). "1 - Biomaterials". Beyond Discovery. Retrieved 2022-05-06.
- ^ "Microstructure". CES Information Guide - Materials Science Engineering. depts.washington.edu. Retrieved 2022-05-06.
- ^ "Introduction to Materials Science". ScienceDirect. Retrieved 2022-05-06.
- ^ "Crystalline Structure: Definition, Structure & Bonding". Study.com. Retrieved 2022-05-06.
- ^ "10.6 Lattice Structures in Crystalline Solids – Chemistry". opentextbc.ca. Retrieved 2022-05-06.
- ^ "Bravais Lattice - 14 Possible Crystal Structures with Illustrations". BYJUS. Retrieved 2022-05-06.
- ^ "crystal defect Definition, Types, & Facts Britannica". www.britannica.com. Retrieved 2022-05-06.
- ^ "Macrostructure". TheFreeDictionary.com. Retrieved 2022-05-06.
- ^ "Natural Biomaterials by Isabel Hand - OpenWetWare". openwetware.org. Retrieved 2022-05-06.
- ^ "Kelp (Laminaria digitata) – Irish Seaweeds". Retrieved 2022-05-06.
- ^ Reis, Lewis A; Chiu, Loraine L Y; Feric, Nicole; Fu, Lara; Radisic, Milica (January 2016). "Biomaterials in myocardial tissue engineering". Journal of Tissue Engineering and Regenerative Medicine. 10 (1): 11–28. doi:10.1002/term.1944. ISSN 1932-7005. PMC 4933503. PMID 25066525.
- ^ Buehler, M. J.; Yung, Y. C. (2009). "Deformation and failure of protein materials in physiologically extreme conditions and disease". Nature Materials. 8 (3): 175–88. Bibcode:2009NatMa...8..175B. doi:10.1038/nmat2387. PMID 19229265.
- ^ Stupp, S. I.; Braun, P. V. (1997). "Molecular manipulation of microstructures: Biomaterials, ceramics, and semiconductors". Science. 277 (5330): 1242–8. doi:10.1126/science.277.5330.1242. PMID 9271562.
- ^ Klemm, D; Heublein, B; Fink, H. P.; Bohn, A (2005). "Cellulose: Fascinating biopolymer and sustainable raw material". Angewandte Chemie International Edition. 44 (22): 3358–93. doi:10.1002/anie.200460587. PMID 15861454.
- ^ Konwarh, Rocktotpal (2019). "Can the venerated silk be the next-generation nanobiomaterial for biomedical-device designing, regenerative medicine and drug delivery? Prospects and hitches". Bio-Design and Manufacturing. 2 (4): 278–286. doi:10.1007/s42242-019-00052-9. S2CID 208833880.
- ^ Mehrotra, Shreya (2019). "Comprehensive Review on Silk at Nanoscale for Regenerative Medicine and Allied Applications". ACS Biomater. Sci. Eng. 5 (5): 2054–2078. doi:10.1021/acsbiomaterials.8b01560. PMID 33405710. S2CID 132470283.