화인산
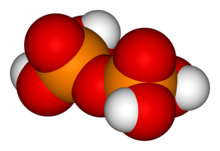
Pyrophosphoric acid | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 디프인산 μ-oxido-bis(dihydroxidoxidophosphorus) | |
| 기타 이름 디프인산 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐벨 | |
| 켐스파이더 | |
| ECHA InfoCard | 100.017.795 |
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| H4P2O7 | |
| 어금질량 | 177.97 g/197 |
| 녹는점 | 71.5°C(160.7°F, 344.6K) |
| 극도로 용해성 | |
| 용해성 | 알코올, 에테르에 매우 용해성 |
| 콘게이트 베이스 | 화인산염 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
화인산(Pyrophosphoric acid, diphosphoric acid)은 HPO 또는 보다427 설명적으로 [(HO)2P(O)]2O라는 공식을 가진 무기 화합물이다. 무색무취로 물, 디에틸에테르, 에틸알코올에 용해된다. 무수산은 두 개의 폴리모르프로 결정되며, 54.3°C와 71.5°C에서 녹는다. 이 화합물은 다인산 성분과 화인산 음이온의 결합산이라는 점 외에는 특별히 유용하지 않다. 음이온, 소금, 화인산 에스테르를 화인산이라고 한다.
준비
그것은 파이로인산나트륨으로부터의 이온 교환이나 황화수소로 납으로인산나트륨을 처리함으로써 가장 잘 준비된다. 그것은 인산의 탈수로 준비되지 않는다. 대신 화인산(火人山)은 제품 중 하나로만 생산된다.
반응
용융될 때, 화인산은 인산, 화인산, 폴리인산 등의 평형 혼합물을 빠르게 형성한다. 화인산 중량에 의한 비율은 약 40%이며 용해로부터 재추정하기 어렵다. 수용액에서는 모든 폴리인산처럼 인산, 파이로인산, 폴리인산 사이에 수산화 및 결국 평형이 성립된다.[1]
- H4P2O7 + H2O ⇌ 2H3PO4
화인산(火人山)은 중강도의 무기산이다.
안전
화로포스포르산은 부식성이 있지만 다른 독성은 없는 것으로 알려져 있다.[2]
역사
피로인산이라는 이름은 1827년 "글라스고의 클라크씨"가 인산염 나트륨의 붉은 열로 가열한 후 발견한 공로를 인정받아 붙여졌다. 붉은 열로 가열하면 인산이 화인산을 형성해 뜨거운 물에 의해 인산으로 쉽게 전환되는 것으로 나타났다.[3]
참고 항목
참조
- ^ Corbridge, D. (1995). "Chapter 3: Phosphates". Studies in inorganic Chemistry vol. 20. Elsevier Science B.V. pp. 169–305. doi:10.1016/B978-0-444-89307-9.50008-8. ISBN 0-444-89307-5.
- ^ 물질안전보건자료 : 화인산MSDS www.sciencelab.com
- ^ Beck, Lewis Caleb (1834). A Manual of Chemistry: Containing a Condensed View of the Present State of the Science, with Copious References to More Extensive Treatises, Original Papers, Etc. E.W & C Skinner. p. 160. Retrieved January 30, 2015.


