염소산
Chlorous acid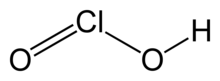 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 염소산, 염소산(III)산 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐스파이더 | |
| 케그 | |
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| HCLO2 | |
| 어금질량 | 68.46 g/190 |
| 산도(pKa) | 1.96 |
| 콘게이트 베이스 | 염소산염 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
클로로산은 HClO라는2 공식을 가진 무기 화합물이다. 그것은 약한 산이다. 염소는 이 산에서 산화상태 +3을 가지고 있다. 순수 물질이 불안정하여 차아염소산(Cl 산화 상태 +1) 및 염소산(Cl 산화 상태 +5)과 불균형하게 된다.
- 2 HClO2 → HClO + HClO3
순수한 물질에서는 산을 얻기 어렵지만, 이 산에서 추출한 결합기층인 클로로사이트는 안정적이다. 이 음이온의 염분의 한 예는 잘 알려진 염소산나트륨이다. 이것과 관련된 염소는 때때로 이산화염소의 생산에 사용된다.
준비
HClO는2 바륨 또는 납 클로로이트 및 희석 황산의 반응을 통해 준비될 수 있다.
- Ba(ClO2)2 + HSO24 → BaaS4 + 2 HClO2
- Pb(ClO2)2 + H2SO4 → PbSO4 + 2 HClO2
안정성
클로로스는 강력한 산화제지만 불균형적인 경향은 산화 잠재력을 상쇄시킨다.
염소는 공식 HXO의2 격리 가능한 산을 형성하는 유일한 할로겐이다.[1] 브롬산도 요오드산도 단 한 번도 고립된 적이 없다. 브롬산, 브롬산염 몇 염은 알려져 있지만 요오드산염은 알려져 있지 않다.[1]
참조
![]() 위키미디어 커먼스의 클로로우산 관련 매체
위키미디어 커먼스의 클로로우산 관련 매체
- ^ a b 에곤 위버그, 아놀드 프레데릭 홀레만(2001) 무기화학, 엘스비에르 ISBN0-12-352651-5