유전성 혈관부종
Hereditary angioedema| 유전성 혈관부종 | |
|---|---|
| 기타이름 | 유전성 혈관신경성 부종(HANE),[1] 가족성 혈관신경성[2] 부종 |
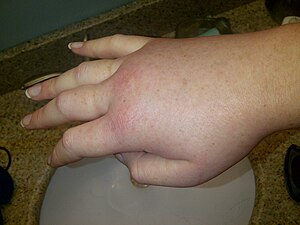 | |
| 유전성 혈관부종 발작 중 오른손이 부었습니다. | |
| 전문 | 혈액학 |
| 증상 | 심한[3] 붓기가 반복적으로 발생 |
| 통상적인 발병 | 어린[3] 시절 |
| 지속 | 공격은 며칠간[3] 지속됩니다. |
| 종류들 | 제1종, 제2종, 제3종[3] |
| 원인들 | 유전적 장애(자가체 우성)[3] |
| 진단방법 | C4 및 C1 억제제 [2]수치 측정. |
| 감별진단 | 장폐색, 다른 종류의[2] 혈관부종 |
| 예방 | C1억제제[1] |
| 치료 | 지원적 치료, 의약품[1] |
| 약 | C1 억제제, 에콜란타이드, 아이카티반트[1] |
| 예후 | (치료 없이) 기도가 관련된 경우 사망 [2]위험 25% |
| 빈도수. | ~5만분의[3] 1 |
유전성 혈관부종(HAE)은 심한 [3]붓기의 재발을 초래하는 질환입니다.붓기는 팔, 다리, 얼굴, 장관, [3]기도에 가장 흔하게 영향을 미칩니다.장관에 영향을 받으면 복통, 구토 [1]등이 나타날 수 있습니다.기도가 붓으면 기도가 막히고 [1]호흡 곤란을 겪을 수 있습니다.예방적인 치료가 없다면, 공격은 보통 2주에 한 번씩 발생하고 며칠 [3]동안 지속됩니다.
HAE의 [3]유형은 크게 세 가지가 있습니다.유형 I과 유형 II는 C1 억제 단백질을 암호화하는 SERPING1 유전자의 돌연변이에 의해 발생하는 반면, 유형 III는 종종 F12(인자 XII) [3]유전자의 돌연변이에 의해 발생합니다.결과적으로 [3]붓기를 촉진하는 브래디키닌의 수치가 증가합니다.이 상태는 상염색체 우성 방식으로 유전되거나 새로운 [3]돌연변이로 발생할 수 있습니다.공격에 대한 트리거는 경미한 외상이나 스트레스를 포함할 수 있지만, 공격은 종종 이전의 명백한 [3]사건 없이 발생합니다.유형 I 및 II의 진단은 C4 및 C1 억제제 [2]수준의 측정을 기반으로 합니다.
HAE의 관리에는 공격을 예방하기 위한 노력과 공격이 [1]발생할 경우의 치료가 포함됩니다.공격 중에는 정맥 수액 및 기도 지지와 같은 보조 치료가 [1]필요할 수 있습니다.C1 억제제는 예방과 치료에 모두 사용될 수 있고, 에칼란타이드와 이카티반트는 급성 [1]발작을 치료하는데 사용될 수 있습니다.
HEA는 [3]약 5만 명 중 1명에게 영향을 미칩니다.이 질환은 일반적으로 [3]어린 시절에 처음 발견됩니다.유형 I과 유형 II는 여성과 남성에게 똑같이 [4]영향을 미치는 반면, 유형 III는 [2]남성보다 여성에게 더 자주 영향을 줍니다.기도가 관련된 경우, 치료를 받지 않으면 사망할 위험이 약 25%[2]에 이릅니다.치료를 받으면 일반적으로 [2]결과가 좋습니다.이 질환은 1888년 캐나다 의사 윌리엄 [5]오슬러에 의해 처음 기술되었습니다.
징후 및 증상
유전성 혈관부종 진단을 받은 사람들은 사지, 생식기, 얼굴, 입술, 후두 또는 지관에 [6]반복적인 붓기가 있습니다.급성 복통을 자주 경험하는 복부 팽만감을 제외하고는 일부 환자들은 포만감을 느끼지만 해당 부위에 통증이나 가려움은 없다고 말합니다.다른 사람들은 목표로 [citation needed]하는 부위에 상관없이 피부 바로 아래의 극심한 가려움과 극심한 열과 함께 뼈에서 바깥쪽으로 방사되는 것으로 묘사되는 극심한 양의 고통을 경험합니다.
호흡기와 위장계를 포함한 부종은 심각한 위험과 고통을 초래할 수 있습니다.목이나 후두와 같은 호흡기 구조물의 개입은 호흡 곤란과 생명을 위협하는 기도 [6][7]폐쇄를 야기할 수 있습니다.위장관을 공격하는 에피소드들은 구토, 경련성 복통, 설사,[7] 그리고 탈수를 포함한 많은 합병증들을 일으킬 수 있습니다.
해를 가진 몇몇 사람들은 '유랑' 공격을 경험합니다.이러한 공격은 사지를 중심으로 이루어질 것입니다.예를 들어,환자의 손이 붓는 경우, 정상적인 붓기 주기를 거친 후 연결 팔다리(이 경우 손목에서 팔뚝)로 이동하거나 반대쪽 손으로 이동합니다.이 증상이 있는 사람은 에피소드가 더 오래 지속되고 트리거를 [citation needed]추적하기가 더 어려워질 수 있습니다.
유전학
HAE는 상염색체 우성 질환이기 때문에, 전염에 있어서 성별 차이가 없고 양성 모두 그들의 부모로부터 돌연변이 유전자를 받을 가능성이 같습니다.예를 들어, HAE에 대한 돌연변이 유전자를 가진 아버지(개인 A)는 질병에 걸린 반면, 그의 아내(개인 B)는 C1 억제 유전자의 2개의 비-돌연변이 유전자를 가지고 있고 질병에 걸린 것은 아닙니다.그들 사이의 교배 가능성은 보여진 것과 같은 가능성을 제공합니다: 그들의 자손들 중 두 명은 그 병(HAE)에 걸리고 다른 사람들은 그렇지 [8][9]않을 것입니다.
HAE를 앓고 있는 환부는 자신의 유전자 중 하나(C1-INH)에 돌연변이가 있습니다.성별에 관계없이 그의 자녀들은 각각 50%의 확률로 그에게서 돌연변이 C1-INH 유전자를 물려받게 됩니다.HAE는 일반적으로 병을 유발하기 위해 담체 내의 두 [10][11]개의 C1-INH 유전자 중 하나의 돌연변이만 취하기 때문에 "지배적" 상태라고 불립니다.
HAE의 유병률은 10,000명당 1명에서 50,000명당 1명으로 비교적 낮습니다.HAE를 가진 대부분의 사람들은 그들의 부모 중 한 명으로부터 C1 에스터레이스 억제제 (C1-INH) 돌연변이를 얻습니다.HEA를 가진 부모는 그림(HEA 상속)과 같이 일반적으로 두 성별 중 한 명의 자녀에게 이 조건을 전달할 확률이 50%입니다.과거력이 없는 사람들은 정자나 난자 세포의 자발적인 변화에 의해 해를 얻을 수 있습니다.가족 중 HAE 병력이 없지만 지속적인 혈관부종을 동반한 변이 C1-INH 수치가 상대적으로 낮은 환자를 대상으로 한 검토에서 HAE를 보유한 신규 환자의 25%는 [citation needed]유전 징후가 나타나지 않는 C1-INH 변화를 가지고 있었습니다.
진단.
| C4(C) | FB (A) | C3 | CH50 | 조건들 |
|---|---|---|---|---|
| · | ↓ | ↓ | ↓ | PSG, C3 NeFAA |
| ↓ | · | ↓ | · | HAE, C4D |
| · | · | · | ↓ | TCPD |
| ↓ | ·/↓ | ↓ | ↓ | SLE |
| ↑ | ↑ | ↑ | ↑ | 염증 |
질병 발현의 변이성이 크기 때문에 해를 인식하는 것이 어려운 경우가 많습니다.그 병의 경과는 다양하고 예측할 수 없으며, 심지어 한 명의 환자에게서도 평생 동안 예측할 수 없습니다.이 질병은 알레르기나 다른 의학적 상태로 인해 발생하는 다른 형태의 혈관부종과 유사할 수 있지만, 원인과 치료에 있어서는 상당히 다릅니다.HAE가 알레르기로 오진될 때, 그것은 보통 HAE 증상을 치료하는데 효과가 없는 약물인 스테로이드와 에피네프린으로 치료됩니다.다른 오진으로 인해 복부 종창 환자들에게 불필요한 탐색 수술이 이루어졌고, 다른 HAE 환자들은 복통이 [citation needed]정신적인 것으로 잘못 진단되었다고 보고합니다.
HAE는 혈관부종의 모든 경우 중 극히 일부만을 차지합니다.상기도 폐쇄와 불필요한 복부 수술과 같은 치명적인 결과를 피하기 위해서는 올바른 진단의 중요성은 아무리 [12]강조해도 지나치지 않습니다.
환자가 다음과 같은 증상을 보이는 경우에는 HAE를 고려해야 합니다.
이상적으로 에피소드 중에 실시하는 혈액 검사를 사용하여 상태를 진단할 수 있습니다.측정: 혈청보충인자 4(C4), C1억제제(C1-INH) 항원 단백질, C1억제제(C1-INH) 기능 수준(가능한 경우).보체 C1 억제제 수준의 분석은 진단에 역할을 할 수 있습니다.C4와 C2는 상호 보완적인 구성요소입니다.
종류들
유전성 혈관부종에는 세 가지 유형이 있습니다.HAE 타입 I 및 II는 모두 보체 C1-인히비터(C1-INH)의 결핍으로 인해 발생합니다. 이는 여러 세린 프로테아제, 특히 보체 시스템 및 접촉 활성화/칼리크레인-키닌 경로뿐만 아니라 섬유소 용해 시스템의 중요한 억제제인 혈장 단백질입니다.
HAE type I에서는 정량적인 C1-억제제 결핍이 있으며 혈장에서 항원뿐만 아니라 기능적인 C1-억제제 수준이 감소합니다.이 유형은 C1 억제제 결핍을 가진 HAE 사례의 약 85%를 차지합니다.
HAE type II에서, 정상적인 C1-억제제 단백질 수준이 - 때로는 심지어 상승하지만 기능적인 C1-억제제 측정치가 감소하는 질적인 결핍이 있습니다.이러한 유형은 C1 억제제 결핍을 가진 HAE 사례의 약 15%에서 볼 수 있습니다.
C1-억제제 결핍은 C1-억제제를 암호화하는 유전자인 SERPING1 유전자의 돌연변이에 의해 발생합니다.700개 이상의 다양한 돌연변이가 [18]설명되었습니다.SERPING1 유전자는 신경성 돌연변이에 대한 상당한 경향을 보여줍니다.이에 따라 부모 모두 영향을 받지 않은 원발성 재발성 혈관부종 발작과 C1 억제제 결핍 환자를 관찰하는 것은 드문 일이 아닙니다.
유전성 혈관부종의 또 다른 유형인 원래 HAE type III는 지난 20년 동안 광범위하게 연구되었습니다.HAE 유형 I 및 II와 대조적으로, 이 유형의 질병은 정상적인 C1 억제제 측정으로 특징지어집니다.따라서, 이 HAE 타입에 대해 "정상적인 C1-억제제를 갖는 유전성 혈관 부종"이라는 용어가 현재 일반적으로 사용되고 있습니다.
정상적인 C1 억제제를 가진 유전성 혈관부종은 유전적으로 이질적인 질환입니다.몇 가지 분자 아형이 확인되었습니다.
2006년에 확인된 첫 번째 아형은 응고 인자 XII(Hageman factor라고도 함)를 암호화하는 F12 유전자의 돌연변이에 의해 발생합니다.[23][24]지금까지 알려진 4개의 돌연변이, 원래 엑손 9에서 설명된 2개의 오감 돌연변이뿐만 아니라 나중에 설명되는 2개의 매우 드문 추가적인 돌연변이는 응고 인자 XII의 프롤린이 풍부한 영역에 영향을 미칩니다.칼리크레인-키닌 시스템의 가속화된 활성화는 F12 돌연변이가 혈관 부종을 유발하는 병리학적 메커니즘을 나타내는 것으로 보입니다.[25]
F12 변이로 인한 유전성 혈관부종의 임상 양상은 바람직하게 발생하지만, 여성 변이 보균자에서만 나타나는 것은 아닙니다.주목할 만한 에스트로겐 민감성은 F12 변이에 의한 HAE형의 특징입니다.예를 들어, 에스트로겐이 함유된 경구 피임약은 혈관 부종 발작을 유발하는 데 중요한 역할을 합니다.임신 중 증상 악화 또한 일반적인 관찰입니다.
정상적인 C1 억제제를 가진 HAE의 두 번째 분자 하위 유형은 플라스미노겐(PLG) 유전자의 돌연변이, 즉 플라스미노겐의 크링글 3 도메인 내에서 드문 오감 돌연변이에 의해 발생하여 새로운 유형의 이형성증을 초래합니다.돌연변이는 크링글 3 도메인 내에 새로운 라이신 결합 부위를 만들고 플라스미노겐의 글리코실화를 바꿉니다.돌연변이 플라스미노겐 단백질은 고분자량의 키니노겐으로부터 브래디키닌을 직접 방출하는 매우 효율적인 키니노겐 효소인 것으로 밝혀졌습니다.혀 붓기는 플라스미노겐 돌연변이로 인한 유전성 혈관 부종 환자에서 매우 빈번하고 특징적인 증상입니다.[27][22]
매우 드문 관찰 결과는 다음 유전자의 돌연변이가 정상적인 C1 억제제를 가진 유전성 혈관부종의 발병에도 원인이 있을 수 있음을 시사했습니다: 앤지오포이에틴 1 [ANGPT1] 돌연변이를 가진 HAE; 마이오페린 [마이오페린 (MYOF) 돌연변이를 가진 HAE]; 키니노겐 1 [키니노겐 1 (KNG1) 돌연변이를 가진 HAE].황산-글루코사민 3-설포전달효소 6 [헤파란 황산-글루코사민 3-설포전달효소 6 (HS3ST6) 돌연변이를 갖는 HAE].
그러나 C1 억제제가 정상인 유전성 혈관부종 환자의 대부분은 유전적인 원인이 현재 알려지지 않았습니다.
예방
ACE 억제제를 사용한 치료는 이 상태에서는 금지됩니다. 이 약물들은 질병의 [29][30]증상을 침전시킬 수 있는 브래디키닌 축적을 초래할 수 있기 때문입니다.
장기
최소 한 달에 한 번 이상 증상이 발생하거나 후두부종이 발생할 위험이 높은 사람은 장기적인 예방이 필요합니다.HAE 예방 및 치료를 다루는 여러 임상 3상이 있습니다.이로 인해 pdC1의 라이센스가 발생했습니다.세계 여러 지역의 INH; 유럽의 브래디키닌 수용체 길항제 (icatibant); 미국의 칼리크레인 억제제 (ecallantide 및 lanadelumab); 및 재조합 C1-INH 대체 요법 (rhC1)유럽에서는 INH; conestat alfa).트라넥삼산은 상대적으로 효과적이지 않은 치료법으로 밝혀졌습니다.다나졸 예방은 여전히 선택사항으로 남아있지만, 치료제는 다나졸의 [31]부작용으로 인해 예방을 위해 더 많이 사용되고 있습니다.장기적인 예방이 필요한 사람들에게, 사람들이 제품을 자가 투여할 수 있게 해주는 가정 요법은 환자들에게 정상적인 [citation needed]삶의 질을 허용하는 데 필수적인 부분으로 여겨집니다.
2018년 미국 식품의약국(FDA)은 12세 이상에서 HAE type I과 II의 공격을 예방하기 위해 주사 가능한 단일클론항체인 라나델루맙을 승인했습니다.라나델루맙은 혈장 효소 칼리크레인을 억제하는데, 칼리딘은 그들의 키니노겐 전구체로부터 키닌 브래디키닌 및 칼리딘을 방출하고, HAE 타입 I 및 [32][33]II를 가진 사람들에서 과도하게 생성됩니다.
베로트랄스타트는 2020년 12월 미국에서 12세 [34][35]이상의 사람들에게 유전성 혈관부종의 공격을 예방하는 것에 대해 승인되었습니다.
단기
단기 예방은 보통 수술이나 치과 치료 전에 시행합니다.독일에서는 이를 위해 C1-INH 농축액을 사용하며 시술 1~1.5시간 전에 투여합니다.C1 억제제 농축액을 사용할 수 없거나 응급 상황에서만 사용할 수 있는 국가에서는 5-7일 [citation needed]동안 고용량 안드로겐 치료를 시행합니다.
관리
급성 치료의 목적은 가능한 한 빨리 부종의 진행을 멈추는 것이고, 이것은 특히 후두에 부기가 있을 경우 생명을 구할 수 있습니다.독일에서 대부분의 급성 치료는 기증자 혈액의 C1 억제제 농축액으로 구성되어 있으며, 이 농축액은 정맥 내에 투여되어야 합니다. 그러나 대부분의 유럽 국가에서는 C1 억제제 농축액은 특별한 프로그램에 참여하는 환자들에게만 제공됩니다.C1 억제제 농축액을 사용할 수 없는 비상 상황에서는 C1 [citation needed]억제제가 포함되어 있기 때문에 신선 냉동 플라즈마(FFP)를 대안으로 사용할 수 있습니다.
다른 치료 방식은 C1 억제제의 합성을 촉진하거나 C1 억제제 소비를 줄일 수 있습니다.인간의 혈액에서 유래된 정제된 C1 억제제는 1979년부터 유럽에서 사용되고 있습니다.여러 C1 억제제 치료제들이 현재 미국 식품의약국에서 판매되고 있고 두 개의 C1 억제제 제품이 현재 캐나다에서 판매되고 있습니다.저온 살균 처리된 베리너트 P (CSL Behring)는 2009년에 급성 공격으로 미국 식품의약국에 의해 승인되었습니다.나노필터링된 Cinryze(ViroPharma)는 2008년 F.D.A.로부터 예방을 위한 허가를 받았습니다.루코네스트(파밍)는 미국과 유럽에서 승인된 재조합 C1 억제제로 사람의 혈액 매개 [36]병원체로 인한 감염병 전파 위험을 가지고 있지 않습니다.
에칼란타이드라는 약은 혈장 칼리크레인을 억제하고 2009년에 급성 공격으로 F.D.A.에 의해 승인되었습니다.아이카티반트는 브래디키닌 B2 수용체를 억제하며, 유럽과 [36][37]미국에서 승인되었으며, HAE에서는 기존에 공격을 유발했던 특정 자극을 향후 피해야 할 수 있습니다.항히스타민제, 코르티코스테로이드,[citation needed] 에피네프린에는 반응하지 않습니다.
2023년 2월, FDA는 2세에서 12세 [38]사이의 소아에서 유전성 혈관부종의 공격을 예방하기 위해 라나델루맙(Takhzyro)의 사용을 확대 승인했습니다.
예후
영향을 받은 사람들의 약 25%가 생애 [39]첫 20년 동안 사망하는데, 이는 주로 치료의 부족 때문입니다.
역학
혈관부종의 역학에 관한 데이터는 제한적입니다.미국과 캐나다에서 HEA의 발병률은 1만-5만 명 중 1명꼴입니다.사망률은 15-33%로 추정되며, 주로 후두부종과 질식으로 인해 발생합니다.HEA는 연간 [40][41]15,000-30,000건의 응급 부서 방문을 유도합니다.
사회와 문화
전 세계 여러 나라에 HEA 환자와 그 가족들을 위한 국가 연합회가 있습니다.이 국가 협회들은 세계적인 조직인 HAEi - C1 억제제 결핍 국제 환자 기구의 회원입니다.HAEi는 전 세계적으로 C1 억제제 결핍에 대한 인식을 높이는 데 전념하고 있습니다.전 [42]세계적으로 C1 억제제 결핍에 대한 효과적인 진단 및 관리를 용이하게 할 수 있도록 돕기 위해 HEA 전문가와 국가 HEA 환자 협회 간의 협력, 조정 및 정보 공유를 촉진하기 위해 설립된 비영리 국제 네트워크입니다.
매년 5월 16일, 국제 해의 날을 계기로 해이와 해공동체는 해이에 대한 인식을 높입니다 [43][44][45]:-)
The Assistance Fund Inc.는 HAE를 치료하는 의약품에 대해 공동 지불 지원을 제공하는 미국 비영리 단체이며 [citation needed]보험에 가입한 미국 시민 또는 육지 이민자에게 열려 있습니다.
뉴욕타임즈 매거진에 게재된 혼란스러운 의학 사례에 대한 칼럼에는 장이 붓는 45세 여성이 등장했는데, 이 여성은 최종적으로 제 3형 해를 가지고 있다고 진단받았습니다.환자의 HAE 공격은 경구 피임약에서 에스트로겐에 노출됨으로써 촉발되었습니다.
조사.
다양한 방법으로 질병 과정에 개입하는 새로운 활성 물질의 임상 개발이 현재 진행 [citation needed]중입니다.
파밍 그룹 NV는 2010년 6월 24일 유럽의약품청이 급성 혈관부종 [47]발작 치료를 위한 C1 억제제인 conestat alfa(상표명 Ruconest)에 대해 긍정적인 의견을 채택했다고 발표했습니다.
칼리크레인의 펩타이드 억제제인 에칼란타이드는 HAE에 대해 고아 지위를 부여받았으며, [48]3상 시험에서 긍정적인 결과를 나타냈습니다.
아이카티반트(Icatibant, Firazyr로 시판)는 선택적 브래디키닌 수용체 길항제로서, 유럽에서 승인되었고 2011년 [49]8월 미국 FDA에서 승인되었습니다.초기 경계선 결과 이후 이 약물은 3상 [50]시험에서 효과가 있는 것으로 나타났습니다.Cinryze는 2008년 [51]10월 FDA 승인을 받았습니다.
참고문헌
- ^ a b c d e f g h i "Hereditary angioedema". GARD. 2017. Archived from the original on 4 July 2017. Retrieved 10 July 2017.
- ^ a b c d e f g h "Orphanet: Hereditary angioedema". www.orpha.net. August 2011. Archived from the original on 9 October 2015. Retrieved 10 July 2017.
- ^ a b c d e f g h i j k l m n o p Reference, Genetics Home (5 July 2017). "hereditary angioedema". Genetics Home Reference. Archived from the original on 10 July 2017. Retrieved 10 July 2017.
- ^ "Hereditary Angioedema - NORD (National Organization for Rare Disorders)". NORD (National Organization for Rare Disorders). 2008. Archived from the original on 14 July 2017. Retrieved 10 July 2017.
- ^ Levin, Alex V.; Enzenauer, Robert W. (2017). The Eye in Pediatric Systemic Disease. Springer. p. 71. ISBN 9783319183893. Archived from the original on 2017-09-10.
- ^ a b Busse PJ, Christiansen SC (2020). "Hereditary Angioedema". N Engl J Med. 382 (12): 1136–1148. doi:10.1056/NEJMra1808012. PMID 32187470. S2CID 214584080.
- ^ a b Nzeako UC, Frigas E, Tremaine WJ (November 2001). "Hereditary angioedema: a broad review for clinicians". Arch Intern Med. 161 (20): 2417–29. doi:10.1001/archinte.161.20.2417. PMID 11700154.
- ^ Ferraro MF, Moreno AS, Castelli EC, Donadi EA, Palma MS, Arcuri HA, Lange AP, Bork K, Sarti W, Arruda LK (October 2011). "A single nucleotide deletion at the C1 inhibitor gene as the cause of hereditary angioedema: insights from a Brazilian family". Allergy. 66 (10): 1384–90. doi:10.1111/j.1398-9995.2011.02658.x. PMID 21623829. S2CID 23036731.
- ^ Bafunno V, Bova M, Loffredo S, Divella C, Petraroli A, Marone G, Montinaro V, Margaglione M, Triggiani M (March 2014). "Mutational spectrum of the c1 inhibitor gene in a cohort of Italian patients with hereditary angioedema: description of nine novel mutations". Ann Hum Genet. 78 (2): 73–82. doi:10.1111/ahg.12052. PMID 24456027.
- ^ Weiler CR, van Dellen RG (July 2006). "Genetic test indications and interpretations in patients with hereditary angioedema". Mayo Clin Proc. 81 (7): 958–72. doi:10.4065/81.7.958. PMID 16835976.
- ^ "Inheritance of Hereditary Angioedema - Patient Information - Shire's Brave Community". Archived from the original on 2014-05-06. Retrieved 2014-05-05.
- ^ "Management of angioedema in the ER" (PDF). Archived from the original (PDF) on 2014-11-03. Retrieved 2014-11-03.
- ^ Zingale LC, Beltrami L, Zanichelli A, et al. (October 2006). "Angioedema without urticaria: a large clinical survey". CMAJ. 175 (9): 1065–70. doi:10.1503/cmaj.060535. PMC 1609157. PMID 17060655.
- ^ "Diagnostic Algorithm". HAE Canada. Archived from the original on 2014-11-03. Retrieved 2014-11-03.
- ^ Donaldson VH, Evans RR (July 1963). "A biochemical abnormality in hereditary angioneurotic edema: Absence of serum inhibitor of C' 1-esterase". Am. J. Med. The American Journal of Medicine. 35 (1): 37–44. doi:10.1016/0002-9343(63)90162-1. PMID 14046003.
- ^ Rosen FS, Pensky J, Donaldson V, Charache P (May 14, 1965). "Hereditary angioneurotic edema: Two genetic variants". Science. 148 (3672): 957–958. Bibcode:1965Sci...148..957R. doi:10.1126/science.148.3672.957. PMID 14277836. S2CID 32776518.
- ^ a b Carugati A, Pappalardo E, Zingale LC, Cicardi M (August 2001). "C1-inhibitor deficiency and angioedema". Mol. Immunol. Molecular Immunology. 38 (2–3): 161–173. doi:10.1016/s0161-5890(01)00040-2. PMID 11532278.
- ^ a b Ponard D, Gaboriaud C, Charignon D, Ghannam A, Wagenaar-Bos IGA, Roem D, López-Lera A, López-Trascasa M, Tosi M, Drouet C (January 2020). "SERPING1 mutation update: Mutation spectrum and C1 Inhibitor phenotypes". Hum. Mutat. Human Mutation. 41 (1): 38–57. doi:10.1002/humu.23917. PMID 31517426.
- ^ Pappalardo E, Cicardi M, Duponchel C, Carugati A, Choquet S, Agostoni A, Tosi M (December 2000). "Frequent de novo mutations and exon deletions in the C1inhibitor gene of patients with angioedema". J. Allergy Clin. Immunol. The Journal of Allergy and Clinical Immunology. 106 (6): 1147–1154. doi:10.1067/mai.2000.110471. PMID 11112899.
- ^ Bork K, Barnstedt SE, Koch P, Traupe H (July 15, 2000). "Hereditary angioedema with normal C1-inhibitor activity in women". Lancet. The Lancet. 356 (9225): 213–217. doi:10.1016/S0140-6736(00)02483-1. PMID 10963200. S2CID 30105665.
- ^ a b Banday AZ, Kaur A, Jindal AK, Rawat A, Singh S (March 2020). "An update on the genetics and pathogenesis of hereditary angioedema". Genes Dis. Genes & Diseases. 7 (1): 75–83. doi:10.1016/j.gendis.2019.07.002. PMC 7063419. PMID 32181278.
- ^ a b c d Jones D, Zafra H, Anderson J (April 22, 2023). "Managing Diagnosis, Treatment, and Burden of Disease in Hereditary Angioedema Patients with Normal C1-Esterase Inhibitor". J Asthma Allergy. Journal of Asthma and Allergy. 16: 447–460. doi:10.2147/JAA.S398333. PMC 10132308. PMID 37124440.
- ^ a b Dewald G, Bork K (May 19, 2006). "Missense mutations in the coagulation factor XII (Hageman factor) gene in hereditary angioedema with normal C1 inhibitor". Biochem. Biophys. Res. Commun. Biochemical-and-Biophysical-Research-Communications. 343 (4): 1286–1289. doi:10.1016/j.bbrc.2006.03.092. PMID 16638441.
- ^ a b c Santacroce R, D'Andrea G, Maffione AB, Margaglione M, d'Apolito M (May 9, 2021). "The Genetics of Hereditary Angioedema: A Review". J. Clin. Med. Journal of Clinical Medicine. 10 (9): 2023. doi:10.3390/jcm10092023. PMC 8125999. PMID 34065094.
- ^ Shamanaev A, Dickeson SK, Ivanov I, Litvak M, Sun MF, Kumar S, Cheng Q, Srivastava P, He TZ, Gailani D (May 23, 2023). "Mechanisms involved in hereditary angioedema with normal C1-inhibitor activity". Front. Physiol. Frontiers in Physiology. 14: 1146834. doi:10.3389/fphys.2023.1146834. PMC 10242079. PMID 37288434.
- ^ Deroux A, Boccon-Gibod I, Fain O, Pralong P, Ollivier Y, Pagnier A, Djenouhat K, Du-Thanh A, Gompel A, Faisant C, Launay D, Bouillet L (September 2016). "Hereditary angioedema with normal C1 inhibitor and factor XII mutation: a series of 57 patients from the French National Center of Reference for Angioedema". Clin. Exp. Immunol. Clinical & Experimental Immunology. 185 (3): 332–337. doi:10.1111/cei.12820. PMC 4991515. PMID 27271546.
- ^ a b c Dewald G (March 25, 2018). "A missense mutation in the plasminogen gene, within the plasminogen kringle 3 domain, in hereditary angioedema with normal C1 inhibitor". Biochem Biophys Res Commun. Biochemical-and-Biophysical-Research-Communications. 498 (1): 193–198. doi:10.1016/j.bbrc.2017.12.060. PMID 29548426.
- ^ Dickeson SK, Kumar S, Sun MF, Mohammed BM, Phillips DR, Whisstock JC, Quek AJ, Feener EP, Law RHP, Gailani D (May 5, 2022). "A mechanism for hereditary angioedema caused by a lysine 311-to-glutamic acid substitution in plasminogen". Blood. Blood. 139 (18): 2816–2829. doi:10.1182/blood.2021012945. PMC 9074402. PMID 35100351.
- ^ Dendorfer A, Wolfrum S, Wagemann M, Qadri F, Dominiak P (May 2001). "Pathways of bradykinin degradation in blood and plasma of normotensive and hypertensive rats". Am. J. Physiol. Heart Circ. Physiol. 280 (5): H2182–8. doi:10.1152/ajpheart.2001.280.5.H2182. PMID 11299220. S2CID 5898184.
- ^ Kuoppala A, Lindstedt KA, Saarinen J, Kovanen PT, Kokkonen JO (April 2000). "Inactivation of bradykinin by angiotensin-converting enzyme and by carboxypeptidase N in human plasma". Am. J. Physiol. Heart Circ. Physiol. 278 (4): H1069–74. doi:10.1152/ajpheart.2000.278.4.H1069. PMID 10749699. S2CID 10371501.
- ^ 유전성 혈관부종: 국제적 합의를 넘어서 - 2010년 12월경 - 캐나다 알레르기 및 임상 면역학 학회 데이비드 맥쿠티 강연
- ^ "FDA Approves Takhzyro (lanadelumab-flyo) for Hereditary Angioedema". Drugs.com.
- ^ "FDA OKs New Prophylactic Drug for Rare Hereditary Angioedema". Medscape.
- ^ "Drug Trials Snapshot: Orladeyo". U.S. Food and Drug Administration. 3 December 2020. Retrieved 25 December 2020.
 이 기사는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다.
이 기사는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다. - ^ "Orladeyo: FDA-Approved Drugs". U.S. Food and Drug Administration (FDA). Retrieved 25 December 2020.
- ^ a b 모건
- ^ Firazyr [패키지 삽입].렉싱턴, MA: Shire Orphan Therapys, Inc.; 2011.
- ^ "FDA Approves sBLA for Takeda's Takhzyro for HAE Attacks in 2y/o and up". Takeda (Press release). Retrieved 2023-02-06.
- ^ Varga, Lilian; Farkas, Henriette (2008-11-01). "Treatment of type I and II hereditary angioedema with Rhucin, a recombinant human C1 inhibitor". Expert Review of Clinical Immunology. 4 (6): 653–661. doi:10.1586/1744666X.4.6.653. ISSN 1744-666X. PMID 20477114. S2CID 11656834.
- ^ 출처: Pinnacle Health System, Harrisburg Hospital, 내과, South Front Street 111, Harrisburg, PA 17101, 그녀의 치료에 대한 최신 정보
- ^ "유전성 혈관부종의 치료에 대한 최신 정보" 부얀체바, 라리사, 사르다나, 니티 및 크레이그, 티모시
- ^ "HAEi website". Archived from the original on 2012-10-22. Retrieved 2017-09-10.
- ^ Chapman, Mary. "HAE Awareness Day 'Stepping Up' With Activity Challenges, Storytelling". Retrieved 2022-05-23.
- ^ Inouye, Daniel K. (2012-01-31). "S.Res.286 - 112th Congress (2011-2012): A resolution recognizing May 16, 2012, as Hereditary Angioedema Awareness Day and expressing the sense of the Senate that more research and treatments are needed for Hereditary Angioedema". www.congress.gov. Retrieved 2022-05-23.
- ^ Jindal, A. K.; Bishnoi, A.; Dogra, S. (2021). "Hereditary Angioedema: Diagnostic Algorithm and Current Treatment Concepts". Indian Dermatology Online Journal. 12 (6): 796–804. doi:10.4103/idoj.idoj_398_21. PMC 8653746. PMID 34934714.
- ^ Sanders, Lisa (28 December 2020). "The New York Times Magazine". The New York Times. Retrieved 2020-12-29.
- ^ 파밍: 파밍, 유럽 의약품청으로부터 루신 제품 이름이 루코네스트로 변경된 것에 대해 긍정적인 의견을 받았습니다.
- ^ Lehmann A (August 2008). "Ecallantide (DX-88), a plasma kallikrein inhibitor for the treatment of hereditary angioedema and the prevention of blood loss in on-pump cardiothoracic surgery". Expert Opin Biol Ther. 8 (8): 1187–99. doi:10.1517/14712598.8.8.1187. PMID 18613770. S2CID 72623604.
- ^ Jerini AG (2008-07-15). "Jerini Receives European Commission Approval for Firazyr (Icatibant) in the Treatment of HAE - Press release". Archived from the original on 2018-09-29. Retrieved 2008-07-28.
- ^ Bernstein JA (January 2008). "Hereditary angioedema: a current state-of-the-art review, VIII: current status of emerging therapies". Ann. Allergy Asthma Immunol. 100 (1 Suppl 2): S41–6. doi:10.1016/S1081-1206(10)60585-6. PMID 18220151.
- ^ 로이터: 업데이트 1-미국, 희귀 부종 질환에 대한 레프파마 약물 승인 웨이백 머신에서 2009-09-09 보관
추가열람
- Busse PJ, Christiansen SC (March 2020). "Hereditary Angioedema". N. Engl. J. Med. 382 (12): 1136–48. doi:10.1056/NEJMra1808012. PMID 32187470. S2CID 214584080.
외부 링크
![]() Wikimedia Commons의 유전성 혈관부종 관련 매체
Wikimedia Commons의 유전성 혈관부종 관련 매체


