아제티딘-2-카르복실산
Azetidine-2-carboxylic acid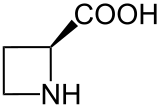 | |
| 이름 | |
|---|---|
| IUPAC 이름 아제티딘-2-카르복실산 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐벨 | |
| 켐스파이더 | |
| ECHA InfoCard | 100.016.693 |
| EC 번호 |
|
| 케그 | |
펍켐 CID |
|
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C4H7NO2 | |
| 어금질량 | 101.1987 g/mb |
| 외관 | 결정 고형 |
| 밀도 | 1.275 g/cm3 |
| 녹는점 | 215°C(419°F, 488K) |
| 비등점 | 242°C(468°F, 515K) |
| 5.0 g/100ml | |
| 위험 | |
| 플래시포인트 | 100.1°C(212.2°F, 373.2K) |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
아제티딘-2-카르복실산(약칭 Aze)은 분자식 CHNO와472 함께 프로라인의 비단백 아미노산 호몰로규어로서, 아제는 질소를 이질소(아제티딘)로 하는 이질소성 순환의 4막 링이며, 고리 탄소 원자 중 하나에 대체되는 카르복실산 그룹이다.아제와 프롤라인의 주요 차이점은 아제의 링은 4명, 프롤라인의 링은 5명이다.[2]아제는 프롤린의 아날로그 역할을 할 수 있는 능력이 있으며 프롤라인 대신 단백질로 통합될 수 있다.
합성
광학적으로 비활성화된 Aze는 신경전달물질 GABA로부터 α-브롬화 α-bromisation에 의해 소량의 수확량으로 얻은 다음, 중간 intermediate-아미노-α-브로무티릭산에서 수소 브롬화물을 제거하고 바륨 수산화물 용액으로 처리하여 링을 폐쇄했다.광학적으로 활성화된 아제는 알파, 감마-다이아미노부티르산 디히드로클로라이드를 질산과 염산을 혼합하여 처리하여 γ-아미노-α-클로로부티르산을 산출한 다음 염화수소를 제거하고 바륨 수산화물로 처리하여 사이클화하였다.[3]
발생
아제티딘-2-카르복실산은 1955년부터 리좀과 특정 식물의 신선한 잎에 존재하는 것으로 알려져 있다.아스파라가과에서 두 종, 즉 콘발라리아 마갈리스(계곡의 릴리), 폴리고나툼(솔로몬의 바다표범)에서 발생하는 것으로 알려져 있다.
아제는 콩과 파브과의 수많은 식물에서도 발견되며 테이블 비엣, 정원 비엣, 설탕 비엣에서도 소량 검출되었다.[4]
독성
아제가 프로라인 대신 단백질로 잘못 결합될 때, 아제는 경쟁하는 식물의 성장을 방해하고 포식자의 독성을 억제하는 것으로 나타났다.다른 연구들은 Aze가 오리, 햄스터, 쥐, 토끼를 포함한 다양한 동물 종에서 다양한 기형을 포함한 광범위한 독성 및 기형 유발 장애를 유발하는 효과를 보여주었다.[2]
Aze를 인간 단백질로 잘못 결합시키면 콜라겐, 케라틴, 헤모글로빈, 단백질 접힘 등을 변화시킬 수 있다.[5]그러나 상세한 독성학적 데이터가 없고 특정 단백질에 대한 Aze 잘못 결합의 해로운 영향에 대한 보다 직접적인 증거가 필요한 것은 현재 인간에 대한 Aze의 독성을 결정할 수 없는 이유다.[2]인간 프롤릴과 알라닐-TRNA 합성물의 분자 연구는 아제가 체내 독성 결과와 함께 프롤라인으로 단백질에 통합된다는 것을 시사한다.[6]아제는 (알라닌과 프롤라인의 이중모사 효과 때문에) 양쪽 tRNA 합성현장에 모두 들어맞는 것처럼 보여도, 알라닐-tRNA 합성 후 편집 시스템에 의해 거부된다.[6]
참조
- ^ 머크 지수, 12판 6089
- ^ a b c Rubenstein E.; T. McLaughlin; R.C. Winant; A. Sanchez; M. Eckart; K.M. Krasinska; A. Chien. (2008). "Azetidine-2-carboxylic Acid in the Food Chain". Phytochemistry. 70 (1): 1–5. doi:10.1016/j.phytochem.2008.11.007. PMID 19101705.
- ^ Fowden, L. (1956). "Azetidine-2-carboxylic Acid: a New Cyclic Imino Acid Occurring in Plants". Biochemical Journal. 64 (2): 323–331. doi:10.1042/bj0640323. PMC 1199734. PMID 13363844.
- ^ Seigler, David S. (1998). Plant secondary metabolism. Kluwer Academic. p. 222. ISBN 0-412-01981-7.
- ^ Rubenstein E.; H. Zhou; K.M. Krasinska; A. Chien; C.H. Becker. (2006). "Azetidine-2-carboxylic Acid in Garden Beets". Phytochemistry. 67 (9): 898–903. doi:10.1016/j.phytochem.2006.01.028. PMID 16516254.
- ^ a b Song, Y; Zhou, H; Vo, MN; Shi, Y; Nawaz, MH; Vargas-Rodriguez, O; Diedrich, JK; Yates, JR; Kishi, S; Musier-Forsyth, K; Schimmel, P (22 December 2017). "Double mimicry evades tRNA synthetase editing by toxic vegetable-sourced non-proteinogenic amino acid". Nature Communications. 8 (1): 2281. Bibcode:2017NatCo...8.2281S. doi:10.1038/s41467-017-02201-z. PMC 5741666. PMID 29273753.



