델타아미노레불린산탈수효소
Delta-aminolevulinic acid dehydratase| 포르포빌리노겐 싱타아제 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 DALA 탈수효소 | |||||||||
| 식별자 | |||||||||
| EC 번호 | 4.2.1.24 | ||||||||
| CAS 번호. | 9036-37-7 | ||||||||
| 데이터베이스 | |||||||||
| 인텐츠 | IntEnz 뷰 | ||||||||
| 브렌다 | 브렌다 입력 | ||||||||
| 엑스퍼시 | 나이스자이메 뷰 | ||||||||
| 케그 | KEG 입력 | ||||||||
| 메타사이크 | 대사통로 | ||||||||
| 프리암 | 프로필 | ||||||||
| PDB 구조 | RCSB PDB PDBe PDBsum | ||||||||
| 진 온톨로지 | 아미고 / 퀵고 | ||||||||
| |||||||||
| 델타아미노레불린산탈수효소 | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호 | 앨러드 | ||||||
| 엔씨비유전자 | 210 | ||||||
| HGNC | 395 | ||||||
| 오밈 | 125270 | ||||||
| RefSeq | NM_001003945 | ||||||
| 유니프로트 | P13716 | ||||||
| 기타자료 | |||||||
| EC 번호 | 4.2.1.24 | ||||||
| 로커스 | 9번 씨 q32 | ||||||
| |||||||
| 앨러드 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 mg2-mg2-mg5-levulinic acid 탈수효소의 고해상도 결정구조 | |||||||||
| 식별자 | |||||||||
| 기호 | 앨러드 | ||||||||
| Pfam | PF00490 | ||||||||
| Pfam 씨 | CL0036 | ||||||||
| 인터프로 | IPR001731 | ||||||||
| 프로사이트 | PDOC00153 | ||||||||
| SCOP2 | 1aw5 / SCOPe / SUPFAM | ||||||||
| |||||||||
델타아미노레불린산탈수소효소(Porphobilinogen synthase, 또는 ALA dehardatase, 또는 아미노레불린탈수소효소)는 인간에서 ALAD 유전자에 의해 인코딩되는 효소(EC 4.2.1.24)이다.[5][6] Porphovilinogen synthase(또는 ALA 탈수화효소, 또는 아미노레불산탈수화효소)는 아미노레불린산 2개 분자의 비대칭 응축을 통해 Porphovilinogen을 합성한다. 헤메스, 엽록소, 비타민 B를12 포함한 모든 천연 사트라피롤은 공통의 전구체로 포르포빌리노겐을 공유한다. Porphobilinogen synthase는 Morphein의 원형이다.[7]
함수
포르피린 생합성의 두 번째 단계인 다음과 같은 반응을 촉진한다.
- Δ-aminolevulinic acid 2 porphobilinogen + 2 HO2
따라서 델타-아미노레불산염의 2개 분자의 응축에 촉매 작용하여 포르포빌로겐(헤메, 사이토크롬 및 기타 혈단백질의 전구체)을 형성한다. 이 반응은 모든 생물학적 사트라피롤의 생합성에서 첫 번째 일반적인 단계다. 아연은 효소 활동에 필수적이다.
구조
PBGS(Porphobilinogen synthase)의 알로스테릭 규제의 구조적 근거는 8진법과 6진법 사이의 2분법 구조 평형(디머를 통한)의 변조를 말하며, 이는 6mer* £ 2mer* £ 2mer* £ 8mer로 도식적으로 표현된다. *는 더 큰 멀티머에서 강직하게 금지되기 때문에 분리된 상태에서 발생하는 각 서브유닛의 두 영역 간의 방향 전환을 나타낸다.[7]
PBGS는 단일 유전자로 암호화되며 각 PBGS 멀티머는 동일한 단백질의 여러 복사본으로 구성된다. 각 PBGS 서브유닛은 그 중심에 효소의 활성 부위가 있는 ~300개의 잔류물 αβ-바렐 영역과 >25개의 잔류물 N-단자 암 영역으로 구성된다. PBGS의 알로스테릭 규제는 N-단자 암 영역과 관련하여 αβ-바렐 영역의 방향 측면에서 설명할 수 있다.
각 N단자 암은 PBGS 멀티머에서 다른 서브유닛과 최대 두 개의 상호작용을 가진다. 이러한 상호작용 중 하나는 활성 사이트 리드의 "닫힘" 준수를 안정화하는 데 도움이 된다. 다른 상호작용은 αβ-바렐의 다른 쪽 끝으로부터의 용매 접근을 제한한다.
비활성 복합체 상태에서는 N-단자 암 영역이 리드 안정화 상호작용에 관여하지 않으며, 비활성 어셈블리의 결정 구조에서는 활성 사이트 리드가 정렬되지 않는다.
알로스테릭 규제 기관
PBGS는 항균제 및/또는 제초제 개발의 주요 대상이 되지 않을 것이다. 반대로 활성 부위는 활성 부지에 비해 유전학적으로 훨씬 더 가변적일 수 있으므로 약물 개발 기회가 더 많다.[7]
PBGS alostery의 phylogenetic 변화는 내인적 요인과 외인적 요인의 측면에서 PBGS alosteric 규제의 논의의 틀로 이어진다.
내인성 알로스테릭 규제기
마그네슘
알로스테릭 마그네슘 이온은 두 개의 친옥타머 디머의 고수화 인터페이스에 있다. 쉽게 분리할 수 없는 것으로 보이며, 체외에서 마그네슘을 제거하면 육각체가 축적되는 것으로 나타났다.[8]
pH
하이드로늄 이온을 알로스테릭 규제기관으로 간주하는 것이 일반적이지는 않지만, PBGS의 경우 활성 부지가 아닌 다른 위치에서의 사이드 체인 양성화가 분기 구조 평형에도 영향을 미치고, 따라서 촉매 반응 속도에도 영향을 미치는 것으로 나타났다.
외측 알로스테릭 규제 기관
소분자 헥사머 안정화
PBGS 6mer* 검사 결과 8mer에는 없는 표면 공동이 나타난다. 이 유전학적으로 가변적인 공동에 결합하는 작은 분자가 목표 PBGS의 6mer*를 안정화시키고 결과적으로 활동을 억제하기 위해 제안되었다.
이러한 알로스테릭 규제기관은 PBGS를 특정 모르핀 형태(6mer*)[9]로 잠그기 때문에 모프록(morphlock)으로 알려져 있다.
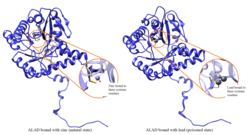
납 중독
ALAD 효소 활성은 납에 의해 억제되며, 한때는 안전하다고 여겨졌던 혈류 납 수준(<10 μg/dL)에서 시작하여 5 ~ 95 μg/dL 범위에서 계속 부정적으로 상관한다.[10] 납에 의한 ALAD 억제는 주로 헤메 합성을 억제하고 순환하는 적혈구의 수명을 단축시키기 때문에 빈혈로 이어지며, 또한 에리트로포이에틴 호르몬의 과도한 생성을 자극하여 그 시조로부터 적혈구가 불충분하게 성숙하게 된다. ALAD 구조 유전자의 결함은 납중독과 급성 간포혈증에 대한 민감도를 증가시킬 수 있다. 대안으로 서로 다른 ISO 양식을 인코딩하는 분할된 대본 변형이 식별되었다.[11]
결핍증
porphobilinogen synthase의 결핍은 보통 (유전이 아닌) 획득되며, 효소가 중금속에 의해 억제되기 매우 쉽기 때문에 중금속 중독, 특히 납중독에 의해 유발될 수 있다.[12]
porphobilinogen synthase의 유전적 결핍은 porphobilinogen synthase (또는 ALA 탈수효소) 결핍 포프라히리아라고 불린다. 지금까지 신고된 건수가 10건도 안 되는 [13]등 극히 드문 포르피린 원인이다.[14] 모든 질병 관련 단백질 변형은 야생형 인간 효소에 비해 헥사머 형성을 선호한다.[13]
Morphein의 프로토타입으로서의 PBGS
PBGS가 예시한 알로스테리의 모르핀 모델은 단백질 기능 조절을 위한 잠재적인 메커니즘에 추가적인 이해 층을 더하고 단백질 과학계가 단백질 구조 역학에 집중하고 있는 증가된 초점을 보완한다.[7]
이 모델은 대체 단백질 순응, 대체 과점 상태 및 과도 단백질-단백질 상호작용과 같은 현상의 역학 관계를 촉매 활성의 알로스테리적 조절에 어떻게 활용할 수 있는지를 보여준다.
참조
- ^ a b c GRCh38: 앙상블 릴리스 89: ENSG00000148218 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리스 89: ENSMUSG000028393 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Eiberg H, Mohr J, Nielsen LS (February 1983). "delta-Aminolevulinatedehydrase: synteny with ABO-AK1-ORM (and assignment to chromosome 9)". Clinical Genetics. 23 (2): 150–4. doi:10.1111/j.1399-0004.1983.tb01864.x. PMID 6839527. S2CID 27267679.
- ^ Beaumont C, Foubert C, Grandchamp B, Weil D, Gross MS, Nordmann Y (May 1984). "Assignment of the human gene for delta aminolevulinate dehydrase to chromosome 9 by somatic cell hybridization and specific enzyme immunoassay". Annals of Human Genetics. 48 (2): 153–9. doi:10.1111/j.1469-1809.1984.tb01010.x. PMID 6378062. S2CID 24098976.
- ^ a b c d Jaffe EK, Lawrence SH (March 2012). "Allostery and the dynamic oligomerization of porphobilinogen synthase". Archives of Biochemistry and Biophysics. 519 (2): 144–53. doi:10.1016/j.abb.2011.10.010. PMC 3291741. PMID 22037356.
- ^ Breinig S, Kervinen J, Stith L, Wasson AS, Fairman R, Wlodawer A, et al. (September 2003). "Control of tetrapyrrole biosynthesis by alternate quaternary forms of porphobilinogen synthase". Nature Structural Biology. 10 (9): 757–63. doi:10.1038/nsb963. PMID 12897770. S2CID 24188785.
- ^ Lawrence SH, Jaffe EK (2008). "Expanding the Concepts in Protein Structure-Function Relationships and Enzyme Kinetics: Teaching using Morpheeins". Biochemistry and Molecular Biology Education. 36 (4): 274–283. doi:10.1002/bmb.20211. PMC 2575429. PMID 19578473.
- ^ Abadin H, Ashizawa A, Stevens YW, Llados F, Diamond G, Sage G, Citra M, Quinones A, Bosch SJ, Swarts SG (August 2007). Toxicological Profile for Lead (PDF). Atlanta, GA: Agency for Toxic Substances and Disease Registry (US). pp. 22, 30. PMID 24049859. Retrieved 22 November 2015.
- ^ "Entrez Gene: ALAD aminolevulinate, delta-, dehydratase".
- ^ ALA 탈수효소 반응, 유타 대학의 넷바이오케미컬. 마지막 수정 1/5/95
- ^ a b Jaffe EK, Stith L (February 2007). "ALAD porphyria is a conformational disease". American Journal of Human Genetics. 80 (2): 329–37. doi:10.1086/511444. PMC 1785348. PMID 17236137.
- ^ 포르피리아스 컨소시엄 (NIH 희귀질환 임상연구 네트워크 (RDCRN)의 일부)의 웨이백 머신에 보관된 포르피리아스의 개요 2011-07-22 2011년 6월 회수
외부 링크
- UCSC 게놈 브라우저의 인간 ALAD 게놈 위치 및 ALAD 유전자 세부 정보 페이지.
- 델타-아미노레불린성+아시드+미국 국립 의학도서관의 탈수효소(MeSH) 제목
- http://www.omim.org/entry/125270?search=pbgs&highlight=pbgs
추가 읽기
- Bernard A, Lauwerys R (1988). "Metal-induced alterations of delta-aminolevulinic acid dehydratase". Annals of the New York Academy of Sciences. 514: 41–7. doi:10.1111/j.1749-6632.1987.tb48759.x. PMID 3327436. S2CID 41966070.
- Jaffe EK (October 2004). "The porphobilinogen synthase catalyzed reaction mechanism". Bioorganic Chemistry. 32 (5): 316–25. doi:10.1016/j.bioorg.2004.05.010. PMID 15381398.
- Roels HA, Buchet JP, Lauwerys RR, Sonnet J (August 1975). "Comparison of in vivo effect of inorganic lead and cadmium on glutathione reductase system and delta-aminolevulinate dehydratase in human erythrocytes". British Journal of Industrial Medicine. 32 (3): 181–92. doi:10.1136/oem.32.3.181. PMC 1008057. PMID 1156566.
- Ishida N, Fujita H, Fukuda Y, Noguchi T, Doss M, Kappas A, Sassa S (May 1992). "Cloning and expression of the defective genes from a patient with delta-aminolevulinate dehydratase porphyria". The Journal of Clinical Investigation. 89 (5): 1431–7. doi:10.1172/JCI115732. PMC 443012. PMID 1569184.
- Dawson SJ, White LA (May 1992). "Treatment of Haemophilus aphrophilus endocarditis with ciprofloxacin". The Journal of Infection. 24 (3): 317–20. doi:10.1016/S0163-4453(05)80037-4. PMID 1602151.
- Astrin KH, Kaya AH, Wetmur JG, Desnick RJ (August 1991). "RsaI polymorphism in the human delta-aminolevulinate dehydratase gene at 9q34". Nucleic Acids Research. 19 (15): 4307. doi:10.1093/nar/19.15.4307-a. PMC 328595. PMID 1678509.
- Wetmur JG, Kaya AH, Plewinska M, Desnick RJ (October 1991). "Molecular characterization of the human delta-aminolevulinate dehydratase 2 (ALAD2) allele: implications for molecular screening of individuals for genetic susceptibility to lead poisoning". American Journal of Human Genetics. 49 (4): 757–63. PMC 1683158. PMID 1716854.
- Plewinska M, Thunell S, Holmberg L, Wetmur JG, Desnick RJ (July 1991). "delta-Aminolevulinate dehydratase deficient porphyria: identification of the molecular lesions in a severely affected homozygote". American Journal of Human Genetics. 49 (1): 167–74. PMC 1683193. PMID 2063868.
- Potluri VR, Astrin KH, Wetmur JG, Bishop DF, Desnick RJ (July 1987). "Human delta-aminolevulinate dehydratase: chromosomal localization to 9q34 by in situ hybridization". Human Genetics. 76 (3): 236–9. doi:10.1007/BF00283614. PMID 3036687. S2CID 32211471.
- Gibbs PN, Jordan PM (June 1986). "Identification of lysine at the active site of human 5-aminolaevulinate dehydratase". The Biochemical Journal. 236 (2): 447–51. doi:10.1042/bj2360447. PMC 1146860. PMID 3092810.
- Wetmur JG, Bishop DF, Cantelmo C, Desnick RJ (October 1986). "Human delta-aminolevulinate dehydratase: nucleotide sequence of a full-length cDNA clone". Proceedings of the National Academy of Sciences of the United States of America. 83 (20): 7703–7. Bibcode:1986PNAS...83.7703W. doi:10.1073/pnas.83.20.7703. PMC 386789. PMID 3463993.
- Wetmur JG, Bishop DF, Ostasiewicz L, Desnick RJ (1986). "Molecular cloning of a cDNA for human delta-aminolevulinate dehydratase". Gene. 43 (1–2): 123–30. doi:10.1016/0378-1119(86)90015-6. PMID 3758678.
- Doss M, von Tiepermann R, Schneider J (1981). "Acute hepatic porphyria syndrome with porphobilinogen synthase defect". The International Journal of Biochemistry. 12 (5–6): 823–6. doi:10.1016/0020-711X(80)90170-6. PMID 7450139.
- Kaya AH, Plewinska M, Wong DM, Desnick RJ, Wetmur JG (January 1994). "Human delta-aminolevulinate dehydratase (ALAD) gene: structure and alternative splicing of the erythroid and housekeeping mRNAs". Genomics. 19 (2): 242–8. doi:10.1006/geno.1994.1054. PMID 8188255.
- Akagi R, Yasui Y, Harper P, Sassa S (September 1999). "A novel mutation of delta-aminolaevulinate dehydratase in a healthy child with 12% erythrocyte enzyme activity". British Journal of Haematology. 106 (4): 931–7. doi:10.1046/j.1365-2141.1999.01647.x. PMID 10519994. S2CID 24044521.
- Akagi R, Shimizu R, Furuyama K, Doss MO, Sassa S (March 2000). "Novel molecular defects of the delta-aminolevulinate dehydratase gene in a patient with inherited acute hepatic porphyria". Hepatology. 31 (3): 704–8. doi:10.1002/hep.510310321. PMID 10706561. S2CID 8998084.
- Kervinen J, Jaffe EK, Stauffer F, Neier R, Wlodawer A, Zdanov A (July 2001). "Mechanistic basis for suicide inactivation of porphobilinogen synthase by 4,7-dioxosebacic acid, an inhibitor that shows dramatic species selectivity". Biochemistry. 40 (28): 8227–36. CiteSeerX 10.1.1.374.9639. doi:10.1021/bi010656k. PMID 11444968.