툴륨(Thulium)III) 요오드화물
Thulium(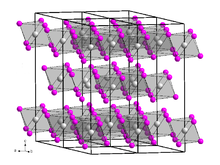 | |
 | |
| 이름 | |
|---|---|
| 기타 이름 요오드화 탈륨 삼요오드화물 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.034.052 |
| EC 번호 |
|
PubChem CID | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| TmI3 | |
| 외모 | 황색 육각형[1] 결정 |
| 녹는점 | 1015 °C[2] |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
툴륨(Thulium)III) 요오드화물은 투륨의 요오드화물로 화학식은 TmI이다3.툴륨(Thulium)III) 금속 할로겐화물 [3]램프의 성분으로 요오드화물을 사용한다.
준비
수은()II) 요오드화물은 탈륨과 함께 가열하여 탈륨을 얻을 수 있다.III) 요오드화물:[4]
- 2 Tm + 3 HgI2 → 2 TmI3 + 3 Hg
반응에서 생성된 수은은 [5][4]증류를 통해 제거될 수 있다.
툴륨(Thulium)III) 용액에서 결정화된 요오드화 수화물을 요오드화 암모늄으로 가열하여 무수 형태로 [6][4]할 수 있다.
특성.
툴륨(Thulium)III) 요오드화물은 요오드화 비스무트(III)형 결정구조를 [4]가진 노란색의 고흡습성 고체이다.그것은 육각형 [6]결정계에서 형성된다.그 하이드레이트는 공기 중에 가열되어 TmOI를 얻을 수 있다.TmI를 [7]얻기2 위해 무수 형태를 탈륨과 함께 가열할 수 있습니다.
- 23 TmI + Tm → 3 TmI2
레퍼런스
- ^ 王世华,谷亚平,蒋盛邦.[ Tm - HgI ] tm2 [ Tm ]나는2[J]物理化学学报,1987(03):334-336.
- ^ Jantch, G.; Zeitschrift fuer Anorganische und Allgemeine Chemie 1933, V212, P65-83 CAPLUS
- ^ Flesch, Peter G. (2007). Light and Light Sources: High-Intensity Discharge Lamps. Springer. p. 45. ISBN 9783540326847.
- ^ a b c d Georg Brauer (Hrsg), Unter Mitarbeit von Marianne Baudler u.:Handbuch der Préparativen Anorganischen Chemie 3. 움게르비테 아우플라주밴드 I, 페르디난드 엔케, 슈투트가르트 1975, ISBN 3-432-02328-6, S. 1077.
- ^ Asprey, L. B.; K. K., K.; Kruse, F. H. 란타니드 및 액티니드 3요오드화물에 대한 준비 및 결정 데이터.Inorg. Chem., 1964. 3 (8) : 1137-1240
- ^ a b 无机化学丛书 第七卷 钪 稀土元素.科学出版社. pp 211
- ^ 파일L.B. Asprey, F.H. Kruse (1960). "Divalent thulium. Thulium di-iodide". Journal of Inorganic and Nuclear Chemistry. 13 (1–2): 32–35. doi:10.1016/0022-1902(60)80232-1. Archived from the original on 2018-06-09. Retrieved 2018-04-13.: Tm+HgI2 Tm나는2

