포스포리보실 피로인산염
Phosphoribosyl pyrophosphate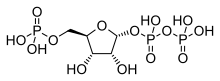 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 (2R, 3R, 4S, 5R)-3, 4-디히드록시-5-[(포스포녹시)메틸]옥소란-2-일 3수소2인산 | |
| 기타 이름 5-인산α-D-리보오스1-이인산 PRPP | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐스파이더 | |
| 드러그뱅크 | |
| 메쉬 | 포스포리보실+피로인산 |
PubChem CID | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| 잘라내다513143 | |
| 몰 질량 | 390.07g/표준 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
포스포리보실 피로인산염(PRPP)은 펜토오스 인산염으로 이노신-5-일인산을 통해 퓨린 뉴클레오티드를 형성하는 생화학 중간체이다.그러므로 그것은 DNA와 [1][2][3]RNA의 구성 요소이다.비타민[4] 티아민, 코발라민,[5] 아미노산 트립토판도 [6]PRPP에서 유래한 파편을 함유하고 있다.리보스는 리보스-인산 디포스포키나아제에 [7]의해 리보스 5-인산(R5P)에서 형성된다.
포스포리보스는 여러 반응에서 포스포리보스기를 전달하는 역할을 하며, 그 중 일부는 회수 [8]경로이다.
푸린 탈노보 생성에서 아미도포스포리보실전달효소(amidophosphoribosyl transferase)는 PRP에 작용하여 포스포리보실아민을 [2]생성한다.히스티딘 생합성 경로는 PRPP와 ATP 사이의 반응을 수반하며, ATP는 후자를 활성화하여 분할을 한다.PRPP의 리보오스로부터의 탄소 원자는 히스티딘의 [15][16][17]이미다졸 고리의 일부와 선형 사슬을 형성한다.트립토판의 생합성에서도 마찬가지이며, 첫 번째 단계는 안트라닐산염 포스포리보실전달효소([15][18][19]안트라닐산)에 의해 촉매되는 N-알킬화이다.
PRPP의 증가
PRPP의 증가는 요산의 과잉 생산과 축적을 통해 고뇨당혈증 및 고뇨당뇨를 일으키는 것이 특징이다.통풍의 원인 [20]중 하나입니다.
Lesch-Nyhan Syndrome에서는 PRPP의 수치가 증가한다.PRPP는 푸린 [21]회수 중에 HGPRT에 의해 사용되는 기질이기 때문에 히포산틴 구아닌 포스포리보실 전이효소(HGPRT)의 감소는 이러한 축적을 일으킨다.
「 」를 참조해 주세요.
레퍼런스
- ^ R. Caspi (2009-01-13). "Pathway: 5-aminoimidazole ribonucleotide biosynthesis I". MetaCyc Metabolic Pathway Database. Retrieved 2022-02-02.
- ^ a b Zhang, Y.; Morar, M.; Ealick, S.E. (2008). "Structural biology of the purine biosynthetic pathway". Cellular and Molecular Life Sciences. 65: 3699–3724. doi:10.1007/s00018-008-8295-8. PMC 2596281. PMID 18712276.
- ^ Gupta, Rani; Gupta, Namita (2021). "Nucleotide Biosynthesis and Regulation". Fundamentals of Bacterial Physiology and Metabolism. pp. 525–554. doi:10.1007/978-981-16-0723-3_19. ISBN 978-981-16-0722-6. S2CID 234897784.
- ^ Chatterjee, Abhishek; Hazra, Amrita B.; Abdelwahed, Sameh; Hilmey, David G.; Begley, Tadhg P. (2010). "A "Radical Dance" in Thiamin Biosynthesis: Mechanistic Analysis of the Bacterial Hydroxymethylpyrimidine Phosphate Synthase". Angewandte Chemie International Edition. 49 (46): 8653–8656. doi:10.1002/anie.201003419. PMC 3147014. PMID 20886485.
- ^ R. Caspi (2019-09-23). "Pathway: 5-hydroxybenzimidazole biosynthesis (anaerobic)". MetaCyc Metabolic Pathway Database. Retrieved 2022-02-10.
- ^ Mehta, Angad P.; Abdelwahed, Sameh H.; Fenwick, Michael K.; Hazra, Amrita B.; Taga, Michiko E.; Zhang, Yang; Ealick, Steven E.; Begley, Tadhg P. (2015). "Anaerobic 5-Hydroxybenzimidazole Formation from Aminoimidazole Ribotide: An Unanticipated Intersection of Thiamin and Vitamin B12 Biosynthesis". Journal of the American Chemical Society. 137 (33): 10444–10447. doi:10.1021/jacs.5b03576. PMC 4753784. PMID 26237670.
- ^ Li, Sheng; Lu, Yongcheng; Peng, Baozhen; Ding, Jianping (January 2007). "Crystal structure of human phosphoribosylpyrophosphate synthetase 1 reveals a novel allosteric site". Biochemical Journal. 401 (1): 39–47. doi:10.1042/BJ20061066. PMC 1698673. PMID 16939420.
- ^ R. Caspi (2022-02-15). "5-phospho-α-D-ribose 1-diphosphate". MetaCyc Metabolic Pathway Database. Retrieved 2022-02-15.
- ^ Silva, Carlos H. T. P.; Silva, Marcio; Iulek, Jorge; Thiemann, Otavio H. (2008). "Structural Complexes of Human Adenine Phosphoribosyltransferase Reveal Novel Features of the APRT Catalytic Mechanism". Journal of Biomolecular Structure and Dynamics. 25 (6): 589–597. doi:10.1080/07391102.2008.10507205. PMID 18399692. S2CID 40788077.
- ^ a b Finette, Barry A.; Kendall, Heather; Vacek, Pamela M. (2002). "Mutational spectral analysis at the HPRT locus in healthy children". Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis. 505 (1–2): 27–41. doi:10.1016/S0027-5107(02)00119-7. PMID 12175903.
- ^ Vinitsky, A.; Grubmeyer, C. (1993). "A new paradigm for biochemical energy coupling. Salmonella typhimurium nicotinate phosphoribosyltransferase". Journal of Biological Chemistry. 268 (34): 26004–26010. doi:10.1016/S0021-9258(19)74485-8. PMID 7503993.
- ^ González-Segura, Lilian; Witte, John F.; McClard, Ronald W.; Hurley, Thomas D. (2007). "Ternary Complex Formation and Induced Asymmetry in Orotate Phosphoribosyltransferase". Biochemistry. 46 (49): 14075–14086. doi:10.1021/bi701023z. PMID 18020427.
- ^ Selwood, Trevor; Jaffe, Eileen K. (2012). "Dynamic dissociating homo-oligomers and the control of protein function". Archives of Biochemistry and Biophysics. 519 (2): 131–143. doi:10.1016/j.abb.2011.11.020. PMC 3298769. PMID 22182754.
- ^ Krenitsky, Thomas A.; Neil, Shannon M.; Miller, Richard L. (1970). "Guanine and Xanthine Phosphoribosyltransfer Activities of Lactobacillus casei and Escherichia coli". Journal of Biological Chemistry. 245 (10): 2605–2611. doi:10.1016/S0021-9258(18)63113-8.
- ^ a b Voet, Donald (2016). Fundamentals of biochemistry : life at the molecular level. Judith G. Voet, Charlotte W. Pratt (Fifth ed.). Hoboken, NJ. ISBN 978-1-118-91840-1. OCLC 910538334.
- ^ R. Caspi (2008-10-10). "Pathway: L-histidine biosynthesis". MetaCyc Metabolic Pathway Database. Retrieved 2022-02-17.
- ^ Stepansky, A.; Leustek, T. (2006). "Histidine biosynthesis in plants". Amino Acids. 30 (2): 127–142. doi:10.1007/s00726-005-0247-0. PMID 16547652. S2CID 23733445.
- ^ C.A. Fulcher (2010-02-12). "Pathway: L-tryptophan biosynthesis". MetaCyc Metabolic Pathway Database. Retrieved 2022-02-17.
- ^ Crawford, Irving P. (1989). "Evolution of a Biosynthetic Pathway: The Tryptophan Paradigm". Annual Review of Microbiology. 43: 567–600. doi:10.1146/annurev.mi.43.100189.003031. PMID 2679363.
- ^ Elliott, Katherine; Fitzsimons, David W. (16 September 2009). Purine and Pyrimidine Metabolism. pp. 143–158. ISBN 9780470717981.
- ^ Cakmakli, Hasan F.; Torres, Rosa J.; Menendez, Araceli; Yalcin-Cakmakli, Gul; Porter, Christopher C.; Puig, Juan Garcia; Jinnah, H.A. (2019). "Macrocytic anemia in Lesch–Nyhan disease and its variants". Genetics in Medicine. 21 (2): 353–360. doi:10.1038/s41436-018-0053-1. PMC 6281870. PMID 29875418.



