네프론
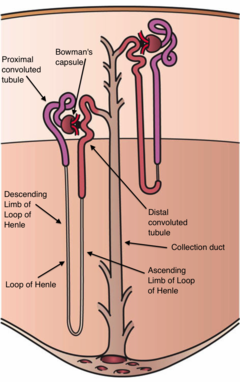
Nephron네프론은 신장의 미세한 또는 미세한 구조 및 기능 단위다. 그것은 신관절과 신관절로 구성되어 있다. 신관절은 글로머룰루스라고 불리는 모세혈관과 보우만의 캡슐이라고 불리는 컵 모양의 구조로 이루어져 있다. 신관튜브는 캡슐에서 뻗어있다. 캡슐과 관은 연결되어 있으며, 상피세포와 루멘으로 구성되어 있다. 건강한 성인은 각 신장에 150만개의 네프론을 가지고 있다.[1]: 22 혈액은 모세혈관벽의 내피세포, 그 지하막, 그리고 캡슐 안벽의 난포세포의 발 작용 사이에 세 겹을 통과하면서 여과된다. 튜불레는 인접한 심막 모세혈관이 있으며, 튜불의 내림 부분과 오름차순 부분 사이를 운행한다. 캡슐에서 나온 액체가 관으로 흘러 내려가면서, 그것은 관에 줄지어 있는 상피세포에 의해 처리된다: 물은 재흡수되고 물질은 교환된다(어떤 것은 첨가된다, 어떤 것은 제거된다). 먼저 관개 바깥의 간액과 함께, 그 다음 내피관을 통해 인접한 경막 모세혈관의 혈장으로 들어간다.모세관 안에 있는 타원들 이 과정은 체액의 부피와 많은 체질의 수치를 조절한다. 관의 끝에서, 남아있는 액체인 urine은 배출된다: 물, 대사 폐기물, 그리고 독소로 구성되어 있다.
보우만의 공간이라 불리는 보우만의 캡슐의 내부는 활석 투프트의 여과 모세혈관에서 여과물을 수집하는데, 이 여과물에는 이러한 모세혈관을 지탱하는 중상세포도 들어 있다. 이 구성품들은 여과장치로서 기능하며 신장 말뭉치를 구성한다. 여과구조(광체 여과 장벽)는 내피세포, 지하막, 난포세포(발 공정)로 구성된 3개 층으로 이루어져 있다. 튜불은 해부학적으로 기능적으로 서로 다른 5개의 부분을 가지고 있다: 근위부 경련된 튜불과 곧은 부분(최소 직선 튜불), 헨리의 내림 루프("descending 루프")와 헨리의 오름 루프("ascending 루프") 두 부분으로 이루어진 헨리의 루프("ascending 루프")이다. 원위 절연된 관("distal 루프"), 연결 관(connecting tubule) 및 네프론의 마지막 부분 수집 덕트. 네프론은 소변 집중력이 다른 두 개의 길이를 가지고 있다: 긴 주축수 네프론과 짧은 피질 네프론이다.
여과물을 만들고 처리하는 데 사용되는 네 가지 메커니즘(혈액을 소변으로 전환시키는 결과)은 여과, 재흡수, 분비, 배설이다. 여과 또는 초유착은 글루머룰루스에서 발생하며 대부분 수동적이다: 그것은 혈압에 의존한다. 혈장의 약 5분의 1은 혈액이 글루머성 모세혈관을 통과할 때 여과된다; 4분의 1은 경막성 모세혈관으로 계속된다. 일반적으로 보우만의 캡슐에 여과되지 않는 혈액의 구성 요소는 혈액 단백질, 적혈구, 백혈구, 혈소판뿐이다. 매일 150리터 이상의 액체가 성인의 글로머룰리 안으로 들어온다: 그 여과물 속 물의 99%가 재흡수된다. 재흡수는 신관절에서 발생하며 확산으로 인해 수동적이거나 농도 구배에 대한 펌핑으로 인해 활성적이다. 분비물도 관류나 집수관 등에서 발생하며 활발하다. 재흡수되는 물질은 물, 염화나트륨, 포도당, 아미노산, 젖산, 마그네슘, 인산칼슘, 요산, 중탄산염 등이다. 분비되는 물질은 요소, 크레아티닌, 칼륨, 수소, 요산 등이다. 관에 신호를 보내 재흡수율이나 분비율을 변화시켜 동점선을 유지하는 호르몬으로는 (피해를 입은 물질과 함께) 항이뇨 호르몬(물), 알도스테론(소듐, 칼륨), 부갑상선호르몬(칼슘, 인산), 심방 나트륨(소듐), 뇌유 펩타이드(소듐) 등이 있다. 신장내 역류계통은 네프론 내에서 용액 없는 물을 회수하여 적절한 경우 정맥정맥으로 되돌릴 수 있도록 하는 고투닉 간막 생성 메커니즘을 제공한다.
네프론의 어떤 질병들은 주로 글로머룰리나 관에 영향을 미친다. 글루머성 질환은 당뇨병성 신혈증, 글루머론염, IgA 신혈증을 포함한다. 신관성 질환은 급성관괴사, 다낭성 신장질환을 포함한다.
구조
네프론은 신장의 기능 단위다.[2] 이것은 각각의 분리된 네프론이 신장의 주요 작업이 수행되는 곳이라는 것을 의미한다.
네프론은 두 부분으로 이루어져 있다.
신장 말뭉치
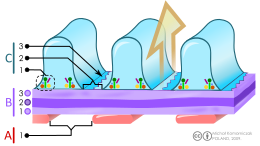
B. 글루머 모양의 지하막: 1. 라미나 라라 인테르나 2. 라미나 밀도 3. 라미나 라라 엑스테나
C. 포데모세포: 1. 효소 및 구조 단백질 2. 여과 슬릿 3. 다이어프램
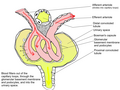
신장 말뭉치는 혈장 여과 지점이다. 신관절은 글로머룰루스와 글로머룰러 캡슐 또는 보우만의 캡슐로 구성된다.[3]: 1027
신관절은 두 개의 극을 가지고 있다: 혈관극과 관상극이다.[4]: 397 신장순환에서 나온 동맥류는 혈관극에 있는 글루머룰루스로 들어가서 떠난다. 글러머 여과물은 소변 폴에 있는 신장 관에 있는 보우만의 캡슐을 떠난다.
글루머룰루스
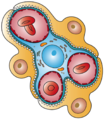
글루머룰루스는 보우만 캡슐에 있는 신장 말뭉치의 혈관극에 위치한 모세혈관을 여과하는 투프트(tuft)라고 알려진 네트워크다. 각 글루머룰루스는 신장 순환의 다른 동맥으로부터 혈액을 공급받는다. 글러머 혈압은 혈장에서 물과 용액이 걸러지는 원동력을 제공하며, 보우만의 공간이라고 불리는 보우만의 캡슐 내부로 들어간다.
혈장의 약 5분의 1만이 글로머룰루스에서 여과된다. 나머지는 동맥경화증으로 들어간다. 폐동맥의 지름은 다른 동맥보다 작으며, 이 차이는 글루머룰루스의 정수압을 증가시킨다.
보우만 캡슐
활석 캡슐이라고도 불리는 보우만의 캡슐이 활석액을 둘러싸고 있다. 갑상구라고 불리는 특수한 세포에 의해 형성된 내장 내층과 단순 편평상피로 구성된 두정외층으로 구성되어 있다. 글루머룰루스의 혈액에서 나오는 액체는 여러 층을 통해 초여과되어 여과물이라고 알려진 것을 만들어 낸다.
여과물은 다음에 신장관까지 이동하며, 그곳에서 소변을 형성하기 위해 추가적으로 처리된다. 이 액체의 다른 단계들은 통관액으로 통칭된다.
레날 튜불레
신관튜브는 글로머룰루스를 통해 여과된 관액을 포함하는 구조물과 같은 긴 파이프다.[5] 신장관을 통과한 후 여과물은 수집용 덕트 시스템으로 계속된다. [6]
신관 튜브의 구성 요소는 다음과 같다.
- 근위부 경련된 튜불(피질에 있고 흡수 면적을 크게 증가시키는 데 도움이 되는 브러시 테두리가 있는 단순한 큐보이드 상피로 정렬되어 있음)
- Henle의 루프(Hair-pin like, 즉 U자형, medulla에 놓여 있음)
- 헨리의 내림쇠
- 헨리의 오르막길
- Henle의 고리의 상승 사지는 2개의 세그먼트로 나뉜다. 상승 사지의 아래쪽 끝은 매우 얇고 단순한 편평상피로 줄지어 있다. 상승 사지의 원위부는 굵고 단순한 입체 상피로 일렬로 늘어서 있다.
- 헨리의 얇은 오르막길
- Henle의 루프에 대한 두꺼운 상승 사지(피질 내부가 되고 원위 절개된 관절이 됨)
- 원위경련관
- 연결 튜브울레
글루머룰루스에 걸러지지 않은 모든 것을 담고 있는 여과된 동맥에서 나온 혈액은 관액이 흐르는 헨리의 고리와 근위부 및 원위부 관을 둘러싸고 있는 작은 혈관인 근위부 모세혈관으로 이동한다. 그리고 나서 물질은 후자에서 다시 혈류로 흡수된다.
그리고 나서 경막 모세혈관은 다시 결합하여 다른 네프론에서 나온 신정맥으로 나오는 신정맥과 결합하여 주혈액과 다시 결합한다.
길이차이
피질 네프론(대부분의 네프론)은 피질에서 높게 시작하며, 헨리의 짧은 고리를 가지고 있어 메둘라 속으로 깊이 침투하지 않는다. 피질 네프론은 피질 네프론과 중질 네프론으로 세분될 수 있다.[7]
헥타메들리 네프론은 메들라 근처의 피질에서 낮게 시작하여 신장 메들라로 깊이 침투하는 긴 헨리의 고리를 가지고 있다. 오직 그들만이 바사 직장에 둘러싸여 헨리의 고리를 가지고 있다. 헨리의 이 긴 루프와 그와 연관된 바사 직장은 집중된 소변 생성을 가능하게 하는 초극성 경사를 생성한다.[8] 또한 머리핀 굴곡은 메둘라의 안쪽 영역까지 침투한다.[9]
헥타메들리 네프론은 새와 포유류에서만 발견되며, 특정한 위치를 가지고 있다: 명상어는 신간 메둘라를 가리킨 반면, 명상(라틴어: near)은 명상 근처인 이 네프론의 신간 말뭉치의 상대적 위치를 가리킨다. 즉, 헥타메들리 네프론은 신장 말뭉치가 메들라 근처에 있고 근위부 경련된 튜불과 헨리의 관련 고리가 다른 종류의 네프론인 피질 네프론보다 더 깊은 메들라에서 발생하는 네프론이다.
대등선 네프론은 인간의 신장에 있는 네프론의 약 15%만을 차지한다.[1]: 24 그러나, 가장 흔히 네프론의 삽화로 묘사되는 것은 이런 종류의 네프론이다.
인간에게 있어서 피질 네프론은 피질의 바깥쪽 3분의 2에 신장 말뭉치를 가지고 있는 반면, 헥타메들리 네프론은 피질의 안쪽 3분의 1에 그들의 말뭉치를 가지고 있다.[1]: 24
기능들
네프론은 혈액을 소변으로 전환하기 위해 여과, 재흡수, 분비, 배설의 네 가지 메커니즘을 사용한다.[4]: 395–396 이것들은 수많은 물질에 적용된다. 네프론이 진행되는 동안 루멘을 라이닝하는 상피세포의 구조와 기능이 변화하며, 위치에 의해 이름이 붙여지고 각기 다른 기능을 반영하는 세그먼트를 가진다.
근위관절
네프론의 한 부분으로서 근위부 관모는 초기 경련 부분과 다음과 같은 직선(후술) 부분으로 나눌 수 있다.[10] 근위부 경련된 관에 들어가는 여과물의 유체는 여과된 소금, 물 및 여과된 모든 유기 용액(주로 포도당과 아미노산)의 80% 이상, 포도당의 절반 이상을 포함한 경련 모세혈관에 재흡수된다.[4]: 400–401
헨리의 루프
Henle의 고리는 근위관으로부터 연장되는 U자형 관이다. 그것은 하강 사지와 상승 사지로 구성되어 있다. 근위 경련관으로부터 여과물을 받아 피질에서 시작하여 내림사지로서 중합관 속으로 확장한 다음, 다시 상승사지로서 피질 쪽으로 돌아와 원위 경련관 속으로 비워진다. Henle의 순환의 주된 역할은 관의 농도를 증가시킴으로써가 아니라 미간 유체의 고음성을 증가시킴으로써 유기체가 집중된 소변을 만들 수 있게 하는 것이다.[1]: 67
상당한 차이가 헨리의 고리의 내림과 상승 사지를 구별하는 데 도움이 된다. 내림 사지는 물에 스며들 수 있고, 눈에 띄게 소금에 덜 스며들며, 따라서 간막의 농도에 간접적으로만 기여한다. 여과물이 신장간막의 고환성간막으로 더 깊숙이 내려오면서 삼투에 의해 하행성 사지에서 여과물과 간낭의 톤이 평형될 때까지 물이 자유롭게 흘러 나온다. 메둘라의 고음질(따라서 오줌의 농도)은 부분적으로 헨리의 루프 크기에 의해 결정된다.[1]: 76
내림 사지와 달리 두꺼운 상승 사지는 물에 불침투성이며, 이는 루프에 의해 사용되는 역류 교환 메커니즘의 중요한 특징이다. 상승 사지는 여과물에서 나트륨을 적극적으로 펌핑하여 역류 교환을 유도하는 고투닉 중간막을 생성한다. 상승 사지를 통과하면 나트륨 함량이 상당 부분 감소했기 때문에 여과물이 저혈압으로 성장한다. 이 저온 여과물은 신장 피질에서 원위성 경련된 관으로 전달된다.[1]: 72
원위경련관
원위부 경련형 관모는 근위부 경련형 관련형과는 구조와 다른 구조와 기능을 가지고 있다. 튜불에 라이닝하는 세포들은 활동적인 수송이 일어나기에 충분한 에너지(ATP)를 생산할 수 있는 수많은 미토콘드리아를 가지고 있다. 원위성 경련관에서 일어나는 이온 수송의 대부분은 내분비계에 의해 조절된다. 부갑상선 호르몬이 있는 상태에서 원위경련된 관모는 더 많은 칼슘을 재흡수하고 인산염을 더 분비한다. 알도스테론이 있으면 더 많은 나트륨이 재흡수되고 더 많은 칼륨이 분비된다. 암모니아도 선택적 재흡수 과정에서 흡수된다. 심방 나트륨 펩타이드로 인해 원위경련된 튜불레가 더 많은 나트륨을 분비하게 된다.
연결 튜브울레
원위 네프론의 한 부분이다. 이것은 관이 집진 덕트 시스템에 들어가기 전의 마지막 부분이다.물, 소금, 그리고 요소와 크레아티닌 같은 질소성 폐기물은 관을 모으는데 사용된다.
집진 덕트 시스템
각 원위성 경련된 관은 그 여과물을 덕트 수집 시스템에 전달하는데, 그 중 첫 번째 부분이 연결 관이다. 집진 덕트 체계는 신장피질에서 시작하여 중수심 깊숙한 곳까지 확장된다. 소변이 집광관 계통을 따라 내려가면서 헨리의 역류 승수 계통의 고리로 인해 나트륨 농도가 높은 명상간막염을 통과한다.[1]: 67
비뇨기, 생식기의 발달 과정에서 다른 네프론의 일부와는 다른 기원을 가지기 때문에, 채취 도관은 네프론의 일부로 여겨지지 않는 경우도 있다. 메탄페로겐성 발진에서 발원하지 않고, 채취 도관은 요관성 싹에서 발원한다.[11]: 50–51
집수관은 일반적으로 물에 불침투성이지만 항이뇨호르몬(ADH)이 있으면 스며들 수 있게 된다. ADH는 아쿠아포린의 기능에 영향을 주어, 수집용 도관을 통과할 때 물 분자가 재흡수되게 된다. 아쿠아포린은 이온과 다른 용액의 통과를 막으면서 물 분자를 선택적으로 전도하는 막 단백질이다. 소변에서 나오는 물의 4분의 3은 삼투에 의해 집수관을 빠져나가기 때문에 재흡수가 가능하다. 따라서 ADH의 수준은 소변이 농축될 것인지 또는 희석될 것인지를 결정한다. ADH의 증가는 탈수증의 징후인 반면, 수분 부족은 ADH의 감소로 인해 소변이 희석된다.[4]: 406

채취 장기의 낮은 부분 역시 요소에게 투과되어 그 일부가 메둘라에 들어갈 수 있게 되어 높은 농도(네프론에게는 매우 중요하다)를 유지하게 된다.[1]: 73–74
소변은 신낭을 통해 수혈관을 빠져나와 신장결반인 신낭골반으로 비우고, 마지막으로 요관을 통해 요로 방광으로 들어간다.[4]: 406–407
헥타글로머 기구
준대칭형 기구(JGA)는 네프론과 관련된 전문 영역이지만 그것과는 별개다. 안지오텐시노겐을 분해해 10가지 아미노산 물질인 안지오텐신-1(A-1)을 만들어 순환으로 분비한다. 그런 다음 A-1은 두 개의 아미노산을 제거함으로써 강력한 혈관신산인 안지오텐신-2로 변환된다: 이것은 안지오텐신 변환 효소(ACE)에 의해 이루어진다. 이러한 일련의 사건을 레닌-안지오텐신계(RAS) 또는 레닌-안지오텐신알도스테론계(RAAS)라고 한다. JGA는 두꺼운 상승 사지와 다른 동맥 사이에 위치한다. 그것은 세 가지 성분을 포함하고 있다: 황반 밀도, 육각체 세포, 외각체 중상세포.[4]: 404
임상적 유의성
네프론의 질병은 주로 글루머룰리나 관에 영향을 미친다. 글루머성 질환은 당뇨병성 신혈증, 글루머론염, IgA 신혈증을 포함한다. 신관성 질환은 급성관괴사, 신장관산증, 다낭성 신장질환을 포함한다.
추가 이미지
참고 항목
참조
- ^ Jump up to: a b c d e f g h Lote, Christopher J. (2012). Principles of Renal Physiology, 5th edition. Springer.
- ^ Pocock, Gillian; Richards, Christopher D. (2006). Human physiology : the basis of medicine (3rd ed.). Oxford: Oxford University Press. p. 349. ISBN 978-0-19-856878-0.
- ^ Jump up to: a b J., Tortora, Gerard (2010). Principles of anatomy and physiology. Derrickson, Bryan. (12th ed.). Hoboken, NJ: John Wiley & Sons. ISBN 9780470233474. OCLC 192027371.
- ^ Jump up to: a b c d e f Mescher, Anthony L. (2016). Junqueira's Basic Histology, 14th edition. Lange.
- ^ 생태학 & 진화 생물학 - 콜로라도 대학교 볼더 "신장 튜불레 1: 소변생성." URL: http://www.colorado.edu/eeb/web_resources/cartoons/nephrex1.html. 액세스 날짜: 2007년 3월 6일. 2007년 10월 2일 웨이백 머신에 보관
- ^ Hook, Jerry B. & Goldstein, Robin S. (1993). Toxicology of the Kidney. Raven Press. p. 8. ISBN 0-88167-885-6.CS1 maint: 작성자 매개변수 사용(링크)
- ^ Nosek, Thomas M. "Section 7/7ch03/7ch03p16". Essentials of Human Physiology. Archived from the original on 2016-03-24.
- ^ Jameson, J. Larry & Loscalzo, Joseph (2010). Harrison's Nephrology and Acid-Base Disorders. McGraw-Hill Professional. p. 3. ISBN 978-0-07-166339-7.CS1 maint: 작성자 매개변수 사용(링크)
- ^ "Regulation of Urine Concentration". Anatomy & Physiology. CliffsNotes. Archived from the original on 25 October 2012. Retrieved 27 November 2012.
- ^ Walter F. Boron (2005). Medical Physiology: A Cellular And Molecular Approaoch. Elsevier/Saunders. p. 743. ISBN 1-4160-2328-3.
- ^ Mitchell, Barry; Sharma, Ram (2009). Embriology, 2nd edition. Churchill Livingstone Elsevier.