족구
Podocyte| 팟사이트* | |
|---|---|
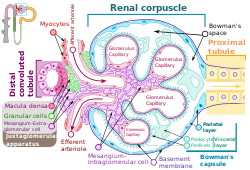 신소체 구조 혈액은 위쪽의 구심성 동맥과 아래쪽의 구심성 동맥으로 흐른다.혈액은 사구체의 모세혈관을 통해 흐르는데, 사구체는 압력에 의해 여과된다.족구(녹색)는 모세혈관을 감싸고 있습니다.혈액은 발 사이 또는 팟구 과정 사이에서 슬릿 다이어프램(또는 여과 슬릿)을 통해 여과됩니다.여과된 혈액은 우측 근위세관(노란색)으로 흐릅니다. | |
| 세부 사항 | |
| 전구체 | 중간 중배엽 |
| 위치 | 신장의 보우만 캡슐 |
| 식별자 | |
| 라틴어 | 포도사이투스 |
| 메쉬 | D050199 |
| 미세해부술의 해부학적 용어 | |
포드 세포는 사구체의 모세혈관을 감싸고 있는 신장의 보먼 캡슐에 있는 세포이다.포드 세포는 혈액의 여과가 [1]일어나는 세 번째 층인 Bowman's capsule의 상피 내벽을 구성합니다.Bowman's capsule은 혈액을 여과하여 단백질과 같은 큰 분자를 유지하는 반면 물, 소금, 설탕과 같은 작은 분자는 소변 형성의 첫 번째 단계로 여과된다.비록 다양한 내장들이 상피층을 가지고 있지만, 내장상피세포라는 이름은 보통 캡슐의 내장층에 상주하는 특화된 상피세포인 포도구를 특별히 지칭한다.특화된 상피세포의 한 종류는 포드칼렉신이다.
이 족구들은 족저세포라고 불리는 긴 발 과정을 가지고 있는데, 이 과정에서 세포들은 (족저세포)라고 이름 붙여집니다.페디셀은 모세혈관을 감싸고 그 사이에 틈을 남긴다.혈액은 여과 슬릿, 슬릿 다이어프램 또는 슬릿 [2]모공을 통해 여과됩니다.페디셀이 모세혈관을 감싸고 기능하기 위해서는 몇 가지 단백질이 필요하다.신생아가 네프린과 CD2AP와 같은 단백질에 특정한 결함을 가지고 태어났을 때, 그들의 신장은 기능을 할 수 없다.사람들은 이러한 단백질에 변이가 있고, 어떤 변이는 그들이 나중에 신부전을 일으키게 할 수 있습니다.네프린은 지퍼처럼 생긴 단백질로, 지퍼의 치아 사이는 설탕과 물이 통과할 수 있을 만큼 크지만 단백질이 통과할 수 있도록 하기에는 너무 작다.네프린 결손은 선천성 신부전의 원인이다.CD2AP는 팟구 세포골격을 조절하고 슬릿 [3][4]다이어프램을 안정화시킵니다.
구조.
팟사이트는 신장의 네프론에서 보우만 캡슐을 배열하는 것을 발견한다.족저구로부터 뻗어나가는 족저돌기로 알려진 족저돌기는 여과 슬릿을 형성하기 위해 사구체의 모세혈관을 감싼다.페디셀은 세포 표면적을 증가시켜 효율적인 여과 [5]효과를 발휘합니다.
포도세포의 기저외측 영역을 따라 다수의 코팅된 소포와 코팅된 피트가 있으며, 이는 소포 트래픽의 높은 비율을 나타낸다.
팟 세포는 잘 발달된 소포체와 큰 골지 기구를 가지고 있으며, 이는 단백질 합성과 번역 후 수식을 위한 높은 용량을 나타낸다.
또한 이러한 세포에서 볼 수 있는 다세포체 및 다른 리소좀 성분의 증거가 증가하고 있으며, 이는 높은 세포내 활성을 나타낸다.
기능.
족구들은 사구체 모세혈관을 [6]감싸는 트라베큘라라고 불리는 1차 과정을 가지고 있다.그리고 트라베큘라는 [6]페디셀이라고 불리는 2차 과정을 가지고 있다.페디셀은 서로 얽혀서 여과 [2]슬릿이라고 불리는 얇은 틈을 만든다.슬릿은 혈청 알부민 및 감마 글로불린과 같은 큰 고분자의 통과를 제한하고 혈류에 [7]남아있게 하는 네프린, 포드칼렉신 및 P-카드헤린을 포함한 다수의 세포 표면 단백질로 구성된 슬릿 다이어프램으로 덮여 있다.슬릿 다이어프램의 올바른 기능에 필요한 단백질에는 네프린,[8] NEPH1, NEPH2,[9] 포드신, CD2AP [10]및 FAT1이 [11]포함된다.
물, 포도당, 이온염과 같은 작은 분자는 여과 슬릿을 통과하여 관상액에 초여과체를 형성할 수 있으며, 이는 네프론에 의해 더욱 처리되어 소변을 생성한다.
포도구는 사구체 여과율(GFR) 조절에도 관여한다.팟구들이 수축하면, 그들은 여과 슬릿의 폐쇄를 일으킨다.이를 통해 여과 가능한 표면적을 줄임으로써 GFR을 줄일 수 있습니다.
임상적 의의
포도구(podocyte)의 발 과정의 손실(즉, 포도구 소실)은 최소 변화 질환의 특징이며, 따라서 때때로 발 과정 [12]질환이라고 불린다.
여과 슬릿의 교란이나 팟구 파괴는 대량의 단백뇨를 유발할 수 있으며, 그곳에서 많은 양의 단백질이 혈액에서 손실된다.
이것의 예는 선천성 장애 핀란드형 신증에서 발생하며, 이는 말기 신부전으로 이어지는 신생아 단백뇨를 특징으로 한다.이 병은 네프린 유전자의 돌연변이에 의한 것으로 밝혀졌다.
소변에 팟구 존재는 [13]전립선증의 조기 진단 지표로 제안되었다.
「 」를 참조해 주세요.
레퍼런스
- ^ 도란드 의학사전에 수록되어 있는 "포도구"
- ^ a b c Lote, Christopher J. Principles of Renal Physiology, 5th edition. Springer. p. 34.
- ^ Wickelgren, I. (1999). "CELL BIOLOGY: First Components Found for Key Kidney Filter". Science. 286 (5438): 225–6. doi:10.1126/science.286.5438.225. PMID 10577188. S2CID 43237744.
- ^ Löwik MM, Groenen PJ, Levtchenko EN, Monnens LA, van den Heuvel LP (November 2009). "Molecular genetic analysis of podocyte genes in focal segmental glomerulosclerosis—a review". Eur. J. Pediatr. 168 (11): 1291–304. doi:10.1007/s00431-009-1017-x. PMC 2745545. PMID 19562370.
- ^ Nosek, Thomas M. "Section 7/7ch04/7ch04p08". Essentials of Human Physiology. Archived from the original on 2016-03-24.
- ^ a b Ovalle, William K.; Nahirney, Patrick C. (28 February 2013). Netter's Essential Histology E-Book. Elsevier Health Sciences. ISBN 9781455703074. Retrieved 2 June 2020.
- ^ Jarad, G.; Miner, J. H. (2009). "Update on the glomerular filtration barrier". Current Opinion in Nephrology and Hypertension. 18 (3): 226–232. doi:10.1097/mnh.0b013e3283296044. PMC 2895306. PMID 19374010.
- ^ Wartiovaara, J.; Ofverstedt, L. G. R.; Khoshnoodi, J.; Zhang, J.; Mäkelä, E.; Sandin, S.; Ruotsalainen, V.; Cheng, R. H.; Jalanko, H.; Skoglund, U.; Tryggvason, K. (2004). "Nephrin strands contribute to a porous slit diaphragm scaffold as revealed by electron tomography". Journal of Clinical Investigation. 114 (10): 1475–1483. doi:10.1172/JCI22562. PMC 525744. PMID 15545998.
- ^ Neumann-Haefelin, E.; Kramer-Zucker, A.; Slanchev, K.; Hartleben, B.; Noutsou, F.; Martin, K.; Wanner, N.; Ritter, A.; Gödel, M.; Pagel, P.; Fu, X.; Müller, A.; Baumeister, R.; Walz, G.; Huber, T. B. (2010). "A model organism approach: Defining the role of Neph proteins as regulators of neuron and kidney morphogenesis". Human Molecular Genetics. 19 (12): 2347–2359. doi:10.1093/hmg/ddq108. PMID 20233749.
- ^ Fukasawa, H.; Bornheimer, S.; Kudlicka, K.; Farquhar, M. G. (2009). "Slit Diaphragms Contain Tight Junction Proteins". Journal of the American Society of Nephrology. 20 (7): 1491–1503. doi:10.1681/ASN.2008101117. PMC 2709684. PMID 19478094.
- ^ Ciani L; Patel A; Allen ND; ffrench-Constant C. (2003). "Mice lacking the giant protocadherin mFAT1 exhibit renal slit junction abnormalities and a partially penetrant cyclopia and anophthalmia phenotype". Mol. Cell. Biol. 23 (10): 3575–82. doi:10.1128/mcb.23.10.3575-3582.2003. PMC 164754. PMID 12724416.
- ^ Ciani L; Massella L; Ruggiero B; Emma F (2017). "Minimal Change Disease". Clin J Am Soc Nephrol. 12 (2): 332–345. doi:10.2215/CJN.05000516. PMC 5293332. PMID 27940460.
- ^ Konieczny, A; Ryba, M; Wartacz, J; Czyżewska-Buczyńska, A; Hruby, Z; Witkiewicz, W (2013). "Podocytes in urine, a novel biomarker of preeclampsia?" (PDF). Advances in Clinical and Experimental Medicine. 22 (2): 145–9. PMID 23709369.
외부 링크
- 해부 사진: 비뇨기/유모기/맥관1/vasc1 - 데이비스 캘리포니아 대학의 비교 기관 - "유모기, 신장 혈관 구조(EM, High)
- 조직학 이미지: 22401loa – 보스턴 대학의 조직학 학습 시스템 - ". 세포의 초미세 구조: 포드 세포와 사구체 모세혈관"
- UIUC 조직학 제목 1400
- Samuel[permanent dead link] Lunenfeld 연구소의 podocyte.ca
- Nosek, Thomas M. "Section 7/7ch04/7ch04p09". Essentials of Human Physiology. Archived from the original on 2016-03-24.
- 조직 이미지: 22402loa – 보스턴 대학의 조직학 학습 시스템
- 조직 이미지: 22403loa – 보스턴 대학의 조직학 학습 시스템





