질소
Nitrogen | |||||||||||||||||||||
| 질소 | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 외관 | 무색의 가스, 액체 또는 고체 | ||||||||||||||||||||
| 표준 원자량 Ar, std(N) | [14.00643, 14.00728] 관습: 14.007[1] | ||||||||||||||||||||
| 주기율표의 질소 | |||||||||||||||||||||
| |||||||||||||||||||||
| 원자번호 (Z) | 7 | ||||||||||||||||||||
| 그룹 | 15그룹(독소제) | ||||||||||||||||||||
| 기간 | 기간 2 | ||||||||||||||||||||
| 블록 | p-block | ||||||||||||||||||||
| 전자 구성 | [He] 2s2 2p3 | ||||||||||||||||||||
| 셸당 전자 | 2, 5 | ||||||||||||||||||||
| 물리적 성질 | |||||||||||||||||||||
| 위상 STP서 | 가스 | ||||||||||||||||||||
| 녹는점 | (N2) 63.23[2] K(-209.86[2] °C, -345.75[2] °F) | ||||||||||||||||||||
| 비등점 | (N2) 77.355 K (−195.795 °C, −320.431 °F) | ||||||||||||||||||||
| 밀도 (STP) | 0.2506 g/L[3](0°C, 1013 mbar) | ||||||||||||||||||||
| 액체가 있을 때 ( ) | 0.808 g/cm3 | ||||||||||||||||||||
| 트리플 포인트 | 63.151K, 12.52kPa | ||||||||||||||||||||
| 임계점 | 126.21 K, 3.39 MPa | ||||||||||||||||||||
| 융해열 | (N2) 0.72 kJ/mol | ||||||||||||||||||||
| 기화열 | (N2) 5.57 kJ/mol | ||||||||||||||||||||
| 어금니열용량 | (N2) 29.124 J/(몰·K) | ||||||||||||||||||||
증기압력
| |||||||||||||||||||||
| 원자성 | |||||||||||||||||||||
| 산화 상태 | -3, -2, -1, +1, +2, +3, +4, +5(강산성 산화물) | ||||||||||||||||||||
| 전기성 | 폴링 스케일: 3.04 | ||||||||||||||||||||
| 이온화 에너지 |
| ||||||||||||||||||||
| 공동 반지름 | 71±1pm | ||||||||||||||||||||
| 반데르발스 반지름 | 오후 155시 | ||||||||||||||||||||
| 질소의 스펙트럼 라인 | |||||||||||||||||||||
| 기타 속성 | |||||||||||||||||||||
| 자연발생 | 원시적인 | ||||||||||||||||||||
| 결정구조 | 육각형의 | ||||||||||||||||||||
| 음속 | 353m/s (가스, 27°C에서) | ||||||||||||||||||||
| 열전도도 | 25.83×10−3 W/(m³K) | ||||||||||||||||||||
| 자기순서 | 반자성의 | ||||||||||||||||||||
| CAS 번호 | 17778-88-0 7727-37-9 (N2) | ||||||||||||||||||||
| 역사 | |||||||||||||||||||||
| 디스커버리 | 대니얼 러더퍼드 (1772) | ||||||||||||||||||||
| 이름: | 장안토인 채프탈 (1790) | ||||||||||||||||||||
| 질소 주 동위 원소 | |||||||||||||||||||||
| |||||||||||||||||||||
질소는 기호 N과 원자 번호 7을 가진 화학 원소다. 1772년 스코틀랜드 의사 다니엘 러더포드에 의해 처음 발견되어 격리되었다. 칼 빌헬름 스크힐과 헨리 카벤디쉬가 거의 동시에 독자적으로 그렇게 했음에도 불구하고 러더포드는 그의 작품이 먼저 출판되었기 때문에 일반적으로 공로를 인정받고 있다. 니트로겐이라는 이름은 1790년 프랑스의 화학자 장 앙투안-클로드 채팔이 질산과 질산염에 질소가 존재한다는 사실을 발견했을 때 제안한 것이다. 앙투안 라부아지에르는 대신 고대 그리스어에서 아조테라는 이름을 제안했다. 아조테는 질식성 가스인 만큼 ἀζoteτι " " "no life"; 이 이름은 대신 프랑스어, 이탈리아어, 러시아어, 루마니아어, 포르투갈어, 터키어와 같은 많은 언어로 사용되며 히드라진, 아지데스, 아조 화합물과 같은 일부 질소 화합물의 영어 이름에 나타난다.
질소는 주기율표 15그룹 중 가장 가벼운 구성원으로, 흔히 pnictorges라고 불린다. 그것은 은하계와 태양계에서 총 7번째로 풍부한 것으로 추산되는 우주에서 흔한 원소다. 표준 온도와 압력에서 원소의 두 원자가 결합하여 N이라는2 공식으로 무색 무취의 이원자 기체인 이뇨제(dinitrogen)를 형성한다. 다이니트로겐은 지구 대기의 약 78%를 형성하고 있어 가장 풍부한 결합되지 않은 원소가 된다. 질소는 주로 아미노산(따라서 단백질), 핵산(DNA 및 RNA) 및 에너지 전달 분자 아데노신 삼인산(adenosine triphosphate)에서 모든 유기체에서 발생한다. 인체는 질량별로 약 3%의 질소를 함유하고 있는데, 이는 체내에서 산소, 탄소, 수소에 이어 네 번째로 풍부한 원소다. 질소 순환은 공기 중에서 원소가 생물권과 유기 화합물로 이동한 다음 다시 대기권으로 이동하는 것을 설명한다.
암모니아, 질산, 유기질산염(프로펠러제와 폭발물), 시안화물과 같이 산업적으로 중요한 많은 화합물들은 질소를 함유하고 있다. 일산화탄소(CO)에 이어 두 번째로 강한 원소 질소(NN)의 삼중결합이 질소화학에 지배적이다.[4] 이것은 N을2 유용한 화합물로 바꾸는 데 있어 유기체와 산업 모두에 어려움을 야기하지만, 동시에 질소 가스를 형성하기 위해 질소 화합물을 태우거나 폭발시키거나 분해하는 것은 많은 양의 유용한 에너지를 방출한다는 것을 의미한다. 합성 생산한 암모니아와 질산염은 주요 산업용 수정제이며, 수정질산염은 물 시스템의 영토화에서 중요한 오염물질이다.
질소는 비료와 에너지 저장소에 사용되는 것 외에도 고강도 직물에 사용되는 케블라와 슈퍼글루에서 사용되는 시아노아크릴레이트만큼 다양한 유기 화합물의 성분이다. 질소는 항생제를 포함한 모든 주요 약리학적 약물의 성분이다. 많은 약물은 천연 질소 함유 신호 분자의 모방 또는 약물로, 예를 들어 유기 질산염 니트로글리세린과 니트로프루시드는 질소산화물로 대사하여 혈압을 조절한다. 천연 카페인과 모르핀 또는 합성암페타민과 같은 많은 주목할 만한 질소 함유 약물은 동물 신경전달물질의 수용체에 작용한다.
역사

질소 화합물은 매우 오랜 역사를 가지고 있는데, 염화암모늄은 헤로도토스에게 알려져 있다. 그것들은 중세시대에 의해 잘 알려져 있었다. 연금술사들은 질산을 아쿠아 포티스(강수)로 알았으며 암모늄염과 질산염과 같은 다른 질소 화합물도 알고 있었다. 질산과 염산의 혼합물은 금속의 왕인 금을 녹이는 능력으로 유명한 아쿠아 레기아(로열수)로 알려져 있다.[5]
질소가 발견된 것은 1772년 스코틀랜드 의사 다니엘 러더포드(Daniel Lutherford)가 질소를 유해한 공기라고 부른 덕분이다.[6][7] 전혀 다른 화학 물질로 인식하지는 않았지만 조셉 블랙의 '고정 공기', 즉 이산화탄소와 분명히 구별했다.[8] 연소를 지원하지 않는 공기의 성분이 있다는 사실은 러더포드에게는 원소라는 것을 알지 못했지만 분명한 사실이었다. 질소도 칼 빌헬름 스힐레,[9] 헨리 카벤디쉬,[10] 조셉 프리스틀리에 의해 거의 동시에 연구되었는데,[11] 그는 질소를 연소된 공기 또는 세련된 공기로 언급하였다. 프랑스의 화학자 앙투안 라부아지에르는 질소 가스를 그리스어 άζ due greek word ( ((Azotikos)에서 '메프티트 공기' 또는 아조테(Azotikos)'로 지칭했는데, 대부분이 불활성이기 때문에 '생명은 없다'는 것이다.[12][13] 순수한 질소의 대기 속에서 동물들이 죽고 불꽃이 꺼졌다. 라부아지에의 이름은 영어로 받아들여지지 않았지만, 거의 모든 가스(사실 산소를 제외한 유일한 가스)가 메피티크(mephatic)라고 지적되었기 때문에, 여러 언어(프랑스어, 이탈리아어, 포르투갈어, 폴란드어, 러시아어, 알바니아어, 터키어 등)에서 사용되고 있다; 독일어 스틱스토프는 이와 유사한 특징인 viz를 가리킨다. 에르스티켄 "질식하거나 질식할 것") 그리고 여전히 히드라진과 아지드 이온의 화합물과 같은 많은 질소 화합물의 공통적인 이름으로 영어로 남아있다. 마침내, 질소가 이끄는 집단의 이름인 "질소"를 그리스 πνγεεν"에서 "질소"로 이끌었다.[5]
영어 단어 질소(1794)는 1790년 프랑스의 화학자 장 앙투안 채프탈(1756–1832)이 만든 프랑스 니트로겐에서,[14] 프랑스 니트로그레(질산칼륨, 소금피터라고도 불림)와 그리스어 -νςς(-genes, "begotten")의 프랑스 접미사 -gen에서 온 언어로 들어갔다. 챕탈의 의미는 질소가 질산의 필수적인 부분이고, 질소는 질소에서 생산된다는 것이었다. 일찍이 niter는 그리스어로 νίτρον(nitron)이라 불리는 이집트어의 "나트론"(탄산수소산염)과 혼동했는데, 그 이름에도 불구하고 질산은 전혀 들어 있지 않았다.[15]
질소 화합물의 가장 초기 군사, 산업 및 농업 용도는 화약에 가장 두드러지게 사용된 염전계(질산염 또는 질산칼륨)를 사용했으며, 나중에는 비료로 사용했다. 1910년, Rayleigh 경은 질소 가스의 전기 방전이 질소의 단원자 할당 로프인 "활성 질소"를 생산한다는 것을 발견했다.[16] 그의 기구에 의해 생성된 "밝은 노란 빛의 휘몰아치는 구름"은 폭발성 질화 수은을 생산하기 위해 수은과 반응했다.[17]
오랫동안, 질소 화합물의 공급원은 제한적이었다. 자연원은 생물학이나 대기 반응에 의해 생성된 질산염의 퇴적물에서 유래한다. 프랭크-카로 공정(1895–1899)과 하버-보쉬 공정(1908–1913)과 같은 산업 공정에 의한 질소 고정은 현재 전 세계 식품 생산의 절반이 합성 질소 수정제에 의존할 정도로 질소 화합물의 부족을 완화시켰다.[18] 이와 동시에 산업용 질소 고정으로부터 질산염을 생산하기 위해 오스왈드 공정(1902)을 사용함으로써 20세기 세계 대전에서 폭발물 제조에 있어서 질산염을 공급원료로 대규모 산업생산이 가능해졌다.[19][20]
특성.
아토믹
질소 원자는 7개의 전자를 가지고 있다. 접지 상태에서는 전자 구성 1s2s2p2p2p2p로2
2
1
x1
y1
z 배열된다. 따라서 2s와 2p 궤도에 5개의 발란스 전자를 가지고 있는데, 그 중 3개(p-electron)는 (p-electron)이 손상되지 않았다. 그것은 원소들 중 가장 높은 전기적 특성(폴링 눈금 3.04) 중 하나로 염소(3.16), 산소(3.44), 불소(3.98)만으로 초과된다. (빛 고귀한 가스, 헬륨, 네온, 아르곤도 추정컨대 더 전기적일 것이며, 사실 앨런 눈금이다.)[21] 주기적인 추세에 따라 오후 71시 1본드 공밸런스 반경은 붕소(84시)와 탄소(76시)보다 작고 산소(66시)와 불소(57시)보다 크다. 질화 음이온 N은3− 146pm으로 산화물(O2−:140pm)과 플루오르화(F−:133pm) 음이온과 비슷해 훨씬 크다.[21] 질소의 처음 3개 이온화 에너지는 1.402, 2.856, 4.577 MJ·몰이며−1, 4번째와 5번째의 합은 16.920 MJ·몰이다−1. 이러한 매우 높은 수치 때문에 질소는 단순한 양이온화학이 없다.[22]
2p 서브셸에 방사형 노드가 없는 것은 특히 질소, 산소, 불소 등 p-블록의 첫 번째 행의 변칙적인 특성 다수를 직접적으로 담당한다. 2p 서브쉘은 매우 작고 2s 쉘과 매우 유사한 반경을 가지고 있어 궤도 잡종을 용이하게 한다. 또한 2s와 2p 껍질에서 핵과 발란스 전자 사이에 매우 큰 정전기력을 발생시켜 매우 높은 전기적 흡수를 초래한다. 고효율성은 2p 원소에서도 거의 알려져 있지 않은데, 이는 높은 전기가중성으로 인해 작은 질소 원자가 전자가 풍부한 3중추 4전자 결합에서 중심 원자가 되기 어렵게 하기 때문이다. 따라서 주기율표에서 그룹 15의 선두에 있는 질소의 위치에도 불구하고, 그것의 화학은 더 무거운 착향료인 인, 비소, 안티몬, 비스무트와는 엄청난 차이를 보인다.[23]
질소는 피닉토겐 기둥, 인, 비소, 안티몬 및 비스무트 내 수직 인접뿐만 아니라 수평 인접 탄소 및 산소와 유용하게 비교될 수 있다. 리튬에서 산소에 이르는 각 주기 2 원소는 다음 그룹의 주기 3 원소(마그네슘에서 염소까지, 이것들은 대각선 관계라고 알려져 있음)와 일부 유사성을 보이기는 하지만, 이들의 정도는 붕소-실리콘 쌍을 지나 갑자기 떨어진다. 질소와 유황의 유사성은 두 원소가 모두 존재하는 경우 대부분 황질화합물로 제한된다.[24]
질소는 탄소의 포화도를 공유하지 않는다. 탄소처럼 질소는 금속과 이온성 또는 금속성 화합물을 형성하는 경향이 있다. 질소는 사슬, 그래피티, 풀레네릭 같은 구조를 가진 질소를 포함하여 탄소를 포함한 광범위한 질화물을 형성한다.[25]
수소 결합에 대한 전기적응력과 응집력이 높고, 단독 전자쌍을 기증해 조정 콤플렉스를 형성하는 능력이 있어 산소와 닮았다. 암모니아 NH와3 물 HO의2 화학성분 사이에는 몇 가지 유사점이 있다. 예를 들어, 두 화합물의 용량은 NH와4+ HO를3+ 주기 위해 양성되거나 NH와2− OH를− 주기 위해 감압되어야 하며, 이들 모든 화합물은 고체 화합물에서 격리될 수 있다.[26]
질소는 p-pππ 상호작용을 통해 일반적으로 탄소, 산소 또는 기타 질소 원자와 복수 결합을 형성하는 선호를 수평적 인접 영역과 공유한다.[24] 따라서2 예를 들어 질소는 이원자 분자로 발생하며 따라서 N 분자는 약한 반데르 발 상호 작용에 의해서만 결합되고 상당한 순간 쌍극점을 생성하기 위해 사용할 수 있는 전자가 거의 없기 때문에 나머지 그룹보다 용융(-210 °C)과 비등점(-196 °C)이 매우 낮다. 이것은 수직 이웃에게는 가능하지 않다. 따라서 질소산화물, 질산염, 질산염, 니트로-, 니트로소-, 아조-와 디아조-복합물, 아지드, 시안산염, 티오시아네이트 및 이미노-데리버스는 인, 비소, 안티몬 또는 비스무트와의 메아리를 발견하지 못한다. 그러나 같은 이유로 인산염의 복잡성은 질소와의 메아리를 발견하지 못한다.[24] 질소와 인은 그 차이를 제쳐두고 서로 광범위한 화합물을 형성한다; 이것들은 체인, 고리, 그리고 케이지 구조를 가지고 있다.[27]
동위 원소
질소에는 N과 N이라는 두 가지 안정된 동위원소가 있다. 첫째는 천연질소의 99.634%를 차지해 훨씬 흔하고, 둘째(약간 무거운)는 나머지 0.366%를 차지한다. 이것은 약 14.007 u의 원자량으로 이어진다.[21] 이 두 가지 안정적인 동위원소는 모두 별에서 CNO 사이클로 생산되지만, 중성자 포획이 속도 제한 단계여서 N이 더 흔하다. 14N은 5개의 안정적인 홀수-오드 핵종(양자와 중성자의 홀수 수를 갖는 핵종) 중 하나이며, 나머지 4개는 H, Li, B, Ta이다.[28]
N과 N의 상대적 풍부함은 사실상 대기에서 일정하지만 생물학적 리독스 반응에 의한 자연 동위원소 분율과 천연 암모니아나 질산의 증발 때문에 다른 곳에서는 다를 수 있다.[29] 생물학적으로 매개된 반응(예: 동화, 질소화, 변성화)은 토양 내 질소 역학을 강력하게 제어한다. 이러한 반응은 일반적으로 기질이 N농축되고 제품이 고갈되는 결과를 초래한다.[30]
무거운 동위원소 N은 인접한 원소 산소와 탄소의 무거운 동위원소가 발견된 직후인 1929년 S. M. Naudé에 의해 처음 발견되었다.[31] 그것은 모든 동위원소 중에서 가장 낮은 열 중성자 포획 단면 중 하나이다.[32] 핵자기공명(NMR) 분광법에 자주 사용돼 질소 함유 분자의 구조를 결정하는 데 사용되는데, 이는 단수 핵 스핀으로 선폭이 좁아지는 등 NMR에 유리하다. 14N은 이론적으로도 사용할 수 있지만 정수의 핵 스핀이 1이므로 4극 모멘트를 가지므로 스펙트럼이 넓어지고 유용성이 떨어진다.[21] 그럼에도 15불구하고 NMR은 보다 일반적인 H와 C NMR 분광법에서는 발생하지 않은 합병증을 가지고 있다. 자연 풍부도가 낮은 N(0.36%)은 감도를 현저히 감소시키는데, 이는 낮은 자석비 때문에만 악화되는 문제(H의 10.14%에 불과하다)이다. 그 결과 H의 신호 대 잡음 비율은 동일한 자기장 강도에서 N의 신호 대 잡음 비보다 약 300배 정도 높다.[33] 이는 화학 교환 또는 부분 증류에 의한 N의 동위원소 농축에 의해 다소 완화될 수 있다. 15N-농축 화합물은 대기에서 멀리 떨어져 있어야 하는 수소, 탄소, 산소 동위원소로 표시된 화합물과 달리 표준 조건에서 대기 질소와 질소 원자의 화학적 교환을 거치지 않는다는 장점이 있다.[21] N:14N 비는 일반적으로 지질화학, 수문학, 고생물학, 고생물학, 고생물학 분야에서 안정적 동위원소 분석에 사용되는데, 여기서 ΔN이라고15 한다.[34]
N에서 N까지의 범위에 걸쳐 합성적으로 생산된 다른 10개의 동위원소 중 N은 10분의 반감기를 가지며, 나머지 동위원소는 초(16N과 N) 또는 밀리초의 순서로 반감기를 가진다. 다른 질소 동위원소는 핵 방울선 밖으로 떨어져 양성자나 중성자가 누출될 수 있기 때문에 불가능하다.[35] 비록 그것의 반감기 여전히, 그리고 또한 그것은은 PET로 현장에서 예를 들어 사이클로트론에서 생산된 것이어야 한다 16O의 양성자 폭격 13N고 알파 입자를 통해 짧은half-life 차이를 감안할 때, 13N이 가장 중요한 질소 방사성 동위 원소, 상대적으로 충분히 양전자 방출 단층 촬영(PET)에 사용할이고 오래 사는.[36]
방사성 동위원소 N은 정상운전 중 가압수형 원자로 또는 비등수형 원자로의 냉각재 내 지배적인 방사성핵종이며, 따라서 1차 냉각재계통에서 2차 증기주기까지의 누출을 민감하고 즉각적인 지표로, 그러한 누설에 대한 1차적인 검출 수단이다. O 원자가 중성자를 포획하고 양성자를 배출하는 (n,p) 반응을 통해 O(물 안)에서 생성된다. 약 7.1초의 짧은 반감기를 가지고 있지만,[35] O로 되돌아가는 동안 고에너지 감마선(5 ~ 7 MeV)을 생성한다.[35][37] 이 때문에 가압수형 원자로의 1차 냉각재 배관에 대한 접근이 원자로 출력 운전 중에 제한되어야 한다.[37]
화학 및 화합물
코로프스

활성 질소라고도 알려진 원자 질소는 반응성이 매우 높으며, 세 개의 전자가 손상되지 않은 삼극성 물질이다. 자유 질소 원자는 질화물을 형성하기 위해 대부분의 원소와 쉽게 반응하며, 심지어 두 개의 자유 질소 원자가 충돌하여 흥분된2 N 분자를 생성할 때에도 이산화탄소와 물과 같은 안정된 분자와 충돌할 때 너무나 많은 에너지를 방출하여 CO와 O 또는 OH와 H와 같은 활성산소로 균질성 핵분열을 일으킬 수 있다. 원자 질소는 0.1~2mmHg의 질소 가스를 통해 방출되는 전기를 통과시켜 준비하는데, 방출이 종료된 후에도 수 분 동안 서서히 여광으로 사라지는 복숭아 황색 방출과 함께 원자 질소를 생산한다.[24]
원자 질소의 큰 반응성을 감안할 때, 원소 질소는 보통 분자2 N, 이니트로겐으로 발생한다. 이 분자는 표준 조건에서 무색, 무취, 무미취의 직경 기체로 -210 °C에서 녹고 -196 °C에서 끓는다.[24] 다이니트로겐은 상온에서는 대부분 비활성화되지만, 그럼에도 불구하고 리튬 금속과 일부 전이 금속 복합체와 반응할 것이다. 이는 NnN 삼중결합이 있다는 점에서 표준 조건에서 이원자 원소들 사이에서 독특한 결합 때문이다. 트리플 본드는 결합 길이가 짧고(이 경우 오후 109.76), 분리에너지(이 경우 945.41 kJ/mol)가 높으며, 따라서 다이니트로겐의 화학적 불활성성을 설명하면서 매우 강하다.[24]
다른 질소 과점자와 폴리머가 가능할지도 모른다는 이론적인 징후들이 있다. 만약 그것들이 합성될 수 있다면, 그것들은 강력한 추진체나 폭발물로 사용될 수 있는 매우 높은 에너지 밀도를 가진 물질로서 잠재적인 응용을 가질 수 있다.[38] N=N 이중결합(418kJ⋅mol−1)이나 N–N 단일결합(160kJ⋅mol−1)보다 N=N 이중결합(본드 에너지 946kJ⋅mol−1)이 훨씬 강한 다이니트로겐으로 분해해야 하기 때문이다. 실제로 트리플결합은 단일 결합의 세 배 이상의 에너지를 갖는다. (다원자 할당제를 선호하는 중량의 피닉토균에 대해서는 그 반대다.[39] 가장 큰 단점은 대부분의 중성 폴리니트로겐이 분해에 대한 큰 장벽이 없을 것으로 예상되며, 몇 가지 예외는 오래되었지만 여전히 알려지지 않은 사면체보다 합성하기가 훨씬 더 어려울 것이라는 점이다. 이것은 잘 특징지어지는 양식과 음이온성 폴리니트로겐스 아지드(N−
3), 펜타제늄(N+
5), 펜타졸라이드(순환 방향제−
5 N)와 대조된다.[38] 다이아몬드 앤빌 셀에서 생산되는 극도로 높은 압력(110만 atm)과 고온(2000 K)에서는 질소 중합체가 단일 본드 입방 거슈 결정 구조로 들어간다. 이 구조는 다이아몬드와 유사하며, 두 가지 모두 극히 강한 공밸런스 결합을 가지고 있어 '질소 다이아몬드'[40]라는 별명이 붙었다.
대기압에서 분자 질소는 77K(-195.79°C)에서 응축되고 63K(-210.01°C)[41]에서 동결되어 베타 육각형 근접 포장 결정 편중성 형태로 된다. 35.4 K(-237.6 °C) 이하의 질소는 입방 결정 편중성 형태(알파 위상이라고 함)[42]를 가정한다. 액체 질소는 겉보기에는 물을 닮았지만 밀도의 80.8%(비등점에서의 액체 질소 밀도는 0.808g/mL)로 일반적인 극저온이다.[43] 고체 질소는 많은 결정적인 변화를 가지고 있다. 그것은 명왕성과[44] 트리톤과 같은 태양계의 외부 달에서 상당한 동적 표면적을 형성한다.[45] 고형질소의 낮은 온도에서도 그것은 상당히 휘발성이 강하며 대기를 형성하거나 다시 질소 서리로 응축될 수 있다. 그것은 매우 약하고 빙하의 형태로 흐르며 질소 가스의 트리톤 간헐천에서는 극지방의 만년설 지역에서 나온다.[46]
다이니트로겐 복합체
처음 발견된 이디트로겐 복합체의 예는 [Ru(NH3)(5N2)]2+ (오른쪽 그림 참조)이었고, 곧 그러한 복합체들이 많이 발견되었다. 질소 분자가 적어도 한 쌍의 전자를 중앙 금속 양이온에 기증하는 이러한 복합체들은 N이2 질소산화물과 하버 공정의 촉매에 어떻게 결합할 수 있는지를 보여준다: 이 과정은 생물학과 수정체 생산에 있어 매우 중요하다.[47][48]
디니트로겐은 다섯 가지 다른 방법으로 금속과 조정할 수 있다. 더욱 잘 특징지어지는 방법은 질소 원자의 외로운 쌍을 금속 양이온에 기증하는 종단면 M←N≡N(η1)과 M←N→M(μ, bis-η1)이다. 덜 특성화된 방법에는 3중 결합의 전자 쌍을 결합 리간드(μ, bis-η) 두 개의 금속 양이온(μ, bis-2)) 또는 단 한 개(η2)에 기증하는 다이니트로겐이 포함된다. 다섯 번째이자 독특한 방법은 브리징 리간드로서 삼중 조율을 수반하는 것으로, 3중 결합(μ-N32)으로부터 3중 전자쌍을 모두 기증한다. 몇 개의 콤플렉스는 복수의2 N 리간드를 특징으로 하고, 어떤 콤플렉스는 다방면으로 결합된 N을2 특징으로 한다. N은2 일산화탄소(CO)와 아세틸렌(CH22)을 포함한 등전자로 되어 있기 때문에, 비록 N이2 CO보다 bonding-도너 및 than-수용체이기는 하지만, 이디로겐 복합체의 결합은 카보닐 화합물에서의 결합과 밀접하게 연관되어 있다. 이론적 연구에서는 주로 N-N 채권을 약화시킬 뿐인 π 백-N 채권보다는 formation 기부가 M-N 채권 형성을 허용하는 더 중요한 요인이며, 사이드온(η2) 기부보다 엔드온(η1)[24] 기부가 더 쉽게 이뤄진다.
오늘날, 다이니트로겐 복합체는 거의 모든 전이 금속으로 알려져 있으며, 수백 개의 화합물을 차지한다. 일반적으로 다음과 같은 세 가지 방법으로 준비된다.[24]
- 질소로2 HO, H− 또는 CO와 같은 실험용 리간드를 직접 대체하는 것: 이것들은 보통 가벼운 조건에서 진행되는 가역 반응이다.
- 질소 가스 하에서의 과도한 콜리간드 존재 시 금속 복합체 감소. 염화 리간드를 원래의 염소 리간드보다 적은 수의 질소 리간드를 보충하기 위해 디메틸페닐인산염(PMePh2)으로 대체하는 것이 일반적인 선택이다.
- 히드라진이나 아지드 같은 N–N 결합을 가진 리간드를 다이니트로겐 리간드로 직접 변환한다.
때때로 N complexN 결합은 금속 복합체 내에서 직접 형성될 수 있다. 예를 들어, 조정된 암모니아(NH3)를 질산(HNO2)과 직접 반응시킴으로써, 그러나 이것은 일반적으로 해당되지 않는다. 대부분의 다이니트로겐 복합체는 흰색-노란색-주황색-적갈색 범위 내에 색상을 가지고 있으며, 청색[{Ti(η-CH555)}-(22N2)][24]과 같은 몇 가지 예외가 알려져 있다.
니트리데스, 아지드, 니트리도 복합체
질소는 처음 3개의 고귀한 기체, 헬륨, 네온, 아르곤을 제외한 주기율표의 거의 모든 원소와 비스무트 이후의 매우 짧은 원소들 중 일부를 결합하여 다양한 성질과 용도를 가진 엄청나게 다양한 이항 화합물을 만들어 낸다.[24] 많은 이항 화합물이 알려져 있다: 질소 하이드리드, 산화물과 불소를 제외하고, 이것들은 일반적으로 질산염이라고 불린다. 일반적으로 대부분의 원소에 대해 많은 정지계량 단계가 존재한다(예: 9.2 < x < 25.3의 경우 MnN, MnN65, MnN32, MnN2, MN4, MN, MNx) 이러한 분류는 일반적으로 그것이 내포하고 있는 이산형 및 분리형 대신 결합형의 연속성에서 기인하는 한계가 있지만 "소금형"(대부분 이오닉), 공밸런트형, "다이아몬드형", 금속성(또는 중간형)으로 분류될 수 있다. 일반적으로 금속을 질소나 암모니아와 직접 반응시키거나(가끔 가열 후) 금속 아미드의 열분해로 준비한다.[49]
- 3 Ca + N2 → Ca3N2
- 3 Mg + 2 NH3 → MgN32 + 32 H (900 °C에서)
- 3Zn(NH2)2 → ZnN32 + 4NH3
이러한 공정에서 많은 변형이 가능하다. 이들 질화물질 중 가장 이온성이 높은 것은 알칼리 금속과 알칼리성 지금속인 LiN3(나, K, Rb, Cs)과 MN32(M = Be, Mg, Ca, Sr, Ba)이다. 이러한 높은 전기적 요소에도 실제로 전하 분리가 완료되지는 않지만, 이러한 것들은 공식적으로3− N 음이온의 소금으로 생각할 수 있다. 그러나 선형 N−
3 음이온이 특징인 알칼리 금속 아지드 NaN과3 KN은3 Sr(N3)2과 Ba(N)와3 마찬가지로 잘 알려져 있다.2B 서브그룹 금속(그룹 11~16)의 아지드들은 이오닉이 훨씬 적고 구조가 복잡하며, 충격을 받았을 때 쉽게 폭발한다.[49]
많은 공동의 이산화질소가 알려져 있다. 예를 들면 시아노겐(CN),2 삼인산 펜타니트라이드35(PN), 이황산 디니트라이드22(SN), 테트라술푸르 테트라황산 테트라니트라이드(SN44) 등이 있다. 기본적으로 질화규소(SiN34)와 질화 게르마늄(GeN34)도 알려져 있다: 특히 질화규소(질화규소)는 그것과 함께 작업하고 소결시키는 어려움이 없다면 유망한 세라믹을 만들 것이다. 특히 반도체 유망주인 13개 질산염 그룹은 흑연, 다이아몬드, 실리콘 카바이드 등이 포함된 등전자로 그룹이 하강하면서 공밸런트에서 부분적으로 이온화, 금속화 등으로 본딩이 바뀌는 구조도 비슷하다. 특히 B-N 단위는 C-C와 등전자로 되어 있고 탄소는 기본적으로 붕소와 질소 사이의 중간 크기이기 때문에 유기 화학의 상당 부분은 붕소-질소 화학에서 메아리를 발견한다("유기농 벤젠"). 그럼에도 불구하고 전자가 부족하여 붕소의 핵포함 공격이 용이하여 유추되는 것이 정확하지 않은데, 이는 완전히 탄소가 함유된 링에서는 가능하지 않다.[49]
질산염의 가장 큰 범주는 공식 MN, MN2, MN4, MN의 중간 질산염이다(변형 구성이 완벽하게 가능하기는 하지만), 작은 질소 원자가 금속 입방체나 육각형 근접 포장 격자 내의 틈새에 위치한다. 그것들은 불투명하고, 매우 단단하며, 화학적으로 불활성이며, 매우 높은 온도에서만 녹는다(일반적으로 2500 °C 이상). 그들은 금속 광택을 가지고 있고 금속처럼 전기를 전도한다. 그들은 암모니아나 질소를 주기 위해 아주 천천히 수력분해한다.[49]
질화 음이온(N3−)은 리간즈 중에서 가장 강한 π 기증자(두2− 번째로 강한 것은 O)이다. 니트리도 콤플렉스는 일반적으로 아지드화물의 열분해나 감응 암모니아에 의해 만들어지며, 주로 단자 {≡N}3− 그룹을 포함한다. 선형 아지드 음이온(N−
3)은 아산화질소, 이산화탄소, 시안산염과 함께 이소전자화되어 많은 조정 콤플렉스를 형성한다. N4−
4(탄산염과 질산염을 함유한 이소전자)이 알려져 있지만, 더 이상의 강도는 드물다.[49]
하이드라이드

산업적으로 암모니아(NH3)는 질소의 가장 중요한 화합물이며 다른 어떤 화합물보다 많은 양으로 준비되는데, 이는 음식과 수정체의 전구체 역할을 함으로써 지상 유기체의 영양 요구에 크게 기여하기 때문이다. 특유의 톡 쏘는 냄새가 나는 무색 알칼리 가스다. 수소 결합의 존재는 암모니아에 매우 큰 영향을 미치며 암모니아에 높은 용해(-78°C)와 비등(-33°C) 지점을 부여한다. 액체로써 기화열이 매우 높은 용매(진공 플라스크에 사용할 수 있게 함)로서 점도와 전기전도도가 낮고 유전체 상수가 높으며, 물보다 밀도가 낮다. 그러나 산소에 비해 질소의 전기성이 낮고 HO에2 2쌍이 아닌 NH에3 1쌍만 존재하기 때문에 NH의3 수소 본딩은 HO에2 비해 약하다. 수성용액(pK 4.74)의 약한 기초로서, 그것의b 결합산은 암모늄, NH+
4. 또한 양자를 잃고 극히 약한 산으로 작용하여 아미드 음이온을 생산할−
2 수 있다. 따라서 암모늄과 아미드를 생산하기 위해 물과 유사한 자가 분열을 겪는다. 암모니아는 질소 가스를 생산하기 위해 공기나 산소에서 연소한다. 암모니아는 녹황색 불꽃과 함께 불소에서 연소하여 질소 3불화물을 만든다. 다른 비금속과의 반응은 매우 복잡하고 제품의 혼합으로 이어지는 경향이 있다. 암모니아는 금속과 난방에 반응하여 질화물을 만든다.[51]
다른 많은 바이너리 질소 하이드라이드가 알려져 있지만 가장 중요한 것은 히드라진(NH24)과 수소 아지드(HN3)이다. 비록 질소 하이드라이드는 아니지만 히드록시아민(NHOH2)은 암모니아, 히드라진과 성질과 구조가 비슷하다. 히드라진은 암모니아와 비슷한 냄새가 나는 훈증기 없는 액체다. 물리적 특성은 물과 매우 유사하다(용융점 2.0°C, 비등점 113.5°C, 밀도 1.00g/cm3). 내열성 화합물임에도 불구하고 운동적으로 안정적이다. 그것은 질소와 수증기를 주기 위해 매우 외기적으로 빠르게 완전히 연소한다. 매우 유용하고 다재다능한 환원제로 암모니아보다 약한 염기성분이 있다.[52] 로켓 연료로도 흔히 쓰인다.[53]
히드라진은 일반적으로 암모니아와 차아염소산나트륨의 알칼리성 반응을 통해 젤라틴이나 접착제가 있는 곳에서 만들어진다.[52]
- NH3 + OCl− → NH2Cl + OH−
- NHCl2 + NH3 → NH
2+
5 + Cl− (느림) - NH
2+
5 + OH− → NH24 + HO2(고속)
(수산화물과 암모니아에 의한 공격은 역전되어 대신 중간 NHCl을− 통과할 수 있다.) 젤라틴을 첨가하는 이유는 모노클로로아민(NHCl2)과 반응해 히드라진 파괴를 촉진하는 Cu2+ 등 금속 이온을 제거해 염화암모늄과 질소를 생산하기 때문이다.[52]
아지드화수소(HN3)는 질산에 의한 수성 하이드라진 산화에 의해 1890년에 처음 생산되었다. 그것은 매우 폭발적이고 심지어 희석된 용액도 위험할 수 있다. 그것은 불쾌하고 짜증나는 냄새를 가지고 있고 잠재적으로 치명적인 독이다. 아지드 음이온의 결합산으로 간주될 수 있으며, 하이드로할산과 유사하다.[52]
할로겐화물과 옥소할라이드
단순 질소 3할라이드 4개가 모두 알려져 있다. 몇 가지 혼합 할로겐화물과 하이드로할라이드는 알려져 있지만 대부분 불안정하다. 예를 들어 NClF2, NClF2, NBrF2, NFH2, NFH2, NClH2, NClH2 등이 있다.[54]
5개의 질소 불소가 알려져 있다. 삼불화질소(NF3, 1928년 처음 준비)는 무색무취의 무취의 기체로 열역학적으로 안정적이며, 무수 수소 불소에 용해된 용융암모늄 불소의 전기분해로 가장 쉽게 생성된다. 테트라플루오르화 탄소처럼 전혀 반응하지 않고 물에서 안정적이거나 수용산이나 알칼리를 희석한다. 가열해야 불소화제 역할을 하며 고온에서 접촉 시 구리, 비소, 안티몬, 비스무트와 반응해 테트라플루오로하이드라진(NF24)을 공급한다. 계량 NF와+
4 NF는
2+
3 부분 이중3 결합을 의미하는 짧은 N–O 거리와 극성 및 긴 N–F 결합으로 관심을 불러일으킨 ONF와 마찬가지로 (후자는 비소 펜타플루오린과 같은 강한 불소 수용체와 함께 테트라플루오로하이드라진을 반응시킴으로써)도 알려져 있다. 테트라플루오로하이드라진은 히드라진 자체와는 달리 상온 이상에서 분리되어 급진적인 NF2•를 부여할 수 있다. 플루오린 아지드(FN3)는 폭발성이 매우 높고 열적으로 불안정하다. 다이니트로겐 이플루오르화(NF22)는 열간 변환성 시스와 트랜스 이소머로 존재하며, FN의3 열분해 산물로 처음 발견되었다.[54]
질소 트리클로라이드(NCL3)는 질소가 풍부하고 휘발성, 폭발성 액체로 물리적 성질이 탄소 테트라클로로이드와 유사하지만, NCl은3 물에 의해 쉽게 가수분해되는 반면4 CCl은 그렇지 않다는 것이 한 가지 차이점이다. 1811년 피에르 루이 둘롱에 의해 처음 합성되었는데, 그는 손가락 세 개와 폭발적인 경향에 대한 눈을 잃었다. 희석된 기체로서 덜 위험하며 따라서 산업적으로 밀가루를 표백하고 살균하는데 사용된다. 1975년 처음 제조된 질소 트리브로마이드(NBr3)는 -100 °C에서도 폭발성이 있는 진한 적색, 온도에 민감한 휘발성 고체다. 질소삼중화(NI3)는 여전히 불안정해 1990년에야 준비됐다. 앞서 알려진 암모니아를 가진 그것의 유도체는 충격에 매우 민감하다. 그것은 깃털의 촉각, 기류 이동 또는 심지어 알파 입자에 의해서도 작동될 수 있다.[54][55] 이 때문에 소량의 질소 3iodide는 고등학교 화학 학생에 대한 데모나 "화학적 마술"[56]의 행위로 합성되기도 한다. 염소 아지드(ClN3)와 브롬 아지드(BrN3)는 극도로 민감하고 폭발적이다.[57][58]
두 종류의 질소산화물이 알려져 있다: 니트로실 할로겐화물(XNO)과 니트로실 할로겐화물(XNO2)이다. 첫번째는 아산화질소를 직접 할로겐화하여 만들 수 있는 매우 반응성이 좋은 기체들이다. NOF(Nitrosyl fluoride)는 무색이며 활력 있는 불소화제다. 염화 니트로실(NOCl)은 거의 같은 방식으로 작용하며 종종 이온화 용매로 사용되어 왔다. 니트로실 브롬화(NOBr)는 붉은색이다. 질화 할로겐화물의 반응은 대부분 비슷하다: 질화 불소화질(Nitryl fluoride, FNO2)[54]과 염화질화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소화질소2
산화제
질소는 9개의 분자 산화물(Nitrooxide2), NO(Nitric oxide), NO23(삼산화질소), NO2(이산화질소), NO(이산화질소), NO24(이산화질소), NO25(이산화질소), NO4(니트로실라자이드),[59] N(Nitrosylazide), N(NO2)3의 첫 번째 기체였다.[60] 모두 열적으로 불안정한 상태로 원소로 분해된다. 아직 합성되지 않은 또 다른 가능한 산화물은 방향족 고리인 옥사테트라졸(NO4)이다.[59]
웃음가스로 더 잘 알려진 아산화질소(NO2)는 250℃에서 녹은 암모늄 질산염의 열분해로 만들어진다. 이것은 리독스 반응이며 따라서 질소산화물과 질소 또한 부산물로 생산된다. 스프레이된 통조림 생크림의 추진제 및 에어로제 등으로 주로 사용되며, 이전에는 마취제로 많이 사용되었다. 겉보기에도 불구하고 저산은 물에 있는 아산화질소의 용해로 생성되지 않기 때문에 저포니틸산(HNO222)의 무수화물로 볼 수 없다. 그것은 다소 비활성적이며(난방에 따라 반응도가 증가하지만 실온에서 할로겐, 알칼리 금속 또는 오존과 반응하지 않음) 비대칭 구조 N–N–O(NHNO+− £−N=N+=O): 600°C 이상에서 약한 N–O 결합을 깨뜨림으로써 분리된다.[59]
산화질소(NO)는 홀수 전자를 가진 가장 단순한 안정 분자다. 인간을 포함한 포유류에서, 그것은 많은 생리적, 병리적 과정에 관여하는 중요한 세포 신호 분자다.[61] 그것은 암모니아의 촉매 산화에 의해 형성된다. 열역학적으로 불안정하여 1100–1200 °C에서 질소와 산소 가스로 분해되는 무색 파라마그네틱 가스다. 그것의 결합은 질소에서의 결합과 유사하지만, 1개의 추가 전자가 orbital* 항균 궤도상에 추가되어 결합 순서는 약 2.5로 감소되었다. 따라서 O=N–N=O로 조광하는 것은 실제적으로 전체 결합 순서와 베카로 증가하지 않기 때문에 비등점 이하(cis isomer가 더 안정적인 곳)를 제외하고는 바람직하지 않다.사용하지 않는 전자는 NO 분자에 걸쳐 분산되어 안정성이 부여된다. 산화질소가 극성 분자와 응축될 때 비대칭 적색 조광기 O=N–O=N에 대한 증거도 있다. 그것은 산소와 반응하여 이산화 갈색의 질소를 주고 할로겐과 반응하여 니트로시릴이 할로겐을 할로겐화시킨다. 또한 전이 금속 화합물과 반응하여 니트로실 콤플렉스를 주기도 하는데, 대부분은 색이 짙다.[59]
삼산화 청색 이산화질소(NO23)는 녹는점 이상으로 빠르게 분리돼 질소산화물, 이산화질소(NO2), 이산화질소(NO24)를 주기 때문에 고체로만 사용할 수 있다. 후자의 두 화합물은 때로는 유전체 상수가 높은 매질에서 질산염과 질산염에 대한 이질성 핵분열에 의해 반응할 수 있지만, 그들 사이의 평형 때문에 개별 연구하기는 다소 어렵다. 이산화질소는 매캐하고 부식성이 있는 갈색 기체다. 두 화합물 모두 건조 금속 질산염을 분해하여 쉽게 준비할 수 있다. 둘 다 물과 반응하여 질산을 형성한다. 디니트로겐 테트로사이드(Dinitrogen Tetroxide)는 무수 금속 질산염과 니트라토 복합체를 준비하는데 매우 유용하며, 1950년대 후반에 이르러서는 미국과 USSR 양쪽에서 많은 로켓에 선택되는 저장성 산화제가 되었다. 하이드라진 기반의 로켓 연료와 결합한 쌍곡 추진체로 상온에서 액체 상태여서 쉽게 저장할 수 있기 때문이다.[59]
열적으로 불안정하고 매우 반응성이 높은 오산화 이디트로겐(NO25)은 질산의 무수체로, 오산화 인을 탈수하여 만들 수 있다. 폭발물 준비에 관심이 쏠린다.[62] 그것은 조명에 민감한 조미료성 무색 결정체 고체다. 고체 상태에서는 [NO2] 구조로 이온성이다[+NO3];− 기체로서 그리고 용액으로는 분자 ON2–O–NO2. 과산화수소와 유사한 반응으로 과산화수소산(HUNO2)을 주는 것과 마찬가지로 질산에 대한 수화도 쉽게 발생한다. 그것은 격렬한 산화제다. 오산화질소 기체 이디트로겐은 다음과 같이 분해된다.[59]
- N2O5 ⇌ NO2 + NO3 → NO2 + O2 + NO
- N2O5 + NO ⇌ 3 NO2
옥소아시드, 옥소아니온, 옥소아시드염
산화질소는 대부분 순수한 화합물로 불안정하고 수용액이나 소금으로만 알려져 있지만 많은 질소산화물이 알려져 있다. 저포니톨산(HNO222)은 HON=NOha1(pK 6.9a2, pK 11.6) 구조를 가진 약한 디프로이트산이다. 산성 용액은 상당히 안정적이지만 pH 4 이상의 염기 촉매 분해는 [HONO]를 통해 아산화질소와 −수산화 음이온으로 발생한다. 저포니트라이트는 (NO
22−
2 음이온을 방출하는) 에이전트 감소에 안정적이며, 더 일반적으로 에이전트 자체를 감소시키는 역할을 한다. 그것들은 질소 사이클에서 발생하는 암모니아와 질산염의 산화의 중간 단계다. 저포니트라이트는 브리징이나 킬레이트 바이덴산 리간드로 작용할 수 있다.[63]
아질산(HNO2)은 순수 화합물로 알려져 있지 않지만 기체 평형성의 일반적인 성분이며 중요한 수용성 시약이다. 아질산 및 아질산화에 대한 상온 불균형이 이미 심하지만 그것의 수용액은 시원한 아큐스 아퀴라이트(NO−
2, 구부러진) 용액으로 만들어질 수 있다. 18 °C에서a pK 3.35를 가진 약한 산이다. 그들은 과망간산염에 의한 질산화에 의해 적정하게 분석될 수 있다. 이산화황에 의해 아산화질소와 아산화질소로, 주석(II)으로 저포니트로, 황화수소로 암모니아로 쉽게 감소한다. NH
2+
5 하이드라지늄의 염은 아지드화물을 생성하기 위해 아지드화물을 생성하며 아지드화물은 아지드화물과 질소를 생성한다. 아질산나트륨은 100mg/kg 이상의 농도에서 약한 독성이 있지만, 적은 양이 육류를 치료하고 세균의 부패를 피하기 위한 방부제로 사용되는 경우가 많다. 또한 [63]다음과 같이 히드록시아민 합성 및 1차 방향족 합성에도 사용된다.
- ArNH2 + HNO2 → [ArNN]Cl + 2 H2O
아질산염은 또한 다섯 가지 방법으로 조정될 수 있는 흔한 리간드다. 가장 흔한 것은 니트로(질소로부터 결합)와 니트리토(산소에서 결합)이다. 니트로-니트리토 이소메르리즘은 흔하며, 니트로리토 형태가 보통 덜 안정적이다.[63]
질산(HNO3)은 질소산화물 중에서 단연코 가장 중요하고 가장 안정적이다. 그것은 3개의 가장 많이 사용된 산들 중 하나이며, 13세기에 연금술사들에 의해 처음 발견되었다. 암모니아에서 질소산화물로의 촉매 산화에 의해 만들어지며, 이는 이산화질소로 산화되었다가 물에 녹아서 진한 질산을 준다. 미국에서는 매년 7백만 톤 이상의 질산이 생산되는데, 그 대부분은 다른 용도 중에서도 비료와 폭발물을 위한 질산염 생산에 사용된다. 무수 질산은 어둠 속에서 유리 기구에 있는 저압으로 오산화 인으로 농축 질산을 증류하여 만들 수 있다. 녹으면 자연적으로 이산화질소로 분해되고 액체 질산은 다음과 같은 다른 공동의 액체보다 더 큰 범위에서 자가이온화를 겪기 때문에 고체 상태에서만 만들 수 있다.[63]
- 2 HNO3 ⇌ HNO
2+
3 + NO−
3 ⇌ HO2 + [NO2]+ + [NO] + [NO3]−
하이드레이트 2개, HNO3·HO2, HNO3·3HO는2 결정화 될 수 있는 것으로 알려져 있다. 강한 산이며 농축액은 강한 산화제지만 금, 백금, 로듐, 이리듐은 공격에 면역이 된다. 아쿠아 리지아라고 불리는 농축 염산과 질산을 3:1로 혼합한 것은 유리염소와 니트로실 염화물이 형성되고 염화 음이온이 강한 콤플렉스를 형성할 수 있기 때문에 여전히 강하고 금과 백금을 성공적으로 용해한다. 농축 황산에서는 질산이 양성되어 니트로늄을 형성하는데, 이는 방향성 질화의 전기적 역할을 할 수 있다.[63]
- HNO3 + 2 H2SO4 ⇌ NO+
2 + H3O+ + 2 HSO−
4
질산염의 열안정성(삼각 평면−
3 NO 음이온의 분해)은 금속의 기본성에 따라 달라지며, 분해(열분해)의 산물도 달라지는데, 이는 질산염(예를 들어 나트륨), 산화물(칼륨과 납) 또는 심지어 금속 자체(은)의 상대 안정성에 따라 달라질 수 있다. 질산염은 또한 많은 조정 방식을 가진 흔한 리간드다.[63]
마지막으로, 정형인산(Othophosphoric acid)과 유사한 정형화된 산(HNO34)은 존재하지 않지만, 사면정직교정산 음이온 NO는3−
4 나트륨과 칼륨 염에서 알려져 있다.[63]
이러한 백색 결정염은 수증기와 공기 중의 이산화탄소에 매우 민감하다.[63]
- Na3NO4 + H2O + CO2 → NaNO3 + NaOH + NaHCO3
직교 음이온은 화학 작용이 제한되어 있음에도 불구하고 규칙적인 사면체 형태와 짧은 N-O 결합 길이 때문에 구조적인 관점에서 흥미롭기 때문에 본딩에 상당한 극성을 의미한다.[63]
유기질소 화합물
질소는 유기화학에서 가장 중요한 요소 중 하나이다. 많은 유기 기능적인 그룹, 아민, imines(RC(=NR)R)(R3N),(청구 통제 담당관)2NR, 이미드 화물 azides(RN3), 아조 화합물, cyanates과 isocyanates(RN2R)(ROCN 또는 RCNO),(ReactorCentrumNederland또는 RNC)(RONO2), nitriles과 isonitriles nitrates, nitrites(RONO), 니트로 화합물(RNO2), 니트로소 화합물,(RNO)oximes(RCR= 아미드 같은 carbon–nitrogen 채권,(RCONR2)을 포함한다.NOH), 그리고 피리딘 유도체. C-N 결합은 질소를 향해 강하게 편광된다. 이러한 화합물에서 질소는 보통 3가(양자 암모늄 염, RN에서4+ 4가(tetravalent)로 할 수 있지만, 양성자로 조정되어 화합물에 기본성을 부여할 수 있는 한 쌍의 짝을 가지고 있다. 이것은 다른 요인에 의해 상쇄될 수 있다. 예를 들어, 아미드는 단독 쌍이 이중 결합으로 분해되기 때문에 기본이 아니며(산소에서 양성되는 매우 낮은 pH에서 산으로 작용할 수 있지만), 피롤은 단독 쌍이 방향 고리의 일부로 분해되기 때문에 산성이 아니다.[64] 화학 물질 내 질소의 양은 크젤달 방법에 의해 결정될 수 있다.[65] 특히 질소는 핵산, 아미노산, 단백질, 에너지 운반 분자 아데노신 삼인산염의 필수 성분으로 지구상의 모든 생명체에 필수적이다.[64]
발생
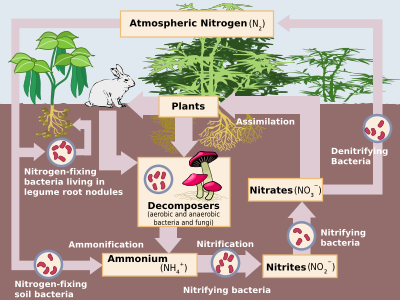
질소는 지구에서 가장 흔한 순수 원소로 대기권의 78.1%를 차지한다.[5] 그럼에도 불구하고, 이것은 니오비움, 갈륨, 리튬과 동등한, 백만분의 19부분만을 차지하는 지구 표면에서는 그리 풍부하지 않다. 중요한 질소 미네랄은 질산칼륨(질산칼륨, 소금페테르)과 소다 질산염(질산염, 칠레산 소금페테르)뿐이다. 그러나 이것들은 암모니아와 질산의 산업 합성이 보편화된 1920년대 이후 질산염의 중요한 공급원이 되지 못했다.[66]
질소 화합물은 끊임없이 대기와 살아있는 유기체들 사이를 교환한다. 질소는 먼저 식물이 사용할 수 있는 형태(보통 암모니아)로 가공하거나 "고정"해야 한다. 일부 질소 고정은 질소산화물을 생성하는 낙뢰에 의해 이루어지지만, 대부분은 질소화합물로 알려진 효소를 통해 디아조티균에 의해 이루어진다(오늘날 암모니아에 대한 산업용 질소 고정도 중요하다). 암모니아는 식물이 차지하면 단백질을 합성하는데 사용된다. 그리고 나서 이 식물들은 질소 화합물을 이용하여 단백질을 합성하고 질소를 함유한 폐기물을 배설하는 동물들에 의해 소화된다. 마지막으로, 이 유기체들은 죽어서 분해되고 박테리아와 환경 산화 및 변성화 과정을 거치며, 대기 중으로 자유이식성분을 되돌려준다. 하버 공정에 의한 산업용 질소 고정은 대부분 비료제로 사용되지만, 질소 주도의 박테리아 성장은 모든 상위 유기체가 죽을 정도로 수산소를 고갈시키기 때문에 과도한 질소 내성 폐기물이 담수의 영농화와 해양 데드존의 생성으로 이어진다. 게다가 변성화 과정에서 생성되는 아산화질소는 대기 오존층을 공격한다.[66]
많은 소금물고기는 환경의 높은 삼투압 효과로부터 그들을 보호하기 위해 많은 양의 트리메틸아민 산화물들을 제조한다; 이 화합물을 디메틸아민으로 전환시키는 것은 신선한 소금물고기의 초기 냄새를 책임진다.[67] 동물들에게 있어서, 프리 래디컬 산화물은 순환을 위한 중요한 규제 분자의 역할을 한다.[68]
동물에서의 물과 질산염의 빠른 반응은 대사 물질인 질산염을 생산하게 한다. 일반적으로 단백질 내 질소의 동물대사는 요소의 배설, 핵산의 동물대사는 요소와 요산의 배설으로 이어진다. 동물성 살점 부패의 특징적인 악취는 각각 아미노산 오르니틴과 리신의 분해 산물인 퍼트레신, 카다베린과 같은 긴 사슬의 질소 함유 아민이 부패 단백질에서 생성되면서 발생한다.[69]
생산
질소 가스는 액체 공기의 분수 증류 또는 기체 공기(압축 역삼투막 또는 압력 스윙 흡착)를 이용하여 기계적으로 생산되는 산업용 가스다. 막이나 압력 스윙 흡착(PSA)을 사용하는 질소 가스 발생기는 일반적으로 대량 공급 질소보다 비용과 에너지 효율이 높다.[70] 상업용 질소는 종종 제강 및 기타 목적을 위한 산업용 산소 농도를 위한 공기 처리의 부산물이다. 실린더에 압축된 상태로 공급될 때 종종 OFN(산소 없는 질소)이라고 불린다.[71] 상업용 질소는 이미 최대 20ppm의 산소를 함유하고 있으며, 최대 2ppm의 산소와 10ppm의 아르곤을 함유한 특수 정제 등급도 이용할 수 있다.[72]
화학 실험실에서는 염화암모늄의 수용액을 아질산나트륨으로 처리하여 제조한다.[73]
- NH4Cl + NaNO2 → N2 + NaCl + 2 H2O
이 반응에서 불순물 NO와 HNO의3 소량도 형성된다. 불순물은 중크롬산칼륨이 함유된 수성황산을 통해 기체를 통과시켜 제거할 수 있다.[73] 매우 순수한 질소는 바륨 아지드화나트륨 아지드화물의 열분해로 준비될 수 있다.[74]
- 2 NaN3 → 2 Na + 3N2
적용들
가스
질소 화합물의 용도는 이 등급의 거대한 크기 때문에 자연적으로 매우 다양하다. 따라서 순수 질소 자체의 용도에 대해서만 고려될 것이다. 산업에서 생산되는 질소의 3분의 2(2/3)는 가스로, 나머지 1/3(1/3)은 액체로 판매된다.
기체는 공기 중의 산소가 화재, 폭발 또는 산화 위험을 일으킬 때마다 대부분 불활성 대기로 사용된다. 일부 예는 다음과 같다.[72]
- 순수하거나 이산화탄소와 혼합된 변형된 대기로서 포장 또는 대량 식품의 신선도를 질소화 및 보존하기 위해(질소화 및 기타 형태의 산화 손상 지연에 의해) 식품 첨가제로서의 순수한 질소는 유럽 연합에 E 941이라는 라벨이 붙어 있다.[75]
- 백열등에서는 아르곤의 저렴한 대안으로 백열등을 사용한다.[76]
- 정보 기술(IT)[72] 장비를 위한 화재 진압 시스템.
- 스테인리스강 제조에 있어서.[77]
- 질화하여 강철을 케이스 경화시키는 경우.[78]
- 화재 위험을 줄이기 위한 일부 항공기 연료 시스템(불활성화 시스템 참조)
- 경주용 자동차와 항공기 타이어를 팽창시키기 위해,[79] 자연 공기의 수분과 산소에 의해 야기되는 일관되지 않은 팽창과 수축의 문제를 줄인다.[72]
질소는 화학적 분석에서 샘플 준비 중에 일반적으로 사용된다. 액체 샘플의 부피를 농축하고 줄이기 위해 사용된다. 가압된 질소 가스의 흐름을 액체 표면에 수직으로 유도하면 용매와 비증발 용매를 남겨둔 채 용매가 증발한다.[80]
질소는 탄산가스를 대체하거나 이산화탄소와 결합하여 맥주통, 특히 스타트와 영국산 에일을 가압할 수 있는데, 이는 분산이 된 맥주를 더 부드럽고 더 잘 보이게 하기 때문이다.[81] 흔히 "위젯"으로 알려진 압력에 민감한 질소 캡슐은 질소를 충전한 맥주를 캔과 병에 담아 포장할 수 있게 해준다.[82][83] 질소 탱크도 페인트볼 총의 주요 동력원으로 이산화탄소를 대체하고 있다. 질소는 CO보다2 높은 압력을 유지해야 하므로 N 탱크가2 무겁고 비싸다.[84]
장비
일부 건설 장비는 유압 시스템이 유압 해머와 같은 장치에 추가 전력을 공급하도록 돕기 위해 가압된 질소 가스를 사용한다. 아지드화나트륨의 분해로 형성된 질소 가스는 에어백의 팽창에 사용된다.[85]
안락사
질소 가스는 불활성 가스를 질식시킬 때 선택하는 불활성 가스가 되었고, 오클라호마에서 치사 주사를 대체할 것으로 검토되고 있다.[86][87]
질소가 질식성 가스인 만큼 일부 관할구역에서는 순수한 질소를 흡입해 불활성 가스를 질식시키는 것을 사형(치사주사의 대체물로서)의 수단으로 간주해 왔다.[88] 그러나 2020년[update] 현재, 아직 어느 관할구역에서도 질소 가스를 이용한 처형은 실시되지 않았으며, 질소 질식사(질소 질식사)를 실행 프로토콜로 간주해 온 적어도 하나의 관할권(오클라호마)은 그 노력을 포기했다.[89]
액체
액체 질소는 극저온성 액체다. 드워 플라스크와 같은 적절한 용기에 절연되었을 때, 그것은 낮은 증발 손실률로 운반되고 보관될 수 있다.[90]
드라이아이스와 마찬가지로 액체 질소의 주된 용도는 저온으로의 냉각에 있다. 혈액과 생식세포(sperm, 달걀)와 같은 생물학적 물질의 극저온 보존에 사용된다. 피부의 낭종과 사마귀 등을 얼려 제거하는데 크라이요법에 쓰인다.[91] 이는 실험실 콜드 트랩과 크라이오펌프에서 진공 펌프 시스템에 낮은 압력을 얻기 위해 사용된다. 적외선 검출기, X선 검출기 등 열에 민감한 전자장치를 냉각하는 데 쓰인다. 다른 용도로는 상온에서 부드럽거나 고무가 있는 동결 그라인딩 및 가공 재료, 수축 및 조립 엔지니어링 부품, 그리고 필요한 경우 매우 낮은 온도를 달성하는 더 일반적인 재료 등이 있다. 액체 질소는 비용이 저렴하기 때문에 식품 냉동, 가축 동결 브랜드화, 밸브가 없을 때 흐름을 멈추기 위한 파이프 동결, 지하에서 굴착이 진행될 때마다 얼려 불안정한 토양을 굳히는 등 저온에서도 냉각에 이용되는 경우가 많다.[72]
안전
가스
질소는 독성이 없지만 밀폐된 공간에 방출되면 산소를 대체할 수 있으므로 질식 위험성이 있다. 이는 경동맥이 상대적으로 열악하고 느린 저산소(저산소증) 감지 시스템이기 때문에 거의 경고 증상이 나타나지 않을 수 있다.[92] 1981년 3월 19일 제1차 우주왕복선 임무 개시 직전, 화재 예방 차원에서 순수 질소로 가압된 우주왕복선 이동식 발사대 플랫폼에 위치한 우주로 기술자 2명이 걸어 들어간 후 질식사해 사망하는 사례가 발생했다.[93]
높은 부분압력(약 4bar 이상, 스쿠버다이빙에서 약 30m 이하 깊이에서 마주치는 것)에서 흡입했을 때 질소는 마취제로, 아산화질소 중독과 유사한 일시적 정신장애 상태인 질소마취증을 일으킨다.[94][95]
질소는 혈액과 체지방에 용해된다. 급속 감압(다이버가 너무 빨리 상승하거나 우주비행사가 승무원 압력에서 우주복 압력으로 너무 빨리 감압할 때)은 혈류, 신경, 관절 및 기타 민감하거나 중요한 질소 거품이 형성될 때 감압병(이전에는 케이슨병 또는 굴곡부라고 알려져 있음)이라는 잠재적으로 치명적인 상태를 초래할 수 있다. 영역.[96][97] 다른 "침입된" 가스(탄소 및 산소 이외의 가스)에서 나오는 거품은 같은 효과를 일으키므로 호흡 가스의 질소 교체가 질소 마취는 막을 수 있지만, 감압 질환은 예방하지 못한다.[98]
액체
극저온성 액체로서, 레이덴프로스트 효과는 매우 짧은 노출(약 1초)에 대한 보호를 제공하지만, 액체 질소는 접촉 시 차가운 화상을 유발하여 위험할 수 있다.[99] 액체 질소를 섭취하면 심각한 내부 손상을 초래할 수 있다. 예를 들어 2012년 영국의 한 젊은 여성은 액체 질소로 만든 칵테일을 마신 뒤 배를 빼야 했다.[100]
질소의 액체 대 가스 팽창비는 20 °C에서 1:694이기 때문에 밀폐된 공간에서 액체 질소가 빠르게 기화되면 엄청난 힘이 발생할 수 있다. 2006년 1월 12일 텍사스 A&M 대학에서 발생한 사건에서 액체 질소 탱크의 압력 완화 장치가 오작동하여 나중에 봉인되었다. 이후 압력 증강에 따라 탱크는 대재앙을 일으켰다. 폭발의 힘은 탱크를 그 바로 위 천장을 통해 밀고, 그 바로 아래 철근 콘크리트 빔을 부수고, 실험실의 벽면을 그 기초로부터 0.1–0.2m 떨어트릴 정도로 충분했다.[101]
액체 질소는 기체 질소를 형성하기 위해 쉽게 증발하며, 따라서 기체 질소와 관련된 주의사항은 액체 질소에도 적용된다.[102][103][104] 예를 들어, 산소 센서는 액체 질소로 작업할 때 작업자에게 제한된 공간으로 가스가 유출되는 것을 경고하는 안전 예방책으로 사용되기도 한다.[105]
액체 질소가 들어 있는 그릇은 공기 중의 산소를 응축할 수 있다. 그러한 용기의 액체는 질소가 증발하면서 산소(베이징 포인트 -183 °C, 질소보다 더 높음)가 점점 더 농축되어 유기 물질의 격렬한 산화를 일으킬 수 있다.[106]
산소결핍모니터
산소 결핍 모니터는 밀폐된 공간과 질소 가스나 액체를 저장하거나 사용하는 모든 장소에서 산소 농도를 측정하기 위해 사용된다. 질소 누출 및 산소량이 사전 설정된 경보 수준으로 감소하는 경우 산소 결핍 모니터를 프로그래밍하여 청각 및 시각 경보를 발생시킬 수 있으므로, 임박한 위험에 대한 알림을 제공할 수 있다. 가장 일반적으로 경보 요원에 대한 산소 범위는 산소 농도가 19.5% 미만이 될 때입니다. OSHA는 위험한 대기는 산소 농도가 19.5% 이하 또는 23.[107]5% 이상인 대기를 포함할 수 있다고 명시한다. 산소 결핍 모니터는 고정하거나 벽에 장착하고 건물의 전원 공급 장치에 유선 연결하거나 전원 콘센트에 간단히 꽂거나 휴대용 휴대용 휴대용 또는 웨어러블 모니터로 연결할 수 있다.
참고 항목
참조
- ^ "Standard Atomic Weights: Nitrogen". CIAAW. 2009.
- ^ a b c Lide, David R. (1990–1991). CRC Handbook of Physics and Chemistry (71st ed.). Boca Raton, Ann Arbor, Boston: CRC Press, inc. pp. 4-22 (one page).
- ^ "Gases - Density". The Engineering Toolbox. Retrieved 27 January 2019.
- ^ 공통 본드 에너지(D) 및 본드 길이(r) 웨이백 머신에 2010-05-15 보관. wiredchemist.com
- ^ a b c 그린우드와 어니쇼, 페이지 406-07
- ^ 러더포드, 다니엘 (1772) "디세르타티오 초창기, 오토 메피티코, 웨이백 기계에 2020-08-06년 보관" (방송 [일명] 고정 또는 메피티치]에 관한 인어공지), M.D.논문, 스코틀랜드 에든버러 대학교. 영어 번역:
- ^ Weeks, Mary Elvira (1932). "The discovery of the elements. IV. Three important gases". Journal of Chemical Education. 9 (2): 215. Bibcode:1932JChEd...9..215W. doi:10.1021/ed009p215.
- ^ 애런 J. Ihde, The Development of Modern Chemistry, New York 1964.
- ^ 칼 빌헬름 스크일, 케미셰 아반들룽 폰 더 루프트와 뎀 페우어 [공기와 화재에 관한 화학적 고찰] (스웨덴 우살라: 마그누스 스웨덴인 1777년; 라이프치히, (독일): 지그프리드 레브레히트 크루시우스, 1777년). "Die Luft muß aus elastischen Flußigkeiten von zweyerley Art, zusammengesetze seyn" (공기는 두 종류의 탄성 액체로 구성되어야 한다)라는 제목의 섹션에서, 6-14페이지에서, Scheele은 공기가 다양한 물질과 반응한 8가지 실험의 결과를 제시한다. He concluded (p. 13): "So viel sehe ich aus angeführten Versuchen, daß die Luft aus 2 von einander unterschiedenen Flußigkeiten bestehe, von welchen die eine die Eigenschaft das Phlogiston anzuziehen gar nicht äussere, die andere aber zur solchen Attraction eigentlich aufgeleget ist und welche zwischen dem 3:ten und 4:ten Theil von der ganzen Luftmass aus machet." (그래서 나는 [이] 실험에서 많은 것을 본다: 공기는 서로 다른 두 개의 액체로 구성된다. 그 중 하나는 Phlogiston을 끌어들이는 모든 성질에서 표현되지 않는다. 그러나 다른 하나는 그러한 매력을 가질 수 있고 전체 질량의 1/3과 1/4을 차지한다.e-a.)
- ^ Priestley, Joseph (1772). "Observations on different kinds of air". Philosophical Transactions of the Royal Society of London. 62: 147–256. doi:10.1098/rstl.1772.0021. S2CID 186210131. 225 페이지 참조. 웨이백 머신에 보관된 2016-09-03
- ^ Priestley, Joseph (1772). "Observations on different kinds of air". Philosophical Transactions of the Royal Society of London. 62: 147–256. doi:10.1098/rstl.1772.0021. S2CID 186210131. ; 참조: "VII. 숯을 태우는 연기에 오염된 공기의." 225-28페이지. 웨이백 머신에 보관된 2016-09-03
- ^ 라부아지에, 앙투안, 로버트 커와 함께, 트랜스, 화학의 요소들, 4번째 에드 (스코틀랜드 에딘버그: 윌리엄 크리치, 1799 페이지 85-86. [p. 85]: 웨이백머신에 보관된 2020-08-06 "이 실험의 상황을 반영하여 우리는 쉽게 인지한다; 우리는 석회화[즉, 공기에 구우면서] 동안 수은이 공기의 용해성과 호흡이 가능한 부분을 흡수하거나, 좀 더 엄격하게 말하면, 이 호흡이 가능한 부분의 밑부분을 흡수한다; 남은 공기는 한 종이다. 메피티[즉, 지구에서 방출되는 유독 가스, 연소나 호흡을 지원할 수 없는 가스]의 경우, … "[p. 86]: 웨이백 기계에 보관된 2020-08-06 "이후 나는 적어도 우리의 기후에서 대기는 호흡이 가능한 공기 및 메피티크 항공기로 구성되며, 27과 73의 비율로; …"
- ^ 라부아지에, 앙투안, 로버트 커와 함께, 트랜스, 화학의 요소들, 4번째 에드 (스코틀랜드 에딘버그: 윌리엄 크리치(1799년), 페이지 101: "대기의 유해한 부분의 화학적 특성은 현재까지 알려져 있지 않지만, 우리는 그것을 숨쉬게 하는 것과 같은 동물들을 죽이는 것으로 알려진 질에서 그 염기성의 이름을 도출하는 데 만족했다. 아조트의 이름을, 그리스 입자 α와 Ωξη, vita로부터. 대기 중 유해한 부분의 이름은 아조틱 가스다."
- ^ 채프탈, J. A.와 니콜슨, 윌리엄 트랜스. (1800) 화학 원소, 3부. London, England: C.C. and J. Robinson, vol. 1. pp. xxxv–xxxvi: "In order to correct the Nomenclature on this head [i.e., in this regard], nothing more is necessary than to substitute to [i.e., for] this word a denomination which is derived from the general system made use of; and I have presumed to propose that of Nitrogene Gas. 애당초 질산의 래디컬을 형성하는 이 가스의 특성과 배타적 성질로부터 추론한다. 이를 통해 우리는 이 물질의 조합[즉, 화합물]에 질산, 질산, 질산염, 질산염, &c와 같은 수신된 [즉, 지배적인] 종파를 보존할 것이다.
- ^ 웨이백 기계에 2017-07-02 질소 보관 Etymonline.com. 2011년 10월 26일 발견
- ^ 스트럿, R. J. (1911년) "베케리안 강의. 화학적으로 활성된 질소 수정, 전기 방전에 의해 생성," 왕립학회 A 웨이백 머신 프로시저 2016-12-20 보관: 85 (577): 219–29.
- ^ 레일리 경의 활성 질소는 웨이백 기계에 2012-11-01을 보관했다. Lateralscience.co.uk. 2011년 10월 26일 발견
- ^ Erisman, Jan Willem; Sutton, Mark A.; Galloway, James; Klimont, Zbigniew; Winiwarter, Wilfried (2008). "How a century of ammonia synthesis changed the world". Nature Geoscience. 1 (10): 636. Bibcode:2008NatGe...1..636E. doi:10.1038/ngeo325.
- ^ GB 190698, 오스트왈드, 빌헬름, "질산 및 질소산화물 제조의 개선" 1902-03-20을 간행
- ^ GB 190208300, 오스트왈드, 빌헬름 "질산 및 질소 산화물 제조에 관한 개선 및 관련" 1903-02-26 출판
- ^ a b c d e 그린우드와 어니쇼, 페이지 411–12
- ^ 그린우드와 어니쇼, 페이지 550
- ^ Kaupp, Martin (1 December 2006). "The role of radial nodes of atomic orbitals for chemical bonding and the periodic table". Journal of Computational Chemistry. 28 (1): 320–25. doi:10.1002/jcc.20522. PMID 17143872. S2CID 12677737.
- ^ a b c d e f g h i j 그린우드와 어니쇼, 페이지 412–16
- ^ Miller, T. S.; Belen, A.; Suter, T. M.; Sella, A.; Corà, A.; McMillan, P. F. (2017). "Carbon nitrides: synthesis and characterization of a new class of functional materials". Physical Chemistry Chemical Physics. 19 (24): 15613–15638. Bibcode:2017PCCP...1915613M. doi:10.1039/C7CP02711G. PMID 28594419.
- ^ House, J. E.; House, K. A. (2016). Descriptive Inorganic Chemistry. Amsterdam: Elsevier. p. 198. ISBN 978-0-12-804697-5.
- ^ Roy, A. K.; Burns, G. T.; Grigora, S.; Lie, G. C. (1994). "Poly(alkyl/aryloxothiazenes), [N=S(O)R]n : New direction in inorganic polymers". In Wisian-Neilson, P.; Alcock, H. R.; Wynne, K. J. (eds.). Inorganic and organometallic polymers II: advanced materials and intermediates. American Chemical Society. pp. 344–357. doi:10.1021/bk-1994-0572.ch026.
- ^ Bethe, H. A. (1939). "Energy Production in Stars". Physical Review. 55 (5): 434–56. Bibcode:1939PhRv...55..434B. doi:10.1103/PhysRev.55.434. PMID 17835673.
- ^ CIAAW (2003). "Atomic Weight of Nitrogen". ciaaw.org. CIAAW. Archived from the original on 14 October 2016. Retrieved 13 October 2016.
- ^ Flanagan, Lawrence B.; Ehleringer, James R.; Pataki, Diane E. (15 December 2004). Stable Isotopes and Biosphere – Atmosphere Interactions: Processes and Biological Controls. pp. 74–75. ISBN 978-0-08-052528-0. Archived from the original on 5 February 2016. Retrieved 20 December 2015.
- ^ 그린우드와 어니쇼, 페이지 408
- ^ "Evaluated Nuclear Data File (ENDF) Retrieval & Plotting". National Nuclear Data Center. Archived from the original on 2020-08-09. Retrieved 2016-11-23.
- ^ Arthur G Palmer (2007). Protein NMR Spectroscopy. Elsevier Academic Press. ISBN 978-0-12-164491-8.
- ^ Katzenberg, M. A. (2008). "Chapter 13: Stable Isotope Analysis: A Tool for Studying Past Diet, Demography, and Life History". Biological Anthropology of the Human Skeleton (2nd ed.). ISBN 978-0-471-79372-4.
- ^ a b c Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties", Nuclear Physics A, 729: 3–128, Bibcode:2003NuPhA.729....3A, doi:10.1016/j.nuclphysa.2003.11.001
- ^ Carlson, Neil (January 22, 2012). Physiology of Behavior. Methods and Strategies of Research. 11th edition. Pearson. p. 151. ISBN 978-0-205-23939-9.
- ^ a b Neeb, Karl Heinz (1997). The Radiochemistry of Nuclear Power Plants with Light Water Reactors. Berlin-New York: Walter de Gruyter. p. 227. ISBN 978-3-11-013242-7. Archived from the original on 2016-02-05. Retrieved 2015-12-20.
- ^ a b Lewars, Errol G. (2008). Modeling Marvels: Computational Anticipation of Novel molecules. Springer Science+Business Media. pp. 141–63. doi:10.1007/978-1-4020-6973 (inactive 31 October 2021). ISBN 978-1-4020-6972-7.CS1 maint: 2021년 10월 현재 DOI 비활성화(링크)
- ^ 그린우드와 어니쇼, 페이지 483
- ^ "Polymeric nitrogen synthesized". physorg.com. 5 August 2004. Archived from the original on 2012-01-24. Retrieved 2009-06-22.
- ^ Gray, Theodore (2009). The Elements: A Visual Exploration of Every Known Atom in the Universe. New York: Black Dog & Leventhal Publishers. ISBN 978-1-57912-814-2.
- ^ Schuch, A. F.; Mills, R. L. (1970). "Crystal Structures of the Three Modifications of Nitrogen 14 and Nitrogen 15 at High Pressure". The Journal of Chemical Physics. 52 (12): 6000–08. Bibcode:1970JChPh..52.6000S. doi:10.1063/1.1672899.
- ^ Iancu, C. V.; Wright, E. R.; Heymann, J. B.; Jensen, G. J. (2006). "A comparison of liquid nitrogen and liquid helium as cryogens for electron cryotomography". Journal of Structural Biology. 153 (3): 231–40. doi:10.1016/j.jsb.2005.12.004. PMID 16427786.
- ^ "Flowing nitrogen ice glaciers seen on surface of Pluto after New Horizons flyby". ABC News. 25 July 2015. Archived from the original on 29 September 2015. Retrieved 6 October 2015.
- ^ McKinnon, William B.; Kirk, Randolph L. (2014). "Triton". In Spohn, Tilman; Breuer, Doris; Johnson, Torrence (eds.). Encyclopedia of the Solar System (3rd ed.). Amsterdam; Boston: Elsevier. pp. 861–82. ISBN 978-0-12-416034-7. Archived from the original on 2016-09-03. Retrieved 2016-04-30.
- ^ "Neptune: Moons: Triton". NASA. Archived from the original on October 15, 2011. Retrieved September 21, 2007.
- ^ Fryzuk, M. D. & Johnson, S. A. (2000). "The continuing story of dinitrogen activation". Coordination Chemistry Reviews. 200–202: 379. doi:10.1016/S0010-8545(00)00264-2.
- ^ Schrock, R. R. (2005). "Catalytic Reduction of Dinitrogen to Ammonia at a Single Molybdenum Center". Acc. Chem. Res. 38 (12): 955–62. doi:10.1021/ar0501121. PMC 2551323. PMID 16359167.
- ^ a b c d e 그린우드와 어니쇼, 페이지 417-20
- ^ 그린우드와 어니쇼, 페이지 434–38
- ^ 그린우드와 어니쇼, 420-26페이지
- ^ a b c d 그린우드와 어니쇼, 페이지 426–33
- ^ Vieira, R.; C. Pham-Huu; N. Keller; M. J. Ledoux (2002). "New carbon nanofiber/graphite felt composite for use as a catalyst support for hydrazine catalytic decomposition". Chemical Communications (9): 954–55. doi:10.1039/b202032g. PMID 12123065.
- ^ a b c d 그린우드와 어니쇼, 페이지 438-42
- ^ Bowden, F. P. (1958). "Initiation of Explosion by Neutrons, α-Particles, and Fission Products". Proceedings of the Royal Society of London A. 246 (1245): 216–19. Bibcode:1958RSPSA.246..216B. doi:10.1098/rspa.1958.0123. S2CID 137728239.
- ^ Ford, L. A.; Grundmeier, E. W. (1993). Chemical Magic. Dover. p. 76. ISBN 978-0-486-67628-9.
- ^ Frierson, W. J.; Kronrad, J.; Browne, A. W. (1943). "Chlorine Azide, ClN3. I". Journal of the American Chemical Society. 65 (9): 1696–1698. doi:10.1021/ja01249a012.
- ^ Lyhs, Benjamin; Bläser, Dieter; Wölper, Christoph; Schulz, Stephan; Jansen, Georg (20 February 2012). "Solid-State Structure of Bromine Azide" (PDF). Angewandte Chemie International Edition. 51 (8): 1970–1974. doi:10.1002/anie.201108092. PMID 22250068. Archived (PDF) from the original on 25 August 2021. Retrieved 25 August 2021.
- ^ a b c d e f 그린우드와 어니쇼, 페이지 443-58
- ^ Rahm, Martin; Dvinskikh, Sergey V.; Furó, István; Brinck, Tore (23 December 2010). "Experimental Detection of Trinitramide, N(NO2)3". Angewandte Chemie International Edition. 50 (5): 1145–48. doi:10.1002/anie.201007047. PMID 21268214.
- ^ Hou, Y. C.; Janczuk, A.; Wang, P. G. (1999). "Current trends in the development of nitric oxide donors". Current Pharmaceutical Design. 5 (6): 417–41. PMID 10390607.
- ^ Talawar, M. B.; et al. (2005). "Establishment of Process Technology for the Manufacture of Dinitrogen Pentoxide and its Utility for the Synthesis of Most Powerful Explosive of Today – CL-20". Journal of Hazardous Materials. 124 (1–3): 153–64. doi:10.1016/j.jhazmat.2005.04.021. PMID 15979786.
- ^ a b c d e f g h i 그린우드와 어니쇼, 459-72페이지
- ^ a b March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3rd ed.), New York: Wiley, ISBN 0-471-85472-7
- ^ Rédei, George P (2008). "Kjeldahl Method". Encyclopedia of Genetics, Genomics, Proteomics and Informatics. p. 1063. doi:10.1007/978-1-4020-6754-9_9066. ISBN 978-1-4020-6753-2.
- ^ a b 그린우드와 어니쇼, 페이지 407-09
- ^ Nielsen, M. K.; Jørgensen, B. M. (Jun 2004). "Quantitative relationship between trimethylamine oxide aldolase activity and formaldehyde accumulation in white muscle from gadiform fish during frozen storage". Journal of Agricultural and Food Chemistry. 52 (12): 3814–22. doi:10.1021/jf035169l. PMID 15186102.
- ^ Knox, G. A. (2007). Biology of the Southern Ocean. CRC Press. p. 392. ISBN 978-0-8493-3394-1. Archived from the original on 2021-10-01. Retrieved 2020-08-24.
- ^ Vickerstaff Joneja; Janice M. (2004). Digestion, diet, and disease: irritable bowel syndrome and gastrointestinal function. Rutgers University Press. p. 121. ISBN 978-0-8135-3387-2. Archived from the original on 2021-10-01. Retrieved 2020-08-24.
- ^ Froehlich, Peter (May 2013). "A Sustainable Approach to the Supply of Nitrogen". www.parker.com. Parker Hannifin Corporation. Archived from the original on 16 March 2016. Retrieved 24 November 2016.
- ^ Reich, Murray; Kapenekas, Harry (1957). "Nitrogen Purfication. Pilot Plant Removal of Oxygen". Industrial & Engineering Chemistry. 49 (5): 869–73. doi:10.1021/ie50569a032.
- ^ a b c d e 그린우드와 어니쇼, 페이지 409–11
- ^ a b Bartlett, J. K. (1967). "Analysis for nitrite by evolution of nitrogen: A general chemistry laboratory experiment". Journal of Chemical Education. 44 (8): 475. Bibcode:1967JChEd..44..475B. doi:10.1021/ed044p475.
- ^ Eremets, M. I.; Popov, M. Y.; Trojan, I. A.; Denisov, V. N.; Boehler, R.; Hemley, R. J. (2004). "Polymerization of nitrogen in sodium azide". The Journal of Chemical Physics. 120 (22): 10618–23. Bibcode:2004JChPh.12010618E. doi:10.1063/1.1718250. PMID 15268087.
- ^ Ministers, Nordic Council of (2002). Food Additives in Europe 2000. p. 591. ISBN 978-92-893-0829-8. Archived from the original on 2016-02-05. Retrieved 2015-12-20.
- ^ Harding, Charlie, ed. (2002). Elements of the p Block. Cambridge: Royal Society of Chemistry. ISBN 978-0-85404-690-4. Archived from the original on 2021-10-01. Retrieved 2020-08-24.
- ^ Gavriliuk, V. G.; Berns, Hans (1999). High nitrogen steels: structure, properties, manufacture, applications. Springer. ISBN 978-3-540-66411-6. Archived from the original on 2021-10-01. Retrieved 2020-08-24.
- ^ Meka, S. R.; Chauhan, A.; Steiner, T.; Bischoff, E.; Ghosh, P. K.; Mittemeijer, E. J. (2015). "Generating duplex microstructures by nitriding; nitriding of iron based Fe–Mn alloy". Materials Science and Technology: 1743284715Y.000. doi:10.1179/1743284715Y.0000000098.
- ^ "Why don't they use normal air in race car tires?". Howstuffworks. 2001-03-16. Archived from the original on 2011-07-12. Retrieved 2006-07-22.
- ^ Kemmochi, Y; Tsutsumi, K.; Arikawa, A.; Nakazawa, H. (2002). "Centrifugal concentrator for the substitution of nitrogen blow-down micro-concentration in dioxin/polychlorinated biphenyl sample preparation". Journal of Chromatography A. 943 (2): 295–97. doi:10.1016/S0021-9673(01)01466-2. PMID 11833649.
- ^ Baxter, E. Denise; Hughes, Paul S. (2001). Beer: Quality, Safety and Nutritional Aspects. Royal Society of Chemistry. p. 22. ISBN 978-0-85404-588-4. Archived from the original on 2020-03-21. Retrieved 2015-06-20.
- ^ "How does the widget in a beer can work?". Howstuffworks. 2000-08-16. Archived from the original on 2007-11-02. Retrieved 2008-07-30.
- ^ Denny, Mark (1 November 2009). Froth!: The Science of Beer. p. 131. ISBN 978-0-8018-9569-2. Archived from the original on 5 February 2016. Retrieved 20 December 2015.
- ^ Kennett, Andrew J. (2008). Design of a pneumatically assisted shifting system for Formula SAE® racing applications (Thesis). Dept. of Mechanical Engineering, Massachusetts Institute of Technology. hdl:1721.1/45820.
- ^ Betterton, E. A. (2003). "Environmental Fate of Sodium Azide Derived from Automobile Airbags". Critical Reviews in Environmental Science and Technology. 33 (4): 423–58. doi:10.1080/10643380390245002. S2CID 96404307.
- ^ Sanburn, Josh (2015-04-10). "The Dawn of a New Form of Capital Punishment". Time. Archived from the original on 2015-04-11. Retrieved 2015-04-11.
- ^ Sexton, Mike (18 December 2012). "Euthanasia campaigner under scrutiny". ABC. Archived from the original on 7 July 2013. Retrieved 6 May 2013.
- ^ Berman, Mark (April 17, 2015). "Oklahoma says it will now use nitrogen gas as its backup method of execution". The Washington Post. Archived from the original on June 23, 2019. Retrieved June 22, 2019.
- ^ "Oklahoma Attorney general says state will resume executions". New York Post. Archived from the original on March 9, 2021. Retrieved March 22, 2020.
- ^ Kaganer, M. G.; Kozheurov, V. & Levina, Zh. L. (1967). "Vessels for the storage and transport of liquid oxygen and nitrogen". Chemical and Petroleum Engineering. 3 (12): 918–22. doi:10.1007/BF01136404. S2CID 96762552.
- ^ Ahmed I; Agarwal S; Ilchyshyn A; Charles-Holmes S; Berth-Jones J (May 2001). "Liquid nitrogen cryotherapy of common warts: cryo-spray vs. cotton wool bud". Br. J. Dermatol. 144 (5): 1006–09. doi:10.1046/j.1365-2133.2001.04190.x. PMID 11359389. S2CID 221325640.
- ^ "Biology Safety – Cryogenic materials. The risks posed by them". University of Bath. Archived from the original on February 6, 2007. Retrieved 2007-01-03.
- ^ "Space Shuttle Columbia Fast Facts". CNN. September 30, 2013. Archived from the original on February 2, 2016. Retrieved January 20, 2016.
- ^ Fowler, B.; Ackles, K. N.; Porlier, G. (1985). "Effects of inert gas narcosis on behavior – a critical review". Undersea Biomed. Res. 12 (4): 369–402. PMID 4082343. Archived from the original on 2010-12-25. Retrieved 2008-09-21.
- ^ Rogers, W. H.; Moeller, G. (1989). "Effect of brief, repeated hyperbaric exposures on susceptibility to nitrogen narcosis". Undersea Biomed. Res. 16 (3): 227–32. OCLC 2068005. PMID 2741255. Archived from the original on 2009-09-01. Retrieved 2008-09-21.
- ^ Acott, C. (1999). "A brief history of diving and decompression illness". South Pacific Underwater Medicine Society Journal. 29 (2). OCLC 16986801. Archived from the original on 2011-09-05. Retrieved 2008-09-21.
- ^ Kindwall, E. P.; Baz, A.; Lightfoot, E. N.; Lanphier, E. H.; Seireg, A. (1975). "Nitrogen elimination in man during decompression". Undersea Biomed. Res. 2 (4): 285–97. OCLC 2068005. PMID 1226586. Archived from the original on 2011-07-27. Retrieved 2008-09-21.
- ^ US Navy Diving Manual, 6th revision. United States: US Naval Sea Systems Command. 2006. Archived from the original on 2008-05-02. Retrieved 2008-04-24.
- ^ Walker, Jearl. "Boiling and the Leidenfrost Effect" (PDF). Fundamentals of Physics: 1–4. Archived (PDF) from the original on 13 December 2019. Retrieved 11 October 2014.
- ^ 액체 질소 칵테일은 2012년 10월 8일 BBC 뉴스의 웨이백 머신에서 10대들을 2017-04-12로 병원에 남겨둔다.
- ^ Mattox, Brent S. "Investigative Report on Chemistry 301A Cylinder Explosion" (PDF). Texas A&M University. Archived from the original (reprint) on 2014-04-30.
- ^ British Compressed Gas Association(2000) BCGA Code of Practice CP30. 최대 50리터까지 액체 질소 듀어의 안전한 사용. 2007-07-18 웨이백 머신 ISSN 0260-4809에 보관.
- ^ 제한된 공간 진입 – 2015-09-22 웨이백머신 Valero 정유소 질식 사고 사례 연구(Wayback Machine, Wayback Machine, Valero 정유소 질식 사고 연구).
- ^ 1999년 10월 25일 BBC 뉴스의 웨이백머신에 2017-01-07년 화학물질 누출로 인한 사망 후 조사.
- ^ Liquid Nitrogen – Code of practice for handling. United Kingdom: Birkbeck, University of London. 2007. Archived from the original on 2018-06-12. Retrieved 2012-02-08.
- ^ Levey, Christopher G. "Liquid Nitrogen Safety". Thayer School of Engineering at Dartmouth. Archived from the original on 2016-03-05. Retrieved 2016-11-23.
- ^ 국립보건원 산소 모니터링 장치의 사용 및 유지보수를 위한 프로토콜. 2014년 2월, UTC 1시 35분. 이용 가능: https://www.ors.od.nih.gov/sr/dohs/documents/protocoloxygenmonitoring.pdf Wayback Machine에 2020-12-05 보관. 2020년 6월 23일 접속
참고 문헌 목록
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.









![{\displaystyle {\ce {NaNO3{}+Na2O->[{\ce {Ag~crucible}}][{\ce {300^{\circ }C~for~7days}}]Na3NO4}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ec729bc88f520e08fdce8a013dec8ae601d28509)





