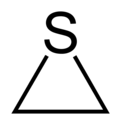
티이레인
Thiirane| | |||
 | |||
| 이름 | |||
|---|---|---|---|
| 선호 IUPAC 이름 티이레인 | |||
| 체계적 IUPAC 이름 티아시클로프로판 | |||
| 기타 이름 | |||
| 식별자 | |||
| |||
3D 모델(JSmol) | |||
| 102379 | |||
| 체비 | |||
| 켐스파이더 | |||
| ECHA InfoCard | 100.006.359 | ||
| EC 번호 |
| ||
| 1278 | |||
| 케그 | |||
| 메슈 | 에틸렌+화이트라이드 | ||
펍켐 CID | |||
| RTECS 번호 |
| ||
| 유니 | |||
| UN 번호 | 1992 | ||
CompTox 대시보드 (EPA) | |||
| |||
| |||
| 특성. | |||
| C2H4S | |||
| 어금질량 | 60.11 g·milital−1 | ||
| 외관 | 연한 노란색 액체 | ||
| 밀도 | 1.01 g cm−3 | ||
| 녹는점 | -109°C(-164°F, 164K) | ||
| 비등점 | 56°C, 133°F, 329K | ||
| 증기압 | 28.6kPa(20°C) | ||
| 열화학 | |||
의 성 엔탈피 대형화 (ΔfH⦵298) | 51-53 kJ mol−1 | ||
의 성 엔탈피 연소시키다 (ΔcH⦵298) | -2.0126 MJ mol−1 | ||
| 위험 | |||
| GHS 라벨 표시: | |||
   | |||
| 위험 | |||
| H225, H301, H318, H331 | |||
| P210, P261, P280, P301+P310, P305+P351+P338, P311 | |||
| NFPA 704(화재 다이아몬드) | |||
| 플래시 포인트 | 10°C(50°F, 283K) | ||
| 관련 화합물 | |||
관련 이성애자 | 산화 에틸렌 아지리딘 보리라네 | ||
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |||
| Infobox 참조 자료 | |||
일반적으로 에틸렌 황화 에틸렌으로 더 잘 알려진 티아레인은 CHS라는24 공식을 가진 순환 화학 화합물이다.[2] 그것은 가장 작은 유황 함유 이질종이며 가장 단순한 에피황이다. 많은 유기황 화합물과 마찬가지로 이 종은 매우 불쾌한 냄새를 가지고 있다. 티아레인은 또한 모체 에틸렌 황화물의 파생물을 설명하는데 사용된다.
구조
전자 회절에 따르면, 에틸렌 황화 에틸렌의 C-C와 C-S 거리는 각각 1.473과 1.811 å이다. C-C-S와 C-S-C 각도는 각각 66.0°와 48.0°[3]
준비 및 반응
그것은 에틸렌 탄산염과 KSCN의 반응에 의해 준비될 수 있다.[4] 이를 위해 KSCN은 먼저 진공 상태에서 용해되어 물을 제거한다.
- KSCN + 초코242 → KOCN + CHS24 + CO2
에틸렌설피드는 아민에 아민을 첨가해 2메르카프토에틸아민(chelting ligands)[5]을 살 수 있다.
- CHS24 + RNH2 → RNCHSH222
이 과정을 흔히 메르캡토에틸화라고 부른다.[6]
티아레인을 치주산염으로 산화시키면 에틸렌에 황산화 에틸렌이 생긴다.
참조
- ^ a b "thiirane (CHEBI:30977)". Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute.
- ^ Warren Chew; David N. Harpp (1993). "Recent aspects of thiirane chemistry". Journal of Sulfur Chemistry. 15 (1): 1–39. doi:10.1080/01961779308050628.
{{cite journal}}: CS1 maint : 복수이름 : 작성자 목록(링크) - ^ Wataru Ando Nami Choi Norihiro Tokitoh (1996). "Thiiranes and Thiirenes: Monocyclic". Comprehensive Heterocyclic Chemistry II. Vol. 1A. pp. 173–240. doi:10.1016/B978-008096518-5.00005-8. ISBN 9780080965185.
{{cite encyclopedia}}: CS1 maint: 작성자 매개변수 사용(링크) - ^ Searles, S.; Lutz, E. F.; Hays, H. R.; Mortensen, H. E. (1962). "Ethylene Sulfide". Organic Syntheses. 42: 59. doi:10.15227/orgsyn.042.0059.
- ^ R. J. Creamlin "Organosulfur 화학 소개" John Wiley and Sons: 치체스터(1996년). ISBN 0-471-95512-4
- ^ Gunars Zelans, Jacquelyn Gervay-Hague, Ivy Maulie (2010). "Ethylene Sulfide". Encyclopedia of Reagents for Organic Synthesis. John Wiley & Sons. doi:10.1002/047084289X.re079.pub2. ISBN 978-0471936237.
{{cite encyclopedia}}: CS1 maint: 작성자 매개변수 사용(링크)