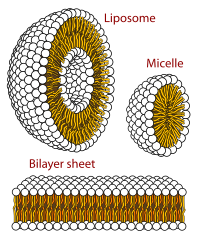
고분자 조립체
Macromolecular assembly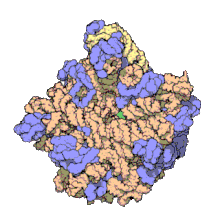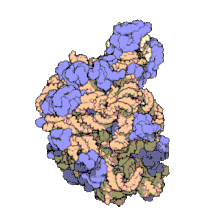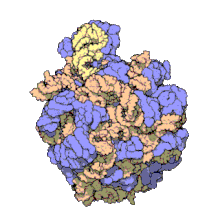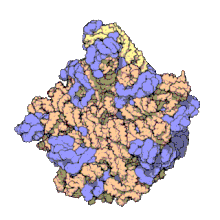
고분자조립체(MA)라는 용어는 폴리펩타이드, 폴리뉴클레오티드, 다당류 또는 기타 고분자 고분자의 혼합물인 바이러스 및 비생물 나노입자, 세포기관 및 막과 리보솜 등 대규모 화학구조를 말한다.이러한 혼합물은 일반적으로 둘 이상의 유형이며, 혼합물은 공간적으로 정의되며(즉, 화학적 형태와 관련하여), 화학적 구성과 구조에 기초한다.고분자는 생물과 무생물에서 발견되며, 공밸런트 결합에 의해 함께 결합된 수백, 수천 개의 원자로 구성되어 있다; 그것들은 종종 반복 단위를 특징으로 한다(즉, 그들은 중합체다.MA 용어가 생물학에서 더 일반적으로 적용되고 초분자 조합이라는 용어는 비생물학적 맥락(예: 초분자 화학 및 나노기술에서)에서 더 자주 적용되지만 이러한 조합은 마찬가지로 생물학적 또는 비생물학적일 수 있다.고분자의 MA는 (공발 결합이 아닌) 비동결 분자간 상호작용에 의해 정의된 형태로 유지되며, 비반복 구조(예: 리보솜(이미지) 및 세포막 구조에서와 같이) 또는 선형, 원형, 나선형 또는 기타 패턴(예: 액틴 필라멘트 및 평활선)에서 반복될 수 있다.모터, 이미지).MA가 형성되는 과정은 분자 자가 결합이라고 불렸는데, 이는 특히 비생물학적 맥락에서 적용되는 용어다.MA의 연구를 위해 매우 다양한 물리적/생물물리학적, 화학적/화학적, 계산적 방법이 존재한다. MA의 규모(분자 치수)를 고려할 때, MA의 구성과 구조를 정교하게 하고 그 기능의 기초를 이루는 메커니즘을 식별하려는 노력이 현대 구조 과학의 최전선에 있다.
생체분자복합체
생체분자 복합체라고도 불리는 생체분자 복합체는 둘 이상의 생체분자(단백질, RNA, DNA, 탄수화물) 또는 큰 비고분자(지질)로 이루어진 생물학적 복합체다.이 생체 분자 사이의 상호작용은 비균형이다.[6] 예:
- 단백질 복합체(proteasome, DNA 중합효소 III holoenzyme, RNA 중합효소 II holoenzyme, 대칭 바이러스 캡시드, 샤페로닌 복합체 GroEL-GroES, 포토시스템 I, ATP synthase, 페리틴 등) 복합체들이다.
- RNA-단백질 복합체: 리보솜, 스플라이소솜, 금고, SnNP. 세포핵에 있는 그러한 복합체를 리보핵단백질(RNP)이라고 한다.
- DNA-단백질 복합체: 뉴클레오솜
- 단백질-지질 복합체: 지질단백질.[7][8]
생체 분자 복합체는 X선 결정학, 단백질 NMR 분광학, 극저온 현미경 및 연속적인 단일 입자 분석, 전자 단층촬영에 의해 구조적으로 연구된다.[9] X선 결정학과 생체분자 NMR 분광법에 의해 얻은 원자 구조 모델은 전자 현미경, 전자 단층촬영, 소각 X선 산란과 같은 저해상도 기법에 의해 얻은 훨씬 더 큰 생체분자 복합체 구조물에 도킹될 수 있다.[10]
고분자의 복합체는 자연에서 보편적으로 발생하는데, 그 곳에서 바이러스와 모든 살아있는 세포의 구조에 관여한다.또한, 그들은 모든 기본적인 생활 과정(단백질 번역, 세포분할, 복실 밀거래, 구획간 물질과 세포간 교환 등)에서 근본적인 역할을 한다.이러한 각각의 역할에서 의 복잡한 혼합물은 특정한 구조적, 공간적 방법으로 구성된다.개별 고분자는 공밸런트 결합과 분자 내 비협착력(즉, 충전 상호작용, 판데르 왈스 힘, 수소 결합과 같은 쌍극-디폴 상호작용을 통한 각 분자 내 부품 간의 연관성)의 조합에 의해 결합되는 반면, 정의에 의해 MA 자체만으로 결합된다.분자 간 작용(즉, 분자간 상호작용)을 제외하고, 비동결력을 통해.[citation needed]
MA 척도 및 예제
위의 이미지는 MA와 관련된 구성과 척도(치수)를 나타내는데, MA는 구조물의 복잡성에 이제 막 접촉하기 시작하지만, 원칙적으로 각 살아있는 세포는 MA로 구성되지만, 그 자체도 MA이다.사례와 기타 그러한 복합체 및 조립체에서 MA는 어느 정도 정밀도로 측정 가능한 성분비(스토이치측정법)를 여전히 가지고 있지만 분자량(즉, 단일 단순 원자의 수백만 배 무게)의 수백만 달톤인 경우가 많다.이미지 범례에서 언급했듯이, 적절하게 준비되었을 때 MA의 MA 또는 성분 하위 복합체는 종종 단백질 결정학 및 관련 방법에 의해 연구를 위해 결정되거나 다른 물리적 방법(예: 분광학, 현미경 검사)에 의해 연구될 수 있다.[citation needed]

바이러스 구조는 처음 연구된 MA에 포함되었다; 다른 생물학적 예로는 리보솜(위의 부분 이미지), 프로테아솜 및 번역 복합체(단백질 및 핵산 성분 포함), 생식 및 진핵전사 복합체, 세포와 세포 콤파 사이의 물질 통과를 가능하게 하는 핵 및 기타 생물학적 모공이 있다.Rtents멤브레인 지질과 지질 빌레이어 내의 단백질의 고유 분자역학을 수용하도록 구조 및 공간 정의 요건이 수정되지만 바이오엠브레인은 또한 일반적으로 MA로 간주된다.[15]
바이러스 조립체
박테리오파지(페이지) T4 처녀리온을 조립하는 동안, 페이지 유전자에 의해 인코딩된 형태생성 단백질은 특징적인 순서로 서로 상호작용한다.바이러스 감염 시 생성되는 이러한 단백질 각각의 양에 적절한 균형을 유지하는 것은 정상적인 페이즈 T4 형태생식에 있어 중요한 것으로 보인다.[16]처녀성을 결정하는 페이지 T4 인코딩 단백질은 주요 구조적 구성 요소, 부구조적 구성 요소, 형태생성 순서에서[17] 특정 단계를 촉매하는 비구조적 단백질 등을 포함한다.
MA에 대한 연구
MA 구조와 기능에 대한 연구는 특히 메가달톤 크기 때문에 어렵지만, 복잡한 구성과 다양한 동적 특성 때문에 어렵다.대부분은 표준 화학 및 생화학적 방법(단백질 정화 및 원심분리 방법, 화학 및 전기화학 특성화 등)을 적용했다.또한, 이들의 연구 방법에는 현대의 단백질 접근법, 계산 및 원자 분해능 구조 방법(예: X선 결정학), 소각 X선 산란(SAXS) 및 소각 중성자 산란(SANS), 힘 분광법, 전송 전자 현미경 및 극저온 현미경 검사 등이 포함된다.애런 클룩은 전자현미경을 이용한 구조해석에 관한 연구, 특히 담배 모자이크 바이러스 (6400 base ssRNA 분자와 >2000 coat 단백질 분자를 포함하는 구조)를 포함한 단백질 핵산 MA에 대한 연구로 1982년 노벨 화학상 수상자로 인정받았다.살아있는 세포의 단백질 합성 '기계'의 일부인 리보솜의 결정화 및 구조용액 MW ~ 2.5 MDA는 토마스 A의 벤카트라만 라마크리쉬난에게 수여된 2009년 노벨 화학상의 대상이었다. 스티츠, 그리고 에이다 E. 요나스.[18]
비생물학적 상대
마지막으로 생물학은 MA의 유일한 영역이 아니다.초분자 화학과 nanotechnology의 필드는. 이 영역에서 특별한 관심, 그리고 새로운 형식과 프로세스에 알려진 기계 설계를 확장하고 분자 기계의 근본적인 과정 설명했던 힘과 원칙 먼저 생물학적 MAs에서 입증된 확장하는 법을 개발하였다 지역이 있다.[표창 필요한]
참고 항목
- 생체분자의 다중 상태 모델링
- 2차 구조
- 멀티프로테인 복합체
- 오르가넬: "장기"의 가장 넓은 정의는 막 결합 세포 구조뿐만 아니라 매우 큰 생체 분자 복합체를 포함한다.
- 생체분자의 다중 상태 모델링
참조
- ^ Ban N, Nissen P, Hansen J, Moore PB, Steitz TA (August 2000). "The complete atomic structure of the large ribosomal subunit at 2.4 A resolution". Science. 289 (5481): 905–920. Bibcode:2000Sci...289..905B. CiteSeerX 10.1.1.58.2271. doi:10.1126/science.289.5481.905. PMID 10937989.
- ^ McClure W. "50S Ribosome Subunit". Archived from the original on 2005-11-24. Retrieved 2019-10-09.
- ^ Osborne AR, Rapoport TA, van den Berg B (2005). "Protein translocation by the Sec61/SecY channel". Annual Review of Cell and Developmental Biology. 21: 529–550. doi:10.1146/annurev.cellbio.21.012704.133214. PMID 16212506.
- ^ 전설, 표지 예술 J. 박테리아올, 2006년 10월.[full citation needed]
- ^ Kleinjung J, Fraternali F (July 2005). "POPSCOMP: an automated interaction analysis of biomolecular complexes". Nucleic Acids Research. 33 (Web Server issue): W342–W346. doi:10.1093/nar/gki369. PMC 1160130. PMID 15980485.
- ^ Moore PB (2012). "How should we think about the ribosome?". Annual Review of Biophysics. 41 (1): 1–19. doi:10.1146/annurev-biophys-050511-102314. PMID 22577819.
- ^ Neuman N (January 2016). "The Complex Macromolecular Complex". Trends in Biochemical Sciences. 41 (1): 1–3. doi:10.1016/j.tibs.2015.11.006. PMID 26699226.
- ^ Dutta S, Berman HM (March 2005). "Large macromolecular complexes in the Protein Data Bank: a status report". Structure. 13 (3): 381–388. doi:10.1016/j.str.2005.01.008. PMID 15766539.
- ^ Russell RB, Alber F, Aloy P, Davis FP, Korkin D, Pichaud M, et al. (June 2004). "A structural perspective on protein-protein interactions". Current Opinion in Structural Biology. 14 (3): 313–324. doi:10.1016/j.sbi.2004.04.006. PMID 15193311.
- ^ van Dijk AD, Boelens R, Bonvin AM (January 2005). "Data-driven docking for the study of biomolecular complexes". The FEBS Journal. 272 (2): 293–312. doi:10.1111/j.1742-4658.2004.04473.x. hdl:1874/336958. PMID 15654870. S2CID 20148856.
- ^ "Structure of Fluid Lipid Bilayers". Blanco.biomol.uci.edu. 2009-11-10. Retrieved 2019-10-09.
- ^ 실험 시스템, 디올렐인스포스틸콜린 빌레이어지질에서 소수성 탄화수소 영역은 중성자와 X선 산란 방법의 조합에 의해 결정되며, 마찬가지로 극/인터페이스 영역(글리세릴, 인산염 및 두 그룹의 결합 수화)은 양쪽에 약 15 å (1.5 nm)이며, 총 두께는 탄화수소 영역과 거의 같다.S.H.를 참조하십시오.흰색 참조, 선행 및 추종.
- ^ Wiener MC, White SH (February 1992). "Structure of a fluid dioleoylphosphatidylcholine bilayer determined by joint refinement of x-ray and neutron diffraction data. III. Complete structure". Biophysical Journal. 61 (2): 434–447. Bibcode:1992BpJ....61..434W. doi:10.1016/S0006-3495(92)81849-0. PMC 1260259. PMID 1547331.
- ^ 탄화수소 치수는 온도, 기계적 응력, PL 구조 및 공형물 등에 따라 이 값들의 한 자릿수에서 낮은 두 자릿수 퍼센트로 다양하다.[citation needed]
- ^ Gerle C (June 2019). "Essay on Biomembrane Structure". The Journal of Membrane Biology. 252 (2–3): 115–130. doi:10.1007/s00232-019-00061-w. PMC 6556169. PMID 30877332.
- ^ Floor E (February 1970). "Interaction of morphogenetic genes of bacteriophage T4". Journal of Molecular Biology. 47 (3): 293–306. doi:10.1016/0022-2836(70)90303-7. PMID 4907266.
- ^ Snustad DP (August 1968). "Dominance interactions in Escherichia coli cells mixedly infected with bacteriophage T4D wild-type and amber mutants and their possible implications as to type of gene-product function: catalytic vs. stoichiometric". Virology. 35 (4): 550–63. doi:10.1016/0042-6822(68)90285-7. PMID 4878023.
- ^ "The Nobel Prize in Chemistry 2009". The Nobel Prize. Nobel Prize Outreach AB 2021. Retrieved 10 May 2021.
추가 읽기
일반평론
- Williamson JR (August 2008). "Cooperativity in macromolecular assembly". Nature Chemical Biology. 4 (8): 458–465. doi:10.1038/nchembio.102. PMID 18641626.
- Perrakis A, Musacchio A, Cusack S, Petosa C (August 2011). "Investigating a macromolecular complex: the toolkit of methods". Journal of Structural Biology. 175 (2): 106–12. doi:10.1016/j.jsb.2011.05.014. PMID 21620973.
- Dafforn TR (January 2007). "So how do you know you have a macromolecular complex?". Acta Crystallographica. Section D, Biological Crystallography. 63 (Pt 1): 17–25. doi:10.1107/S0907444906047044. PMC 2483502. PMID 17164522.
- Wohlgemuth I, Lenz C, Urlaub H (March 2015). "Studying macromolecular complex stoichiometries by peptide-based mass spectrometry". Proteomics. 15 (5–6): 862–79. doi:10.1002/pmic.201400466. PMC 5024058. PMID 25546807.
- Sinha C, Arora K, Moon CS, Yarlagadda S, Woodrooffe K, Naren AP (October 2014). "Förster resonance energy transfer - an approach to visualize the spatiotemporal regulation of macromolecular complex formation and compartmentalized cell signaling". Biochimica et Biophysica Acta (BBA) - General Subjects. 1840 (10): 3067–72. doi:10.1016/j.bbagen.2014.07.015. PMC 4151567. PMID 25086255.
- Berg JM, Tymoczko J, Stryer L (2002). Biochemistry (5th ed.). New York: W.H. Freeman. ISBN 978-0-7167-4955-4.
- Lehninger AL, Cox M, Nelson DL (2005). Lehninger principles of biochemistry (Fourth ed.). New York: W.H. Freeman. ISBN 978-0-7167-4339-2.
특정 MA에 대한 리뷰
- Valle M (May 2011). "Almost lost in translation. Cryo-EM of a dynamic macromolecular complex: the ribosome". European Biophysics Journal : EBJ. 40 (5): 589–97. doi:10.1007/s00249-011-0683-6. PMID 21336521. S2CID 26027815.
- Monie TP (2017). "The Canonical Inflammasome: A Macromolecular Complex Driving Inflammation". Sub-cellular Biochemistry. 83: 43–73. doi:10.1007/978-3-319-46503-6_2. ISBN 978-3-319-46501-2. PMID 28271472.
- Perino A, Ghigo A, Damilano F, Hirsch E (August 2006). "Identification of the macromolecular complex responsible for PI3Kgamma-dependent regulation of cAMP levels". Biochemical Society Transactions. 34 (Pt 4): 502–3. doi:10.1042/BST0340502. PMID 16856844.
일차 출처
- Lasker K, Förster F, Bohn S, Walzthoeni T, Villa E, Unverdorben P, et al. (January 2012). "Molecular architecture of the 26S proteasome holocomplex determined by an integrative approach". Proceedings of the National Academy of Sciences of the United States of America. 109 (5): 1380–1387. Bibcode:2012PNAS..109.1380L. doi:10.1073/pnas.1120559109. PMC 3277140. PMID 22307589.
- Russel D, Lasker K, Webb B, Velázquez-Muriel J, Tjioe E, Schneidman-Duhovny D, et al. (January 2012). "Putting the pieces together: integrative modeling platform software for structure determination of macromolecular assemblies". PLOS Biology. 10 (1): e1001244. doi:10.1371/journal.pbio.1001244. PMC 3260315. PMID 22272186.
- Barhoum S, Palit S, Yethiraj A (May 2016). "Diffusion NMR studies of macromolecular complex formation, crowding and confinement in soft materials". Progress in Nuclear Magnetic Resonance Spectroscopy. 94–95: 1–10. doi:10.1016/j.pnmrs.2016.01.004. PMID 27247282.
기타 출처
외부 링크
- Beck Group (2019), 대형 고분자 조립체의 구조 및 기능 (Beck Group Home page), Beck Group - 대형 분자 조립체의 구조와 기능 - EMBL, 2011년 6월 13일에 접속.
- DMA 그룹(2019), 고분자 어셈블리의 다이내믹스(DMA 그룹 홈 페이지), 고분자 어셈블리 섹션의 다이내믹스(Dynamics of Macromol 분자 어셈블리 섹션 국립 생물의학 영상 및 생명공학 연구소)가 2011년 6월 13일에 액세스했다.