타파미디스
Tafamidis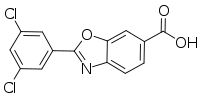 | |
| 임상 데이터 | |
|---|---|
| 상호 | 빈다멜, 빈다막스, 기타 |
| AHFS/Drugs.com | 모노그래프 |
| 라이선스 데이터 | |
| 임신 카테고리 |
|
| 루트 행정부. | 입으로 |
| ATC 코드 | |
| 법적 상태 | |
| 법적 상태 | |
| 식별자 | |
| |
| CAS 번호 | |
| PubChem CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 첸블 | |
| CompTox 대시보드 (EPA ) | |
| ECHA 정보 카드 | 100.246.079 |
| 화학 및 물리 데이터 | |
| 공식 | C14H7클론2NO3 |
| 몰 질량 | 308.11g/120−1 |
| 3D 모델(JSmol) | |
| |
| |
| | |
Vyndaqel과 Vyndamax라는 상표명으로 판매되는 [4]Tafamidis는 특정 형태의 트란스티레틴 아밀로이드증을 가진 성인의 질병 진행을 지연시키는 데 사용되는 약물이다.그것은 유전 형태, 가족성 아밀로이드 심근증, 가족성 아밀로이드 다발성 신경증뿐만 아니라 이전에 노인성 전신 아밀로이드증이라고 불렸던 야생형 트란스티레틴 아밀로이드증을 치료하는데 사용될 수 있다.단백질 트랜스스티레틴의 4차 구조를 안정화시킴으로써 작용합니다.트란스티레틴 아밀로이드증이 있는 사람들에게서, 트란스티레틴은 분해되어 [5][6]신경과 심장을 포함한 조직을 손상시키는 아밀로이드라고 불리는 덩어리를 형성합니다.
미국 식품의약국(FDA)은 타파미디스를 최고급 [7]의약품으로 간주하고 있다.
의료용
Tafamidis는 다발성 뉴로파시가 있는 트란스티레틴 아밀로이드증이 있는 성인의 신경 손상이나 심근증이 [3][4][6][8]있는 트란스티레틴 아밀로이드증이 있는 성인의 심장 질환을 지연시키는 데 사용됩니다.입으로 [3][4]먹는 거예요.
여성은 복용 중에 임신을 해서는 안 되며 복용 중에 모유를 먹이면 안 된다.가족성 아밀로이드 다발성 뉴로파시가 있는 사람은 [3]간 이식 수술을 받아서는 안 된다.
부작용
임상 시험에서 10% 이상의 사람들이 하나 이상의 요로 감염, 질 감염, 상복부 통증 또는 설사를 [3]경험했습니다.
상호 작용
Tafamidis는 시토크롬 P450과 상호작용하는 것으로 보이지 않지만 ATP 결합 카세트 슈퍼 패밀리 G 멤버 2를 억제하기 때문에 메토트렉세이트, 로즈바스타틴, 이마티닙 등의 특정 약물의 농도에 영향을 미칠 가능성이 있다.또한 유기 음이온 트랜스포터 1 및 유기 음이온 트랜스포터 3/용질 캐리어 패밀리 22 8을 억제하므로 비스테로이드성 항염증제 및 이들 트랜스포터에 의존하는 [3]다른 약물과 상호작용할 가능성이 높다.
약리학
Tafamidis는 Transthyretin 단백질의 올바르게 접힌 4중합체 형태를 안정시키는 약리학적 샤페론이다.[8]가족성 아밀로이드 다발성 뉴로파시가 있는 사람에서는 개별 단량체가 테트라머에서 떨어져 나와 잘못 접히고 골재가 신경을 [8]손상시킵니다.
최대 혈장 농도는 투여 후 약 2시간 후에 달성됩니다. 혈장에서는 거의 완전히 단백질에 결합됩니다.임상 전 데이터에 따르면 글루쿠론화에 의해 대사되고 담즙을 통해 배설되는 것으로 보인다. 사람의 경우 약 59%가 대변에서, 약 22%가 [3]소변에서 회수된다.
화학
타파미디스의 화학명은 2-(3,5-디클로로페닐)-1,3-벤조옥사졸-6-카르복실산이다.그 분자는 두 개의 결정 형태와 하나의 비정질 형태를 가지고 있다; 그것은 가능한 결정 형태 중 하나로 제조된다.메글루민 소금으로 판매되고 있습니다.그것은 [9]물에 약간 녹는다.
역사
스크립스 연구소의 Jeffery W. Kelly의 연구실은 1990년대에 [10]: 210 트란스티레틴 섬유소 형성을 억제하는 방법을 찾기 시작했다.Tafamidis는 구조 기반 의약품 설계 전략을 사용하여 Kelly 팀에 의해 결국 발견되었다.[11][12] 화학 구조는 2003년에 처음 발표되었다.2003년 켈리는 매사추세츠공대, 화이트헤드연구소의 [12][13]수잔 린드퀴스트와 함께 FoldRx라는 회사를 공동 설립했고,[11] FoldRx는 2010년 초 유럽 시장 승인 신청서를 제출해 Tafamidis를 개발했다.FoldRx는 그해 [11]말에 화이자사에 인수되었다.
Tafamidis는 2011년 11월 유럽의약청에 의해 트란스티레틴 관련 유전성 아밀로이드증이 [8]있는 성인의 말초 신경 장애를 지연시키는 것을 승인받았다.미 식품의약국은 2012년 임상시험에서 기능적 끝점을 기준으로 효과가 나타나지 않는다는 이유로 시판승인 신청을 기각하고 추가 임상시험을 [14]의뢰했다.2019년 5월 FDA는 트랜스스티레틴 매개 심근증 [6]치료를 위해 두 가지 타파미디스 제제인 Vyndaqel(타파미디스 메글루민)과 Vyndamax(타파미디스)를 승인했다.이 약은 2013년 일본에서 승인되었으며, 규제 당국은 효능의 [15]더 나은 증거를 보여주는 추가 임상 시험에 따라 승인을 결정했다.
FDA는 벨기에, 브라질, 캐나다, 체코, 스페인, 프랑스, 그리스, 이탈리아, 일본, 네덜란드, 스웨덴, 영국, 미국의 [16]60개 진료소에서 441명의 성인 환자를 대상으로 실시한 임상시험의 증거를 토대로 타파미디스 메글루민을 승인했다.
심근증이 있는 트란스티레틴 아밀로이드증 치료에 대한 타파미디의 유익성과 부작용을 평가한 한 번의 시도가 있었다. 이 실험에서 환자는 무작위로 타파미디스(20 또는 80mg) 또는 위약을 30개월 [16]동안 투여 받았다.임상시험 환자의 약 90%가 심부전으로 다른 약을 복용하고 있었다(관리 [16]기준과 일치한다.
유럽 의약품청은 타파미디스를 고아[5] 의약품으로, 식품의약국은 타파미디스 메글루민을 고아 [17]의약품으로 지정했다.
사회와 문화
법적 상태
Tafamidis는 2011년 유럽연합(EU)에서 다발성 뉴로파시에 의한 트란스티레틴 아밀로이드증 치료를 승인받았으며,[5][15] 일본에서는 2013년에 승인되었다.미국에서는 식품의약국([18][6]FDA)이 그 효능에 대한 증거가 불충분하다고 판단했기 때문에 다발성 뉴로파시에 의한 트란스티레틴 아밀로이드증 치료에 대해 거부당했다.
타파미디스는 또한 심근증이 있는 트란스티레틴 아밀로이드증을 치료하는데 사용될 수 있다.2019년에는 미국에서, 2020년에는 유럽연합에서 이 형태의 질병 치료를 위해 승인되었다.미국에서는 승인된 두 가지 제제가 있습니다: Tafamidis Meglumin(Vyndaqel)과 Tafamidis(Vyndamax)[6][19][16]입니다.두 제제는 동일한 활성 부분인 타파미디스를 가지고 있지만 밀리그램에서 밀리그램 [6]단위로 대체될 수는 없습니다.
타파미디스(빈다막스)와 타파미디스 메글루민(빈다켈)은 2020년 [20]3월에 호주에서 의료용으로 승인되었다.
레퍼런스
- ^ a b "Vyndamax and Vyndaqel Australian prescription medicine decision summary". Therapeutic Goods Administration (TGA). 17 July 2020. Retrieved 16 August 2020.
- ^ "Summary Basis of Decision (SBD) for Vyndaqel". Health Canada. 23 October 2014. Retrieved 29 May 2022.
- ^ a b c d e f g "Vyndaqel 20 mg soft capsules - Summary of Product Characteristics". Electronic Medicines Compendium. Retrieved 2 April 2018.
- ^ a b c d "Vyndaqel- tafamidis meglumine capsule, liquid filled Vyndamax- tafamidis capsule, liquid filled". DailyMed. 30 August 2019. Retrieved 24 November 2019.
- ^ a b c d "Vyndaqel EPAR". European Medicines Agency. 16 October 2019. Retrieved 24 November 2019.
- ^ a b c d e f "FDA approves new treatments for heart disease caused by a serious rare disease, transthyretin mediated amyloidosis". U.S. Food and Drug Administration. 14 September 2019. Archived from the original on 14 September 2019. Retrieved 24 November 2019.
 이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다..
이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다.. - ^ "New Drug Therapy Approvals 2019". U.S. Food and Drug Administration. 31 December 2019. Retrieved 15 September 2020.
- ^ a b c d Said, G; Grippon, S; Kirkpatrick, P (1 March 2012). "Tafamidis". Nature Reviews. Drug Discovery. 11 (3): 185–6. doi:10.1038/nrd3675. PMID 22378262.
- ^ "Assessment report: Vyndaqel tafamidis meglumine Procedure No.: EMEA/H/C/002294" (PDF). EMA. 2011. 업데이트에 대해서는 EMA 인덱스 페이지를 참조하십시오.
- ^ Labaudiniere, Richard (2014). "Chapter 9: Discovery and Development of Tafamidis for the Treatment of TTR Familial Amyloid Polyneuropathy". In Pryde, David C; Palmer, Michael J (eds.). Orphan Drugs and Rare Diseases. RSC Drug Discovery Series No. 38. Royal Society of Chemistry. ISBN 978-1-84973-806-4.
- ^ a b c Jones, Dan (29 October 2010). "Modifying protein misfolding". Nature Reviews Drug Discovery. 9 (11): 825–827. doi:10.1038/nrd3316. PMID 21030987. S2CID 30702908.
- ^ a b Borman, Stu (25 January 2010). "Attacking Amyloids". Chemical & Engineering News. 88 (4): 30–32. doi:10.1021/cen-v088n004.p030.
- ^ Breznitz, Shiri M.; O'Shea, Rory P.; Allen, Thomas J. (March 2008). "University Commercialization Strategies in the Development of Regional Bioclusters". Journal of Product Innovation Management. 25 (2): 129–142. doi:10.1111/j.1540-5885.2008.00290.x.
- ^ Grogan, Kevin (19 June 2012). "FDA rejects Pfizer rare disease drug tafamidis". Pharma Times.
- ^ a b "Report on the Deliberation Results" (PDF). Evaluation and Licensing Division, Pharmaceutical and Food Safety Bureau Ministry of Health, Labour and Welfare. 2 September 2013.
- ^ a b c d "Drug Trial Snapshots: Vyndaqel/Vyndamax". U.S. Food and Drug Administration (FDA). 28 May 2019. Archived from the original on 19 December 2019. Retrieved 18 December 2019.
 이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다..
이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다.. - ^ "Tafamidis meglumine Orphan Drug Designation and Approval". U.S. Food and Drug Administration. 3 May 2019. Archived from the original on 19 December 2019. Retrieved 18 December 2019.
 이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다..
이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다.. - ^ "FDA rejects Pfizer rare disease drug tafamidis". PharmaTimes online. 19 June 2012. Retrieved 2 June 2021.
- ^ "Drug Approval Package: Vyndaquel & Vyndamax". U.S. Food and Drug Administration. 13 June 2019. Retrieved 24 November 2019.
 이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다..
이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다.. - ^ "AusPAR: Tafamidis and Tafamidis meglumine". Therapeutic Goods Administration. 10 September 2020. Retrieved 23 September 2020.
추가 정보
- Adams D (March 2013). "Recent advances in the treatment of familial amyloid polyneuropathy". Ther Adv Neurol Disord. 6 (2): 129–39. doi:10.1177/1756285612470192. PMC 3582309. PMID 23483184.
- Coelho T, Maia LF, Martins da Silva A, et al. (August 2012). "Tafamidis for transthyretin familial amyloid polyneuropathy: a randomized, controlled trial". Neurology. 79 (8): 785–92. doi:10.1212/WNL.0b013e3182661eb1. PMC 4098875. PMID 22843282.
외부 링크
- "Tafamidis". Drug Information Portal. U.S. National Library of Medicine.
- "Tafamidis meglumine". Drug Information Portal. U.S. National Library of Medicine.


