포르피리노겐
Porphyrinogen생화학에서 포르피린겐은 4개의 메틸렌 교량으로 연결된 4개의 피롤링의 매크로사이클인 테트라피롤 코어를 가진 자연발생 화합물의 한 종류에 속한다.[1]그것들은 가장 바깥쪽(20-탄소) 링에서 수소 원자에 대한 다양한 기능 그룹의 대체에 의해 모화합물 헥사히드롭포핀에서 파생된 것으로 볼 수 있다.
포르피린균은 미오글로빈, 헤모글로빈, 시토크롬, 엽록소 등 많은 효소와 단백질에서 발견되는 포르피린 코어를 가진 공작용제인 포르피린(porphine core)[2]의 생합성 물질이다.
포르피린들은 메틴 브리지로 연결된 4개의 피롤 링을 가지고 있기 때문에 포르피린제와 다르다. =메틸렌 브리지 대신 -CH-2, 그리고 네 개의 아민 중 두 개의 수소 원자가 부족함.NH-그룹, 이미인=N-.포르피린 생합성에서는 모포폴로피리노겐 산화효소에 의해 모포피리노겐이 탈수된다.
포피리노균은 한정된 탈색 때문에 무색이다.핵 안에 있는 4개의 중앙 수소 원자가 모두 상실되면 금속 양이온에 대한 리간드 역할을 할 수 있는 사분위 음이온이 생성되어 조정 화합물이 생성된다.[3]포르피린으로 가는 길의 후속 생합성 매개체는 색이 짙고 종종 식물성 독성이 있다.
천연포피리노균
살아있는 유기체에서 발생하는 포르피로겐은 보통 각 피롤링의 가장 바깥쪽 탄소 원자의 일부 또는 전부를 대체하는 측면 체인을 가지고 있다(메틸렌 교량의 수소 원자와 반대).
우로포피리노겐 3세, 코프로포피리노겐 3세 전조.
코프로포피리노겐 3세, 프로토폴피피리노겐 IX의 전조.
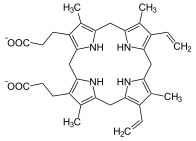
프로토폴피피리노겐 IX, 프로토폴피피린 IX의 전조.
비자연성 포르피린제
다양한 합성 포르피린제가 생산되어 연구실에서 연구되고 있다.이것들은 종종 자연에서 발생하지 않는 측면 그룹을 가지고 있으며, 아마도 피롤 링 대신 메틸렌 교량의 탄화수소(메소 위치)에서 발생할 수 있다.메소 대체성 포르피린제는 소위 메소 대체 포르피린들의 린지 합성에서 매개체들이다.산화 작용은 중심 헥사히드롭모르핀 코어를 포핀 코어로 바꾸어 원하는 포르피린을 산출한다.[4]
산성 촉매 하에서 피롤과 케톤 R-(C=O)-R' 또는 알데히드 R-(C=O)-H는 주기성 과점 [-(CRR42')---]\n를 포함한 많은 과점자를 응축한다.그런 다음 원하는 포르피린제(n = 4)를 분리할 수 있다.[4]8개의 비수소 사이드 체인을 가진 메소 대체성 포르피린제를 칼릭스[4]피롤이라고도 한다.이 제품들은 천연 포르피린제보다 외부 링의 탈수성을 더 잘 견디고 있다.[3]
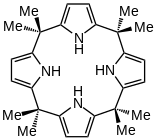
예를 들어 벤조알데히드 CH-65(C=O)-H로 응결하면 메소-테트라페닐포피리노겐이 생성되는데, 메소-테트라페닐포피린으로 산화될 수 있다.[4]아세톤 HC-3(C=O)-를 사용한 응축CH는3 메소옥타메틸포르피린(meso-octamethylporphyinen)을 생산한다.[3]
또는 탄소 3과 4에서 대체된 사이드 체인이 있는 피롤은 포름알데히드 H-(C=O)-H로 응축하여 자연산과 더 가까운 포르피린체를 제공할 수 있다.예를 들어 3,4-diethylpyrrole로 옥타에틸포르피린겐을 얻는다.[citation needed]
참조
- ^ 포르피린제 - IUPAC 골드북
- ^ Paul R. Ortiz de Montellano (2008). "Hemes in Biology". Wiley Encyclopedia of Chemical Biology. John Wiley & Sons. doi:10.1002/9780470048672.wecb221. ISBN 978-0470048672.
- ^ a b c Sessler, Jonathan L.; Anzenbacher, Pavel Jr.; Miyaji, Hidekazu; Jursikova, Karolina; Bleasdale, Ellen R.; Gale, Philip A. (2000). "Modified Calix[4]pyrroles". Industrial & Engineering Chemistry Research. 39 (10): 3471–3478. doi:10.1021/ie000102y.
- ^ a b c Lindsey, Jonathan S. (2000). "Synthesis of meso-substituted porphyrins". In Kadish, Karl M.; Smith, Kevin M.; Guilard, Roger (eds.). Porphyrin Handbook. Vol. 1. pp. 45–118. ISBN 0-12-393200-9.