우로포피리노겐 3세
Uroporphyrinogen III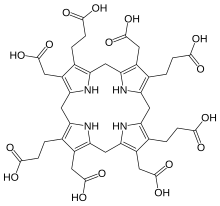 | |
| 식별자 | |
|---|---|
| 메슈 | 우로포피리노겐+III |
펍켐 CID | |
CompTox 대시보드 (EPA) | |
| 특성. | |
| C40H44N4O16 | |
| 어금질량 | 836.795 g/190 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
우로포피리노겐 III는 테트라피롤(tetrapyrrole)로, 헤메, 엽록소, 비타민 B12, 시로헴의 생합성에서 첫 번째 매크로순환 중간이다.그것은 다른 포르피린제와 마찬가지로 무색 화합물이다.[1]
구조
uroporphyrinogen III의 분자 구조는 헥사히드롭포핀 코어로 설명될 수 있는데, 여기서 각 피롤 링은 아세트산 그룹으로 대체된 가장 바깥쪽 두 탄소에 수소 원자를 가지고 있다.-CH-COOH2, "A") 및 프로피온산 그룹(-CH-CH-COOH22, "P")그룹들은 비대칭적인 방식으로 첨부된다: 매크로 사이클을 돌면, 순서는 AP-AP-AP-AP-PA이다.
생합성과 신진대사
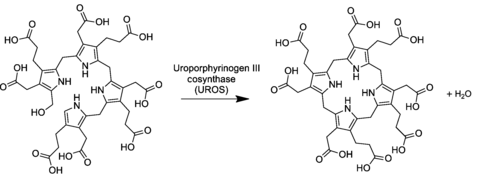
일반적인 포르피린 생합성 경로에서 uroporphyrrole preuroporphylbilane(대체 하이드록시메틸빌레인)은 효소 uropyrrole propyrongen-III cosynthase의 작용으로 선형 테트라피롤에서 유래한다.[2][3]
변환은 마지막 피롤 유닛의 역전과 첫 번째 링의 수소 원자로 최종 히드록실 -OH를 제거함으로써 매크로 사이클을 닫는 응축 반응을 수반한다.
헴과 엽록소의 생합성에서 uroporphyrinogen III는 효소 uroporphyrinogen III decarboxylase에 의해 coproporphyrinogen III로 전환된다.시로헴의 생합성에서는 우로포피리노겐3가 2개의 메틸전달제에 의해 디하이드로시하이드로클로린으로 전환되고, 이후 시로헴 보형물군의 전구체인 시로하이드로클로로인 산화된다.
의학적 의의
uroporphyrinogen-III synthase가 존재하지 않거나 비활성화된 경우, 히드록시메틸빌레인은 자발적으로 구조 이소머인 uroporphyrinogen I로 사이클화되며, 이는 아세트산("A")과 프로피온산(P") 그룹이 회전 대칭 순서인 AP-AP-AP-AP-AP-AP로 배열된다는 점에서 III와 다르다.이 경우 다음 단계에서는 코프로포피리노겐 I이 생성되어 축적되어 병적 상태 선천성 홍반성 포르피린증(Eythropoietic porphyria[3]
참고 항목
참조
- ^ Dalton, J (1969). "Formation of the Macrocyclic Ring in Tetrapyrrole Biosynthesis". Nature. 223 (5211): 1151–1153. Bibcode:1969Natur.223.1151D. doi:10.1038/2231151a0. PMID 5810686. S2CID 4177167.
- ^ Paul R. Ortiz de Montellano (2008). "Hemes in Biology". Wiley Encyclopedia of Chemical Biology. John Wiley & Sons. doi:10.1002/9780470048672.wecb221. ISBN 978-0470048672.
- ^ a b S. Sassa와 A.카파스(2000년) : "유전된 포르피리아들의 분자적 측면"내과 저널, 247권, 발행 2, 169-178페이지. doi:10.1046/j.1365-2796.2000.00618.x