체외막산소화
Extracorporeal membrane oxygenation| 체외막산소화 | |
|---|---|
 | |
| 기타 이름 | 체외생명유지장치(ECLS) |
| ICD-10-PCS | 5A15223 |
| ICD-9-CM | 39.65 |
| 메슈 | 29295 |
| 메드라인플러스 | 007234 |
| HCPCS-L2 | 36822 |
체외막산소화(ECMO)는 심장과 폐가 생명을 유지하기 위해 적절한 양의 가스 교환이나 관류를 제공할 수 없는 사람에게 장기간의 심장과 호흡 지원을 제공하는 체외막산소화 기술이다.ECMO 기술은 주로 심폐 우회술에서 파생되는데, 심폐 우회술은 구속된 토종 순환기로 단기적인 지원을 제공한다.사용되는 장치는 인공 폐로도 알려진 막 산소 생성기다.
ECMO는 적혈구의 인공산소와 이산화탄소 제거를 위해 일시적으로 몸에서 혈액을 뽑아내는 작업을 한다.일반적으로 심폐소생술은 심폐소생술 후 우회술이나 심장 및/또는 폐부전이 심한 사람의 말기 치료에 사용되지만, 현재는 특정 센터에서 심정지 치료로 사용되어 순환과 산소가 뒷받침되는 동안 근본적인 구속 원인을 치료할 수 있다.또한 인공호흡만으로는 혈액 산소화 수준을 유지하기에 충분하지 않은 경우 COVID-19와 관련된 급성 바이러스성 폐렴 환자를 지원하기 위해 ECMO를 사용한다.
의학적 용법
ECMO의 적응증 및 실천요강을 기술하는 지침은 체외수명지원기구(ELSO)에서 발표한다.ECMO의 개시 기준은 기관별로 다르지만 일반적으로 잠재적으로 가역성이 있고 기존 관리에 반응하지 않는 급성심장 또는 폐부전이 포함된다.ECMO의 시작을 촉진할 수 있는 임상 상황의 예는 다음과 같다.[1]
- 인공 산소(FiO2) 분율, 양적 호기압(PEEP), 호기 대 흡기(I:E) 비율 등 인공 산소 설정을 최적화했음에도 불구하고 <100mmHg의 산소 분율(PaO2/FiO2)에 대한 동맥 장력 비율이 포함된 저산소 호흡기 고장
- 동맥 pH <7.20>에 의한 초자극 호흡부전
- 내화성심장충격
- 심정지
- 심장 수술 후 심폐 우회술 실패
- 심장 이식 또는 심실 보조 장치 배치를 위한 교량으로서
- 폐 이식을 위한 가교로서
- 패혈성 쇼크는 더 논란이 많지만 점점 더 연구되고 있는 ECMO의 사용법이다.
- 저체온증, 코어 온도는 28~24°C이고 심장은 불안정하며 코어 온도는 24°C 미만이다.[2]
심장마비나 심장성 쇼크가 있는 사람들에게, 그것은 생존과 좋은 결과를 향상시키는 것으로 보인다.[3]
COVID-19 환자에 사용
2020년 2월 초부터 중국의 의사들은 사스-CoV-2 감염과 관련된 급성 바이러스성 폐렴에 걸린 환자에 대한 보조 지원으로 ECMO를 점점 더 많이 사용하고 있는데, 이때에만 환기만으로는 여전히 혈중 산소 농도가 너무 낮아 환자를 지탱할 수 없다.[4]초기 보고서는 그것이 이용된 중증 환자의 약 3% 중에서 환자의 혈중 산소 포화도를 회복하고 사망률을 감소시키는 데 도움을 주고 있다는 것을 보여준다.[5]중환자의 경우, 사망률은 재래식 치료의 경우 약 59~71%에서 체외막산소화를 통해 약 46%로 감소한다.[6]2021년 3월 로스엔젤레스 타임즈 커버스토리는 극도로 까다로운 COVID 환자에게서 ECMO의 효능을 보여주었다.[7]2021년 2월, COVID-19의 "매우 심각한" 사례를 가진 3명의 이스라엘 임산부에게 ECMO 치료를 받았고, 이 치료 방법은 계속될 것으로 보였다.[8]
결과
초기 연구들은 특히 급성 호흡곤란 증후군의 설정에서 급성 호흡부전 환자에 대한 ECMO의 사용으로 생존에 도움이 된다는 것을 보여주었다.[9][10]ELSO가 ECMO를 받은 약 5만1천명을 대상으로 관리하는 등록부는 신생아 호흡부전 생존율 75% 소아 호흡부전 생존율 56% 성인 호흡부전 생존율 55% 등의 결과를 보고했다.[11]다른 관찰 및 통제되지 않는 임상 실험에서는 생존율이 50~70%[12][13]라고 보고했다.이렇게 보고된 생존율은 역사적 생존율보다 낫다.[14][15][16]ECMO는 사망률이 다른 다양한 조건에 사용되지만 조기 발견이 열화의 진행을 막고 생존 결과를 높이는 데 핵심이다.[17]
영국에서는 잠재적으로 관리를 개선하고 더 나은 결과를 촉진하기 위해 지정 ECMO 센터에 Veno-venous ECMO 배치가 집중된다.
콘트라인커뮤니케이션
대부분의 금기사항은 절차의 위험과 잠재적 편익의 균형을 맞추면서 상대적이다.상대적 금지는 다음과 같다.
- 사람이 회복하는 경우 정상 생활과 호환되지 않는 조건
- 삶의 질에 영향을 미치는 기존 조건(CNS 상태, 말기 악성종양, 항응고 시 전신 출혈 위험)
- 나이와 크기
- 무의미: 너무 아프거나, 너무 오랫동안 관습적인 치료를 받았거나, 치명적인 진단을 받은 사람들.
부작용과 합병증
신경학
ECMO 치료 성인에게서 흔히 나타나는 결과는 뇌내출혈, 뇌하수체하출혈, 뇌 취약부 허혈성 경색, 저산소성 뇌병증, 설명할 수 없는 혼수상태, 뇌사 등이 포함될 수 있다.[18]출혈은 ECMO를 받은 사람의 30~40%에서 발생하며 생명을 위협할 수 있다.필요한 지속적인 헤파린 투약과 혈소판 기능 모두 때문이다.꼼꼼한 수술 기법, 혈소판 계수가 10만/mm3 이상 유지되고 표적 활성화 응고 시간을 유지하면 출혈 가능성이 줄어든다.[citation needed]
피
헤파린 유도 혈소판감소증(HIT)은 ECMO를 받는 사람들 사이에서 점점 흔해지고 있으며, HIT가 의심되면 헤파린 주입은 대개 비헤파린 항응고제로 대체된다.[19]
대퇴동맥과 정맥이 VA(Veno-Aterial) ECMO에 사용될 때마다 내림 대동맥에 역행성 혈류가 흐른다. 좌심실 출력이 유지되지 않으면 혈전증이 발생할 수 있다.[citation needed]
Bridge-to-Assist 장치
VA ECMO에서 심장 기능이 충분히 회복되지 않은 사람은 심실보조장치(VAD) 또는 이식에 연결될 수 있다.식인 중에 출혈이 있는 혈관 천공, 동맥 절개, 원위 허혈, 잘못된 위치(예: 동맥 내에 정맥 캐뉼라) 등 다양한 합병증이 발생할 수 있지만 이러한 현상은 매우 드물게 발생한다.[citation needed]
아이들.
임신 전 유아는 임신 32주 미만의 나이에 ECMO를 투여할 경우 심실내출혈(IVH)에 걸릴 위험이 매우 높다.[20]
감염
ECMO 기간 중 병원 감염의 유병률은 10~12%(다른 중환자 대비)이다.코아굴라제 음성 포도상구균, 칸디다 spp, 엔테로박테리아과, 녹농균 등이 가장 많이 관여하는 병원균이다.ECMO 환자들은 엔토박테리아과가 주요 역할을 하는 인공호흡기 관련 폐렴(24.4건/1000 ECMO일) 발생률이 높은 것으로 나타났다.감염 위험은 감염 발생에 가장 중요한 위험 요소인 ECMO 실행 기간에 따라 증가하는 것으로 나타났다.감염을 일으키는 다른 ECMO 특유의 요인으로는 ECMO 환자의 질병의 심각성, 장에서 세균이 전이될 위험이 높은 경우 및 면역체계의 ECMO 관련 손상 등이 있다.또 다른 중요한 문제는 카테터, ECMO 캐뉼러 및 산소 공급기의 미생물 결장이다.[21]
종류들
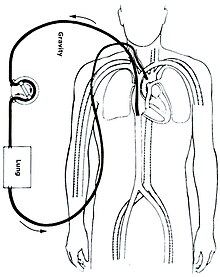

ECMO에는 몇 가지 형태가 있다. 가장 흔한 두 가지 형태는 정맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동VA ECMO에서는 이 혈액을 동맥계로, VV ECMO에서는 정맥계로 돌려준다.VV ECMO에서는 심장 지원이 제공되지 않는다.
정맥동맥
정맥동맥(VA) ECMO에서는 정맥 캐뉼라를 추출하기 위해 보통 오른쪽 또는 왼쪽 공통 대퇴정맥에 배치하고, 동맥 캐뉼라는 주입을 위해 대개 오른쪽 또는 왼쪽 대퇴동맥에 배치한다.[23]대퇴정맥 캐뉼라의 끝은 하대정맥과 우심방 접합부 부근에 유지되어야 하며 대퇴동맥 캐뉼라의 끝은 장골동맥에 유지되어야 한다.[23]성인의 경우 삽입이 간단하기 때문에 대퇴동맥에 접근하는 것이 선호된다.[23]심폐 우회술이 이미 확립되었거나 응급 재멸균이 수행된 경우(또는 우심방(또는 삼첨판 수리를 위한 SVC/IVC) 및 상승 대동맥) 중앙 VA ECMO를 사용할 수 있다.
VA ECMO는 일반적으로 대동맥 캐뉼라에 의해 전달되는 역행 흐름에 대한 펌핑과 관련된 증가된 심장 뇌졸중 작업을 완화하기 위해 기본 심장 기능이 최소일 때 유지된다.
정맥주사
정맥(VV) ECMO에서 캐뉼러는 배수를 위해 오른쪽 대퇴정맥에, 주입을 위해 오른쪽 내경정맥에 배치된다.[24]또는 우측 내경정맥에 이중루멘 카테터를 삽입하여 상·하대 정맥의 혈액을 빼내어 우심방으로 되돌려 보낸다.
입문
ECMO는 시작, 유지보수 및 중단에 대한 훈련과 경험이 있는 임상의만 수행해야 한다.ECMO 삽입은 일반적으로 흉부외과 의사가 수술실 환경에서 수행한다.ECMO 관리는 일반적으로 등록된 간호사, 호흡기 치료사 또는 관류사가 수행한다.일단 ECMO를 초기화하기로 결정되면, 환자는 혈전 형성이 산소 발생기에서 응고되는 것을 막기 위해 정맥 헤파린으로 항응고된다.시작에 앞서 활성 응고 시간(ACT)이 300초에서 350초 사이인지 확인하기 위해 헤파린의 IV 볼루스를 주고 측정한다.일단 ACT가 이 범위 사이에 있게 되면, ECMO를 개시할 수 있고 유지보수를 한 후에 헤파린 드립을 시작할 것이다.[17]: 143
식인
캐뉼러는 비교적 간단하고 일반적인 방법으로 혈관에 접근할 수 있는 셀딩거 기법이나 외과적 절단을 통해 경피적으로 배치될 수 있다.혈관에 넣을 수 있는 가장 큰 캐뉼러를 사용해 흐름을 극대화하고 전단 응력을 최소화한다.
심장마비 수술 후 합병증에 필요한 ECMO는 심장의 적절한 챔버나 훌륭한 혈관에 직접 배치될 수 있다.측면 개흉술을 통한 중앙식인식은 폐 이식을 기다리는 환자들을 치료하지 않고 이동하도록 한다.[25]
적정
식인 후 ECMO 회로에 연결한 후 혈류역학적 파라미터와 신체 검사를 사용하여 ECMO 회로를 통과하는 적절한 혈류량을 결정한다.ECMO 회로를 통한 기관 내 관류를 유지하려는 목표는 심장을 통한 충분한 생리학적 혈류로 균형을 이루며 정상과 그에 따른 혈전 형성을 예방한다.
유지 관리

일단 초기 호흡과 혈류역학적 목표가 달성되면, 혈류량은 그 속도로 유지된다.빈번한 평가와 조정은 ECMO 회로의 정맥 사지에 있는 혈액의 옥시헤모글로빈 포화도를 직접 측정하는 지속적인 정맥산소측정에 의해 촉진된다.
특별 고려사항
VV ECMO는 일반적으로 호흡부전에, VA ECMO는 심장부전에 사용된다.경영에 영향을 미치는 ECMO의 유형별로 고유한 고려사항이 있다.
혈류
산소 공급을 최적화하기 위해 VV ECMO 동안 거의 최대 유속이 필요하다.이와는 대조적으로 VA ECMO 동안 사용되는 유량은 적절한 관류 압력과 정맥 옥시헤모글로빈 포화(배수혈에 대한 측정값)를 제공할 수 있을 정도로 높지만 좌심실 출력을 유지하기에 충분한 예하중을 제공할 수 있을 만큼 충분히 낮아야 한다.
이오레시스
대부분의 사람들은 ECMO가 시작되면 액체가 과다하게 쌓이기 때문에 일단 환자가 ECMO에서 안정되면 공격적인 이뇨가 보장된다. 환자가 소변 출력이 불충분하면 ECMO 회로에 초유입이 쉽게 추가될 수 있다.ECMO "chatter" 또는 ECMO 파형의 불안정성은 저소비를 나타내며 공격적인 이뇨나 초유입의 중단을 지원할 수 있다.
좌심실 모니터링
좌심실 출력은 VA ECMO 동안 엄격하게 모니터링되는데, 이는 좌심실 기능이 애프터로드 증가로 인해 손상될 수 있고, 이는 심장 내에 혈전 형성을 초래할 수 있기 때문이다.[26][27]
웨이닝 및 중단
호흡기 장애가 있는 사람의 경우 방사선 외관, 폐 적합성 및 동맥 옥시헤모글로빈 포화도가 개선되면 ECMO 지원을 중단할 준비가 되어 있을 수 있다.심부전이 있는 사람들의 경우 강화된 대동맥 유동성은 개선된 좌심실 출력과 상관관계가 있으며 ECMO 지원을 중단할 준비가 되어 있음을 나타낸다.모든 마커의 상태가 양호하면 ECMO의 혈류량이 서서히 감소하고 환자가 변화를 견딜 수 있도록 이 시간 동안 환자 파라미터를 관찰한다.흐름이 분당 2리터 미만일 경우 영구 제거를 시도하고 이 시간 동안 캐뉼러를 제거할 수 있을 때까지 환자를 계속 모니터링한다.[17]: 149
Veno-venous ECMO 해방 재판
VV ECMO 시도는 산소 생성기를 통해 모든 역류 스위프 가스를 제거하여 수행된다.체외 혈류는 일정하게 유지되지만 기체 전달은 일어나지 않는다.그런 다음 몇 시간 동안 관찰되며, 그 동안 적절한 산소 공급과 ECMO의 환기를 유지하는 데 필요한 인공호흡기 설정은 동맥 및 정맥혈 가스 결과에 따라 결정된다.
Veno-arterial ECMO 해방 재판
VA ECMO 시험에서는 ECMO 회로가 동맥과 정맥 사지 사이의 다리를 통해 순환되도록 하면서 배수 라인과 주입 라인의 임시 클램핑이 필요하다.이것은 ECMO 회로 내에서 정체된 혈액의 혈전증을 예방한다.또한 동맥과 정맥선은 헤파린화된 식염수로 연속적으로 또는 간헐적으로 회로의 헤파린화된 혈액을 사용하여 플러싱해야 한다.일반적으로 VA ECMO 시험 기간은 혈전 형성 위험이 높기 때문에 VV ECMO 시험보다 짧다.
역사
ECMO는 1950년대에 존 깁본에 의해 개발되었고, 그 후 C에 의해 개발되었다. 월튼 릴레헤이신생아를 위한 첫 번째 용도는 1965년이었다.[28][29]
그레이 라리를[30] 금지하는 것은 정맥 산소가 생명을 유지할 수 있다는 것을 처음 보여주었다.그의 연구 결과는 1951년 11월 외과적 포럼에 발표되었다.[31]라리는 2007년 발표에서 자신의 초기 작업에 대해 "우리의 연구는 처음으로 순수한 질소를 호흡하면서 동물을 살아있게 하는 장치를 조립하는 것으로 시작되었다.이것은 혈류로 아주 작은 산소의 거품이 주입되어 이루어졌다.이 거품들은 자기 필터를 통해 정맥 혈류로 강제 유입되는 산소에 '침착제'를 첨가하여 만들어졌다.이 기구는 미국 외과대학에 처음 발표한 직후, DeWall과 함께 버블 산소 조절기를 사용하는 최초의 실용적인 심장[–] 기계를 만든 Walton Lillehee에 의해 검토되었다.변형과 함께 그러한 기계들은 그 후 20년 동안 사용되었다."
사회와 문화
제조자
- 메드트로닉[32]
- 마케[32](Geting Group)
- Xenios AG[32](Fresenius Medical Care)
- 소린 그룹[32]
- 테루모[32]
- 니프로[32]
- 마이크로포트[32]
유용성
| 국가/영토 | 대륙 | 장비된 병원 | 단위 |
|---|---|---|---|
| 미국 | 북아메리카 | 264(2019년)[33] | |
| 캐나다 | 북아메리카 | 19(2020년)[34] | |
| 호주. | 오세아니아 | 146(2020년) | |
| 브라질 | 남아메리카 | 21(2021년)[36] | |
| 잉글랜드와 웨일스 | 유럽 | 5(2020년)[37] | 15(2020년)[37] |
| 북아일랜드 | 유럽 | 0(2020년)[38] | 0(2020년)[38] |
| 스코틀랜드 | 유럽 | 1(2020년)[38] | 6(2020년)[38] |
| 독일. | 유럽 | 214(2020년)[39] | 779(2021년)[40] |
| 폴란드 | 유럽 | 47(2020년)[41] | |
| 스웨덴 | 유럽 | 7개 이상(2020년)[42] | |
| 알바니아 | 유럽 | 0(2020년)[43] | 0(2020년)[43] |
| 러시아 | 유럽 | 124 + 17(2020년)[44] | |
| 모스크바 | 유럽 | 16(2020년)[45] | |
| 러시아 상트페테르부르크 | 유럽 | 7 | 19(2020년)[46] |
| 일본. | 아시아 | 2208(2020년)[47] | |
| 중국 본토 | 아시아 | 400(2020년 약)[48] | |
| 타이완 | 아시아 | 51(2016년)[49] | 105(2016년)[49] 129개(2016년 임대차 포함)[50] |
리서치
무작위 제어 시행(RCT)
호흡기 장애 환자의 ECMO 효과를 평가하기 위해 네 번의 무작위 제어 시험(RCT)이 수행되었다.자폴 외와 [51]모리스 [52]외가 실시한 초기 실험은 1970년대와 1990년대에 이용할 수 있는 ECMO 기술과 관련된 기술적 난제에 시달렸다.CSAR와[53] EOLIA[54] 실험은 현대적인 ECMO 시스템을 활용했으며, 중앙 ECMO RCTs로 간주된다.
CSAR Trial(2009)
재래식 인공호흡기 지원 vs.중증성인호흡기 장애(CSAR) 시험을 위한 체외막산소화는 심하지만 되돌릴 수 있는 호흡기 장애가 있는 성인의 기존 기계적 인공호흡기와 비교하여 ECMO의 안전성, 유효성 및 비용 효율을 평가하는 것을 목적으로 하는 영국 기반의 다중점자 RCT였다.[53]병원에서 퇴원하기 6개월 전 사망이나 심각한 장애가 주된 결과였다.1차 결과는 오직 치료할 목적으로 분석되었다.경제 분석에는 품질 조정 수명년(QALY), 비용 발생 사건 분석, 6개월 후 비용 유용성 분석 및 수명 비용 효용성의 모델링이 포함되었다.재판에서는 팔마다 90명씩 180명의 환자를 등록할 계획이었다.
그 재판은 180명의 환자 등록 목표를 달성했다.ECMO로 치료하고자 하는 환자의 90명(75%) 중 68명이 실제로 ECMO로 치료되었다. ECMO 그룹에 할당된 환자의 생존율(즉, ECMO로 치료를 고려하기 위해 참조)은 기존 환기 그룹에 할당된 환자(63% 대 47%, p=0.03)보다 상당히 높았다.ECMO 그룹에 대한 의뢰는 6개월간의 후속 조치에서 기존 환기 그룹에 비해 0.03 QALY가 증가했다.ECMO 그룹에 대한 추천은 체류 기간이 길어지고 비용이 더 많이 들었다.[53]
기존 인공호흡기 그룹에 대한 표준화된 치료 프로토콜은 CSAR 연구의 주요 제한사항이다.[53][55] 재판 저자들은 이것이 사이트에 등록하여 프로토콜에 동의할 수 없기 때문에 발생했다는 점에 주목한다.[53]이로 인해 제어 환자는 ARDS 환자의 사망률을 높이는 것으로 알려진 폐 보호 환기를[53][56] 받지 못했다.[57]
저자들은 중증, 잠재적으로 가역할 수 있는 호흡기 장애가 있는 환자를 ECMO 센터에 의뢰하면 6개월의 중증 장애 없는 생존이 크게 개선될 수 있다고 결론짓는다.[53]ECMO 그룹의 75%만이 실제로 ECMO로 치료되었기 때문에 CSAR 시험 결과는 ECMO를 사용한 치료와 기존 기계 환기만을 위한 직접적인 생존 비교를 제공한다.[56]
EOLIA Trial(2018)
중증 ARDS(Emergency ARDS)에서 폐 부상을 구제하기 위한 ECMO Trial은[54] 중증 ARDS 환자의 지속적인 관리 표준(일반적인 기계적 인공호흡)과 비교하여 초기 ECMO 시작의 영향을 평가하기 위해 설계되었다.60일의 사망률이 주요 종말점이었다.계산된 표본 크기는 ECMO 그룹에서 절대 사망률이 20% 감소하는 것을 보여주려는 의도를 가진 331명의 환자였다.주요 2차 엔드포인트는 치료 실패 – 내화성 저산소혈증 또는 대조군 사망으로 인한 ECMO로 교차 전환 및 ECMO 그룹의 사망이었다.
네 번째 계획된 중간 분석 이후 재판은 무의미하게 끝났다.총 249명의 환자가 연구종료에 등록되었다.대조군 환자 35명(28%)은 ECORMO로 긴급 교차가 필요했으며, EOLIA의 결과는 ECMO군과 대조군(각각 35% 대 46%)의 60일 사망률에 큰 차이가 없는 것으로 나타났다.[54]그러나 이 결과에 대한 해석은 크로스오버 환자에 의해 복잡하다.[58]보조 엔드포인트인 치료 실패는 ECMO 그룹에 유리하게 0.62(p<0.001)의 상대적 위험을 보여주었다.2차 엔드포인트의 결과는 1차 엔드포인트 결과 때문에 조심스럽게 해석되어야 한다.안전성에 관해서, ECMO 그룹은 심각한 혈소판감소증과 수혈이 필요한 출혈의 비율이 훨씬 높았지만 허혈성 뇌졸중의 비율은 더 낮았다.[54]
EOLIA 재판의 주된 제한 사항은 전력이 부족하다는 것이었다.EOLIA가 11%의 사망률 감소의 중요성을 감지하기 위해 적절하게 동력을 공급받으려면 총 624명의 환자가 등록되어야 할 것이다.이런 재판은 EOLIA 채용률 기준으로 9년이 걸리며 실현 가능성이 희박하다.[55]
연구 저자들이 이러한 결과에서 도출한 주요 결론은 중증 ARDS 환자의 초기 ECMO 개시는 지속적인 치료 표준에 비해 사망률 편익을 제공하지 않는다는 것이다.[54]주요 오피니언 리더들의 후속 사설은 기존의 ARDS 치료에 실패한 환자들을 위한 구조 요법으로 사용될 경우 ECMO가 사망률을 개선할 수 있다는 실질적인 시사점을 제시한다.[58][59]
참조
- ^ "General Guidelines for all ECLS Cases" (PDF). Extracorporeal Life Support Organization. Retrieved April 15, 2015.
- ^ State of New Hampshire Patient Care Protocols v7. New Hampshire: NH Medical Control Board. 2018. p. 2.10.
- ^ Ouweneel DM, Schotborgh JV, Limpens J, Sjauw KD, Engström AE, Lagrand WK, et al. (December 2016). "Extracorporeal life support during cardiac arrest and cardiogenic shock: a systematic review and meta-analysis". Intensive Care Medicine. 42 (12): 1922–1934. doi:10.1007/s00134-016-4536-8. PMC 5106498. PMID 27647331.
- ^ "30 to 39 pct of severe COVID-19 patients discharged from Wuhan hospitals: official - Xinhua English.news.cn". xinhuanet.com. Retrieved February 16, 2020.
- ^ CDC (February 11, 2020). "2019 Novel Coronavirus (2019-nCoV)". Centers for Disease Control and Prevention. Retrieved February 16, 2020.
- ^ Melhuish TM, Vlok R, Thang C, Askew J, White L (January 2021). "Outcomes of extracorporeal membrane oxygenation support for patients with COVID-19: A pooled analysis of 331 cases". The American Journal of Emergency Medicine. 39: 245–246. doi:10.1016/j.ajem.2020.05.039. ISSN 0735-6757. PMC 7256518. PMID 32487460.
- ^ Curwen T (March 3, 2021). "She was dying of COVID-19. Her last hope was a device that would save or kill her". LA Times.
{{cite news}}: CS1 maint : url-status (링크) - ^ Ben-Nun S (February 4, 2021). "Pregnant women must not get COVID vaccine in first trimester - Health Min". The Jerusalem Post.
- ^ Peek GJ, Moore HM, Moore N, Sosnowski AW, Firmin RK (September 1997). "Extracorporeal membrane oxygenation for adult respiratory failure". Chest. 112 (3): 759–764. doi:10.1378/chest.112.3.759. PMID 9315812.
- ^ Lewandowski K, Rossaint R, Pappert D, Gerlach H, Slama KJ, Weidemann H, et al. (August 1997). "High survival rate in 122 ARDS patients managed according to a clinical algorithm including extracorporeal membrane oxygenation". Intensive Care Medicine. 23 (8): 819–835. doi:10.1007/s001340050418. PMID 9310799. S2CID 25107418.
- ^ Thiagarajan RR, Barbaro RP, Rycus PT, Mcmullan DM, Conrad SA, Fortenberry JD, Paden ML (April 1, 2017). "Extracorporeal Life Support Organization Registry International Report 2016". ASAIO Journal. 63 (1): 60–67. doi:10.1097/MAT.0000000000000475. PMID 27984321. S2CID 205758344.
- ^ Hemmila MR, Rowe SA, Boules TN, Miskulin J, McGillicuddy JW, Schuerer DJ, et al. (October 2004). "Extracorporeal life support for severe acute respiratory distress syndrome in adults". Annals of Surgery. 240 (4): 595–605, discussion 605–07. doi:10.1097/01.sla.0000141159.90676.2d. PMC 1356461. PMID 15383787.
- ^ Brogan TV, Thiagarajan RR, Rycus PT, Bartlett RH, Bratton SL (December 2009). "Extracorporeal membrane oxygenation in adults with severe respiratory failure: a multi-center database". Intensive Care Medicine. 35 (12): 2105–2114. doi:10.1007/s00134-009-1661-7. PMID 19768656. S2CID 526020.
- ^ Kolla S, Awad SS, Rich PB, Schreiner RJ, Hirschl RB, Bartlett RH (October 1997). "Extracorporeal life support for 100 adult patients with severe respiratory failure". Annals of Surgery. 226 (4): 544–64, discussion 565–66. doi:10.1097/00000658-199710000-00015. PMC 1191077. PMID 9351722.
- ^ Rich PB, Awad SS, Kolla S, Annich G, Schreiner RJ, Hirschl RB, Bartlett RH (March 1998). "An approach to the treatment of severe adult respiratory failure". Journal of Critical Care. 13 (1): 26–36. doi:10.1016/S0883-9441(98)90026-0. PMID 9556124.
- ^ Ullrich R, Lorber C, Röder G, Urak G, Faryniak B, Sladen RN, Germann P (December 1999). "Controlled airway pressure therapy, nitric oxide inhalation, prone position, and extracorporeal membrane oxygenation (ECMO) as components of an integrated approach to ARDS". Anesthesiology. 91 (6): 1577–1586. doi:10.1097/00000542-199912000-00007. PMID 10598597.
- ^ a b c Lich B (2004). The Manual of Clinical Perfusion (2nd ed.). Fort Myers, Florida: Perfusion.com. ISBN 978-0-9753396-0-2.
- ^ Mateen FJ, Muralidharan R, Shinohara RT, Parisi JE, Schears GJ, Wijdicks EF (December 2011). "Neurological injury in adults treated with extracorporeal membrane oxygenation". Archives of Neurology. 68 (12): 1543–1549. doi:10.1001/archneurol.2011.209. PMC 7816483. PMID 21825216.
- ^ Cornell T, Wyrick P, Fleming G, Pasko D, Han Y, Custer J, et al. (2007). "A case series describing the use of argatroban in patients on extracorporeal circulation". ASAIO Journal. 53 (4): 460–463. doi:10.1097/MAT.0b013e31805c0d6c. PMID 17667231. S2CID 26942284.
- ^ Jobe AH (2004). "Post-conceptional age and IVH in ECMO patients". The Journal of Pediatrics. 145 (2): A2. doi:10.1016/j.jpeds.2004.07.010.
- ^ Biffi S, Di Bella S, Scaravilli V, Peri AM, Grasselli G, Alagna L, et al. (July 2017). "Infections during extracorporeal membrane oxygenation: epidemiology, risk factors, pathogenesis and prevention". International Journal of Antimicrobial Agents. 50 (1): 9–16. doi:10.1016/j.ijantimicag.2017.02.025. PMID 28528989.
- ^ a b Van Meurs K, Lally K, Zwischenberger JB, Peek G, eds. (2005). ECMO: Extracorporeal Cardiopulmonary Support in Critical Care. Ann Arbor: Extracorporeal Life Support Organization. ISBN 978-0-9656756-2-8.[페이지 필요]
- ^ a b c Madershahian N, Nagib R, Wippermann J, Strauch J, Wahlers T (2006). "A simple technique of distal limb perfusion during prolonged femoro-femoral cannulation". Journal of Cardiac Surgery. 21 (2): 168–169. doi:10.1111/j.1540-8191.2006.00201.x. PMID 16492278. S2CID 11052174.
- ^ Wang D, Zhou X, Liu X, Sidor B, Lynch J, Zwischenberger JB (2008). "Wang-Zwische double lumen cannula-toward a percutaneous and ambulatory paracorporeal artificial lung". ASAIO Journal. 54 (6): 606–611. doi:10.1097/MAT.0b013e31818c69ab. PMID 19033774. S2CID 25384012.
- ^ Chierichetti M, Santini A, Pagan F, Crotti S, Lissoni A, Gattinoni L (2012). "ECMO in nonintubated patients as a bridge to lung transplant: Our experience". Critical Care. 16 (Suppl 1): 97. doi:10.1186/cc10704. PMC 3363515.
- ^ Cohen G, Permut L (2005). "Decision making for mechanical cardiac assist in pediatric cardiac surgery". Seminars in Thoracic and Cardiovascular Surgery. Pediatric Cardiac Surgery Annual. 8: 41–50. doi:10.1053/j.pcsu.2005.02.004. PMID 15818357.
- ^ Vural KM (November 2008). "Ventricular assist device applications". Anadolu Kardiyoloji Dergisi. 8 (Suppl 2): 117–130. PMID 19028644.
- ^ Rodriguez-Cruz E, Walters III H, Aggarwal S, Schwartz DS (August 3, 2021). Windle ML, Mancini MC, Berger S (eds.). "Pediatric Extracorporeal Membrane Oxygenation". Medscape. WebMD LLC.
- ^ Mosier JM, Kelsey M, Raz Y, Gunnerson KJ, Meyer R, Hypes CD, et al. (December 2015). "Extracorporeal membrane oxygenation (ECMO) for critically ill adults in the emergency department: history, current applications, and future directions". Critical Care. 19: 431. doi:10.1186/s13054-015-1155-7. hdl:10150/621244. PMC 4699333. PMID 26672979.
- ^ "Banning Gray Lary, MD". banninggraylary.com.
{{cite web}}: CS1 maint : url-status (링크) - ^ Lary BG (1951). "Experimental maintenance of life by intravenous oxygen; preliminary report". Surgical Forum: 30–5. PMID 14931193 – via W.B. Saunders Company, Philadelphia 1952 (publisher) The Proceedings of the Forum Sessions 37th Clinical Congress of the American College of Surgeons, San Francisco, California, November, 1951.
- ^ a b c d e f g "ExtraCorporeal Membrane Oxygenation Market 2020 Recent Trends, Analysis, Business Growth, Share Estimation and Regional Overview Forecast by 2026". MarketWatch. April 16, 2020. Archived from the original on June 25, 2020.
- ^ Bailey M (June 17, 2019). "Miracle medical machine ECMO makes heroic rescues, but leaves patients in limbo". USA Today.
- ^ "ELSO Center Identification List". Extracorporeal Life Support Organization. July 23, 2020.
- ^ Litton E, Bucci T, Chavan S, Ho YY, Holley A, Howard G, et al. (June 2020). "Surge capacity of intensive care units in case of acute increase in demand caused by COVID-19 in Australia". The Medical Journal of Australia. 212 (10): 463–467. doi:10.5694/mja2.50596. PMC 7264562. PMID 32306408.
- ^ "Tratamento de Paulo Gustavo custa R$ 30 mil por dia e não é mais ofertado pelo SUS" [Paulo Gustavo's treatment costs BRL 30,000 per day and is no longer offered by SUS]. Correio Braziliense (in Portuguese). April 5, 2021.
- ^ a b Mason R (February 27, 2020). "Coronavirus: England only has 15 beds for worst respiratory cases]". The Guardian.
- ^ a b c d Smyth L (April 5, 2020). "Coronavirus: Not providing special oxygen machine will cost lives in Northern Ireland, warns expert". The Belfast Telegraph.
- ^ "DIVI-Intensivregister" [DIVI intensive register] (in German). May 10, 2020.
- ^ "DIVI Intensivregister". www.intensivregister.de. Retrieved December 9, 2021.
- ^ "Walka z koronawirusem. Ile w Polsce jest urządzeń do wspomagania oddychania?" [Fighting the Coronavirus. How many breathing devices are there in Poland?]. TVN24 (in Polish). March 12, 2020.
- ^ "Få Ecmo-platser för svårt coronasjuka på Nya Karolinska" [Ecmo places for severe coronary heart disease at the New Karolinska Hospital]. Dagens Nyheter (in Swedish). March 10, 2020.
- ^ a b "Mjeku shqiptar në Gjermani: Ka disa kushte për vetizolimin, në Shqipëri nuk ka aparat ECMO, rreziku është I madh" [Albanian doctor in Germany: There are some conditions for self-isolation, in Albania there is no ECMO device, the risk is great]. Ora News (in Albanian). March 12, 2020.
- ^ "Голикова заверила, что медики в РФ готовы к любому развитию ситуации с COVID-19" [Golikova assured that doctors in the Russian Federation are ready for any development of the situation with COVID-19]. Interfax.ru (in Russian). Interfax. March 16, 2020.
- ^ "НОВАЯ ИНФЕКЦИОННАЯ БОЛЬНИЦА СМОЖЕТ ПРИ НЕОБХОДИМОСТИ ПРИНЯТЬ ДО 500 ЧЕЛОВЕК" [The New Infectious Hospital Will Be Able to Take Up to 500 People if Necessary] (in Russian). Moscow City Health Department. March 13, 2020.
- ^ "'Свободны 400 аппаратов': в Смольном опровергли дефицит ИВЛ в Петербурге" ['400 devices are free': in Smolny they denied the shortage of mechanical ventilation in St. Petersburg] (in Russian). Department of Health of Moscow. April 12, 2020.
- ^ "国内の病院における人工呼吸器等の取扱台数推計値" [Estimated number of ventilators handled in domestic hospitals] (PDF) (in Japanese). Japanese Association for Acute Medicine. May 2020.
- ^ "疫情关键时刻救命的ECMO:全国只有400台 为何这么少?" [ECMO that saves lives at the critical moment of the epidemic: There are only 400 units in the country, why are so few?] (in Chinese). Sina Corp. February 10, 2020.
- ^ a b "全台爆葉克膜荒 醫護:已無武器可用!" [The whole Taiwan explodes, and the film is in short supply. Medical care: no weapons are available!]. Liberty Times (in Chinese (Taiwan)). March 4, 2016. Archived from the original on June 5, 2021. Retrieved June 5, 2021.
- ^ "衛福部與衛生局已啟動流感應變醫院及醫療調度機制" [The Ministry of Health and Welfare and the Health Bureau have activated the influenza response hospital and medical dispatch mechanism]. 105年衛生福利部新聞/3月新聞 (Ministry of Health and Welfare News) (in Chinese (Taiwan)). Department of Medical Affairs, Ministry of Health and Welfare (Taiwan). March 4, 2016. Archived from the original on June 5, 2021. Retrieved June 5, 2021.
- ^ Zapol WM, Snider MT, Hill JD, Fallat RJ, Bartlett RH, Edmunds LH, et al. (November 1979). "Extracorporeal membrane oxygenation in severe acute respiratory failure. A randomized prospective study". JAMA. 242 (20): 2193–2196. doi:10.1001/jama.242.20.2193. PMID 490805.
- ^ Morris AH, Wallace CJ, Menlove RL, Clemmer TP, Orme JF, Weaver LK, et al. (February 1994). "Randomized clinical trial of pressure-controlled inverse ratio ventilation and extracorporeal CO2 removal for adult respiratory distress syndrome". American Journal of Respiratory and Critical Care Medicine. 149 (2 Pt 1): 295–305. doi:10.1164/ajrccm.149.2.8306022. PMID 8306022.
- ^ a b c d e f g Peek GJ, Mugford M, Tiruvoipati R, Wilson A, Allen E, Thalanany MM, et al. (October 2009). "Efficacy and economic assessment of conventional ventilatory support versus extracorporeal membrane oxygenation for severe adult respiratory failure (CESAR): a multicentre randomised controlled trial". Lancet. 374 (9698): 1351–1363. doi:10.1016/S0140-6736(09)61069-2. PMID 19762075. S2CID 15191122.
- ^ a b c d e Combes A, Hajage D, Capellier G, Demoule A, Lavoué S, Guervilly C, et al. (May 2018). "Extracorporeal Membrane Oxygenation for Severe Acute Respiratory Distress Syndrome". The New England Journal of Medicine. 378 (21): 1965–1975. doi:10.1056/NEJMoa1800385. PMID 29791822. S2CID 44106489.
- ^ a b Gattinoni L, Vasques F, Quintel M (July 2018). "Use of ECMO in ARDS: does the EOLIA trial really help?". Critical Care. 22 (1): 171. doi:10.1186/s13054-018-2098-6. PMC 6034241. PMID 29976250.
- ^ a b "A final verdict for ECMO use in severe ARDS?". ESICM. July 19, 2018. Retrieved January 3, 2022.
- ^ Brower RG, Matthay MA, Morris A, Schoenfeld D, Thompson BT, Wheeler A (May 2000). "Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome". The New England Journal of Medicine. 342 (18): 1301–1308. doi:10.1056/NEJM200005043421801. PMID 10793162.
- ^ a b Hardin CC, Hibbert K (May 2018). "ECMO for Severe ARDS". The New England Journal of Medicine. 378 (21): 2032–2034. doi:10.1056/NEJMe1802676. PMID 29791819.
- ^ Sameed M, Meng Z, Marciniak ET (September 2019). "EOLIA trial: the future of extracorporeal membrane oxygenation in acute respiratory distress syndrome therapy?". Breathe. 15 (3): 244–246. doi:10.1183/20734735.0363-2018. PMC 6717615. PMID 31508163.
외부 링크
| 위키미디어 커먼스는 체외막산소와 관련된 미디어를 보유하고 있다. |
| 스콜리아는 체외막산소화(Q1385195)에 대한 프로필을 가지고 있다. |
- "What is ECMO?" (PDF). American Thoracic Society Patient Education.




