브로마이드 세슘
Caesium bromide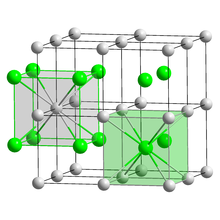 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 브로마이드 세슘 | |
| 기타 이름 세슘브로마이드, 세슘(I)브로마이드 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.029.209 |
| EC 번호 |
|
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| CsBr | |
| 어금질량 | 212.809 g/198[1] |
| 외관 | 화이트솔리드 |
| 밀도 | 4.43 g/cm3[1] |
| 녹는점 | 636°C(1,177°F, 909K)[1] |
| 비등점 | 1,300 °C(2,370 °F, 1,570 K)[1] |
| 1230 g/L(25 °C)[1] 분쟁 발생. 420 g/L(11°C) 참조 | |
자기 감수성(magnetic susibility) | -67.2·10cm−63/190cm[2] |
굴절률(nD) | 1.8047 (0.3µm) 1.6974 (0.59 µm) 1.6861(0.75µm) 1.6784(1µm) 1.6678(5µm) 1.6439(20µm)[3] |
| 구조 | |
| CsCl, cP2 | |
| 221번[4] Pm3m | |
a = 0.4291 nm | |
격자 부피(V) | 0.0790nm3 |
공식 단위(Z) | 1 |
| 큐빅(Cs+) 세제곱(Br−) | |
| 위험 | |
| GHS 라벨 표시: | |
 | |
| 경고 | |
| H302, H315, H319, H335 | |
| P261, P264, P270, P271, P280, P301+P312, P302+P352, P304+P340, P305+P351+P338, P312, P321, P330, P332+P313, P337+P313, P362, P403+P233, P405, P501 | |
| NFPA 704(화재 다이아몬드) | |
| 플래시 포인트 | 불연성 |
| 치사량 또는 농도(LD, LC): | |
LD50(중간 선량) | 1400mg/kg(도덕, 랫드)[5] |
| 관련 화합물 | |
기타 음이온 | 플루오르화 세슘 염화 세슘 요오드화 세슘 아스타타이드 세슘 |
기타 양이온 | 브롬화 나트륨 브롬화칼륨 브로민화 루비듐 브롬화 프랑슘 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
세슘브로마이드 또는 세슘브로마이드(Cesium Bromide)는 화학 공식 CsBr과 함께 세슘과 브롬인의 이온 화합물이다. 636 °C에서 녹는점이 있는 흰색 또는 투명한 고체로 물에 쉽게 용해된다. 그것의 벌크 크리스털은 입방형 CsCl 구조를 가지고 있지만, 구조는 mica, LiF, KBr 또는 NaCl 기판에서 자라는 나노미터 두께의 필름에서 암석암형으로 바뀐다.[6]
합성
브로민화 세슘은 다음과 같은 반응을 통해 준비될 수 있다.
- 중화:
- CsOH (aq) + HBr (aq) → CsBr (aq) + H2O (l)
- Cs2(CO3) (aq) + 2 HBr (aq) → 2 CsBr (aq) + H2O (l) + CO2 (g)
- 직접 합성:
- 2 Cs (s) + Br2 (g) → 2 CsBr (s)
직접 합성은 세슘이 다른 할로겐과 활발하게 반응하는 것이다. 비용이 많이 들기 때문에 준비에는 사용되지 않는다.
사용하다
세슘브로마이드(Cesium Bromide)는 광학에서 광대역 분광도계의 빔플리터 성분으로 사용되기도 한다.
참조
- ^ a b c d e 헤인즈, 페이지 4.57
- ^ 헤인즈, 4.132 페이지
- ^ 헤인즈, 페이지 10.240
- ^ Vallin, J.; Beckman, O.; Salama, K. (1964). "Elastic Constants of CsBr and CsI from 4.2°K to Room Temperature". Journal of Applied Physics. 35 (4): 1222. Bibcode:1964JAP....35.1222V. doi:10.1063/1.1713597.
- ^ 브로마이드 세슘. nlm.nih.gov
- ^ Schulz, L. G. (1951). "Polymorphism of cesium and thallium halides". Acta Crystallographica. 4 (6): 487–489. doi:10.1107/S0365110X51001641.
* Crystran Ltd 실험 데이터 2021년 7월
인용된 출처
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. ISBN 1-4398-5511-0.
외부 링크
| 위키미디어 커먼스는 세슘 브로마이드와 관련된 미디어를 보유하고 있다. |



