3D 바이오프린팅
3D bioprinting3차원(3D) 바이오프린팅은 세포, 성장인자 및/또는 생체소재를 결합하여 종종 자연 조직의 특성을 모방할 목적으로 생물의학 부품을 제작하는 3D 프린팅과 같은 기술을 사용하는 것입니다.일반적으로 3D 바이오프린팅은 바이오링크라고 알려진 재료를 층별로 퇴적시켜 나중에 다양한 의료 [1][2]및 조직 공학 분야에서 사용되는 조직과 같은 구조를 만들 수 있습니다. 3D 바이오프린팅은 광범위한 바이오프린팅 기술과 생체 재료를 포함합니다.현재 바이오프린팅은 약물 및 잠재적 [3]치료법을 연구하는 데 도움이 되는 조직 및 장기 모델을 인쇄하는 데 사용될 수 있습니다.bioprinted 살고 있는 휴대 구문의 임상 응용 프로그램에서 그럼에도 불구하고, 번역은 몇몇 문제의 복잡성과 휴대 전화 번호 기능 장기를 만드는 데 필요한 때문에[4] 하지만, 혁신 세포외 기질의 bioprinting hydrogels 계층의 원하는 조직 생산에 넣어 세포들과 어울리는 데에 걸치는 경우에만 충족된다..[5]또한 3D 바이오프린팅은 발판 인쇄를 통합하기 시작했습니다.이 발판은 관절과 [6]인대를 재생하는 데 사용될 수 있다.
과정
3D 바이오프린팅은 일반적으로 프리바이오프린팅, 바이오프린팅,[7][8] 포스트바이오프린팅의 세 가지 단계를 따릅니다.
바이오프린트 전
프리바이오프린트는 프린터가 나중에 만들 모델을 만들고 사용할 재료를 선택하는 과정입니다.첫 단계 중 하나는 장기의 조직검사를 받는 것이다.바이오프린트에 사용되는 일반적인 기술은 컴퓨터 단층촬영(CT)과 자기공명영상(MRI)입니다.레이어별로 인쇄하려면 영상에 단층 재구성이 수행됩니다.그런 다음 2D 이미지가 프린터로 전송되어 만들어집니다.영상이 생성되면 특정 셀이 분리되고 [7]증식됩니다.그리고 나서 이 세포들은 산소와 다른 영양분을 공급하는 특별한 액화 물질과 섞인다.일부 공정에서는 세포는 직경 500μm의 세포성 구상체에 봉입된다.이러한 세포 집적에는 발판이 필요하지 않으며,[9]: 165 압출과 같은 과정을 위해 관상 조직 융접에 배치하기 위해 필요합니다.
바이오프린트
두 번째 단계에서는 세포, 매트릭스 및 바이오링크라고 알려진 영양소의 액체 혼합물을 프린터 카트리지에 넣고 환자의 의학 [10]스캔을 사용하여 증착한다.생체 인쇄된 사전 조직이 인큐베이터로 옮겨지면 이 세포 기반 사전 조직이 조직으로 성숙합니다.
생물학적 구조를 제작하기 위한 3D 바이오프린팅은 일반적으로 조직과 같은 3차원 [11]구조를 생성하기 위해 연속적인 층별 접근방식을 사용하여 생체적합성 골격에 세포를 분사하는 것을 포함한다.3D 바이오프린팅에 의해 만들어진 간이나 신장 같은 인공 장기는 작동하는 혈관, 소변을 채취하기 위한 튜브, 그리고 이러한 장기에 필요한 수십억 개의 세포의 성장과 같은 신체에 영향을 미치는 중요한 요소들이 부족한 것으로 나타났다.이러한 성분들이 없다면 신체는 [11]그들의 내부 깊숙이 필수 영양소와 산소를 섭취할 방법이 없다.체내의 모든 조직이 자연적으로 다른 세포 유형으로 구성되어 있기 때문에, 이러한 세포를 인쇄하는 많은 기술은 제조 공정에서 세포의 안정성과 생존성을 보장하는 능력에 있어 다양합니다.세포의 3D 바이오프린트에 사용되는 방법으로는 포토 리소그래피, 자기 3D 바이오프린트, 입체 리소그래피, 직접 세포 압출 [9]: 196 등이 있습니다.
바이오프린트 후
생물학적 물질로부터 안정적인 구조를 만들기 위해서는 바이오프린트 후 프로세스가 필요합니다.이 공정을 제대로 유지하지 않으면 3D 프린팅된 물체의 기계적 무결성과 기능이 위험에 [7]처할 수 있습니다.물체를 유지하기 위해서는 기계적 자극과 화학적 자극이 모두 필요합니다.이러한 자극은 세포에 신호를 보내 조직의 리모델링과 성장을 조절한다.또한, 최근 개발에서 생물반응기 기술은[12] 조직의 빠른 성숙, 조직의 혈관 형성 및 이식 [8]생존 능력을 가능하게 했다.
생물반응기는 대류성 영양소 수송을 제공하고, 미소 중력 환경을 조성하고, 셀을 통해 용액이 흐르게 하는 압력을 변화시키거나, 동적 또는 정적 부하를 위해 압축을 추가하는 역할을 합니다.각 유형의 생물반응기는 다른 유형의 조직에 이상적이며, 예를 들어 압축 생물반응기는 연골 [9]: 198 조직에 이상적입니다.
바이오프린팅 어프로치
그 분야의 연구자들은 적절한 생물학적, 기계적 성질을 가진 살아있는 장기를 생산하는 방법을 개발했다.3D 바이오프린팅은 생체모방, 자율 자가조립 및 미니 조직 구성 블록의 [13]세 가지 주요 접근 방식을 기반으로 합니다.
생체모방
바이오프린팅의 첫 번째 접근법은 생체모방이라 불린다.이 접근법의 주요 목표는 인체 내 조직과 장기에서 발견되는 자연 구조와 동일한 인공 구조를 만드는 것이다.생체모방은 형태, [14]골격, 그리고 장기나 조직의 미세환경의 복제를 필요로 한다.바이오프린팅에서 생체모방의 적용은 장기의 세포 부분과 세포 외 부분을 똑같이 만드는 것을 포함한다.이 접근방식이 성공하려면 조직을 마이크로스케일로 복제해야 합니다.따라서 미세환경, 이 미세환경에서의 생물학적 힘의 성질, 기능적 및 보조세포의 정확한 구성, 용해성 인자 및 세포외 [13]매트릭스의 구성을 이해할 필요가 있다.
자율 자기 조립
바이오프린팅의 두 번째 접근법은 자율적인 자기조립입니다.이 접근법은 관심 [14]조직을 복제하는 모델로서 배아 장기 발달의 물리적 과정에 의존한다.세포가 초기 발달 단계에 있을 때, 그들은 필요한 생물학적 기능과 [13]마이크로 아키텍처를 제공하기 위해 그들만의 세포외 매트릭스 구성 블록, 적절한 세포 신호 전달, 독립적인 배열과 패턴을 만듭니다.자율적인 자가조립은 [14]배아의 조직과 장기의 발달 기술에 대한 구체적인 정보를 요구한다.진화하는 조직을 닮기 위해 융합과 세포 배열을 하는 자가조립 스페로이드를 사용하는 "스카폴드 프리" 모델이 있습니다.자율적인 자가조립은 조직 형성의 기본 동인으로서 세포에 의존하며, 이러한 조직의 구성 요소, 구조 및 기능적 특성을 안내합니다.그것은 배아 조직 메커니즘이 어떻게 발달하는지 그리고 바이오프린트된 [13]조직을 만들기 위해 둘러싸인 미세 환경에 대한 더 깊은 이해를 요구한다.
미니 티슈
바이오프린팅의 세 번째 접근법은 생체모방과 미니 조직이라고 불리는 자기조립 접근법의 조합이다.장기와 조직은 매우 작은 기능적 구성요소로 만들어진다.미니 조직 접근법은 이러한 작은 부품을 더 큰 [14][13]프레임워크로 제작하고 배열합니다.
프린터
일반 잉크 프린터와 마찬가지로 바이오프린터에는 세 가지 주요 구성 요소가 있습니다.사용하는 하드웨어, 바이오잉크의 종류 및 인쇄물(바이오머티리얼)[7]입니다.바이오잉크는 살아있는 세포로 만든 물질로 액체처럼 반응하며 원하는 모양을 만들기 위해 인쇄를 할 수 있습니다.바이오잉크를 만들기 위해 과학자들은 카트리지에 넣고 특별히 설계된 프린터에 삽입할 수 있는 셀과 바이오 페이퍼라고 불리는 젤을 포함한 [15]다른 카트리지를 만듭니다."바이오프린트에는 크게 3종류의 프린터가 사용되고 있습니다.잉크젯 프린터, 레이저 지원 프린터, 압출 프린터입니다.잉크젯 프린터는 주로 고속 및 대규모 제품의 바이오 프린팅에 사용된다.드롭 온 디맨드 잉크젯 프린터라고 불리는 잉크젯 프린터는 정확한 양의 재료를 인쇄하여 비용과 [16]낭비를 최소화합니다.레이저를 사용하는 프린터는 고해상도 인쇄를 실현합니다만, 이러한 프린터는 고액의 인쇄가 되는 경우가 많습니다.압출 프린터는 3D 프린팅으로 3D 구조를 만드는 것과 마찬가지로 셀을 층별로 인쇄합니다.압출 프린터는 셀뿐만 아니라 [7]셀이 주입된 하이드로겔도 사용할 수 있습니다.
압출 기반 방식
압출 기반 프린팅은 3D 프린팅 분야에서 매우 일반적인 기술로,[17] 녹은 고체 물질이나 점성이 있는 액체를 일종의 오리피스를 통해 연속적으로 밀어내거나 강제하는 것을 수반합니다.압출 기반 바이오 프린팅에 관해서는 크게 세 가지 유형의 압출이 있습니다.공압구동, 피스톤구동 및 나사구동입니다.각 압출법은 각각의 장점과 단점을 가지고 있다.공기압 압출은 가압된 공기를 사용하여 액체 바이오잉크를 증착제를 통과시킵니다.바이오잉크를 이동하는 데 사용되는 공기에는 오염물질이 없어야 합니다.공기 필터는 일반적으로 [18]공기를 사용하기 전에 살균하는 데 사용됩니다.피스톤 구동 압출은 가이드 나사에 연결된 피스톤을 사용합니다.피스톤의 선형 운동은 노즐에서 재료를 짜냅니다.나사 구동 압출은 오거 나사를 사용하여 재료를 압출합니다.회전 운동으로 인해 재료가 아래로 밀리고 [19]노즐에서 빠져나갑니다.나사 구동 장치를 사용하면 점도가 높은 재료를 사용할 수 있으며 더 많은 체적 [17]제어 기능을 제공합니다.일단 인쇄가 완료되면 많은 재료들이 구조에서 원하는 기계적 특성을 달성하기 위해 가교 단계를 필요로 합니다. 예를 들어 화학제나 포토 가교제를 처리함으로써 가교 단계를 달성할 수 있습니다.
직접 압출은 가장 일반적인 압출 기반 바이오프린트 기술 중 하나로, 가압력에 의해 바이오잉크가 노즐 밖으로 흘러나와 별도의 주조 없이 [20]직접 발판을 인쇄합니다.이 접근방식의 바이오잉크 자체는 폴리머 하이드로겔, 콜라겐과 같은 자연유래 물질 및 용액에 [20]현탁된 살아있는 세포를 혼합한 것일 수 있습니다.이와 같이 비계를 인쇄 후 배양할 수 있으며 세포 파종을 위한 추가 처리가 필요하지 않다.다이렉트 프린트 기법의 사용에는, 동축 노즐 어셈블리 또는 동축 압출의 사용에 근거하고 있습니다.동축 노즐 설정은 단일 압출 공정으로 [21]다층 발판을 만들 수 있는 여러 재료 바이오링크를 동시에 압출할 수 있도록 합니다.튜브형 구조의 개발은 이러한 기술을 통해 달성된 층상 압출이 동축 노즐이 바이오잉크 흐름을 [21]위한 내부 및 외부 튜브를 제공하기 때문에 재료 특성에서 제공할 수 있는 방사상 가변성에 바람직하다는 것을 발견했습니다.바이오프린트를 위한 간접압출기술은 오히려 셀을 이용한 하이드로겔의 모재를 인쇄해야 하지만, 직접압출과는 달리 열 또는 화학적 [22]추출을 통해 인쇄 후를 제거할 수 있는 희생 하이드로겔을 포함하고 있습니다.나머지 수지는 응고되어 원하는 3D 프린팅 구조물이 됩니다.
기타 인쇄 방법
액체 기반 바이오프린팅은 세포 및/또는 하이드로겔의 바이오잉크 블렌드를 물방울에 정확한 위치에 배치하는 기술이다.이러한 접근 방식 중 가장 일반적인 것은 열 및 압전 드롭 온디맨드 [23]기술입니다.열 기술은 짧은 지속 시간 신호를 사용하여 바이오 잉크를 가열하여 작은 기포의 형성을 유도합니다.압전 바이오프린트는 오히려 압전 액튜에이터에 인가되는 짧은 지속전류를 가지며, 노즐을 통해 소량의 바이오잉크를 토출할 수 있는 기계적 진동을 유도한다.바이오프린트에 대한 액체 기반 접근법의 연구의 중요한 측면은 노즐 팁 근처의 바이오잉크 경험 내에서 기계 및 열응력 셀이 압출될 때 이를 고려하는 것입니다.
레이저 기반의 바이오 프린팅은 일반적으로 세포 전송 기술 또는 광중합 기술에 기초한 두 가지 주요 클래스로 구분할 수 있습니다.세포전사 레이저 인쇄에서 레이저는 에너지 흡수 물질(예를 들어 금, 티타늄 등)과 희생 물질을 포함한 바이오 잉크 사이의 계면을 자극한다.이 희생적인 '공여층'은 레이저의 조사로 증발하여 [24]제트에서 퇴적된 바이오잉크층에서 기포를 형성합니다.광중합 기술은 오히려 광개시 반응을 이용하여 잉크를 굳히고 레이저의 빔 경로를 움직여 원하는 구조를 형성하도록 유도한다.재료에 적재된 세포를 손상시키지 않고 광중합 반응과 짝을 이루는 특정 레이저 주파수를 실행할 수 있다.
| 바이오프린트 방법 | 인쇄 모드 | 이점 |
|---|---|---|
| 다이렉트 프린트 | 압출 기반 | 간단한 실행, 캐스팅 없음 |
| 동축 압출 | 압출 기반 | 다층 구조의 단일 단계 구성 |
| 간접적인 | 압출 기반 | 구조 형성을 지원하기 위해 제거 가능한 '희생 재료'가 필요합니다. |
| 레이저 | 레이저 베이스 | 잉크에 떠 있는 셀에 전단 응력이 없음 |
| 물방울 | 액적 베이스 | 흐름 및 비계 형성 정밀 제어 |
적용들
이식 가능한 장기 및 연구용 장기
의료 분야에는 3D 바이오프린팅을 위한 몇 가지 응용 프로그램이 있습니다.기관연화증(TBM)으로 알려진 희귀 호흡기 질환이 있는 유아 환자에게 3D 프린팅으로 [25]만들어진 기관 부목을 투여했습니다. 3D 바이오프린팅을 사용하여 신체 여러 부위의 조직을 재구성할 수 있습니다.말기 방광 질환 환자들은 손상된 [26]장기를 재건하기 위해 조작된 방광 조직을 사용하여 치료될 수 있다.이 기술은 뼈, 피부, 연골, 근육 [27]조직에도 적용될 수 있다.3D 바이오프린팅 기술의 장기적인 목표 중 하나는 전체 장기를 재구성하는 것이지만, 완전히 기능하는 [28]장기를 프린팅하는 데는 거의 성공하지 못했습니다.이식 가능한 스텐트와 달리 장기는 복잡한 형태를 가지고 있고 바이오프린트가 상당히 어렵습니다.예를 들어 생체 인쇄된 심장은 구조 요구 사항뿐만 아니라 혈관 형성, 기계적 부하 및 전기 신호 전파 [29]요구 사항도 충족해야 합니다.이스라엘 연구원들은 2019년에 [30]인간의 세포로 토끼 크기의 심장을 만들었다.
2022년에는 환자 자신의 세포인 마이크로티아를 [31]치료하기 위한 외이(外 ear)를 이용한 3D 바이오프린트 이식 임상시험이 최초로 성공했다고 [32]보고되었다.
배양육
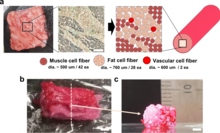
바이오프린팅은 배양육에도 사용할 수 있다.2021년에는 3종류의 소세포 섬유로 이루어진 스테이크 모양의 배양육이 생산되었다.와규 소고기는 원래 [33][34]고기와 비슷한 구조를 가지고 있습니다.
영향
3D 바이오프린팅은 생체 재료라고 불리는 혁신적인 재료에 대한 연구가 이루어짐으로써 조직 공학의 의학 분야에서 상당한 발전에 기여합니다.생체 재료는 3차원 물체를 인쇄하는 데 적합하고 사용되는 재료입니다.가장 주목할 만한 생물 공학 물질들 중 일부는 보통 연조직과 뼈를 포함한 평균적인 신체 물질보다 강합니다.이러한 구성 요소는 원래 차체 재료의 미래 대체물, 심지어 개선물 역할을 할 수 있습니다.예를 들어 알긴산염은 음이온성 고분자이며, 음이온성 고분자로 신체 일부 구조 [35]재료에 비해 실현 가능성, 강력한 생체 적합성, 낮은 독성 및 더 강력한 구조적 능력을 포함한다.합성 하이드로겔도 PV 기반 젤을 포함하여 일반적입니다.UV-initiated PV-based 가교제와 산의 조합은 Wake Forest Medicine Institute of Medicine에 의해 평가되었고 적합한 생체 [36]물질로 결정되었다.엔지니어들은 또한 주변 [10]조직으로부터 영양소와 산소의 확산을 극대화할 수 있는 마이크로 채널 인쇄와 같은 다른 옵션들을 연구하고 있다.게다가, 국방위협감축국은 심장, 간, 폐와 같은 작은 장기를 새로운 약물을 더 정확하게 시험할 수 [10]있는 가능성으로 인쇄하는 것을 목표로 하고 있으며 아마도 동물 실험을 할 필요가 없을 것이다.
「 」를 참조해 주세요.
레퍼런스
- ^ Roche CD, Brereton RJ, Ashton AW, Jackson C, Gentile C (2020). "Current challenges in three-dimensional bioprinting heart tissues for cardiac surgery". European Journal of Cardio-Thoracic Surgery. 58 (3): 500–510. doi:10.1093/ejcts/ezaa093. PMC 8456486. PMID 32391914.
- ^ Chimene D, Lennox KK, Kaunas RR, Gaharwar AK (2016). "Advanced Bioinks for 3D Printing: A Materials Science Perspective". Annals of Biomedical Engineering. 44 (6): 2090–2102. doi:10.1007/s10439-016-1638-y. PMID 27184494. S2CID 1251998.
- ^ Hinton TJ, Jallerat Q, Palchesko RN, Park JH, Grodzicki MS, Shue HJ, et al. (October 2015). "Three-dimensional printing of complex biological structures by freeform reversible embedding of suspended hydrogels". Science Advances. 1 (9): e1500758. Bibcode:2015SciA....1E0758H. doi:10.1126/sciadv.1500758. PMC 4646826. PMID 26601312.
- ^ Murphy, Sean V.; De Coppi, Paolo; Atala, Anthony (April 2020). "Opportunities and challenges of translational 3D bioprinting". Nature Biomedical Engineering. 4 (4): 370–380. doi:10.1038/s41551-019-0471-7. ISSN 2157-846X. PMID 31695178. S2CID 207912104.
- ^ Roche CD, Sharma P, Ashton AW, Jackson C, Xue M, Gentile C (2021). "Printability, durability, contractility and vascular network formation in 3D bioprinted cardiac endothelial cells using alginate–gelatin hydrogels". Frontiers in Bioengineering and Biotechnology. 9: 110. doi:10.3389/fbioe.2021.636257. PMC 7968457. PMID 33748085.
- ^ Nakashima Y, Okazak K, Nakayama K, Okada S, Mizu-uchi H (January 2017). "Bone and Joint Diseases in Present and Future". Fukuoka Igaku Zasshi = Hukuoka Acta Medica. 108 (1): 1–7. PMID 29226660.
- ^ a b c d e Shafiee A, Atala A (March 2016). "Printing Technologies for Medical Applications". Trends in Molecular Medicine. 22 (3): 254–265. doi:10.1016/j.molmed.2016.01.003. PMID 26856235.
- ^ a b Ozbolat IT (July 2015). "Bioprinting scale-up tissue and organ constructs for transplantation". Trends in Biotechnology. 33 (7): 395–400. doi:10.1016/j.tibtech.2015.04.005. PMID 25978871.
- ^ a b c Chua CK, Yeong WY (2015). Bioprinting: Principles and Applications. Singapore: World Scientific Publishing Co. ISBN 9789814612104.
- ^ a b c Cooper-White M (1 March 2015). "How 3D Printing Could End The Deadly Shortage Of Donor Organs". Huffpost Science. TheHuffingtonPost.com, Inc. Retrieved 17 February 2016.
- ^ a b Harmon K (2013). "A sweet solution for replacing organs" (PDF). Scientific American. 308 (4): 54–55. Bibcode:2013SciAm.308d..54H. doi:10.1038/scientificamerican0413-54. Archived from the original (PDF) on 2016-02-17. Retrieved 17 February 2016.
- ^ Singh D, Thomas D (April 2019). "Advances in medical polymer technology towards the panacea of complex 3D tissue and organ manufacture". American Journal of Surgery. 217 (4): 807–808. doi:10.1016/j.amjsurg.2018.05.012. PMID 29803500. S2CID 44091616.
- ^ a b c d e Murphy SV, Atala A (August 2014). "3D bioprinting of tissues and organs". Nature Biotechnology. 32 (8): 773–85. doi:10.1038/nbt.2958. PMID 25093879. S2CID 22826340.
- ^ a b c d Yoo J, Atala A (2015). "Bio-printing: 3D printing comes to life". ProQuest 1678889578.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ Manappallil JJ (2015). Basic Dental Materials. JP Medical Ltd. ISBN 9789352500482.
- ^ "3D Printing Technology At The Service Of Health". healthyeve. Archived from the original on 14 September 2016. Retrieved 4 August 2016.
- ^ a b Lepowsky E, Muradoglu M, Tasoglu S (2018). "Towards preserving post-printing cell viability and improving the resolution: Past, present, and future of 3D bioprinting theory" (PDF). Bioprinting. 11: e00034. doi:10.1016/j.bprint.2018.e00034. ISSN 2405-8866. S2CID 69929012 – via Elsevier Science Direct.
- ^ Gu Z, Fu J, Lin H, He Y (September 2020). "Development of 3D bioprinting: From printing methods to biomedical applications". Asian Journal of Pharmaceutical Sciences. 15 (5): 529–557. doi:10.1016/j.ajps.2019.11.003. PMC 7610207. PMID 33193859.
- ^ Derakhshanfar S, Mbeleck R, Xu K, Zhang X, Zhong W, Xing M (June 2018). "3D bioprinting for biomedical devices and tissue engineering: A review of recent trends and advances". Bioactive Materials. 3 (2): 144–156. doi:10.1016/j.bioactmat.2017.11.008. PMC 5935777. PMID 29744452.
- ^ a b Datta, Pallab; Ayan, Bugra; Ozbolat, Ibrahim T. (March 2017). "Bioprinting for vascular and vascularized tissue biofabrication". Acta Biomaterialia. 51: 1–20. doi:10.1016/j.actbio.2017.01.035. ISSN 1742-7061. PMID 28087487.
- ^ a b Gupta, Prerak; Mandal, Biman B. (2021-06-12). "Tissue‐Engineered Vascular Grafts: Emerging Trends and Technologies". Advanced Functional Materials. 31 (33): 2100027. doi:10.1002/adfm.202100027. ISSN 1616-301X. S2CID 236235572.
- ^ Hinton, Thomas J.; Jallerat, Quentin; Palchesko, Rachelle N.; Park, Joon Hyung; Grodzicki, Martin S.; Shue, Hao-Jan; Ramadan, Mohamed H.; Hudson, Andrew R.; Feinberg, Adam W. (2015-10-30). "Three-dimensional printing of complex biological structures by freeform reversible embedding of suspended hydrogels". Science Advances. 1 (9): e1500758. Bibcode:2015SciA....1E0758H. doi:10.1126/sciadv.1500758. ISSN 2375-2548. PMC 4646826. PMID 26601312.
- ^ Munaz, Ahmed; Vadivelu, Raja K.; St. John, James; Barton, Matthew; Kamble, Harshad; Nguyen, Nam-Trung (March 2016). "Three-dimensional printing of biological matters". Journal of Science: Advanced Materials and Devices. 1 (1): 1–17. doi:10.1016/j.jsamd.2016.04.001. ISSN 2468-2179.
- ^ Devillard, Raphaël; Pagès, Emeline; Correa, Manuela Medina; Kériquel, Virginie; Rémy, Murielle; Kalisky, Jérôme; Ali, Muhammad; Guillotin, Bertrand; Guillemot, Fabien (2014), "Cell Patterning by Laser-Assisted Bioprinting", Methods in Cell Biology, Elsevier, 119: 159–174, doi:10.1016/b978-0-12-416742-1.00009-3, ISBN 978-0-12-416742-1, PMID 24439284, retrieved 2021-10-27
- ^ Zopf DA, Hollister SJ, Nelson ME, Ohye RG, Green GE (May 2013). "Bioresorbable airway splint created with a three-dimensional printer". The New England Journal of Medicine. 368 (21): 2043–5. doi:10.1056/NEJMc1206319. PMID 23697530.
- ^ Atala A, Bauer SB, Soker S, Yoo JJ, Retik AB (April 2006). "Tissue-engineered autologous bladders for patients needing cystoplasty". Lancet. 367 (9518): 1241–6. doi:10.1016/S0140-6736(06)68438-9. PMID 16631879. S2CID 17892321.
- ^ Hong N, Yang GH, Lee J, Kim G (January 2018). "3D bioprinting and its in vivo applications". Journal of Biomedical Materials Research Part B: Applied Biomaterials. 106 (1): 444–459. doi:10.1002/jbm.b.33826. PMID 28106947.
- ^ Sommer AC, Blumenthal EZ (September 2019). "Implementations of 3D printing in ophthalmology". Graefe's Archive for Clinical and Experimental Ophthalmology. 257 (9): 1815–1822. doi:10.1007/s00417-019-04312-3. PMID 30993457. S2CID 116884575.
- ^ Cui H, Miao S, Esworthy T, Zhou X, Lee SJ, Liu C, et al. (July 2018). "3D bioprinting for cardiovascular regeneration and pharmacology". Advanced Drug Delivery Reviews. 132: 252–269. doi:10.1016/j.addr.2018.07.014. PMC 6226324. PMID 30053441.
- ^ Freeman D (April 19, 2019). "Israeli scientists create world's first 3D-printed heart using human cells". NBC News. Retrieved 2019-04-20.
- ^ "A Multicenter, Single Arm, Prospective, Open-Label, Staged Study of the Safety and Efficacy of the AuriNovo Construct for Auricular Reconstruction in Subjects With Unilateral Microtia". clinicaltrials.gov. 15 October 2021. Retrieved 19 July 2022.
- ^ Rabin, Roni Caryn (2 June 2022). "Doctors Transplant Ear of Human Cells, Made by 3-D Printer". The New York Times. Retrieved 19 July 2022.
- ^ "Japanese scientists produce first 3D-bioprinted, marbled Wagyu beef". New Atlas. 25 August 2021. Retrieved 21 September 2021.
- ^ Kang DH, Louis F, Liu H, Shimoda H, Nishiyama Y, Nozawa H, et al. (August 2021). "Engineered whole cut meat-like tissue by the assembly of cell fibers using tendon-gel integrated bioprinting". Nature Communications. 12 (1): 5059. Bibcode:2021NatCo..12.5059K. doi:10.1038/s41467-021-25236-9. PMC 8385070. PMID 34429413.
- ^ Crawford M (May 2013). "Creating Valve Tissue Using 3-D Bioprinting". ASME.org. American Society of Mechanical Engineers. Retrieved 17 February 2016.
- ^ Murphy SV, Skardal A, Atala A (January 2013). "Evaluation of hydrogels for bio-printing applications". Journal of Biomedical Materials Research. Part A. 101 (1): 272–84. doi:10.1002/jbm.a.34326. PMID 22941807.
추가 정보
- Tran J (2015). "To Bioprint or Not to Bioprint". North Carolina Journal of Law and Technology. 17: 123–78. SSRN 2562952. Archived from the original on 2019-03-10. Retrieved 2019-01-12.
- Tran J (May 7, 2015). "Patenting Bioprinting". Harvard Journal of Law and Technology Digest. 29. SSRN 2603693.
- Vishwakarma A (2014-11-27). Stem Cell Biology and Tissue Engineering in Dental Sciences. Elsevier, 2014. ISBN 9780123971579.