지상 유리 불투명도
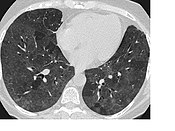
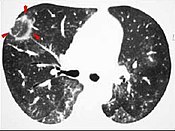
Ground-glass opacityGGO(Ground-glass oppacity)는 폐의 흉부 X선(라디오그래프) 또는 컴퓨터 단층촬영(CT)에서 볼 수 있는 소견이다.일반적으로 유체, 기도 붕괴, 섬유화 또는 신가소성 공정에 의한 공기 변위에 의한 흐릿한 오패시화(x-ray) 또는 증가된 감쇠(CT)의 영역으로 정의된다.[1]공기가 아닌 물질이 폐의 한 영역을 채우면 그 지역의 밀도가 높아진다.X-ray와 CT 모두에서, 이것은 보통 어둡게 보이는 폐와는 반대로 더 회색으로 보이거나 흐릿하게 보인다.간혹 정상적인 폐에서 볼 수 있지만 일반적인 병리학적 원인으로는 감염, 간성폐질환, 폐부종 등이 있다.[2][3]
정의
CT와 흉부 방사선 촬영 모두 주변 조직에 비해 공기 밀도가 상대적으로 낮아 정상적인 폐가 어둡게 나타난다.공기가 다른 물질(유체나 섬유화 등)으로 대체되면 부위의 밀도가 높아져 조직이 더 가벼워지거나 더 회색으로 보이게 된다.[4]
지상 유리 불투명도는 흉부 방사선 촬영법을 설명할 때도 사용되지만, 흉부의 고해상도 CT 촬영에서 발견 사항을 설명하는 데 가장 많이 사용된다.CT에서 이 용어는 폐정맥의 은폐 없이 감쇠(밀도)가 증가된 한 개 또는 여러 영역을 가리킨다.이것은 CT 영상촬영에서 일반적으로 어둡게 보이는 폐(공기충전)와는 반대로 더 회색으로 보인다.흉부 방사선 사진에서, 이 용어는 일반적으로 더 어둡게 보이는 (공기 충진) 폐가 더 불투명하거나, 흐리거나, 흐린 것처럼 보이는 하나 또는 여러 영역을 가리킨다.지면 유리 불투명도는 폐혈관 표시가 가려지는 통합과는 대조적이다.[3][5]GGO는 밀도가 증가하는 초점과 확산 영역을 모두 설명하는데 사용될 수 있다.[5]GGO의 하위 유형에는 확산, 결절, 중추, 모자이크, 미친 포장,[6] 후광 기호, 역광 표시가 있다.
원인들
지상 유리 공간에 대한 차등 진단은 광범위하다.일반적인 식이론으로는 감염, 간성폐질환, 폐부종, 폐출혈, 신엽 등이 있다.이미지와 환자의 임상적 특징의 상관관계는 진단의 범위를 좁히는 데 유용하다.[7][8]GGO는 정상적인 폐에서 볼 수 있다.만기가 되면 폐에 공기가 적어져 조직의 밀도가 상대적으로 증가하게 되고, 따라서 CT의 감쇠가 증가하게 된다.나아가 CT촬영을 위해 환자가 누워서 누우면 후폐가 종속적인 위치에 있어 후부 폐포도 부분적으로 붕괴된다.이것은 조직의 밀도를 증가시켜 감쇠가 증가되고 CT에 지반 유리가 나타날 수 있다.[3]
감염원인
폐렴의 설정에서 GGO(통합 반대)의 존재는 유용한 진단 단서가 된다.대부분의 박테리아 감염은 로바 결합을 유도하는 반면 비정형 폐렴은 GGO를 유발할 수 있다.유의할 점은 아래에 열거된 많은 폐 감염이 GGO로 이어질 수 있지만, 모든 경우에 이러한 현상이 발생하는 것은 아니라는 점이다.[2][6][8][9][10]
세균
바이러스
- 아데노바이러스
- 코로나바이러스(메르스-코브, 사스-코브, 사스-코브-2 포함)
- 사이토메갈로바이러스(CMV)
- 헤르페스 심플렉스 바이러스(HSV)
- 인간 메타폴리스공해바이러스(HMPV)
- 독감
- 홍역
- Respiratory Syncytal Virus(RSV)
- 바리셀라 조스터
풍갈
기생충
비감염원인
노출
특발성 간염성 폐렴
신가소성 공정
추가원인
- 급성유소성 폐렴
- 콜레스테롤 그라눌로마스
- 초점간섬유화
- 다낭염에 의한 과립증
- 림프성 과립증
- 폐 치경 단백질증
- 폐석회화
- 폐모세관혈모세포증
- 폐유착
- 폐부종
- 폐출혈
- 폐경색
- 사코이데스증
- 흉부내막증
패턴
지상 유리 공간의 일반적인 패턴은 7가지다.[6]환자의 임상 징후와 증상과 결합하면 영상촬영에서 보이는 GGO 패턴이 차등진단을 좁히는 데 유용하다.어떤 질병 과정은 하나의 패턴으로만 나타나지만, 많은 질병들은 GGO 패턴의 혼합으로 나타날 수 있다는 점을 유념해야 한다.[6]
확산
확산 패턴은 일반적으로 한쪽 또는 양쪽 폐의 여러 로브에 있는 GGO를 가리킨다.일반적으로 GGO의 확산 패턴은 유체, 염증성 파편 또는 섬유증으로 인해 발생할 수 있다.심장성 폐부종과 ARDS는 액체가 가득 찬 폐의 일반적인 원인이다.확산성 치경 출혈은 몇몇 종류의 혈관염, 자가면역 질환, 출혈 장애에서 나타나는 확산성 GGO의 희귀한 원인이다.[6]
염증과 섬유증은 또한 GGO를 확산시킬 수 있다. 일반적으로 면역항암제(예: 에이즈 환자) 또는 면역억제 환자에서 나타나는 감염인 폐렴구균 폐렴은 GGO를 확산시키는 전형적인 원인이다.많은 바이러스성 폐렴과 특발성 간 폐렴도 GGO 패턴 확산으로 이어질 수 있다.폐방사선치료의 부작용인 방사선폐렴증은 폐섬유화 및 GGO 확산으로 이어질 수 있다.[6]
결절형
결절 GGO는 양성 조건과 악성 상태로 광범위하게 분리될 수 있는 수많은 잠재적 원인이 있다.결절성 GGO의 형성으로 이어질 수 있는 양성 질환으로는 아스페르길루시스, 급성오신성 폐렴, 초점간섬유화, 다낭염에 의한 과로마토시스, IgA 혈관염, 조직성 폐렴, 폐결핵구균, 흉부내막염 등이 있다.초점간 섬유증은 CT 촬영에서 악성 결절성 GGO와 구별할 때 독특한 도전이 나타난다.그것은 일반적으로 장기간의 영상촬영 후속조치에 대해 지속적이며 악성 결절성 GGO와 유사한 외형을 공유한다.[10]
결절성 GGO의 사전 악성 또는 악성 원인으로는 선각종, 현시점에서의 선각종, 비정형 선각성 과대증(AAH) 등이 있다.한 대규모 리뷰 연구에서는 반복적인 CT 촬영에 존재하는 결절성 GGO의 80%가 이전 악성 성장 또는 악성 성장을 나타낸다는 것을 발견했다.CT만으로 전 악성종양과 악성종양을 구분하는 것은 방사선 전문의에게 어려움을 줄 수 있지만, 사전 악성종양 결절을 나타내는 몇 가지 특징이 있다.AAH는 결절 GGO의 사전 악성 원인이며, 일반적으로 자궁내막종에 비해 CT상 감쇠율이 낮고 결절 크기(<10 mm)[11]가 작다.게다가, AAH는 종종 악성 성장과 관련이 있는 견고한 특징과 가시가 있는 외관이 결여되어 있는 경우가 많다.[10]이와는 대조적으로, 선각종은 침습적이 되면 인접한 늑막의 수축이 더 자주 발생하게 되고 혈관 표시가 증가하는 것을 보일 수 있다.15 mm이상의 결절은 거의 항상 침습성 아데노카르시노종을 나타낸다.[10][11]
구심체
중추성 GGO는 호흡기관지, 작은 폐동맥, 주변 조직으로 구성된 폐의 1개 또는 복수의 이차엽 내에서 발생하는 오백성을 가리킨다.[3]이러한 GGO의 결정적인 특징은 글로브 간 정격막의 관여 부족이다.중심성 GGO의 잠재적 원인으로는 전이성 질환에 의한 폐석회화, 특발성 간 폐렴의 일부 유형, 과민성 폐렴염, 흡인성 폐렴염, 콜레스테롤 그래눌로마, 폐모세혈관 혈전증 등이 있다.[6]
모자이크
GGO의 모자이크 패턴은 CT에서 감쇠가 증가하거나 감쇠가 감소하는 여러 불규칙한 영역을 가리킨다.그것은 종종 작은 폐동맥의 폐쇄나 공기 트랩으로 이어지는 작은 기도의 방해로 인해 발생한다.[6]사코이데오증은 중간 부위에 그라눌로마(Granulomas)가 형성돼 모자이크 GGO의 추가 원인이다.이는 다낭염에 의한 과립증(Granulomatosis)과 공존할 수 있으며, 이는 지면 유리 외관에 따라 감쇠가 증가하는 확산 영역으로 이어질 수 있다.[6]
크레이지 포장
미친 포장 패턴은 기단간과 세포내 확장이 있을 때 발생할 수 있다.이것은 때때로 불규칙한 벽돌이나 기와로 포장된 길을 닮았다.그것은 일반적으로 확산되며 하나 또는 여러 개의 로브의 더 큰 영역을 포함한다.폐렴구균 폐렴, 말기 아데노카르신종, 폐부종, 특발성 간폐렴, 확산성 치경출혈, 사코이도증, 폐 치경단백질증 등 다양한 잠재적 원인이 있다.[6]또한 COVID-19는 가끔 미친 포장 패턴을 가진 GGO를 유발하는 것으로 나타났다.[12]
헤일로 기호
후광 기호는 통합 또는 결절 주위의 영역을 채우는 GGO를 가리킨다.이것은 CMV 폐렴, 결핵, 심초음파 감염, 일부 진균성 폐렴, 패혈성 색전증 등 다양한 종류의 폐 감염에서 가장 흔히 볼 수 있다.기생충 감염인 시스토소미아시스(Schistosomiasis)도 흔히 후광 표지와 함께 나타난다.중요한 비감염 원인으로는 다낭염에 의한 과립증, 폐출혈에 의한 전이성 질환, 특발성 간 폐렴이 있다.[6]
역헤일로 기호
뒤바뀐 후광 기호는 보다 밀도가 높은 통합으로 둘러싸인 중앙 지상 유리 불투명이다.발표된 기준에 따르면, 통합은 원의 4분의 3 이상을 형성해야 하며 두께는 최소 2mm 이상이어야 한다.[13]폐렴을 조직하는 것을 암시하는 경우가 많지만,[14] 이런 증상을 가진 사람의 약 20%에서만 볼 수 있다.[13]또한 후광이 출혈로 이루어진 폐경색에서는 [15]물론 파라코키디오이디오미디옥시증, 결핵, 아스페르길루증 등의 전염성 질환에서도 나타날 수 있으며, 다낭염, 림프성 과립증, 사르코이데스증에서도 나타날 수 있다.[16]
COVID-19
지상 유리 불투명도는 COVID-19가 확인된 환자에게서 가장 흔한 영상 소견 중 하나이다.[17][18]한 체계적 검토 결과 CT상 이상 폐결핵(COVID-19) 소견이 있는 환자 중 80% 이상이 GGO를, 50% 이상이 GGO와 결합을 혼합한 것으로 나타났다.[17]혼합 통합형 GGO는 노인 인구에서 가장 많이 발견되었다.[19]여러 연구에서 COVID-19의 질병 과정에서 초기, 중간 및 병원 퇴원 영상 소견 사이의 패턴을 설명하였다.가장 일반적으로, 초기 CT 촬영은 폐 주변에 있는 양자의 GGO를 보여준다.초기 단계에서는 상엽과 우측 중엽의 관여가 질병 코스의 초기에 보고되었지만, 이것은 하엽에서 가장 많이 발견된다.[17][19]이는 사스와 메르스라는 유사한 두 코로나바이러스와는 대조적인 것으로, 초기 영상 촬영 시 폐가 하나만 더 많이 관여한다.[20][21]COVID-19 감염이 진행됨에 따라 GGO는 일반적으로 더 확산되어 통합으로 진전되는 경우가 많다.[12][19]이것은 때때로 미친 포장 패턴과 기단간 패혈성 두꺼워짐의 발달과 동반된다.[19]많은 경우에서 가장 심각한 폐 CT 이상은 증상이 시작된 후 2주 이내에 발생했다.[18]이때 증세가 호전되면서 많은 개인들이 통합과 GGO의 해결을 보이기 시작한다.그러나 일부 환자들은 증상이 악화되고 영상 소견이 나타나면서 패혈증, GGO, 합병증 등이 추가로 증가하기도 한다.이러한 환자들은 치료 에스컬레이션이 필요한 급성 호흡곤란 증후군(ARDS)으로 진행되면서 폐 "화이트 아웃"이 발생할 수 있다.[18][22]
예비 보고서에 따르면 퇴원 시 많은 환자들이 GGO 잔류량을 갖고 있는 것으로 나타났다.COVID-19의 참신성 때문에, 장기 폐 CT 변화를 조사하는 대규모 연구가 아직 완료되지 않았다.다만 사스와 메르스 회복 후 환자들에게 장기간의 폐변화가 나타나 급성 COVID-19 감염에서 회복한 환자들에게도 유사한 장기 합병증이 나타날 가능성을 시사했다.[23]
역사
주요 방사선학회에 의한 "지상 유리 불투명도"의 첫 번째 사용은 1984년 미국 뢴트겐학 저널에서 일어났다.흉부 영상 방사선 전문의 그룹인 Fleischner Society에서 추천한 명칭 용어집의 일부로 출판되었다.[24]원래 발표된 정의는 다음과 같다: "정상 해부학적 디테일이 부분적으로 가려지는 확장되고 미세한 폐 불투명성 패턴; 에칭되거나 마모된 유리와 유사함".[24]그것은 2008년 Fleischner Society에 의해 업데이트된 용어집에 더 상세한 정의와 함께 다시 포함되었다.[25]
참고 항목
참조
- ^ Goodman LR (2015). Felson's principles of chest roentgenology (Fifth ed.). Philadelphia, PA: Elsevier. pp. Supplement 3, e36–e80. ISBN 978-0-323-77795-7. OCLC 1134689400.
- ^ a b Mettler Jr FA (2019). Essentials of radiology (Fourth ed.). Philadelphia, PA: Elsevier. pp. 299–331. ISBN 978-0-323-56787-9. OCLC 1053711279.
- ^ a b c d Sharma A, Abbott G (2019). Thoracic imaging (Third ed.). Philadelphia, PA: Elsevier. ISBN 978-0-323-59699-2. OCLC 1022265855.
- ^ Herring W (2020). Learning radiology : recognizing the basics (4th ed.). Philadelphia: Elsevier. pp. 2–4. ISBN 978-0-323-56728-2. OCLC 1096282271.
- ^ a b Walker CM, Chung JH (2019). Müller's imaging of the chest (2nd ed.). Philadelphia, PA: Elsevier. pp. 109–137. ISBN 978-0-323-53179-5. OCLC 1051135278.
- ^ a b c d e f g h i j k El-Sherief AH, Gilman MD, Healey TT, Tambouret RH, Shepard JA, Abbott GF, Wu CC (2014). "Clear vision through the haze: a practical approach to ground-glass opacity". Current Problems in Diagnostic Radiology. 43 (3): 140–58. doi:10.1067/j.cpradiol.2014.01.004. PMID 24791617.
- ^ El-Sherief AH, Gilman MD, Healey TT, Tambouret RH, Shepard JA, Abbott GF, Wu CC (2014). "Clear vision through the haze: a practical approach to ground-glass opacity". Current Problems in Diagnostic Radiology. 43 (3): 140–58. doi:10.1067/j.cpradiol.2014.01.004. PMID 24791617.
- ^ a b Parekh M, Donuru A, Balasubramanya R, Kapur S (July 2020). "Review of the Chest CT Differential Diagnosis of Ground-Glass Opacities in the COVID Era". Radiology. 297 (3): E289–E302. doi:10.1148/radiol.2020202504. PMC 7350036. PMID 32633678.
- ^ Rossi SE, Erasmus JJ, McAdams HP, Sporn TA, Goodman PC (1 September 2000). "Pulmonary drug toxicity: radiologic and pathologic manifestations". Radiographics. 20 (5): 1245–59. doi:10.1148/radiographics.20.5.g00se081245. PMID 10992015.
- ^ a b c d Park CM, Goo JM, Lee HJ, Lee CH, Chun EJ, Im JG (1 March 2007). "Nodular ground-glass opacity at thin-section CT: histologic correlation and evaluation of change at follow-up". Radiographics. 27 (2): 391–408. doi:10.1148/rg.272065061. PMID 17374860.
- ^ a b Lee HY, Choi YL, Lee KS, Han J, Zo JI, Shim YM, Moon JW (March 2014). "Pure ground-glass opacity neoplastic lung nodules: histopathology, imaging, and management". AJR. American Journal of Roentgenology. 202 (3): W224-33. doi:10.2214/AJR.13.11819. PMID 24555618.
- ^ a b Ye Z, Zhang Y, Wang Y, Huang Z, Song B (August 2020). "Chest CT manifestations of new coronavirus disease 2019 (COVID-19): a pictorial review". European Radiology. 30 (8): 4381–4389. doi:10.1007/s00330-020-06801-0. PMC 7088323. PMID 32193638.
- ^ a b Foley R, et al. "Reversed halo sign (lungs)". Radiopaedia. Retrieved 2 January 2018.
- ^ Elicker BM, Webb WR (2012). Fundamentals of High-Resolution Lung CT: Common Findings, Common Patterns, Common Diseases, and Differential Diagnosis. Lippincott Williams & Wilkins. ISBN 9781469824796.
- ^ Wu G, Schmit B, Arteaga V, Palacio D (2017). "Medical image of the week: pulmonary infarction- the "reverse halo sign"". Southwest Journal of Pulmonary and Critical Care. 15 (4): 162–163. doi:10.13175/swjpcc124-17. ISSN 2160-6773.
- ^ Karthikeyan D (2013). High Resolution Computed Tomography of the Lungs: A Practical Guide. JP Medical Ltd. p. 256. ISBN 9789350904084.
- ^ a b c Bao C, Liu X, Zhang H, Li Y, Liu J (June 2020). "Coronavirus Disease 2019 (COVID-19) CT Findings: A Systematic Review and Meta-analysis". Journal of the American College of Radiology. 17 (6): 701–709. doi:10.1016/j.jacr.2020.03.006. PMC 7151282. PMID 32283052.
- ^ a b c Salehi S, Abedi A, Balakrishnan S, Gholamrezanezhad A (July 2020). "Coronavirus Disease 2019 (COVID-19): A Systematic Review of Imaging Findings in 919 Patients". AJR. American Journal of Roentgenology. 215 (1): 87–93. doi:10.2214/AJR.20.23034. PMID 32174129.
- ^ a b c d Salehi S, Abedi A, Balakrishnan S, Gholamrezanezhad A (July 2020). "Coronavirus Disease 2019 (COVID-19): A Systematic Review of Imaging Findings in 919 Patients". AJR. American Journal of Roentgenology. 215 (1): 87–93. doi:10.2214/AJR.20.23034. PMID 32174129.
- ^ Ooi GC, Daqing M (November 2003). "SARS: radiological features". Respirology. 8 Suppl (s1): S15-9. doi:10.1046/j.1440-1843.2003.00519.x. PMC 7169195. PMID 15018128.
- ^ Das KM, Lee EY, Langer RD, Larsson SG (June 2016). "Middle East Respiratory Syndrome Coronavirus: What Does a Radiologist Need to Know?". AJR. American Journal of Roentgenology. 206 (6): 1193–201. doi:10.2214/AJR.15.15363. PMID 26998804.
- ^ Carotti M, Salaffi F, Sarzi-Puttini P, Agostini A, Borgheresi A, Minorati D, et al. (July 2020). "Chest CT features of coronavirus disease 2019 (COVID-19) pneumonia: key points for radiologists". La Radiologia Medica. 125 (7): 636–646. doi:10.1007/s11547-020-01237-4. PMC 7270744. PMID 32500509.
- ^ George PM, Barratt SL, Condliffe R, Desai SR, Devaraj A, Forrest I, et al. (November 2020). "Respiratory follow-up of patients with COVID-19 pneumonia". Thorax. 75 (11): 1009–1016. doi:10.1136/thoraxjnl-2020-215314. PMC 7447111. PMID 32839287.
- ^ a b Tuddenham WJ (September 1984). "Glossary of terms for thoracic radiology: recommendations of the Nomenclature Committee of the Fleischner Society". AJR. American Journal of Roentgenology. 143 (3): 509–17. doi:10.2214/ajr.143.3.509. PMID 6380245.
- ^ Hansell DM, Bankier AA, MacMahon H, McLoud TC, Müller NL, Remy J (March 2008). "Fleischner Society: glossary of terms for thoracic imaging". Radiology. 246 (3): 697–722. doi:10.1148/radiol.2462070712. PMID 18195376.